铼(VII)催化的烯丙醇异构化反应及其在天然产物全合成中应用的研究进展
2020-04-20胡家栋高冬梅
文 雯,胡家栋,2,高冬梅
(1. 杨凌职业技术学院 药物与化工分院,陕西 杨凌712100;2. 西北农林科技大学 化学与药学院,陕西 杨凌712100)
前 言
烯丙醇异构化反应是由烯丙醇的羟基[1,3]迁移伴随双键移位组成的一类反应。在天然产物全合成中,此异构化反应是一种将容易构建的烯丙醇转化为难以构建的烯丙醇的有效手段[1]。七价铼(VII)中高铼酸(酐)酯类催化剂是一种温和的催化烯丙醇异构化反应的试剂[1]。本文对近几年铼(VII)催化的烯丙醇异构化反应进展及其在天然产物全合成中的应用进行了综述。
1 铼(VII)催化的烯丙醇异构化反应
1997年,Osborn 等[2]首次报道了R3SiOReO3体系催化的烯丙醇异构化反应(图1a)。与V[3]、W[4]和Mo[5]的氧化物相比,此体系可以在室温条件下进行。然而,得到的是一对位置异构体的混合物,说明此催化反应可逆。

图1 铼(VII)催化的烯丙醇异构化反应Fig. 1 The Re(VII)-catalyzed isomerization of allyl alcohol
为了打破这一热力学平衡,提高异构化反应的区域选择性从而增加该反应的合成潜力,有机化学家们做了一系列工作。2005年,Morrill 等[6]对Ph3SiOReO3催化的烯丙醇异构化反应的区域选择性进行了系统的研究。结果表明(图1b),当异构化产物的双键与苯环形成共轭时,反应向形成热力学稳定产物的方向进行;当加入N,O- 双(三甲基硅烷基)乙酰胺(BSA)时,由于BSA 对伯醇的硅烷化速率大于叔醇,占有动力学优势,反应朝生成伯醇的方向移动。
2006年,Hansen 等[7]以Re2O7为催化剂,利用异构化产物与烯基硼酸酯形成新的硼酸酯的策略,提高了反应的区域选择性(图1b)。该反应通过顺式导向亲电的硼酸酯捕获了异构化产物的醇羟基。在该反应中,硅基保护的烯丙醇可以直接参与异构化反应。并且反应的产物可以进一步参与Suzuki 偶联反应。
可以看出,热力学和动力学手段均可提高异构化反应的区域选择性,拓展了该异构化反应的合成潜力。
2 铼(VII)催化的烯丙醇异构化串联反应
进一步的实验观察和理论研究表明[2,8],铼(VII)催化的烯丙醇异构化反应(图2)可能主要历经协同的[3,3]- 重排过程(path a),获得E 式构型为主的产物。然而,少量Z 式产物的存在,以及手性转移实验中观察到ee 值部分降低的现象[9]说明该反应也存在离子化- 重组过程(path b)。基于以上机理研究,合成化学家们利用部分极化的中间体I 和离子化的中间体II 作为亲核或亲电试剂,开发了一系列铼(VII)催化的烯丙醇异构化参与的串联反应。
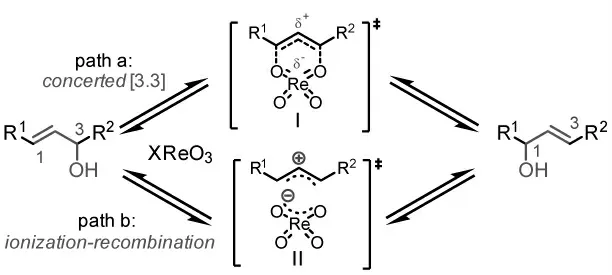
图2 铼(VII)催化的烯丙醇异构化反应可能的机理Fig. 2 The possible mechanism of Re(VII)-catalyzed isomerization of allyl alcohol
首先,是中间体I 作为亲核试剂参与的串联反应。2011年,Xie 等[10]以Re2O7为催化剂,利用铼(VII)氧化物与烯丙醇形成部分极化的中间体I 为亲核试剂,以酮羰基、缩酮或Michael 受体作为亲电试剂,发生烯丙醇异构化/亲核加成串联反应构建了螺环体系(图3a)。在此反应中,Re2O7除了作为烯丙醇异构化试剂以外,还作为Lewis 酸活化了亲电试剂,使得反应可以顺利进行。2013年,该小组[11]将酮羰基、环氧和α,β- 不饱和羰基化合物等亲电试剂集成到一个线性分子上,通过Re2O7催化的烯丙醇异构化与多步亲核加成反应串联,一步构建了多环体系(图3b)。
2016年,Hu 等[12]报道了一种Re2O7催化的烯丙醇异构化/oxa-Michael 加成串联反应,可以一步构建顺式双环体系(图3c)。该反应在Re2O7催化下先发生烯丙基移位,然后对二烯酮进行去对称化加成反应,非对映选择性地构建了氧杂双环体系。若将Re2O7与BINOL 衍生的手性磷酸联合使用[13],可以获得手性加成的双环产物。

图3 铼(VII)催化的烯丙醇异构化串联反应Fig. 3 The Re(VII)-catalyzed isomerization tandem reaction of allyl alcohol
然后,是中间体II 作为亲电试剂参与的串联反应。2017年,Wan 等[14]报道了Re2O7催化的单烯二醇的环醚化反应构建氧杂环(图3d)。该反应利用Re2O7催化烯丙醇形成烯丙基碳正离子,另一分子游离的醇羟基作为亲核试剂对其进行加成得环合产物。手性转移实验发现得到的是完全消旋化的产物,进一步佐证了该反应历经离子化-- 重组的过程。同年,Rohrs 等[15]报道了Re2O7·SiO2催化的相同的环醚化反应。应用此反应,该小组完成了Herboxidiene 及其类似物的全合成。
可以看出,应用铼(VII)催化的烯丙醇异构化反应的两种不同中间体,与亲电或亲核反应组成串联反应,可以提高异构化反应的区域选择性,并且构建出多样的环状骨架。
3 在天然产物全合成中的应用
由于铼(VII)高效的催化能力和温和的反应条件,该类烯丙醇异构化反应被广泛地应用于天然产物的合成中。2000年,Trost 等[16]报道的用于调节乙酰胆碱受体表达而治疗重症肌无力和阿尔兹海默症的药物(-)-Galanthamine 的全合成中(图4a),由于运用常规的烯丙位氧化方法无法构建出分子中的烯丙醇,因此通过环氧化、苯硒加成开环和氧化消除几步转化构建了异位的烯丙醇底物,最后在Ph3SiOReO3催化下发生烯丙醇异构化反应,最终以50%的异构化收率合成了目标分子。
2007年,Jung 等[17]报道的具有抗真菌活性和细胞毒活性的大环内酯类海洋天然产物Leucascandrolide A 的全合成中(图4b),运用了Re2O7催化的手性烯丙醇的异构化反应串联缩醛化反应以69%的收率构建了半缩醛中间体。最终,此中间体经两步转化合成了目标天然产物。
2013年,Volchkov 等[18]报道的具有体外抗人表皮瘤和小鼠淋巴瘤活性的大环内酯类海洋天然产物(-)-Amphidinolide V 的全合成中(图4c),运用Re2O7催化的烯丙醇硅醚的异构化反应,通过形成稳定的六元环硅醚的手段提高了反应的区域选择性,以85%的收率构建了关键中间体。

图4 铼(VII)催化的烯丙醇异构化反应在全合成中的应用Fig. 4 The application of Re(VII)-catalyzed isomerization of allyl alcohol in total synthesis of natural products
2017年,Floreancig 等[15]报道的具有剪接体抑制活性的潜在抗肿瘤的聚酮类化合物Herboxidiene的全合成中(图4d),运用了Re2O7·SiO2催化的烯丙醇异构化串联亲核加成反应,历经正离子-- 重组过程,以82%的收率构建了吡喃环。最后,经两步转化完成了目标分子的合成。
4 结束语
综上所述,铼(VII)催化的烯丙醇异构化反应具有高效、温和的特点。反应主要历经协同的[3,3]重排途径,也伴随离子化- 重组过程。通过形成热力学稳定产物的策略可以提高异构化反应的区域选择性。这一温和高效的异构化反应为天然产物全合成中构建难以获得的烯丙醇结构单元提供了有效的转化策略,解决了包括抗阿尔兹海默症的药物(-)-Galanthamine 在内的多种活性天然产物全合成的关键问题,在新型医药、农药产品的开发方面具有广阔的应用前景。
