Claisen-Schmidt 缩合反应的研究进展
2020-04-20符鑫博
符鑫博
(渤海大学 实验中心,辽宁 锦州121013)
前 言
α,β- 不饱和酮是一类重要的有机化合物,广泛存在于天然产物中,同时也是一种重要的有机合成中间体,被广泛应用于香料和药物中间体的合成[1]。查尔酮是α,β- 不饱和酮化合物的典型代表,因其具有独特的结构和生理活性而备受研究[2],查尔酮类化合物具有抗癌[3~6]、抗炎[7]、抗菌[8~10]等活性。
Claisen-Schmidt 缩合反应是指一个无α- 氢原子的醛与含有α- 氢原子的脂肪族醛、酮在碱性条件下发生交错羟醛缩合,失水后得到α,β- 不饱和醛或酮的反应。如图1 所示,苯甲醛和乙醛发生Claisen-Schmidt 缩合反应生成肉桂醛。该方法具有操作简便、反应条件温和等特点。Claisen-Schmidt 缩合反应为这类化合物提供了一个简便的合成方法,它是合成查尔酮类化合物的主要方法之一。
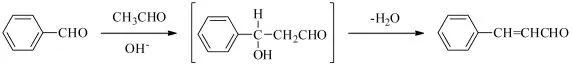
图1 苯甲醛和乙醛的Claisen-Schmidt 缩合反应Fig.1 The Claisen-Schmidt condensation reaction of benzaldehyde with acetaldehyde
为了更好地了解这方面研究的最新动态,本文综述了近年来涉及Claisen-Schmidt 缩合反应的有机合成部分。
1 无机碱促进的Claisen-Schmidt 缩合反应
2014年,我们课题组[11]报道了一种超声辅助Claisen-Schmidt 反应合成含胡椒环的吲哚查尔酮。3- 乙酰基-2- 氯-1-(4- 氯苄基)吲哚和胡椒醛在5%KOH 作为碱、1,4- 二氧六环作为溶剂、超声辅助条件下经Claisen-Schmidt 缩合反应以78%的收率得到(E)-3-(5- 胡椒基)-1-(2- 氯-1-(4- 氯苄基)-1H-3- 吲哚)查尔酮,其反应式如图2 所示。
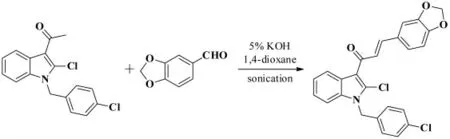
图2 3-乙酰基-2-氯-1-(4-氯苄基)吲哚和胡椒醛的Claisen-Schmidt 缩合反应Fig.2 The Claisen-Schmidt condensation reaction of 1-(2-chloro-1-(4-chlorobenzyl)-1H-indol-3-yl)ethanone with benzo[d][1,3]dioxole-5-carbaldehyde
我们对溶剂和碱进行了筛选,发现在2%NaOH作为碱、MeOH 作为溶剂的条件下反应未得到目标产物;在5%KOH 作为碱、MeOH 作为溶剂的条件下反应以30%的收率得到目标产物;当溶剂换成1,4- 二氧六环时,其收率提高到52%;在超声辅助下反应2h,目标产物的收率达78%;而在此条件下反应8h,目标产物的收率没有提高。
另外,我们还尝试在无溶剂研磨的条件下进行此反应,也能以类似的收率得到目标产物。这两种方法具有操作简便、反应条件温和、收率高等优点。
2016年,Mao 等[12]报道了室温下4- 氟苯乙酮和N,N- 二甲基-4- 氨基苯甲醛在KOH 作为碱、EtOH 作为溶剂的条件下经Claisen-Schmidt 缩合反应得到(E)-3-(4-(二甲基氨基)苯基)-1-(4- 氟苯基)-2- 丙烯-1- 酮,其反应式如图3 所示。

图3 4-氟苯乙酮和N,N-二甲基-4-氨基苯甲醛的Claisen-Schmidt缩合反应Fig.3 The Claisen-Schmidt condensation reaction of 1-(4-fluorophenyl)ethanone with N,N-dimethyl-4-(dimethylamino)benzaldehyde
2016年,杨永青等[13]报道了3,3- 二亚甲基-2,4- 戊二酮和苯甲醛在Ba(OH)2作为碱、MeOH 作为溶剂的条件下发生Claisen-Schmidt 缩合反应以90%的收率得到3,5- 二氧代-4,4- 二亚甲基-1,7-二苯基-1,6- 庚二烯,其反应式如图4 所示。
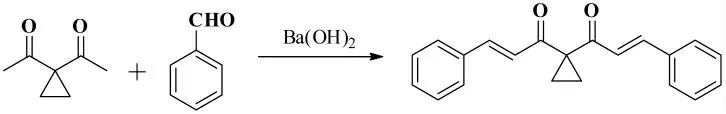
图4 3,3-二亚甲基-2,4-戊二酮和苯甲醛的Claisen-Schmidt 缩合反应Fig.4 The Claisen-Schmidt condensation reaction of 3,3-dimethylene-2,4-pentanedione with benzaldehyde
3,3- 五亚甲基-2,4- 戊二酮和3,4- 二甲氧基苯甲醛在Ba(OH)2作为碱的条件下意外地得到了1- 环己基-3-(3,4- 二甲氧基苯基)丙烯酮(如图5所示),其收率小于5%。作者在筛选条件时发现改变投料顺序和提高反应液浓度会导致目标产物收率的提高,把醛加入二酮与碱的混合液中改为把碱加入醛和二酮的混合物中,目标产物的收率提高到65%,当反应液浓度从0.05mol/L 变为0.5mol/L 时,目标产物的收率提高到86%。作者尝试选用同浓度的NaOH 作为碱,其收率也低于Ba(OH)2。作者还尝试选用DBU 和三乙胺等有机碱,其中DBU 作为碱的反应收率低于同浓度的Ba(OH)2,而三乙胺作为碱反应4d 没有观察到反应的发生。
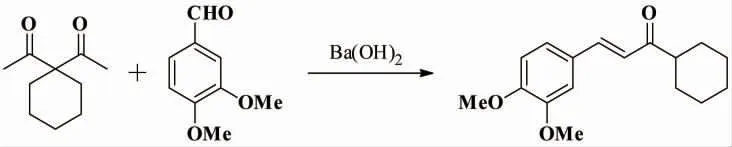
图5 3,3-五亚甲基-2,4-戊二酮和3,4-二甲氧基苯甲醛的Claisen-Schmidt 缩合反应Fig.5 The Claisen-Schmidt condensation reaction of 3,3-cyclopentane-2,4-pentanedione with 3,4-dimethoxy benzaldehyde
2016年,Damodar 等[14]报道了一种合成丙烯酰胺和吡喃查尔酮的有效方法,其合成的关键步骤是取代苯乙酮和芳醛在KOH 作为碱、MeOH/H2O 作为溶剂的条件下发生Claisen-Schmidt 缩合反应,其反应式如图6 所示。作者还对所合成的目标化合物的抗炎作用进行研究,发现部分化合物表现出明显的活性,且无细胞毒性。
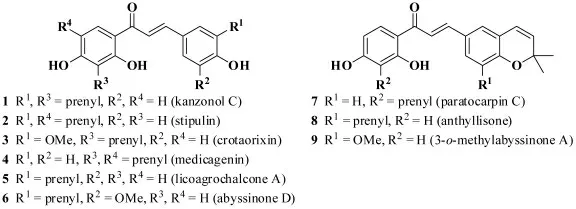
图6 天然丙烯酰胺和吡喃查尔酮的结构Fig.6 The structures of natural acrylamide and pyranochalcones
2016年,Bhat 等[15]报道了一系列具有抗氧化、抗癌的1,2,3- 三唑基查尔酮衍生物的合成,以1-(1-(2,3- 二氯-6- 甲基-5-(三氟甲基)苯基)-5-甲基-1H-1,2,3- 三氮唑-4- 基)苯乙酮为底物,与多种芳醛在NaOH 作为碱、EtOH 作为溶剂的条件下经Claisen-Schmidt 缩合反应生成(E)-1-(1-(2,3- 二氯-6- 甲基)-5-(三氟甲基)苯基)-5- 甲基-1,2,3- 三氮唑-4- 基)-3- 芳基-2- 丙烯-1-酮和(E)-1-(1-(2,3- 二氯-6- 甲基)-5-(三氟甲基)苯基)-5- 甲基-1H-1,2,3- 三氮唑-4- 基)-3-(1,3- 二芳基-1H- 吡唑-4- 基)-2- 丙烯-1- 酮,其反应式如图7 所示。
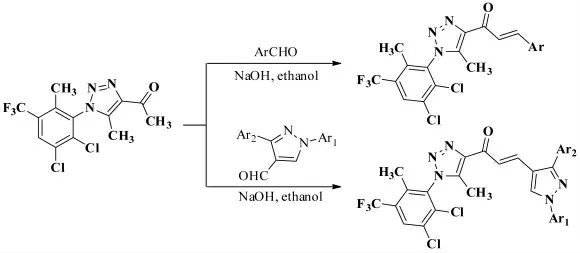
图7 1-(1-(2,3-二氯-6-甲基-5-(三氟甲基)苯基)-5-甲基-1H-1,2,3-三氮唑-4-基)苯乙酮和芳醛的Claisen-Schmidt 缩合反应Fig.7 The Claisen-Schmidt condensation reaction of 1-(1-(2,3-dichloro-6-methyl-5-(trifluoromethyl)phenyl)-5-methyl-1H-1,2,3-triazol-4-yl)ethanone with aromatic aldehydes
2017年,Li 等[16]报道了一系列卤代氮杂查尔酮的合成,以2- 乙酰基吡啶为底物和卤代苯甲醛在NaOH 作为碱、EtOH 作为溶剂的条件下经Claisen-Schmidt 缩合反应生成卤代3- 苯基-1-(2-吡啶基)-2- 丙烯-1- 酮衍生物,其反应式如图8所示。

图8 2-乙酰基吡啶和卤代苯甲醛的Claisen-Schmidt 缩合反应Fig.8 The Claisen-Schmidt condensation reaction of 1-(pyridine-2-yl)ethanone with halo-substituted benzaldehydes
2017年,Coskun 等[17]报道了一类具有抗癌活性的查尔酮衍生物的合成,室温下以1-(7- 乙氧基-2- 苯并呋喃基)乙酮为底物和多种芳醛在NaOH作为碱、MeOH 作为溶剂的条件下经Claisen-Schmidt 缩合反应生成了1-(7- 乙氧基-1-苯并呋喃-2- 基)取代的查尔酮衍生物,其反应式如图9 所示。作者研究发现所合成的查尔酮衍生物对乳腺癌(MCF-7)、非小细胞肺癌(A549)和前列腺癌(PC-3)的细胞株有生长抑制作用。
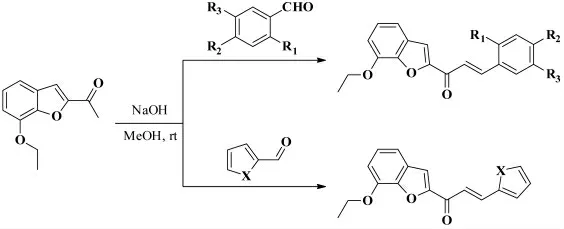
图9 1-(7-乙氧基-2-苯并呋喃基)乙酮和芳醛的Claisen-Schmidt缩合反应Fig.9 The Claisen-Schmidt condensation reaction of 1-(7-ethoxybenzofuran-2-yl)ethanone with aromatic aldehydes
2017年,Salinas-Ortega 等[18]报道了对乙炔基苯甲醛和邻羟基苯乙酮在KOH 作为碱、EtOH 作为溶剂的条件下经Claisen-Schmidt 缩合反应得到(E)-3- (4- 乙炔基苯基)-1- (2- 羟基苯基)-2- 丙烯-1- 酮,其反应式如图10 所示。

图10 对乙炔基苯甲醛和邻羟基苯乙酮的Claisen-Schmidt 缩合反应Fig.10 The Claisen-Schmidt condensation reaction of 4-ethynylbenzaldehyde with 2-hydroxyacetophenone
2017年,Syahri 等[19]报道了一类具有抗疟活性的查尔酮衍生物的合成,是由取代苯乙酮和取代苯甲醛在60% NaOH 作为碱、EtOH 作为溶剂的条件下室温搅拌过夜生成一系列查尔酮衍生物,其反应式如图11 所示。
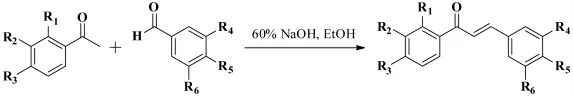
图11 取代苯乙酮和取代苯甲醛的Claisen-Schmidt 缩合反应Fig.11 The Claisen-Schmidt condensation reaction of substituted acetophenones with substituted benzaldehydes
2018年,Hamama 等[20]报道了2- 硫代吗啉基喹啉-3- 乙醛和取代苯乙酮在无水K2CO3作为碱、EtOH 作为溶剂、室温下微波促进的条件下经Claisen-Schmidt 缩合反应合成(E)-1- 芳基-3-(2-硫代吗啉喹啉-3- 基)-2- 丙烯-1- 酮衍生物,其反应式如图12 所示。

图12 2-硫代吗啉基喹啉-3-乙醛和取代苯乙酮的Claisen-Schmidt缩合反应Fig.12 The Claisen-Schmidt condensation reaction of 2-thiomorpholinoquinoline-3-acetaldehyde with substituted acetophenones
2018年,Javed 等[21]报道了一种高效、绿色的吡啶(哌啶)类离子液体的合成,并以此作为催化剂对Claisen-Schmidt 缩合反应进行研究。取代苯乙酮和丙酮在K2CO3作为碱、吡啶(哌啶)类离子液体催化条件下发生Claisen-Schmidt 缩合反应以高达98%的收率生成具有对称结构的取代(1E,4E)-1,5- 二苯基-1,4- 戊二烯-3- 酮衍生物,其反应式如图13所示。

图13 取代苯乙酮和丙酮的Claisen-Schmidt 缩合反应Fig.13 The Claisen-Schmidt condensation reaction of substituted acetophenones with acetone
2019年,Zhang 等[22]报道了以(E)-4- 苯基-3-丁烯-2- 酮为底物和苯甲醛在Ca(OH)2作为碱的条件下经Claisen-Schmidt 缩合反应得到具有对称结构的(1E,4E)-1,5- 二苯基-1,4- 戊二烯-3- 酮,其反应式如图14 所示。该反应的优点在于选用廉价温和的氢氧化钙作为碱、选用绿色安全的乙醇水溶液作为溶剂和分离提纯操作简便。
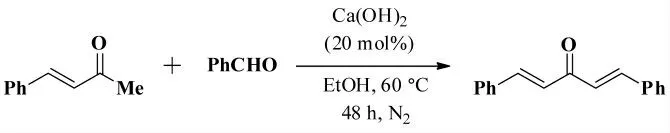
图14 (E)-4-苯基-3-丁烯-2-酮和苯甲醛的Claisen-Schmidt 缩合反应Fig.14 The Claisen-Schmidt condensation reaction of(E)-4-phenyl-3-butene-2-one with benzaldehyde
作者对Ca(OH)2的浓度和反应温度进行优化,发现当Ca(OH)2的量为(E)-4- 苯基-3- 丁烯-2-酮的10%、温度为80℃时,目标产物的收率最高。在此条件下,作者还进行了以(E)-4- 苯基-3- 丁烯-2- 酮为底物和多种取代醛进行放大反应,以较好的收率得到目标产物。
2019年,杨争等[23]报道了以卤代苯甲醛和取代苯乙酮为原料在KOH 作为碱、EtOH 作为溶剂、微波促进条件下经Claisen-Schmidt 缩合反应合成了一系列卤代查尔酮衍生物,其反应式如图15 所示。作者还采用MTT 法研究了化合物对人子宫颈癌细胞(SiHa 和HeLa)的抑制活性,发现化合物对人子宫颈癌细胞株均有一定的抑制作用。

图15 卤代苯甲醛和取代苯乙酮的Claisen-Schmidt 缩合反应Fig.15 The Claisen-Schmidt condensation reaction of halobenzaldehyde with substituted acetophenones
2019年,Burmaoglu 等[24]报道了采用Claisen-Schmidt 缩合反应合成了8 个具有对称结构的双查尔酮衍生物,并对其抗MCF-7、Caco-2 肿瘤细胞和抑制黄嘌呤氧化酶的能力进行了评估。其中室温下1,1’-(2- 羟基-4,6- 二甲氧基-1,3- 苯撑)二乙醇和2,5- 二氟苯甲醛在KOH 作为碱、MeOH 作为溶剂的条件下经Claisen-Schmidt 缩合反应生成的目标产物对MCF-7 的IC50值为1.9μM,其抑制黄嘌呤氧化酶的能力大约是别嘌呤醇的7 倍,其反应式如图16 所示。
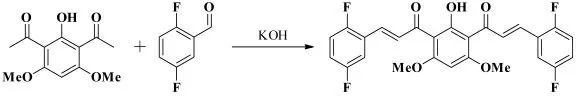
图16 1,1’-(2-羟基-4,6-二甲氧基-1,3-苯撑)二乙醇和2,5-二氟苯甲醛的Claisen-Schmidt 缩合反应Fig.16 The Claisen-Schmidt condensation reaction of 1,1’-(2-hydroxy-4,6-dimethoxy-1,3-phenylene)di-alcohol with 2,5-difluorobenzaldehyde
2 有机碱促进的Claisen-Schmidt 缩合反应
2016年,Verma 等[25]报道了采用Claisen-Schmidt缩合反应合成含有异恶唑和苯并恶嗪酮环的查尔酮化合物。作者尝试以4-(3- 乙酰基-4,5- 二氢异恶唑-5- 基)-6- 溴-4- 甲基-1H- 苯并[d][1,3]恶嗪-2(4H)- 酮为底物和4- 氟苯甲醛在温度为40℃、MeOH 作为溶剂、NaOH 作为碱的条件下反应,没有得到目标产物。把NaOH 换成KOH、t-BuOH,MeOH换成EtOH、t-BuOH,均没有得到目标产物。选用EtOH 作为溶剂、吡啶作为碱的条件下,以45%的收率得到目标产物。通过一系列实验比较,作者发现在乙醇作为溶剂、2 倍量的哌啶作为碱的条件下回流反应6h,以85%的收率得到目标产物。
作者还尝试微波促进反应,通过一系列实验对反应条件的优化,发现在微波条件下80℃时反应经15min,就以92%的收率得到目标产物。
在微波促进、温度为80℃、EtOH 作为溶剂、哌啶作为碱的条件下,以4-(3- 乙酰基-4,5- 二氢异恶唑-5- 基)-6- 溴-4- 甲基-1H- 苯并[d][1,3]恶嗪-2(4H)- 酮或4- ((3- 乙酰基-4,5- 二氢异恶唑-5- 基)甲基)-6- 溴-4- 甲基-1H- 苯并[d][1,3]恶嗪-2(4H)- 酮为底物,和多种芳醛经Claisen-Schmidt缩合反应得到(E)-6- 溴-4-(3- 肉桂酰基-4,5- 二氢异恶唑-5- 基)-4- 甲基-1H- 苯并[d][1,3]恶嗪-2(4H)- 酮或(E)-6- 溴-4-((3- 肉桂酰基-4,5- 二氢异恶唑-5- 基)甲基)-4- 甲基-1H- 苯并[d][1,3]恶嗪-2(4H)- 酮衍生物,其反应式如图17 所示。

图17 4-(3-乙酰基-4,5-二氢异恶唑-5-基)-6-溴-4-甲基-1H-苯并[d][1,3]恶嗪-2(4H)-酮衍生物和芳醛的Claisen-Schmidt 缩合反应Fig.17 The Claisen-Schmidt condensation reaction of 4-(3-acetyl-4,5-dihydroisoxazol-5-yl)-6-bromo-4-methyl-1H-benzo[d][1,3]oxazine-2(4H)-one with aromatic aldehydes
2016年,我们课题组[26]报道了7- 乙基-2- 吲哚酮和苯甲醛及取代苯甲醛在回流的EtOH 作为溶剂、哌啶作为碱的条件下进行Claisen-Schmidt 缩合反应,以较好的收率得到(Z)-3- 亚苄基-7- 乙基吲哚-2- 酮衍生物,其反应式如图18 所示。我们还尝试了选用EtONa、K2CO3、KOH 等碱,但收率都低于哌啶。
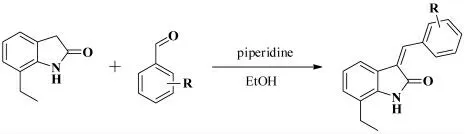
图18 7-乙基-2-吲哚酮和芳醛的Claisen-Schmidt缩合反应Fig.18 The Claisen-Schmidt condensation reaction of 7-ethyl-2-indolin with aromatic aldehydes
3 酸促进的Claisen-Schmidt 缩合反应
2013年,Li 等[27]报道了一种高性能的酸性催化剂的制备及其催化的Claisen-Schmidt 缩合反应。140℃下,在石墨烯酸(GA)作为催化剂、电磁搅拌条件下,苯甲醛和苯乙酮发生Claisen-Schmidt 缩合反应生成(E)- 查尔酮,其反应式如图19 所示。作者通过实验发现当GA 的用量为5g 时,其目标化合物的收率最高。
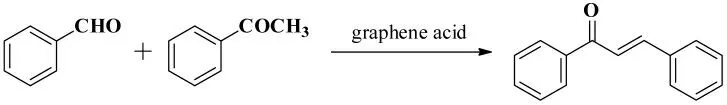
图19 苯甲醛和苯乙酮的Claisen-Schmidt 缩合反应Fig.19 The Claisen-Schmidt condensation reaction of benzaldehyde with acetophenone
4 金属氧化物促进的Claisen-Schmidt缩合反应
2013年,Pal 等[28]报道了邻羟基苯乙酮和苯甲醛经Claisen-Schmidt 缩合反应生成了(E)-1-(2- 羟基苯基)-3- 苯基-2- 丙烯-1- 酮,其反应式如图20 所示。该反应选用碱性的Cs-MgO 作为催化剂、DMF 作为溶剂,明显提高了目标产物的收率。

图20 邻羟基苯乙酮和苯甲醛的Claisen-Schmidt 缩合反应Fig.20 The Claisen-Schmidt condensation reaction of 1-(2-hydroxyphenyl)ethanone with benzaldehyde
2014年,Yadav 等[29]报道了一个以Al2O3/CaO作为催化剂的Claisen-Schmidt 缩合反应,其反应式如图21 所示。在15%(w/w)Al2O3/CaO 的催化下呋喃-2- 甲醛和苯乙酮反应生成(E)-3- (呋喃-2-基)-1- 苯基-2- 丙烯-1- 酮,此催化剂性质稳定、可重复使用。

图21 呋喃-2-甲醛和苯乙酮的Claisen-Schmidt 缩合反应Fig.21 The Claisen-Schmidt condensation reaction of furan-2-carbaldehyde with acetophenone
微波促进的无溶剂绿色合成在有机合成领域受到了合成工作者的广泛关注[30,31]。
2015年,Tamuly 等[32]报道了取代苯甲醛和苯乙酮在纳米氧化锌作为催化剂、无溶剂、微波促进的条件下经Claisen-Schmidt 缩合反应以88%~98%的收率得到取代(E)- 查尔酮衍生物,其反应式如图22 所示。该反应的优点是反应时间短、目标产物的收率高。
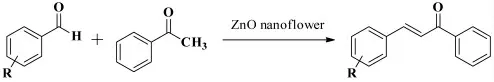
图22 取代苯甲醛和苯乙酮的Claisen-Schmidt 缩合反应Fig.22 Claisen-Schmidt condensation reaction of substituted benzaldehyde with acetophenone
2015年,Climent 等[33]报道了90℃下邻硝基苯乙酮和苯甲醛在MgO-Pt/TiO2作为催化剂、二甲苯作为溶剂的条件下经Claisen-Schmidt 缩合反应2h以98%的收率得到(E)-1-(2- 硝基苯基)-3- 苯基-2- 丙烯-1- 酮,其反应式如图23 所示。
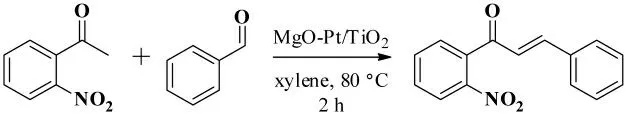
图23 邻硝基苯乙酮和苯甲醛的Claisen-Schmidt 缩合反应Fig.23 The Claisen-Schmidt condensation reaction of 1-(2-nitrophenyl)ethanone with benzaldehyde
2017年,Li 等[34]报道了取代苯甲醛和取代苯乙酮在一种绿色的石墨烯负载氧化锌纳米粒子(ZnO/RGO) 作为催化剂、微波促进的条件下经Claisen-Schmidt 缩合反应合成查尔酮衍生物,其反应式如图24 所示。
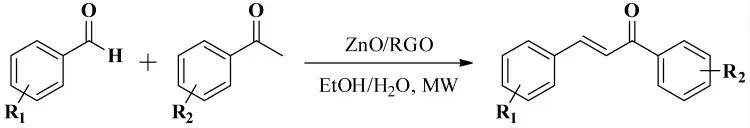
图24 取代苯甲醛和取代苯乙酮的Claisen-Schmidt 缩合反应Fig.24 The Claisen-Schmidt condensation reaction of substituted benzaldehydes with substituted acetophenone
2018年,Jadhav 等[35]报道了不同MgO 纳米结构在不同离子液体中的碱度变化对Claisen-Schmidt缩合反应的影响。通过对反应温度、催化剂用量、溶剂种类、反应时间等条件的优化,确定了最佳反应条件。苯甲醛和苯乙酮经Claisen-Schmidt 缩合反应以95%的收率得到(E)- 查尔酮,其反应式如图25所示。
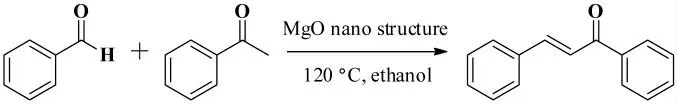
图25 苯甲醛和苯乙酮的Claisen-Schmidt 缩合反应Fig.25 The Claisen-Schmidt condensation reaction of benzaldehyde with acetophenone
5 复合材料促进的Claisen-Schmidt缩合反应
2014年,Kakati 等[36]报道了黄当归醇J 的全合成路线,其中关键的一步Claisen-Schmidt 缩合反应采用新的绿色方法实现。取代的苯乙酮和对羟基苯甲醛在KHSO4-SiO2作为可回收催化剂、聚乙二醇(PEG)作为溶剂、微波促进的条件下经Claisen-Schmidt缩合反应得到目标产物,其反应式如图26 所示。

图26 中间化合物的合成路线Fig.26 The synthetic route of intermediate compound via Claisen-Schmidt condensation reaction
2015年,Wu 等[37]报道了一种多孔网状金属-有机骨架材料(IRMOF-3)催化Claisen-Schmidt 缩合反应,苯甲醛和苯乙酮在IRMOF-3 作为催化剂、DMSO 作为溶剂的环境友好条件下反应生成(E)-查尔酮,其反应式如图27 所示。通过对温度、催化剂用量和溶剂等对目标产物收率的影响发现,IRMOF-3 具有较高的催化活性。

图27 苯甲醛和苯乙酮的Claisen-Schmidt 缩合反应Fig.27 The Claisen-Schmidt condensation reaction of benzaldehyde with acetophenone
2016年,Winter 等[38]报道了苯乙酮和对硝基苯甲醛在活性炭作为催化剂、常压、室温的条件下经Claisen-Schmidt 缩合反应生成(E)-3- (4- 硝基苯基)-1- 苯基-2- 丙烯-1- 酮,其反应式如图28 所示。
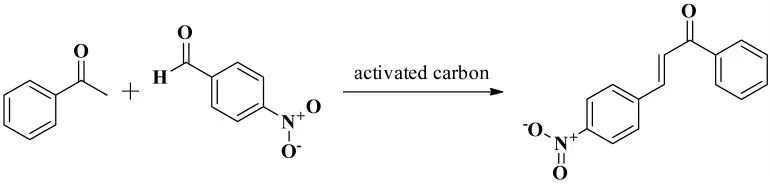
图28 苯乙酮和对硝基苯甲醛的Claisen-Schmidt 缩合反应Fig.28 The Claisen-Schmidt condensation reaction of acetophenone with p-nitrobenzaldehyde
2017年,Siddiqui 等[39]报道了一种新型高效的铜掺杂二氧化硅负载磷钨酸(CuPTA/SiO2)催化剂参与的Claisen-Schmidt 缩合反应,其反应式如图29所示。80℃下以3- 甲基-5-(2- 硝基苯氧甲基)-1-苯基-1H- 吡唑-4- 乙醛为底物和1,3- 二甲基-2,4,6- 嘧啶三酮在CuPTA/SiO2作为催化剂、无溶剂的条件下反应10min 以94%的收率得到1,3- 二甲基-5- ((3- 甲基-5- (2- 硝基苯氧甲基)-1- 苯基-1H- 吡唑-4- 基)亚甲基)嘧啶-2,4,6(1H,3H,5H)- 三酮。作者尝试选用甲醇、乙醇、异丙醇、聚乙二醇、乙酸乙酯等作为溶剂进行反应,发现其目标产物的收率均低于70%,且反应时间比无溶剂时的反应时间长。
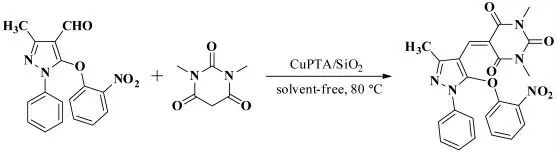
图29 3-甲基-5-(2-硝基苯氧甲基)-1-苯基-1H-吡唑-4-乙醛和1,3-二甲基-2,4,6-嘧啶三酮的Claisen-Schmidt 缩合反应Fig.29 The Claisen-Schmidt condensation reaction of 3-methyl-5-(2-nitrophenoxy)-1-phenyl-1H-pyrazole-4-acetaldehyde with 1,3-dimethyl-2,4,6-pyrimidinetrione
2017年,Murugesan 等[40]报道了一种乙基哌嗪基喹啉基查尔酮衍生物的合成路线,2- (4- 乙基哌嗪-1- 基)喹啉-3- 甲醛和取代苯乙酮在新型钛纳米材料结合N- 丙基三亚乙基四胺磺酸(TiO2-BPTETSA)作为催化剂、无溶剂的条件下经Claisen-Schmidt 缩合反应得到(E)-3-(2-(4- 乙基哌嗪-1- 基)喹啉-3- 基)-1- 苯基-2- 丙烯-1-酮衍生物,其反应式如图30 所示。该反应具有目标产物收率高、操作简便、反应时间短等优点。

图30 2-(4-乙基哌嗪-1-基)喹啉-3-甲醛和取代苯乙酮的Claisen-Schmidt 缩合反应Fig.30 The Claisen-Schmidt condensation reaction of 2-(4-ethylpiperazin-1-yl)quinoline-3-carbaldehyde with substituted acetophenones
2018年,Wagh 等[41]报道了一种绿色合成α-甲基肉桂醛的方法,即苯甲醛和丙醛在温度为443K、20%(w/w)Mg-Zr/HMS(镁- 锆/ 六方相介孔二氧化硅)作为催化剂、甲苯作为溶剂的条件下经Claisen-Schmidt 缩合反应得到α- 甲基肉桂醛,其反应式如图31 所示。
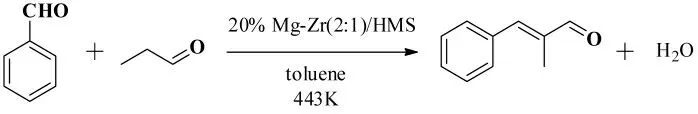
图31 苯甲醛和丙醛的Claisen-Schmidt 缩合反应Fig.31 The Claisen-Schmidt condensation reaction of benzaldehyde with propionaldehyde
6 结论与展望
Claisen-Schmidt 缩合反应是合成查尔酮类化合物的重要方法之一,其在有机合成、药学、农业等领域有广泛的应用。该反应具有操作简便、反应条件温和、收率高等特点。本文总结了近几年报道的关于无机碱、有机碱、酸、金属氧化物以及复合材料促进的Claisen-Schmidt 缩合反应在合成查尔酮类化合物中的应用。相信在不久的将来,Claisen-Schmidt缩合反应会合成出越来越多具有较高活性的查尔酮类化合物,为以后进一步研究Claisen-Schmidt 缩合反应提供参考和帮助。
