印制板化学镀镍阶梯镀层问题研究
2020-04-18陈光辉李小兵赖海祥黎小芳
陈光辉 李小兵 赖海祥 黎小芳
(广东东硕科技有限公司,广东 广州 510288)
1 引言
印制电路板(PCB)化学镍/金(ENIG,Electroless Nickel and Immersion Gold)是一种在铜面线路图形上进行化学镀镍,然后化学浸金的表面涂覆工艺。化镍/金镀层在焊接、散热、接触导通、平整性[1]等方面的表现优异,还具有可打线接合,可耐多次回流焊接等特点,因此被广泛应用。
目前化学镀Ni-P 合金有四种沉积机理,分别为原子氢、氢化物传输机理、电化学理论及羟基镍离子配位理论[2]-[5],其中以原子氢理论被认可程度最高。原子氢机理首先由A.Brenner和G.E.Riddel[6]提出,后来Gutzeitl[7]也支持该机理。原子氢机理认为化学镀镍过程主要包括如下几个反应步骤:

PCB化学镀镍/金除了工艺比较复杂之外,也容易受到人员操作、设备条件、板件状况、车间环境等多种因素的影响,故经常出现各种品质问题,如金面色差、漏镀、渗镀、镀层剥离等等[8]。其中镀层边缘阶梯镀层(step plating,edge pull back),也是比较常见的一种外观不良,且会影响镀层的性能,目前有薄镀、贫镀、肩薄、毛边等多种不同的名称。典型的阶段状镀层如图1所示。阶梯镀层一般容易发生在光学点(mark)、BGA(Ball Grid Array)、孔边、小焊盘(Pad)边缘等位置。本文将从化学镍槽镀液、镍槽过滤循环强度等方面进行研究(见图1)。
2 实验部分
2.1 化学镀镍工艺
2.1.1 工艺流程
实验测试流程:除油→热水洗→双水洗→微蚀→双水洗→酸洗→双水洗→预浸→活化→双水洗→后浸→双水洗→化镍→双水洗→吹干
2.1.2 基础配方及参数
实验化学镀镍液以硫酸镍为主盐,次磷酸钠为还原剂,络合剂主要为乳酸等有机酸,金属铅离子作为稳定剂见表1。实验使用恒温水浴锅DF-101S(巩义市予华仪器有限公司),磁力搅拌转子C20,配制1升烧杯药液。以循环伏安极谱仪Metrohm797VA(瑞士万通)分析铅离子。以BX51型金相显微镜(奥林巴斯),JEOL JSM-6510LV型扫描电子显微镜(日本电子)观察镀层状况,OXFORD X-MAX 250能谱仪进行元素分析。测试板BGA直径0.55 mm,方形焊盘1.5 mm×1.5 mm(见表1)。
2.2 实验方案
2.2.1 化学镀镍液的影响
化学镀镍槽如果不添加稳定剂,槽液就易有金属镍析出并分解,实验无法正常进行。实验过程中我们将Pb2+浓度从0.3×10-6开始,并逐步提高至10×10-6,实验过程中并未开启磁力搅拌,镍槽温度80 ℃,pH值4.4,测试负载0.3 dm2/L,观察实验测试板BGA边缘镀层状况。在出现阶梯镀层条件下调整镍槽温度、pH值、负载,比较调整前后镀层边缘的变化,因此还将测试镍槽促进剂,在出现阶梯镀层的镀液中添加一定量的含S促进剂,评估其对此问题的影响。
2.2.2 镍槽过滤强度影响模拟
为了模拟镍槽循环流量的强度,使用带磁力搅拌的恒温水浴锅DF-101S,通过改变磁力搅拌速度来调整药水的流动性。DF-101S最高转速为2600 rpm,调整刻度分区间为0-60(0表示无搅拌,60为转速最快挡),实验过程用10、30、50三挡,转速从低至高。镍槽温度80 ℃,pH值4.4,负载0.3 dm2/L。实验分为两组,第一组稳定剂Pb2+0.3×10-6,第二组稳定剂Pb2+0.9×10-6。

图1 阶梯镀层(a)BGA边缘轻微台阶,(b)BGA边缘切片,(c)镀层边缘斜坡

表1 化学镀镍槽组成
3 结果与讨论
3.1 化学镀镍液的影响
3.1.1 稳定剂Pb2+的影响
在化学镀镍过程中,除了在催化底材上正常的镍沉积反应外,X.Yin等[9]认为反应溶液会不可避免地产生胶体尺寸级别的镍固体颗粒,这些胶体尺寸级别的固体颗粒是不受控制的。因为镍的自催化性,这些颗粒变为活化中心,镍容易在其表面沉积,导致镀液不稳定,甚至发生急剧反应而分解。为了维持化学镀镍溶液的稳定性,常在其中加入稳定剂,毒化活性中心,从而达到稳定镀液的作用,而Pb2+是最为常用的一种稳定剂,以下重点对此进行研究。
实验观察发现,在1.1×10-6以下时,镀层边缘没有阶梯镀层出现;在1.3×10-6时轻微的阶梯镀层,如图2(d);在1.7×10-6时阶梯镀层比较明显,如图2(e);随着Pb2+浓度提高至2×10-6、6×10-6、10×10-6,阶梯镀层越来越严重,甚至边缘出现漏镀(skip plating),如图2中(f)、(g)、(h)。在高浓度组别中测试片上的BGA焊盘(Ball Grid Array),除了边缘部分未沉积上镍层,中间部分的镀层也开始出现点状漏镀,说明随着镍槽Pb2+浓度的提高,其影响从镀层边缘逐渐向中间区域扩展(见图3)。
3.1.1.1 稳定剂Pb2+传统扩散模型
稳定剂Pb2+的添加实验可以明确说明阶梯镀层受到化学镀镍液中Pb2+的影响,而其根源在于Pb2+的扩散模式。Van der Putten and de Backer[10][11],S.Zhang等[12]研究提出,化学镀镍过程中稳定剂Pb2+存在两种扩散模式:线性扩散(linear diffusion)与非线性扩散(nonlinear diffusion),扩散模式不同会影响微小焊盘镀层厚度,甚至会导致孤立小焊盘漏镀(见图4)。
根据Van der Putten and de Backer[10][11],S.Zhang等[12]人的观点,当孤立微小焊盘尺寸小于100 μm(一般扩散层厚度大约为100 μm)时,稳定剂Pb2+的非线性扩散行为不能被忽略。对于临近位置有大的裸露底材,或者孤立微小焊盘临近位置有一组一定数量、类似大小的焊盘,可以认为稳定剂表现为线性扩散模式,在尺寸较大的焊盘上也被认为线性扩散。如图4(a)、(b)所示,在非线性扩散区域,稳定剂吸附密度高,在线性扩散区域稳定剂吸附密度较低,如图4(c)、(d)、(e)所示。在稳定剂的非线性扩散区域,吸附较多的稳定剂,因此镍的沉积会受到抑制,如图4中(c)、(d)、(e)。

图2 镀层边缘阶梯镀层(化学镀镍槽不同Pb2+浓度)

图3 化学镀镍槽Pb2+浓度6×10-6 BGA图片

图4 微小焊盘稳定剂扩散模式
S.Zhang等[12]提出在化学镀镍沉积中由两个竞争过程所形成的反应路线:稳定剂Pb2+的扩散与稳定剂在镍沉积过程的掩埋(与镍共沉积)。稳定剂Pb2+扩散速率决定于扩散机理,其掩埋速率正比于镍的沉积速率。如果Rd表示稳定剂的扩散速率,Rb表示稳定剂的掩埋速率,则当Rd>Rb即会出现漏镀,而当Rd<Rb镍会正常沉积,而Rd=Rb是一种不稳定的平衡,很难维持,因此在Pb2+吸附较多区域镍的沉积反应会受到抑制(见图4)。
3.1.1.2 稳定剂Pb2+扩散模型修正
在实验中我们研究发现,即使较大的焊盘,比如BGA盘直径0.55 mm,或者焊盘1.5 mm×1.5mm,远大于0.10 mm直径级别,当镀液中稳定剂Pb2+含量提高到一定值时,也会出现边缘阶梯镀层,结果表明在较大尺寸的焊盘上,边缘区域和中间区域Pb2+的吸附量也存在一定差异,即焊盘边缘区域相比中间区域Pb2+的扩散速率Rd更快。因此对于图4中的扩散模型,做了一些修正,如图5所示。我们认为化学镀镍过程中,所有的焊盘在其边缘位置均存在一定的非线性扩散,Pb2+在边缘扩散速度较中间区域更快一些,但是在孤立的小焊盘上非线性扩散的密度更高,所以孤立的小焊盘更容易出现阶梯镀层,甚至漏镀。对于较大的焊盘,即使边缘区域存在Pb2+的非线性扩散,吸附的Pb2+相对要多,但是由于整个焊盘在占更大面积的区域为线性扩散,吸附的Pb2+并不多,能够正常进行反应。次磷酸根氧化产生还原氢,释放电子,会通过催化底材传输到边缘位置(Potential Pinning:两个或更多导电区域相连接时,它们具有相同的电势[12]),因此在Rb(稳定剂Pb2+掩埋速率)与Rd(稳定剂Pb2+扩散速率)的竞争中,Rb可能更具有优势,焊盘边缘不容易出现阶梯镀层(见图5)。

图5 稳定剂扩散模型(修正)
S.Zhang等[12]与M.Fleischmann等[13]研究提出,溶液中稳定剂浓度与扩散通量成正比。当不断提高化学镍镀液中稳定剂浓度使其到达某个极限浓度时,不管是焊盘边缘还是中间区域,其稳定剂的吸附量均会上升,而焊盘边缘部分因非线性扩散的原因,其吸附的稳定剂量更多,覆盖密度更高。大量的Pb2+与镍共沉积后会降低镀层界面的还原电位,抑制新生镀层的催化活性[9],此时焊盘中间区域和边缘区域的反应活性均出现下降,焊盘边缘先出现阶梯镀层,如继续提高稳定剂Pb2+的浓度,阶梯镀层会逐渐向中间区域扩散,并且中间区域出现点状的漏镀现象。
从以上分析可知,改善阶梯镀层比较明显的措施是降低稳定剂Pb2+的浓度,实验中尝试将镀液Pb2+1.3×10-6通过拖缸(大负载铜板生产)消耗,使其降低至0.8×10-6,再制作测试板,如图6(c),镀层未观察到阶梯镀层)。
3.1.2 化学镀镍液参数的影响
化学镀镍液中稳定剂Pb2+的极限浓度(即到达某个浓度会出现阶梯镀层、漏镀),是我们比较关注的。Pb2+的极限浓度会受反应参数影响,如温度、pH值、负载(单位体积药水承载的受镀面积)[9],较高的温度、pH值、负载能够容忍较高的稳定剂Pb2+极限浓度。在出现严重阶梯镀层的实验组Pb2+6×10-6中,如图2(g),将镀液温度由80℃提高到82 ℃,pH值4.4提高至4.7,负载0.3 dm2/L提高至0.8 dm2/L,三个参数均向上调整,然后可观察到阶梯镀层得到一定程度的改善,如图6(a)。阶梯镀层之所以能变得轻微,是因为提升化学镀镍的反应活性,反应更加剧烈,溶液中胶体尺寸级别的镍固体颗粒增多[9],这些活性颗粒因表面较大,能吸附并消耗反应界面附近的稳定剂Pb2+,从而降低Pb2+在镀层表面的吸附量(见图6)。
3.1.3 化学镀镍液促进剂的影响
有研究文献[14]提出,在化学镀镍过程中硫脲还有促进镍晶粒生长的作用,日本的黑坂成吾、佐藤诚等业内专家[15]也提到含S添加剂可以改善肩薄问题。因此,在实验组Pb2+10×10-6中,如果我们添加一定量的含S促进剂(20 ml/L),阶梯镀层改善更为明显,如图6(b)。我们推测,含硫的促进剂可能与硫脲有类似促进镍生长的作用,并与Pb2+抑制镍生长出现竞争,从而让阶梯镀层获得改善。
3.2 化学镀镍槽中过滤循环强度的影响
由于测试条件有限,我们实验以搅拌来模拟化学镀镍槽的过滤循环。模拟实验中可以发现,Pb2+0.3×10-6搅拌挡位逐步提高,挡位1030并未出现阶梯镀层,当挡位设置为50时,开始出现阶梯镀层,见图7(c)。当Pb2+0.9×10-6时,在低挡位10即可观察到明显的阶梯镀层,见图7(d);而到50挡位时,出现严重的边缘漏镀,见图7(f)。结果表明化学镀镍液中的搅拌速率变快,将加速稳定剂Pb2+向反应界面的扩散,并吸附在催化表面上,抑制镍的沉积。
仔细对比高稳定剂浓度和高速搅拌条件两者的阶梯镀层情况,可以我们发现BGA侧面有明显区别。高稳定剂Pb2+浓度达到10×10-6时,未搅拌,BGA侧面未观察到明显的镍沉积层,进行线性元素扫描,显示靠近油墨边缘有较厚的镍层存在,然后急剧变薄,如图8(a);而Pb2+浓度达到0.9×10-6,搅拌挡位50,仔细观察有镍的瘤状沉积结构见图8(b),元素扫描显示侧面镍层很厚,接近焊盘中心区域镍层偏厚。图8(c)中将测试板用氢氧化钠褪除阻焊油墨层,镀液Pb2+浓度0.9×10-6,搅拌挡位50,结果显示侧面的镍层厚度明显降低,比图8(b)薄不少,导致此差异是由于镀液中Pb2+的浓度与药水的流速均直接影响其扩散速率。BGA侧面基材存在油墨覆盖层,油墨的厚度与镀层总厚度(铜层与镍层)基本相同,因此在强搅拌过程中BGA侧面药水流速相比焊盘边缘更小,在褪除油墨后,焊盘侧面完全裸露,更易受到镀液Pb2+扩散的影响。Sam Siau等[16]研究提出微小焊盘旁覆盖的油墨厚度越厚,稳定剂Pb2+的扩散速率越慢,反之扩散速率变快。结合以上实验,说明油墨厚度对于较大的焊盘的边缘也有一定的影响(见图8)。

图6 阶梯镀层改善

图7 不同搅拌档的阶梯镀层
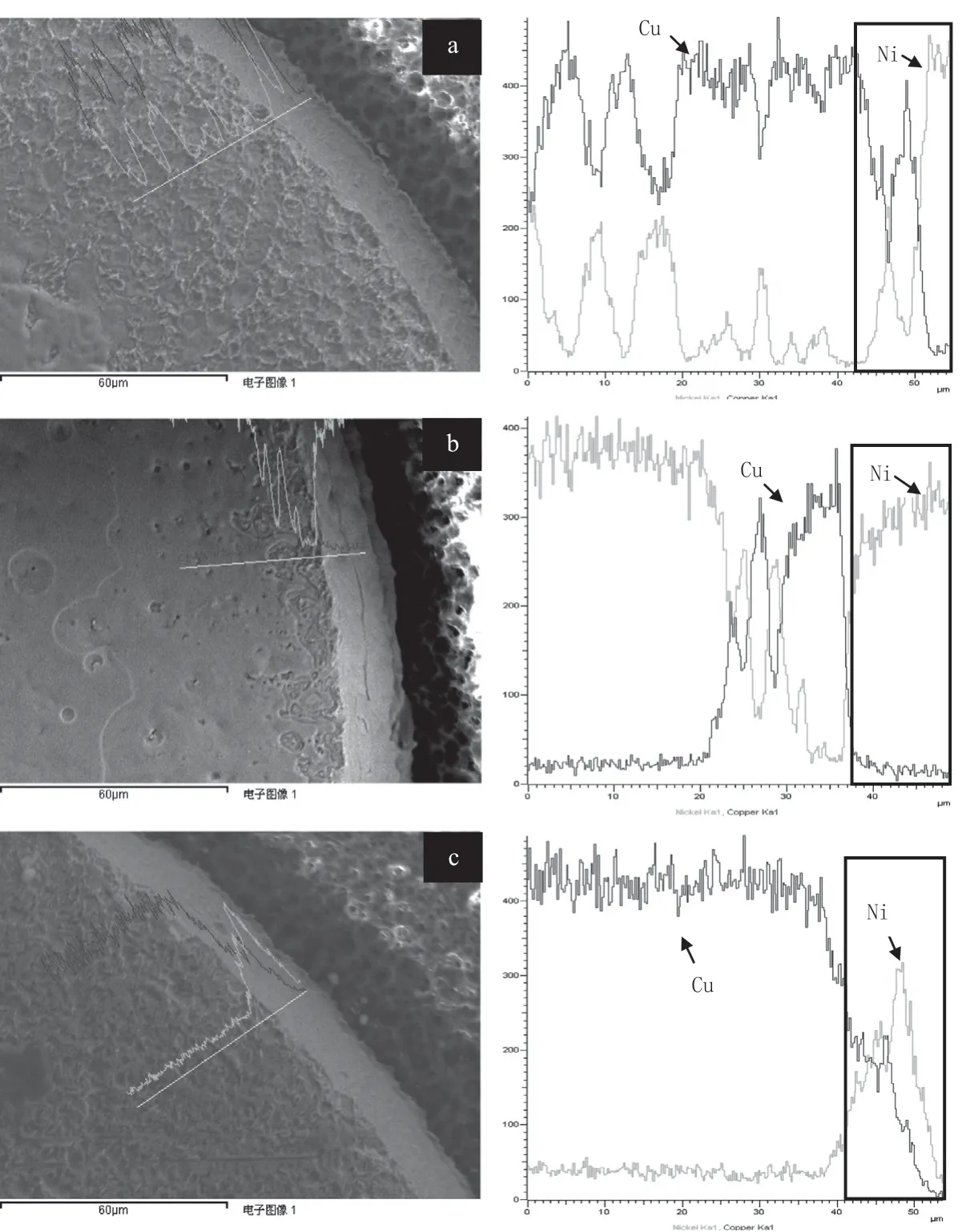
图8 焊盘边缘元素扫描:(a)Pb2+浓度10×10-6,无搅拌;(b)Pb2+浓度0.9×106,搅拌挡位50;(c)褪除阻焊油墨后,Pb2+浓度0.9×10-6,搅拌挡位50
C.Gabrielli,F.Raulin[17]研究表明,化学镀镍槽搅拌速率在较低的范围内(<1000 rpm)可以提高镍的沉速,在1000 rpm时沉速最快,当到达2000 rpm后镍的沉速略为降低趋于稳定。依据此结论,可以推测镍槽搅拌速率对阶梯镀层的影响主要是体现改变稳定剂Pb2+的扩散速率,而非镍的沉积速率。
实验室研究表明化学镀镍液流速过快将容易导致阶梯镀层出现,因此生产过程控制好镍槽的循环量也相当重要。目前多数用于PCB的化学镀镍药水,其要求槽体的循环量在4-10TO/h(turn over,即每小时的总流量与实际槽液体积的倍数)。
4 总结
根据以上研究发现,化学镀镍过程的阶梯镀层问题主要是稳定剂浓度偏高,镍槽三大参数(温度、pH值、负载)控制偏低所致,另外镍槽药水的流动速度太快(过滤循环强度太大)也有一定影响。本文重点研究了稳定剂Pb2+在化学镀镍过程中的扩散模型,所有的焊盘边缘部分均存在非线性吸附,且在一定条件下会导致阶梯镀层出现。另外根据吕小伟[18]、孟凡义[19]等人的研究,二次干膜、油墨等成分会影响化学镀镍层的沉积,因此待镀板件表面上残留这些有机成分也可能导致产生阶梯镀层。
在实际PCB化学镀镍生产操作中,出现阶梯镀层常见的原因是化学镀镍体系稳定剂含量偏高,而镍槽活性控制太低。化学镀镍槽的温度、pH值、负载有严格管控范围,促进剂添加过多则影响镀层其他诸如磷含量、镍腐蚀等问题,稳定剂Pb2+的调整更加复杂,所以当出现阶梯镀层问题时,建议由专业技术人员进行调整。
