Fe-Beta分子筛类Fenton降解罗丹明B染料废水
2020-04-12司慧萍张思权
司慧萍,张思权,朱 浩,沈 峥
(1. 同济大学新农村发展研究院,上海200092;2. 中国农村技术开发中心,北京100045)
Fenton法是染料废水降解工艺中应用最广泛的一种高级氧化技术(AOPs)。由于体系中Fe2+和H2O2能在酸性条件下生成具有强氧化性的羟基自由基(·OH),因此可以有效降解染料废水中成分复杂的有机污染物[1-2]。传统Fenton法受限于狭窄的pH值范围,需要消耗大量H2O2以产生·OH,由此生成的大量含铁污泥可能产生二次污染[3]。研究表明,利用固体催化剂代替Fe2+/Fe3+催化H2O2而产生·OH,可以有效解决上述Fenton 法存在的问题,减少设备的腐蚀并实现催化剂的重复利用,因此这种非均相类Fenton技术成为了研究热点[4]。
非均相类Fenton 反应过程中,由于在催化剂的表面存在固-液两相传质,因此选取比表面积大且化学性质稳定的催化剂能显著提高催化效果[5-6]。Beta 分子筛作为一种常见的非均相催化材料,因具有独特的三维十二元环孔道结构,使其具备了酸催化特性及结构选择性。催化裂化催化剂中加入少量Beta 分子筛或改性Beta 分子筛,可以显著提高催化剂的水热稳定性以及抗积炭及耐磨等特性[7-9]。在Beta 分子筛的改性方面,Wolf 等[10]以固态离子交换方式制备Sn-Beta 分子筛,合成时间短,操作简易,随后又通过类似的方法合成了Ti-Beta和Zr-Beta分子筛。孙宝盛[11]通过液相离子交换法和浸渍法制备出Fe-Beta 分子筛,用来催化分解一氧化二氮(N2O)。刘海燕[12]利用过渡金属(Fe、Cu)改性Beta分子筛,使其具有良好的选择性催化还原(SCR)反应活性与抗水热老化性能。朱永军[13]以无模板剂法合成的Beta 分子筛(物质的量之比nSi∶nAl=9)作为载体,通过无水条件下铁改性,构建了具有优异低温NH3-SCR脱硝性能的Fe-Beta-9催化剂。Wu等[14]通过酸预处理使Beta 分子筛微孔孔道扩大,采用液相离子交换法负载金属铁得到Fe-Beta 分子筛,以Fe负载量增加来提高分子筛催化消除N2O的活性。基于以上研究,合成了基于Beta 分子筛载体的Fe2+/Fe3+型催化剂(Fe-Beta),并探讨其在类Fenton体系中对罗丹明B 的催化性能与反应机理,最后用实际染料废水进行了验证。
1 实验部分
1.1 实验试剂及装置
实验使用的过氧化氢(质量分数30%,H2O2)、乙酸亚铁(C4H6FeO4)、罗丹明B(C28H31N2O3Cl)、盐酸(质量分数37%,HCl)、氢氧化钠(NaOH)由上海国药集团化学试剂有限公司提供;Beta 分子筛(nSi∶nAl=25)由南开大学催化剂厂提供;pH 计型号为PHSJ-4A,上海雷磁仪器有限公司生产;紫外可见分光光度计型号为UV2600,上海一恒科学仪器有限公司生产;实验用水为去离子水。
实验染料废水取自河北武强县某染料工厂的废水,水样指标如表1所示。

表1 染料厂废水样品指标Tab.1 Indicators of wastewater samples from dye factories
1.2 实验方法
1.2.1 Fe-Beta分子筛的制备
将Beta分子筛置于盛有浓硝酸的三口圆底烧瓶(1 g Beta分子筛投加浓硝酸20 mL),烧瓶置于80 ℃油浴锅中,以200 r·min-1搅拌速率冷凝回流脱铝20 h。将脱铝后的固液混合物通过高速离心机分离(3 000 r·min-1,20 min),再将用去离子水多次洗涤离心后的固体组分清洗至pH显中性,最后将清洗后的固体在150 ℃下烘干,获得脱铝Beta分子筛(记为deAl-Beta分子筛)[15]。以deAl-Beta分子筛为载体,采用固体离子交换法[10],按Fe 负载量为10%(质量分数)将乙酸亚铁与deAl-Beta分子筛混合后于研钵中研磨30 min,研磨后的样品在管式炉中于550 ℃条件下焙烧6 h后自然冷却至室温,经过300目筛网筛分,制成Fe-Beta分子筛。
1.2.2 Fe-Beta分子筛的表征
采用X 射线衍射仪(XRD)来表征样品晶相结构,辐射源为Cu 靶,仪器扫描速率为2°·min-1,扫描角度为10°~70°。材料样品显微结构采用Philips XL 30 型Philips XL 30 扫描电子显微镜(SEM)表征。催化剂比表面积通过氮气吸附/脱附仪(Micromeritics ASAP 2020)测试。催化剂测试前在300 ℃、氮气流条件下脱气过夜。比表面积通过比表面积计算获得[16]。
1.2.3 Fe-Beta 分子筛在类Fenton 体系中的催化实验
Fe-Beta 分子筛与H2O2可构成非均相的类Fenton体系,通过降解罗丹明B来考察Fe-Beta分子筛的催化降解性能。在70 ℃下,取100 mg·L-1的罗丹明B溶液100 mL于锥形瓶中,用盐酸或氢氧化钠调节初始pH值,加入一定量的H2O2和Fe-Beta分子筛后开始搅拌并计时,在一定时间间隔下取样,用紫外可见分光光度计在波长λ=552 nm下测定溶液的吸光度,直至溶液接近无色,即认为反应结束。所有实验数据均基于3 次实验的平均值,所有实验的相对误差始终小于10%。根据罗丹明B标准曲线来换算浓度c,剩余色素率和脱色率计算式如下所示:

式中:c0为初始浓度;c为反应测得浓度。
1.2.4 实际染料废水降解体系
根据国标法测出原水色度,并将原水分别稀释250、500、1 000倍后取样,然后进行全波长扫描。各取30 mL 原水分别置于50 mL 反应釜中,为减少实验误差,每组设置1 个平行样。考虑到实际染料废水的COD很高,实际罗丹明B浓度远高于模拟废水浓度,为提高反应速率,选择反应温度为200 ℃,反应时间为2 h。加入不同体积的H2O2,考虑铁离子浓度不宜过高,Fe-Beta 分子筛可加80 mg。反应后离心,取上清液,并釆用紫外可见分光光度计对反应溶液进行全波长扫描,扫描波长范围为200 ~800 nm。溶液组分分析采用Finnigan Voyager-EI 70eV 气相色谱(GC)/质谱(MS)联用仪,色谱柱为HP-Wax石英毛细管色谱柱(30 m×0.25 mm×0.25 μm),以氦气为载气,体积流量为1 mL·min-1。
2 结果与讨论
2.1 催化剂的表征
2.1.1 XRD分析
利用XRD 分别对Beta、deAl-Beta、10%负载量Fe-Beta(记10%Fe-Beta)和20%负载量Fe-Beta(记20%Fe-Beta)分子筛进行晶型分析。XRD图谱如图1所示。

图1 XRD图谱Fig.1 XRD spectra
由图1可知,4种Beta分子筛的主峰位置明显且统一,在22.4°左右,可判断为Beta 分子筛的特征衍射峰。该特征衍射峰的出现说明水热老化过程没有破坏样品结构,并且使样品结晶度增强,Beta分子筛具有很好的水热稳定性。负载Fe 之后Beta 分子筛的峰比负载前的峰低,这表明负载Fe的Beta分子筛孔道受到了一定程度的阻塞。图1 中Fe-Beta 分子筛的FeOx峰明显,主要在33.1°和35.9°[17]左右,说明Fe在Beta分子筛中以离子形态存在,或者生成的FeOx弥散分布于分子筛表面,未达到检测限(<3 nm)。比较图1 中10% Fe-Beta 与20% Fe-Beta分子筛的衍射峰,位置基本一致且峰高相近,但随着负载量增加,合成的催化剂颜色加深,表明Fe2O3增多。在负载量比较的预实验中,初始pH 值为3.0,初始罗丹明B 质量浓度为100 mg·L-1,Fe-Beta分子筛投加量为30 mg,H2O2投加量为0.4 mL,反应温度为70 ℃,反应时间为2 h,对Fe负载量在0、5%、10%、15%、20%下罗丹明B溶液脱色率进行了探究。Fe 负载量5%时脱色率为65%,Fe 负载量10%时脱色率达到95%,而10%之后更高的Fe 负载量,实际催化效果增加并不明显,因此综合考虑成本与脱色效果,选择Fe负载量10%进行实验。
2.1.2 SEM分析
SEM图谱如图2所示。负载前后分子筛基本都呈球状颗粒,表面紧密,颗粒与颗粒之间可能为独立结构。负载前的deAl-Beta分子筛包面更光滑,颗粒间更紧凑,说明样品晶化非常完全,并且是单一个体;经过铁离子改性后10%Fe-Beta 分子筛颗粒之间疏松,表面不光滑。

图2 SEM图谱Fig.2 SEM spectra
2.1.3 比表面积分析
为进一步研究催化剂结构,表2 列出了分子筛负载前后的比表面积、孔容和孔径。当催化剂负载Fe 后,比表面积、孔容、孔径均略微下降,表明作为负载物的Fe 离子键合在载体的孔道中。随着Fe 含量的增多,比表面积和孔容减小,这可能是由于Fe的加入阻塞了分子筛的孔道,从而表现出较小的比表面积和孔容。孔径变化不大,这说明Beta 分子筛的孔道结构没有塌陷,保持了原有的催化剂结构。
2.2 催化降解反应影响因素与动力学分析
2.2.1 反应温度对催化效果的影响
伪一级动力学方程如下所示:

式中:k为反应速率常数;t为反应时间;b为常数。
考察反应温度对催化效果的影响。实验条件为:初始pH 值3.0,初始罗丹明B 溶液质量浓度100 mg·L-1,Fe-Beta 分子筛投加量30 mg(其中Fe3+的浓度0.504 mmol·L-1),H2O2投加量0.4 mL,反应温度20、30、50、70、90 ℃。
按照实验方法,分别在5、20、45、60、90、120 min时取样测吸光度,根据罗丹明B 标准曲线算得浓度c。以c/c0为纵坐标作图,如图3a所示。化学反应一般随着温度升高反应速率加快,适当提高反应温度可以提高Fenton 法对罗丹明B 溶液的脱色率。60 min 内脱色率与时间成正相关,70 ℃与90 ℃下反应时间在2 h 时的脱色率达到95%。为了减少能源消耗,最优温度选在70 ℃较合理。

表2 不同Beta分子筛的理化特性Tab.2 Physicochemical properties of different Betazeolites
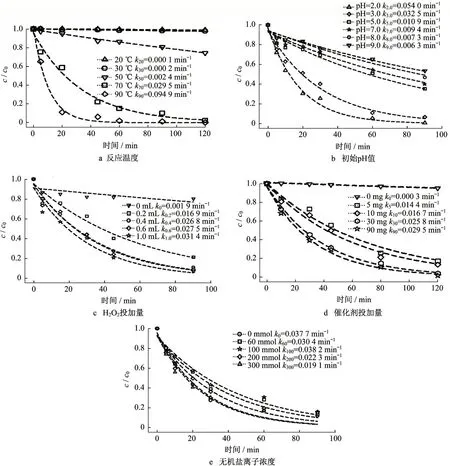
图3 各因素对罗丹明B溶液脱色效果的影响Fig.3 Effect of each factor on decolorization of Rhodamine B solution
2.2.2 初始pH值对催化效果的影响
考察初始pH 值对催化效果的影响。实验条件为:初始罗丹明B 溶液质量浓度100 mg·L-1,Fe-Beta 分子筛投加量30 mg(其中Fe3+的浓度0.504 mmol·L-1),H2O2投加量0.4 mL,反应温度70 ℃,初始pH 值2.0、3.0、5.0、7.0、8.0、9.0。按照实验方法,分别在5、10、20、30、60、90 min取样测吸光度,根据罗丹明B标准曲线算得浓度c。以c/c0为纵坐标作图,如图3b所示。
当pH 值为2.0 时,罗丹明B 溶液的脱色率最高;当pH 值大于3.0 时,随着pH 值的增加,脱色率也明显下降。由Fenton 反应机理可知,Fenton 试剂生成氧化能力很强的·OH时可发生以下反应[18-19]:

c(·OH)与c(OH-)/c(Fe3+)成反比,罗丹明B溶液的pH 值过高将抑制·OH 的生成,而且H2O2在碱性条件下很容易分解,从而导致脱色率降低。适宜的溶液初始pH 值为2.0~6.0,考虑到经济成本,选择pH值3.0作为最优条件。
2.2.3 H2O2投加量对催化效果的影响
考察H2O2投加量对催化效果的影响。实验条件为:初始pH 值3.0,初始罗丹明B 溶液质量浓度100 mg·L-1,Fe-Beta 分子筛投加量30 mg(Fe3+的浓度0.504 mmol·L-1),反应温度70 ℃,H2O2投加量0、0.2、0.4、0.6、1.0 mL。按照实验方法,分别在5、15、30、45、90 min取样测吸光度,根据罗丹明B标准曲线算得浓度c。以c/c0为纵坐标作图,如图3c所示。
在H2O2投加量为0~0.4 mL 时,罗丹明B 溶液的脱色率随着H2O2投加量的增加有所提高,在H2O2投加量为0.6、1.0 mL时脱色率与0.4 mL时脱色率接近。原因可能是由于过多的H2O2与·OH反应,而HO2·比·OH的氧化电势低[20],导致脱色率降低。因此,最优H2O2的投加量选0.4 mL。
2.2.4 催化剂投加量对催化效果的影响
考察Fe-Beta 分子筛投加量对催化效果的影响。实验条件为:初始pH值3.0,初始罗丹明B溶液质量浓度100 mg·L-1,Fe-Beta 分子筛投加量0、5、10、30、90 mg,H2O2投加量0.4 mL,反应温度70 ℃。按照实验方法,分别在10、30、45、80、120 min取样测吸光度,根据罗丹明B 标准曲线算得浓度c。以c/c0为纵坐标作图,如图3d所示。
催化剂越多降解速度越快,相同时间内催化剂投加量越多脱色率越高。在没有催化剂时罗丹明B部分降解,但降解速度较慢,原因可能是在可见光照射条件下H2O2会对少量罗丹明B 氧化降解[21]。当催化剂投加量为30、90 mg 时,与投加量为5、10 mg时相比,反应速度较快,120 min 时脱色率达到95%以上,30 mg 的降解速度接近90 mg 时的降解速度。考虑到成本,催化剂投加量取30 mg。
2.2.5 无机盐离子浓度对催化效果的影响
考察无机盐离子浓度对催化效果的影响。实验条件为:初始pH值3.0,初始罗丹明B溶液质量浓度100 mg·L-1,Fe-Beta 分子筛投加量30 mg(其中Fe3+的浓度0.504 mmol·L-1),H2O2投加量0.4 mL,反应温度70 ℃,无机盐NaCl 投加量0、60、100、200、300 mmol。按照实验方法,分别在5、10、20、30、60、90 min取样测吸光度。根据罗丹明B标准曲线算得浓度c。以c/c0为纵坐标作图,如图3e所示。
当Cl-浓度为0~1.0 mol·L-1时,反应几乎不受影响;当Cl-浓度为2.0 mol·L-1时,反应有一定的影响;随着Cl-浓度增加,反应速率降低。这是因为Cl-在水溶液中反应生成HOCl。HOCl 作为一种强氧化剂,能够氧化降解罗丹明B分子,Cl2和HOCl的生成反应[22]如下所示:

Cl-浓度较高时,Cl-作为控制·OH 扩散的捕捉剂,ClOH-逐渐减少,同时·OH 与Cl-发生副反应,因此降低了罗丹明B 的降解效率。反应式如下所示:

此外,Fe3+和Cl-通过进一步反应,可以形成具有不同稳定性的复合离子,但化学平衡常数K 相对较小。因此,对整个反应过程的影响不大。
综上所述,一定浓度范围内的Cl-不会影响类Fenton 反应,但是Cl-浓度较高时,由于副反应的发生,会降低体系的氧化能力。因此,适宜的Cl-浓度范围不超过2.0 mol·L-1。
2.2.6 各因素的影响程度分析
各因素对罗丹明B溶液降解反应速率的影响程度如图4所示。由图4可知,各因素中温度对反应速率影响最大,其次是初始pH 值,而无机盐离子浓度的影响最小。各因素对反应速率的影响大小依次为反应温度>初始pH 值>H2O2投加量>催化剂投加量>无机盐离子浓度,并且在不同反应体系中,罗丹明B 降解均符合伪一级动力学。根据这一结论,在实际运用中,首先应该通过寻找适宜的反应温度和初始pH值来最大化提高催化剂的催化降解性能。

图4 各因素对反应速率的影响程度Fig.4 Impact of each factor on reaction rate
2.3 罗丹明B溶液反应后的TOC测试
色度的去除并不能完全反映罗丹明B溶液的降解情况,TOC 去除率能够很直接地反映有机物总量,因此通过TOC去除率来确定罗丹明B溶液的降解程度。实验条件为:初始pH 值3.0,H2O2投加量0.4 mL,Fe-Beta 分子筛投加量30 mg(其中Fe3+的浓度0.504 mmol·L-1),反应温度70 ℃。TOC 去除率如图5所示。
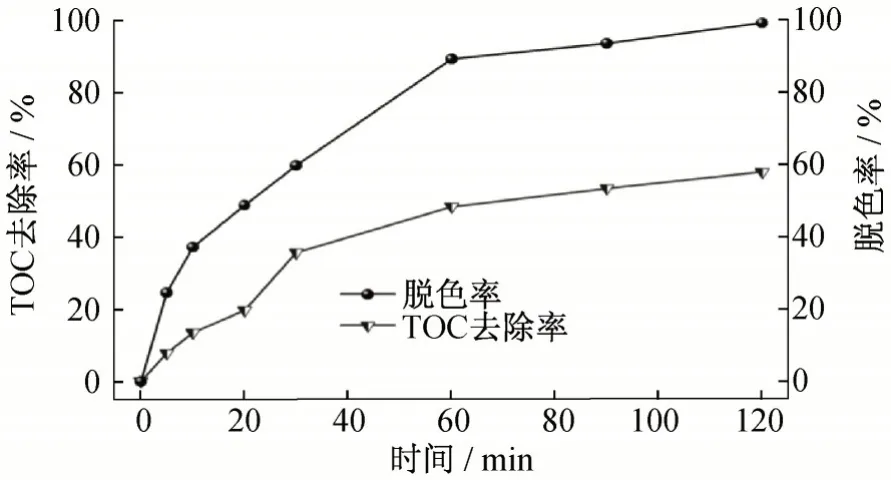
图5 罗丹明B溶液的TOC去除率与脱色率Fig.5 Degradation rate and TOC removal rate of Rhodamine B solution
由图5可知,在最优条件下,随着反应时间的增加,TOC 的去除率逐渐增大,但罗丹明B 溶液的脱色率远大于TOC 的去除率,反应120 min 时罗丹明B 溶液的脱色率达到99%,而TOC 的去除率为57.9%。这说明罗丹明B没有完全被降解而是被氧化成了其他物质,因此在反应产物气相色谱-质谱(GC-MS)分析的基础上进一步探究降解机理[23]。
2.4 降解机理分析
罗丹明B 溶液的脱色率最高可达99%,处理过程中最首要的脱色问题已得到解决。为了分析罗丹明B 的降解机理,同时为该废水的后续处理提供方向,又对催化反应的中间产物(反应1 h)及最终产物(反应2 h)进行了检测,得到的降解中间产物和最终产物如表3所示,√和×表示有、无该产物。

表3 罗丹明B降解的中间产物与最终产物Tab.3 Intermediates and final products of Rhodamine B degradation
从表3 可以看出,催化降解之后,罗丹明B 大多被转化成了羧酸类物质,经过类Fenton 降解之后所得产物的组分基本相同(见图6),产物的分析结果与Yu等[24]和Wang等[25]的研究类似。

图6 GC-MS分析Fig.6 GC-MS analysis
在类Fenton 氧化处理罗丹明B 的过程中,目前认为存在2种反应途径。第1种为脱乙基过程[24],罗丹明B首先吸附在催化剂材料上,接着逐步脱除4个乙基;第2种为染料生色基团的破坏[26],即催化材料受激发产生的·OH 直接攻击罗丹明B 的共轭结构,从而使其迅速脱色到一定程度。2 种情况可能同时发生,但是考虑到材料的脱色较为迅速,降解过程中很可能是生色基团苯氨基、羰基键破坏占主导作用。首先,·OH攻击罗丹明B结构中杂环的两侧乙基,使其逐步脱离苯环,导致染料结构分解,杂环断裂,生成顺丁烯二酸、邻苯二甲酸、对苯二甲酸、苯甲酸及对羟基苯甲酸等一些初级降解产物;然后,·OH会继续攻击其中的某些产物使其开环降解,裂解为不同的直链羧酸类,这些物质经过进一步降解生成小分子物质如乙二酸、丁二酸和丙三醇等;最后,经过一系列反应后逐步矿化为二氧化碳和水。具体的反应路径如图7 所示,类似于微电解Fenton 氧化法降解染料废水的路径[27]。
2.5 催化剂的回用
在考察Fe-Beta分子筛降解罗丹明B实验中,在确定的最优反应条件(初始pH值3.0,H2O2投加量0.4 mL,Fe-Beta分子筛投加量30 mg(其中Fe3+的浓度0.504 mmol·L-1),反应温度70 ℃,反应时间2 h)下,将每次反应后的催化剂离心分离,放入烘箱中低温烘干后再次进行降解实验,结果如图8所示。相同实验进行了2次,得到2组实验结果。催化剂重复使用第2次时,脱色率依然和第1次近似,达到95%以上,重复使用第5次时,脱色率仍在80%以上。
在使用Fe-Beta分子筛降解罗丹明B时脱色率有很少量的下降,可能是由于负载的Fe在使用过程中有很小部分的流失或催化剂回收时有很少量的损失。

图7 罗丹明B降解可能途径Fig.7 Possible reaction pathway for Rhodamine B degradation

图8 催化剂重复利用率Fig.8 Catalyst reuse efficiency
综上,Fe-Beta 分子筛的重复利用率很高,具有良好的稳定性。
3 实际染料废水催化降解
为了考察工业化的应用前景,进行了Fe-Beta分子筛催化降解罗丹明B实际染料废水的研究。反应前后指标与反应条件如表4所示。投加量为10%(体积比,下同)H2O2的COD去除效果与同条件下投加量为20%H2O2的COD 去除率近似,因此选择投加量10%H2O2反应条件更为经济。前3组实验只加入了H2O2,而第4 组实验则另加入了80 mg 的Fe-Beta 分子筛。从表4 可以看出,第4 组的COD 去除率为66.62%,脱色率平均达到96.00%,催化降解效果非常显著。
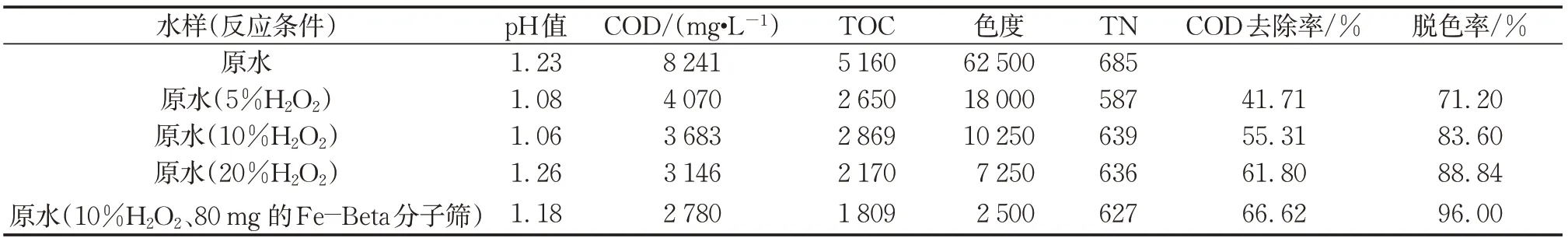
表4 不同实验条件下COD去除率和脱色率Tab.4 COD removal rate and degradation rate of Rhodamine B under different conditions
原水和分别稀释了250、500、1 000 倍的样品的紫外可见吸收光谱如图9a所示。因为有过多其他物质的干扰,原水吸收峰较为复杂,稀释相应倍数后特征峰为552 nm左右,可见与模拟废水中的物质基本统一,主要为罗丹明B。
稀释250 倍溶液加催化剂(10%H2O2、80 mg 的Fe-Beta分子筛)与不加催化剂(10%H2O2)反应后的紫外可见吸收光谱如图9b所示。在200~350 nm处的吸收峰是由于罗丹明B 存在共辄结构,如苯环结构,加入催化剂后,许多共辄结构被催化降解,罗丹明B特征峰(552 nm)几乎消失。体系中的强氧化性活性组分,如H2O2和·OH,通过攻击罗丹明B 的共轭结构,使罗丹明B的4个环开环,从而降解为无毒无害的小分子物质,这说明对罗丹明B 的降解效果十分明显。不加催化剂的溶液在552 nm 处仍然有吸收峰,表明降解效果较差。
稀释250 倍溶液反应前后的紫外吸收可见光谱如图9c 所示。为了便于分析,取稀释250 倍的废水溶液吸收图谱。从机理方面分析,552 nm 处的吸收峰主要是由电子从n非键轨道跃迁到π*反键轨道造成的[28]。
在反应120 min 后,2 个主要区域的特征峰基本消失并且没有新的峰出现,这表明催化降解反应过程中产生的氧化活性物质,如·OH和高价铁等,已经将该染料废水中的显色基团和共辄基团的不饱和键破坏[29],使得染料废水中的大分子结构分解,从而无法产生相应的电子跃迁,最终导致废水中2 个主要的特征峰基本消失[30],因此该催化剂有着较好的催化效果。
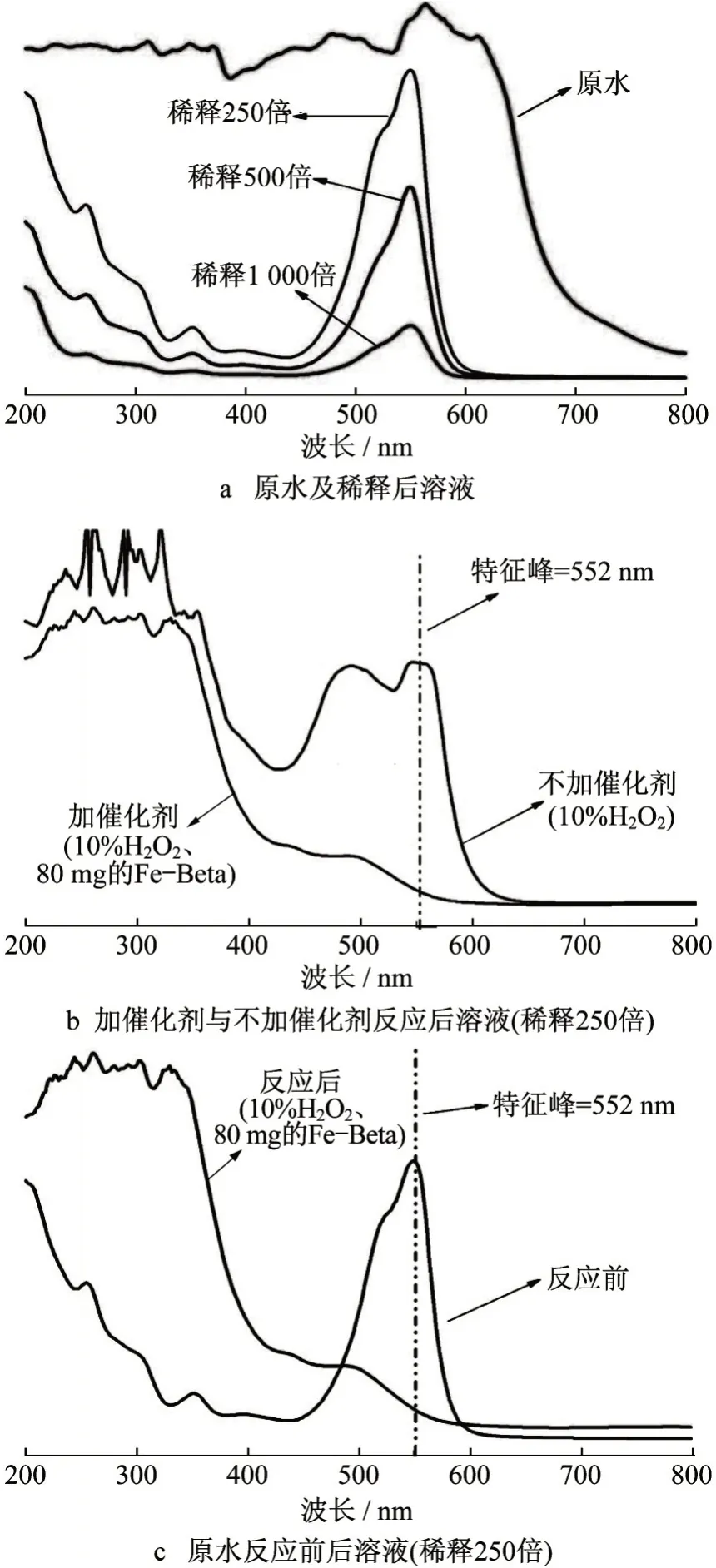
图9 紫外可见吸收光谱Fig.9 UV-visible absorption spectra
4 结论
(1)综合考虑技术可行性及经济合理性,对于100 mL的100 mg·L-1罗丹明B溶液的降解实验,影响因素的最佳选择为:初始pH 值3.0,H2O2投加量0.4 mL,催化剂投加量30 mg(其中Fe3+的浓度为0.504 mmol·L-1),反应温度70 ℃。
(2)各因素对反应的影响程度大小顺序为:反应温度>初始pH 值>H2O2投加量>催化剂投加量>无机盐离子浓度。在不同的反应温度、初始pH 值、H2O2投加量、催化剂投加量、无机盐离子浓度的反应体系中,罗丹明B降解符合伪一级动力学。
(3)Fe-Beta分子筛在降解罗丹明B的实验中体现出很高的重复使用性,经5 次回用后脱色率仍维持在80%以上,具有良好的稳定性。
(4)在实际染料废水的催化降解反应中,针对30 mL 原水样,H2O2投加量为10%,Fe-Beta 分子筛投加量为80 mg,在200 ℃下反应2 h后,脱色率可达96%,这说明Fe-Beta 分子筛对实际染料废水具有较好的催化降解效果。
