托吡酯改善非典型抗精神病药所致体质量增加的meta分析
2020-04-07
上海交通大学医学院附属精神卫生中心生化研究室,上海 200030
非典型抗精神病药(atypical antipsychotic drugs,AAPs)是精神科使用较广泛的药物,其抗精神病作用显著,但往往带来一系列不良反应,其中体质量增加是其主要症状,尤以施用氯氮平、奥氮平最为明显[1]。其机制不甚清楚,可能与药物通过阻断H1受体、瘦素抵抗、激活5-羟色胺1A(5-hydroxytryptamine 1A,5-HT1A)受体等影响神经内分泌系统活动以及影响与调节进食相关的肽类物质有关[2]。体质量的过度增加与患者依从性降低,高血压、高脂血症、糖尿病、阻塞性睡眠呼吸暂停综合征和心血管疾病风险增加有关[3]。因此,减轻AAPs所带来的体质量增加,是目前临床上亟待解决的难题之一。
托吡酯为天然单糖基右旋果糖硫化物,可增强γ-氨基丁酸A型受体(γ-aminobutiric acid type A receptors,GABAA)和(或)α-氨基-3-羟基-5-甲基-4-异唑丙酸(α-amino-3-hydroxy-5-methylisoxazole-4-propionate,AMPA)受体而拮抗兴奋性谷氨酸,抑制电压门控的钠、钙通道,抑制碳酸酐酶等,近年来已用于酒精使用相关障碍、双相障碍和进食障碍等精神疾病的治疗[4-5]。既往有研究表明,辅助托吡酯治疗可显著改善APPs所致的体质量增加、胰岛素抵抗等不良反应,然而研究结果并不一致,同时研究的样本量也不够大。故本研究对托吡酯联用AAPs影响体质量的随机对照试验(randomized controlled trial,RCT)文献进行meta分析,探讨托吡酯改善AAPs所致体质量增加的疗效,以期为指导临床合理用药提供循证医学依据。
1 资料与方法
1.1 检索策略
计算机检索中国知网、万方数据库、中国生物医学文献服务系统、Cochrane Library以及PubMed、Embase、PsycINFO数据库。检索文献起始时间不限,截止时间为2019年3月。中文检索字段包括“非典型抗精神病药” “氯氮平” “奥氮平” “利培酮” “喹硫平” “齐拉西酮”“托吡酯”等。英文检索过程首先以topiramate为主题词在医学主题词表(Medical Subject Headings,MeSH)、Embase数据库中的Emtree词表进行主题词检索,再进行包括“topiramate” “epitomax” “atypical antipsychotic*”“second generation antipsychotic*” “olanzapine” “clozapin”“risperidone” “quetiapine” “ziprasidone”等的文献检索。
1.2 纳入标准和排除标准
纳入标准:①受试者为使用AAPs治疗的精神分裂症、分裂情感性障碍、双相障碍等精神疾病患者。患者符合《国际疾病及有关健康问题分类第10版》(International Classification of Diseases-10,ICD-10)或《精神病协会诊断与统计手册(第4版)》(Diagnostic and Statistical Manual of Mental Disorders Fourth Edition,DSM-Ⅳ)或《中国精神障碍分类与诊断标准第3版》(Chinese Classification and Diagnostic Criteria of Mental Disorder-3,CCMD-3)诊断标准。②实验设计的研究组为常规治疗合用托吡酯的患者,对照组为常规治疗不合用托吡酯的患者。接受托吡酯治疗的给药种类、剂量和疗程均不限。治疗期间不联用其他影响体质量的药物或干预措施。③患者年龄、性别不限。④主要结局指标为RCT试验结束时的体质量值或其改变值,体质量指数(body mass index,BMI)或其改变值。
排除标准:①重复发表的文献。②仅有摘要而未查见全文的文献。③数据不全或未报道的文献。④结果不涉及体质量或BMI的文献。⑤文献内容为方法学研究或meta分析及系统评价。⑥研究对象为健康人群、妊娠期或哺乳期妇女或动物的实验。⑦研究对象使用过其他影响体质量的药物或其他种类的抗精神病药物。
1.3 文献筛选
文献由2名研究者严格按照制定的纳入和排除标准进行筛选,独立进行质量评价、数据提取并交叉核对,遇到分歧与第3名研究者讨论决定。同一研究多处发表时将数据最完整的一篇纳入。未能获取全文信息的通过邮件与通信作者联系获取。
1.4 数据提取
数据提取采用自制表格,主要内容:①研究基本信息,包括研究者姓名、发表时间、地区等。②2组对象的年龄、所使用AAPs类型、托吡酯给药剂量。③随访时间和样本量大小。④所提取的结局指标,包括体质量、BMI(表 1)。

表1 纳入研究的基本特征Tab 1 Characteristics of included studies
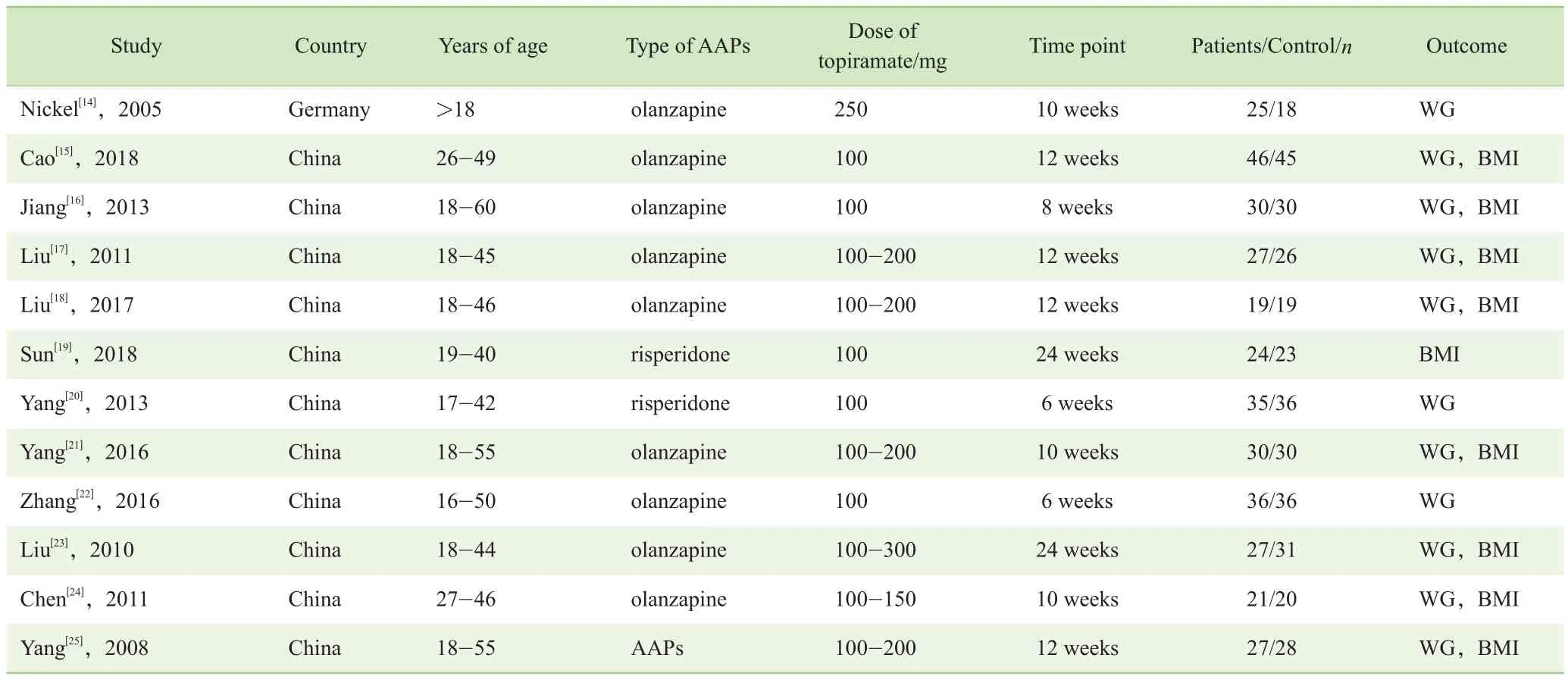
Continued Tab
1.5 统计学方法
采用Cochrane协作网RevMan 5.3软件对数据进行meta分析。连续性变量采用加权均数差(weighted mean difference,WMD)为效应值,区间估计使用95%置信区间(95% confidence intervals,95%CI),异质性检验采用I2统计量检验法表示。对纳入研究的异质性采用χ2检验:当P≥0.100、I2≤50%时,显示纳入各研究间存在统计学同质性,meta分析采用固定效应模型;当P<0.100、I2>50%时,显示纳入各研究间存在统计学异质性,则选用随机效应模型估计合并效应值;合并效应值是指全部入组研究的某观察指标改变量的加权平均值。同时根据药物使用、数据提取等情况进行亚组分析或敏感度分析以检验结果的稳定性。P<0.05 表示差异具有统计学意义。
2 结果
2.1 文献检索及数据提取
按图1进行文献筛选,经初检获取英文文献421篇、中文文献193篇,通过去重后剩余352篇,进行阅读标题和摘要初筛后剩余100篇;进一步阅读全文,根据制定的纳入和排除标准,结合文献质量评价进行筛选,最终纳入20篇RCT文献[6-25],其中英文文献9篇[6-14]、中文文献11篇[15-25];经统计共入组1 024例患者,其中英文文献378例、中文文献646例。

图1 文献筛选流程图Fig 1 Flowchart of literatures screening
2.2 纳入文献质量评价
文献偏倚风险质量评价按照《Cochrane干预措施系统评价手册》里的针对RCT最新偏倚风险的评估工具进行评价。评价结果以偏倚风险表和偏倚风险总结图的形式呈现(图2、图3)。由图2的偏倚风险表可知:有3篇研究[10, 12, 17]呈高风险偏倚,其余均呈风险偏倚不确定。由图3的偏倚风险总结图可知:高风险的研究问题在于未实施双盲及研究报告结果不完整。

图2 文献的风险偏倚表Fig 2 Risk bias table of the literatures

图3 文献的偏倚风险总结图Fig 3 Summary chart of bias risk of the literatures
2.3 统计分析结果
2.3.1 体质量 17篇研究[7-10, 12-18, 20-25]报道了治疗前后体质量水平或体质量变化水平,总计纳入892例患者。异质性检验的结果显示I2=61%、P=0.001,认为纳入的文献异质性较大,故采用随机效应模型合并数据。根据提取的数据,针对干预后体质量值与干预前后体质量变化值进行亚组分析(WMD=-4.23,95%CI-5.66~-2.81,P=0.000;WMD=-3.40,95%CI-7.55 ~ 0.75,P=0.110); 总 的 合 并 效 应 值 WMD=-4.09(95%CI-5.74~-2.44,P=0.000),差异具有统计学意义,即托吡酯能有效改善AAPs所致体质量增加(图4)。
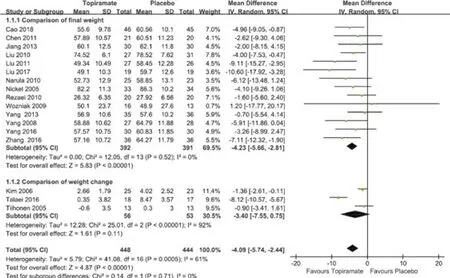
图4 AAPs和托吡酯联用对体质量增加的控制效果的森林图Fig 4 Forest plot of the effect of AAPs combined with topiramate on weight gain
2.3.2 BMI 13篇研究[6, 7, 9, 11, 15-19, 21, 23-25]报道了干预后BMI或其变化值,总计纳入696例患者。异质性检验结果显示I2=62%、P=0.002,认为纳入的文献异质性较大,故采用随机效应模型合并数据。同样,根据提取的数据,针对BMI终值及前后变化值进行亚组分析(WMD=-2.37,95%CI-3.02~ -1.71,P=0.000;WMD=-2.96,95%CI-4.05~-1.87,P=0.000);总的合并效应值 WMD=-2.42,95%CI-3.02~-1.82,P=0.000,差异具有统计学意义,认为托吡酯能够有效降低AAPs所致的BMI增加。

图5 AAPs和托吡酯联用对BMI控制效果的森林图Fig 5 Forest plot of the effect of AAPs combined with topiramate on BMI
2.3 敏感度分析
在报道了结局指标体质量的17项研究中,若剔除Talaei等[7]在2016年发表的1篇文献则异质性检验由原来的I2=61%(P=0.001),降为I2=33%(P=0.100)。同时总的合并效应值(WMD=-2.40,95%CI-3.28~-1.52,P=0.000)较去除前的总效应值(WMD=-4.09,95%CI-5.74~-2.44,P=0.000)精度更高。
同理,在报道了结局指标BMI的13项研究中,若剔除孙乃建[19]与刘增龙等[23]发表的2篇文献则异质性检验由原来的I2=62%(P=0.002),降为I2=0(P=0.460)。总的合并效应值由原来的WMD=-2.42(95%CI-3.02~-1.82,P=0.000),变成 WMD=-2.52(95%CI-2.93~ -2.11,P=0.000)。
2.4 疗效及安全性
这项对20个RCT包含1 024名精神分裂症谱系障碍患者的meta分析表明,在AAPs治疗中添加托吡酯,无论是体质量还是BMI都有明显的降低。我们对没有特定语言限制的RCT进行综合meta分析提示:托吡酯100~300 mg/d连续使用6~24周的患者的体质量、BMI均显著降低。
在安全性方面,12篇文献[6, 9-12, 15-19, 23, 25]报道了试验过程中的不良反应。绝大部分研究提示:试验组与对照组间的不良反应的差异无统计学意义,2组均未发生严重不良反应。仅刘丽等[18]在2007年发表的文献显示试验组的不良反应发生率显著低于对照组。Afshar等[11]发现不良反应多为轻度至中度(如嗜睡、口干、乏力、头晕等),且一般在用药早期出现。
3 讨论
本文结果表明,托吡酯与抗精神病药物配伍是减轻精神分裂症谱系患者体质量增加的一种有效和安全的治疗选择。本次meta分析的主要结局指标为体质量和BMI,其结果均显示差异有统计学意义。分别去除影响较大的研究后,异质性结果显示P>0.100,即异质性没有统计学差异;合并效应值置信区间的精度也相应提高。
根据提取数据的不同进行亚组分析后,干预后体质量与BMI值及合并后的总效应值均提示,在改善AAPs所致体质量增加方面,托吡酯组明显优于对照组。在干预前后差值的亚组比较中,显示了非常大的异质性,可能与纳入的研究样本量小、试验时间不同、托吡酯使用剂量不一致有关。
Batterham等[26]认为体质量基线低的人在经减重干预后,减重效果更加迅速且更显著。Goh等[27]的meta分析中也得出了类似结论:使用AAPs治疗的精神疾病患者中,BMI<25 kg/m2的患者使用托吡酯后减重效果更明显;并且,在对患者所在地区进行分层分析后发现,欧美地区患者的体质量变化小于东南亚地区,而这一差异可能是由于欧美地区患者体质量基线值高于东南亚地区患者;同时发现减重效果与基线症状严重程度也有关,基线症状重的患者其托吡酯减重效果更加明显;药物使用方面,较使用氯氮平的患者,托吡酯对使用奥氮平的精神分裂症患者的减重效果更加明显,但托吡酯对不同AAPs所致体质量增加的影响需要更加系统的评价。另有meta分析[28]表明,在使用托吡酯8、10、12、24周的结果中,第10、12周的托吡酯干预效果更加突出。
托吡酯改善患者体质量增加的机制目前尚不明确,可能与以下几个方面有关:①在各种动物模型中,已证实托吡酯可降低动物食欲并降低能量利用率[29-31]。②托吡酯可直接增强葡萄糖代谢过程中对胰岛素的敏感度,从而提高葡萄糖代谢率,引起厌食等[32]。③托吡酯可刺激脂肪组织和骨骼肌中的脂蛋白脂肪酶,抑制参与脂肪合成中起关键作用的碳酸酐酶[33]。
大多数报道[6,10-12,34]提示:在治疗过程中,托吡酯的不良反应主要有头晕、头痛、嗜睡、恶心呕吐、厌食、共济失调、心电图改变。报道最多关于托吡酯的不良反应是感觉异常[35]。托吡酯是一种碳酸酐酶抑制剂(对碳酸酐酶亚型Ⅱ和Ⅳ表现出选择性),感觉异常是这种效应的典型症状[36];并且,这一不良反应可能与其改善患者体质量增加的作用相关。
虽然本研究检索全面,文献纳入、排除标准严格,但仍存在以下不足:①本研究包括20个RCT,但每项研究的样本量相对较小,而且大多试验中的信息有限或不完整,这可能会降低研究结果的全面性和准确性。②本研究纳入文献均为公开发表的RCT文献,缺乏未公开发表的文献、研究数据和会议交流等,可能会遗漏托吡酯降低AAPs所致体质量增加的RCT文献(尤其是阴性结果的RCT文献)而产生发表偏倚。另外,我们的meta分析应考虑偏倚风险,以上20篇RCT中有3篇呈高风险偏倚,且缺乏低风险偏倚的研究。③本研究纳入的RCT文献多为短期随访,最长的随访时间是24周,因此无法得出托吡酯干预对AAPs所致体质量增高的长期干预效果及停止干预后疗效能否保持的结论。
综上,托吡酯能有效改善AAPs所引起的体质量增加及BMI增加,其可能的作用机制包括降低食欲、提高糖代谢以及抑制碳酸酐酶,其不良反应轻且与对照组无显著差异。
