纳米孔隙内甲烷水合物微观分解特性
2020-04-04万丽华臧小亚关进安梁德青
万丽华 ,臧小亚 ,关进安 ,梁德青
(1. 中国科学院 广州能源研究所,广东 广州 510640;2. 中国科学院 天然气水合物重点实验室,广东 广州 510640)
天然气水合物储量巨大[1-3],是重要的可替代高清洁化石能源[4-7]。天然气水合物床主要存在于海洋架和大洋中,散布在高压下在粗粒和细粒沉积物的孔隙中,以块状形式存在的天然气水合物仅仅约占总量的6%。天然气水合物在纳米级沉积物中的分解过程与海洋天然气水合物微纳米尺度赋存和开采储存技术密切相关[8]。在纳米多孔材料中,受限环境存在大的吸附势和限域效应[9],能够极大地增加水和甲烷之间的接触面积,从而加速成核动力学,实现有效快速的水合物形成[10]。当前纳米尺度多孔介质中水合物的形成研究主要围绕提高甲烷吸附量、实现最佳水-水合物转化、储存容量、水与水合物产率等而展开。对纳米多孔材料内气体水合物的分解研究,目前局限于采用基于van der Waals和Platteuw (vdWP)热力学新模型或者基于Gibbs-Thomson关系的扩展热力学模型,计算水合物-液体-水的界面能,预测纳米多孔介质中水合物分解条件。Klauda等[11]提出了vdWP模型,考虑多孔材料的孔径分布。Anderson等[12]提出了一种基于Gibbs-Thomson关系的扩展热力学模型。Zarifi等[13]测量了孔径为10 nm和15 nm的硅胶合成混合物气体水合物在冰点以上、压力3.30~6.22 MPa范围内的分解条件,建立了基于vdWP固溶理论的热力学模型。Uchida等[14]测量了直径为6.0,15.0,30.0 nm的硅胶孔中二元CH4+水和CO2+水混合水合物分解条件,发现孔隙水合物的三相H-LW-V平衡曲线转移至较高压力区域。然而,纳米尺度受限空间是一个高度复杂的系统与存在方式,纳米尺度受限空间内甲烷水合物的分解过程和分解机制尚不清楚。
本工作通过拉曼光谱仪测试常压和不同温度下纳米硅胶孔隙内甲烷水合物的微观分解过程,考察纳米尺度甲烷水合物的分解微观特性。同时为了探求影响纳米尺度甲烷水合物的分解微观特性的内在控制因素,采用拉曼光谱仪测试硅胶纳米孔隙水的拉曼结构,探求二者之间的内在联系。
1 实验部分
1.1 纳米孔隙水的合成
甲烷水合物在含水的硅胶纳米孔隙内合成。所使用的硅胶孔径范围为15~20 nm人造硅胶,由青岛硕远集团提供。硅胶的孔径、孔体积与比表面积由ASAP2010型表面及孔径分析测定仪(Micromeritics公司)测定,平均孔体积为1.19 mL/g,比表面积为300~500 m2/g。
在实验中,首先将无水硅胶在377.15 K下烘干24 h,冷却至室温称重,室内保持干燥,将与硅胶孔隙体积相同的水量和硅胶试样充分混合,然后将试样放置在离心机以3 500 r/min的转速旋转0.5 h,密封静置5天,以保证蒸馏水均被多孔介质吸收。
1.2 纳米孔隙甲烷水合物的合成
纳米孔隙甲烷水合物由含水硅胶与甲烷气体在低温高压下合成。图1为甲烷水合物试样合成装置系统。在反应釜中加入6 g含水硅胶,对反应釜以及管路抽真空。在常温下向反应釜内注入甲烷气体,释放压力,多次洗涤反应釜,确保釜内无空气。空气浴设置温度273.15 K。待釜内温度和缓冲罐温度稳定后,釜内加压至11.9 MPa。硅胶孔隙内的水与甲烷气体合成甲烷水合物,大约经过3天,釜内压力稳定在9.5 MPa左右,甲烷水合物试样合成完毕。合成的甲烷水合物试样由液氮保冷转移至液氮罐内保存,备用。
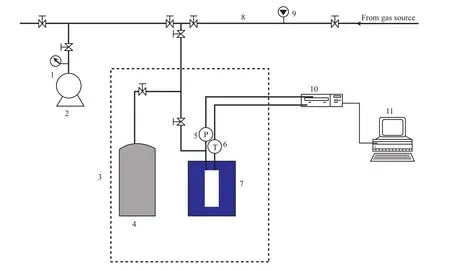
图1 实验装置系统Fig.1 Experimental device system.1 Vacuum pressure gauge;2 Vacuum pump;3 Air bath;4 Buffer tank;5 Pressure sensor;6 Platinum resistance temperature sensor;7 Stainless steel reactor;8 Pipeline;9 Pressure gauge;10 Data acquisition instrument;11 Computer
1.3 拉曼光谱测试孔隙水结构
通过LabRam HR显微激光拉曼光谱仪(Horiba公司)测试硅胶孔隙水的拉曼结构和常压、不同温度下的甲烷水合物的分解过程。表1为显微激光拉曼光谱仪工作条件。试样测定前,用单晶硅(520 cm-1)对显微激光拉曼光谱仪进行校正。室温下测定含水硅胶试样中孔隙水的拉曼结构,温度约为 293 K。

表1 显微激光拉曼光谱仪工作条件Table1 Working parameters of the laser micro-Raman spectrometer
1.4 甲烷水合物微观分解过程
通过拉曼光谱仪测试常压和不同温度下纳米尺度硅胶孔隙中甲烷水合物的分解过程。合成的甲烷水合物试样通过液氮转移至拉曼冷台中,冷台为Renishaw公司LINK THMSG 600 型冷台,见图2。控温范围77~873 K,控温精度0.1 K。水合物分解测试开始前,测定甲烷水合物试样稳定态下的结构。拉曼冷台控温在213 K,水合物处于稳定态,此时测定硅胶孔隙中的甲烷水合物的拉曼结构。在水合物分解测定过程中,拉曼冷台分别控制温度在263,253,243 K,对水合物试样进行拉曼结构扫描。完成一次拉曼结构扫描耗时约4 min,每次拉曼结构扫描结束后,紧接着开始下一次的拉曼结构扫描,直到水合物拉曼特征峰全部消失。

图2 拉曼冷台实物Fig.2 Physical device diagram of Raman spectrometer cooling stage.
2 结果与讨论
2.1 硅胶孔隙水的微观结构
常态下水分子中的OH键在1 640 cm-1处出现弯曲振动峰,在2 800~3 800 cm-1处出现伸缩振动峰。通常OH键伸缩振动峰可以分解为4~5个高斯峰对应的结构(水分子局部氢键网络结构),分别为DAA (single donor-double acceptor)、DDAA (double donor-double acceptor)、DA (single donor-single acceptor)、DDA(double donor-single acceptor)和自由OH结构[15-16]。其中,DDAA和DA结构的高斯峰对温度变化敏感[16],在一定温度范围内,随着温度的降低,DA结构部分转化为DDAA结构[15]。
本工作测试了在常压下,293 K自由水和不同含水率硅胶孔隙水的OH键拉曼光谱,结果见图3;含水率为100%的硅胶孔隙水的伸缩振动峰对应的拉曼位移见表2。

表2 水和孔隙水的DDAA和DA结构比较Table 2 DDAA and DA structure comparison of free water and pore water
结合图3和表2可知,含水率为100%的硅胶293 K孔隙水的拉曼光谱中,DDAA和DA结构的拉曼位移分别为3 087 cm-1,3 288 cm-1,相对于293 K的自由水,DDAA和DA结构的拉曼位移向低波数偏移,分别偏移144 cm-1和153 cm-1。硅胶孔隙水OH键弯曲振动峰的拉曼位移为1 587 cm-1,相对于293 K的自由水在1 640 cm-1处出现弯曲振动峰,它向低波数偏移。这主要是由于纳米孔隙中,水分子间的吸引力增强,使得OH化学键增长,削弱了OH化学键的作用,从而使拉曼频率降低。293 K在硅胶孔隙水中DDAA和DA二种结构高斯峰占90%以上,与常态下的自由水水分子的OH键高斯峰比较,硅胶孔隙水的DDAA结构高斯峰明显增强,而DA的高斯峰明显减弱,相对于常态下的自由水,硅胶孔隙水中部分DA结构转化为DDAA结构,使DDAA结构的比例高于DA结构,从而水分子被圈闭在水分子构成的四面体氢键网络结构中。这种结构使硅胶孔隙水极易形成水合物,在满足相平衡条件下,可快速形成水合物。硅胶孔隙中水的拉曼结构与过冷水的拉曼结构十分相似,且向低波数偏移。含水率为33%和67%的硅胶孔隙内水表现出与含水率为100%的硅胶孔隙水类似的拉曼特征。
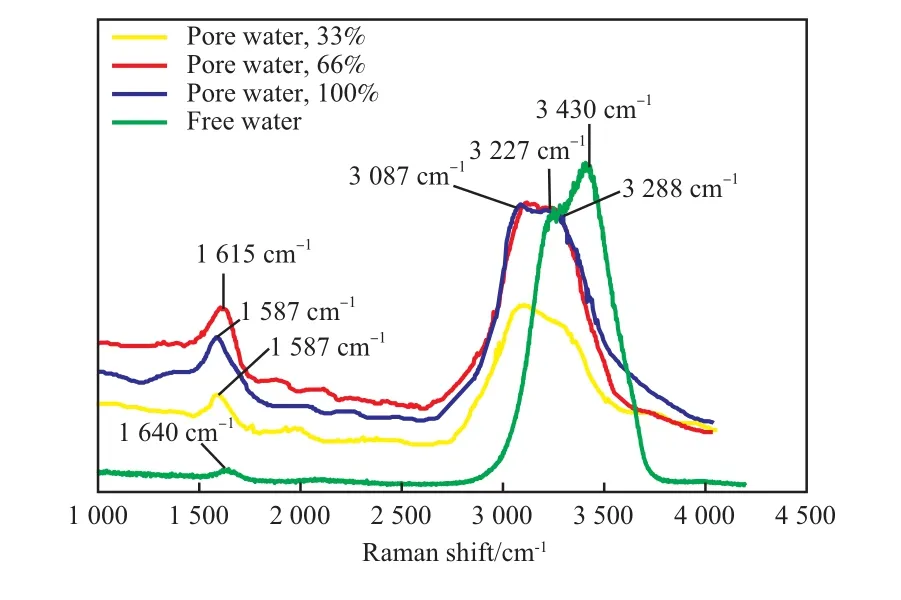
图3 293 K下不同含水率硅胶孔隙水的拉曼谱图Fig.3 Raman spectroscopy of pore water inside silica gel pores with different water content at 293 K.
2.2 甲烷水合物微观分解过程
2.2.1 在263 K分解结果
图4为甲烷水合物在263 K常压下分解过程的拉曼谱图。由图4可知,0 min,213 K的拉曼谱图在拉曼位移为2 905 cm-1和2 915 cm-1处分别出现了甲烷分子的CH振动拉曼光谱特征峰[17-23],反映了甲烷分子的CH键在水合物大笼和小笼中的不同振动情况。大尺寸的甲烷水合物的水分子间的OH收缩峰出现在位移为3 101 cm-1处,而对应的硅胶纳米孔隙中形成的甲烷水合物的OH收缩峰的位移向高波数偏移至3 137 cm-1处,反映了在纳米孔隙中形成的甲烷水合物的晶格参数的变化。因此,合成的试样为Ⅰ型甲烷水合物晶体。在263 K分解过程中,分解进行到4 min时,相对于初始时刻,CH键拉曼光谱在2 905 cm-1和2 915 cm-1处的峰强度均降低,水分子的OH键的拉曼峰强度同步减弱,说明甲烷水合物试样分解。而在分解进行到8 min时,CH键在2 905 cm-1和2 915 cm-1处的峰强度均增强,水分子的OH键的拉曼峰强度同步增强,说明有新的甲烷水合物形成,且强度高于初始(0 min)峰。同时,OH键的峰强度高于试样初始时的峰强度,说明此时甲烷水合物的量高于初始时的量,推断新形成的甲烷水合物不仅仅来源于分解所产生水的二次形成反应,也来自于未反应完全水的形成反应。相对于8 min时,在12 min时CH键在2 905 cm-1和2 915 cm-1处的峰强度均降低,水分子的OH键的拉曼峰强度同步减弱,说明甲烷水合物又开始分解,而后CH峰和OH键的拉曼峰强度继续降低,直到消失,说明此后甲烷水合物分解,直到甲烷水合物晶体消失。整个过程,甲烷水合物经历分解—二次形成—继续分解,直到晶体消失的过程。
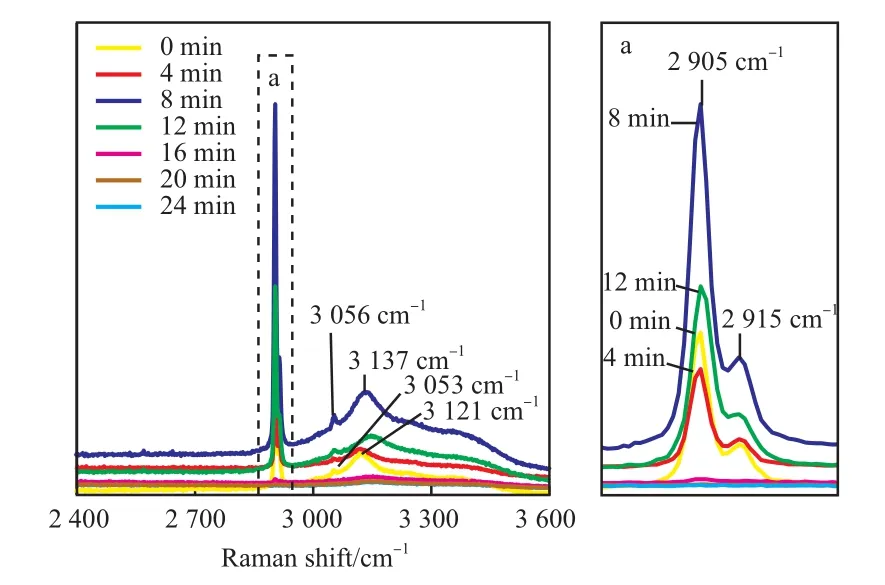
图4 硅胶孔隙甲烷水合物试样在263 K常压下分解过程的拉曼谱图Fig.4 Raman spectra of methane hydrate inside silica gel pores during the decomposition process at 263 K and atmospheric pressure.
在大体量系统中,273.15 K以下甲烷水合物减压分解过程中会出现分解产生的水冻结成冰,覆盖在未分解的甲烷水合物表面,使某一温度范围内天然气水合物的分解速率减慢,这一分解速率异常的现象称为“自保护效应”。研究人员用实验对自保护效应的机制展开了一系列的研究[24-27]。Stern等[24]测定了甲烷水合物在193~273 K的常压分解速率,表明温度范围为242~271 K是甲烷水合物的自保护区。本工作拉曼光谱测试硅胶孔隙中甲烷水合物试样在263 K常压下分解过程,没有冰的特征峰,因此在纳米尺度受限空间内,273.15 K以下甲烷水合物减压分解过程无自保护现象。
2.2.2 在253 K分解结果
图5为甲烷水合物在253 K常压下分解过程的拉曼谱图。由图5可知,在253 K分解过程中,与263 K分解类似,分解进行到4 min时,相对于初始时刻,甲烷分子的CH键和水分子的OH键的拉曼峰强度同步减弱,说明甲烷水合物试样分解,而在分解进行到8 min时,CH键和水分子的OH键的拉曼峰强度同步增强,说明有甲烷水合物形成,且强度高于初始(0 min)峰,同时OH键的峰强度高于试样初始时候的峰,说明新形成的甲烷水合物来源于分解所形成水的二次形成反应和未反应完全水的二次形成反应。之后CH键和水分子的OH键的拉曼峰强度同步减弱,直到32 min消失,说明甲烷水合物在这一阶段为分解过程。36 min时CH键和OH键的拉曼峰强度增强,说明有水合物再次形成。可能由于硅胶孔隙内的压力不足,只有极少量的甲烷水合物形成。此后,甲烷水合物分解,直到甲烷水合物晶体消失。整个过程中甲烷水合物经历分解—二次形成—继续分解—少量形成—分解的过程,直到CH键拉曼峰消失时, 依然可见OH键的拉曼峰,说明即使在甲烷水合物晶体消失时,依然保存着大量的水合物笼型结构。整个过程无冰的拉曼特征峰,无自保护现象。
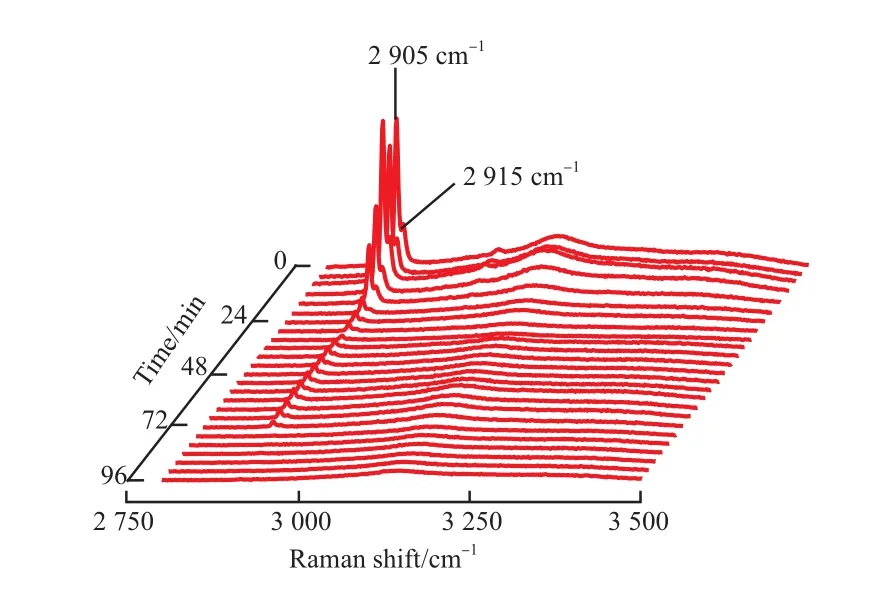
图5 硅胶孔隙甲烷水合物试样在253 K常压下分解过程的拉曼谱图Fig.5 Raman spectra of methane hydrate inside silica gel pores during the decomposition process at 253 K and atmospheric pressure.
2.2.3 在243 K分解结果
图6为甲烷水合物在243 K常压下分解过程的拉曼谱图。由图6可知,在整个分解过程出现多个二次形成过程,比253 K和263 K常压下分解过程中出现的二次形成过程耗时长。说明温度越低,越有利于二次形成。整个过程无冰的拉曼特征峰,无自保护现象。在整个分解过程结束后,依然保存着大量的水合物笼型结构。由于每一次的拉曼结构扫描耗时约4 min,在出现二次形成的过程中,根据图4~6可推断水合物的形成时间在4 min内,说明形成反应本身十分迅速,与文献数据吻合[9-10]。
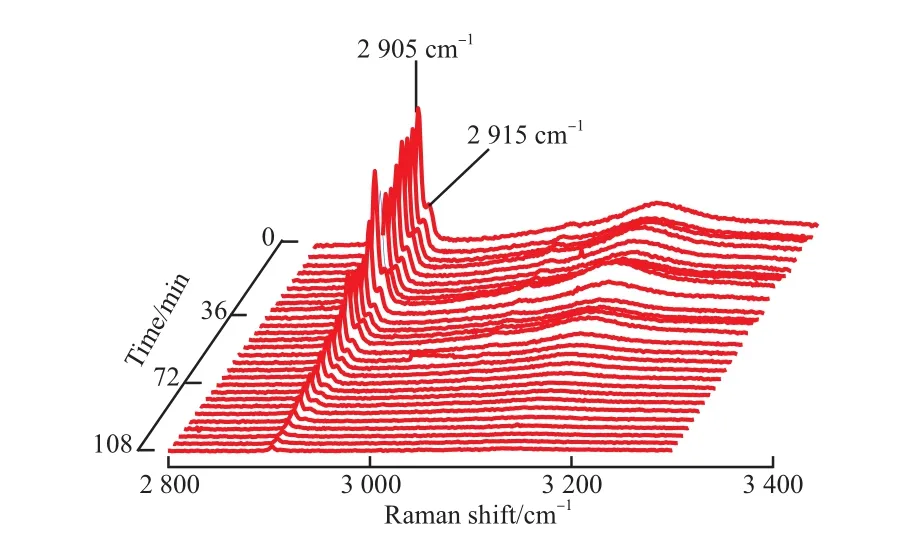
图6 硅胶孔隙甲烷水合物试样在243 K常压下分解过程的拉曼谱图Fig.6 Raman spectra of methane hydrate inside silica gel pores during the decomposition process at 243 K and atmospheric pressure.
2.3 微观分解机理分析
与大尺度体系的水合物相比较,水合物在纳米多孔介质中,由于毛细压力作用,纳米多孔介质中水合物的相平衡曲线随着孔径的减小而向上移动[11-14,28],即纳米多孔介质孔径越小,形成水合物所需的压力越高或者温度越低。由于水合物的分解过程是固态水合物转化为液态水和甲烷气,形成过程是液态水和甲烷气转化为固态水合物。因此,硅胶孔隙水合物的分解过程相当于硅胶有效孔径增大的过程,而形成过程相当于有效孔径减小的过程。在形成过程结束后相平衡曲线上移,分解过程结束后相平衡曲线下移。也就是说因分解产生气体而形成的压力高于分解后的温度对应的相平衡压力。
硅胶孔隙内甲烷水合物的分解过程包含了一系列的子过程,即甲烷水合物本身的分解、甲烷分子和水分子在孔内的扩散、由孔内向孔外的扩散、以及脱附离开硅胶孔。在分解过程中,分解产生的甲烷分子以超临界态吸附在硅胶孔内,经过脱附作用离开硅胶孔隙进入气相。在孔外常压下分解,孔隙内自由气体已经释放,孔内甲烷气体的释放源自于孔内甲烷分子向孔外的扩散,而由于纳米环境中的限域效应,在硅胶孔隙内甲烷向孔外的的扩散系数要比大体量系统甲烷的扩散系数小3~5个数量级[29],而且几乎不随着孔内压力的改变而改变。因此由甲烷水合物分解产生的甲烷分子较长时间地停留在孔隙内。当甲烷分子由脱附作用离开孔隙的速率小于分解产生的甲烷分子的速率[30-32],分解释放的甲烷分子来不及脱附而较长时间停留在硅胶孔隙内,使得硅胶孔隙内的压力迅速增大。由于相平衡曲线的下移,当压力超过纳米孔隙内甲烷水合物相平衡压力时,就出现了甲烷水合物的形成反应,产生了二次形成过程。形成过程结束后,孔隙内压力减小,同时硅胶有效孔径减小,相平衡曲线上移;加上甲烷的缓慢脱附过程进一步使得孔隙内压力减小,使得孔内甲烷水合物落在不稳定区域,从而又开始分解。
纳米孔隙水的结构本身十分有利于甲烷水合物的形成,在满足相平衡条件下,可快速形成水合物,可以说这是二次形成的内在结构条件。此外,而在受限环境中存在限域效应,使得孔隙内的甲烷分子以超临界态吸附于硅胶孔隙内的SiO2表面。研究表明,纳米环境中甲烷分子有序度增加,流动阻力小,扩散系数比宏观环境增大2个数量级[30-32],这也加速了纳米孔隙内甲烷水合物的成核,从而能够迅速二次形成甲烷水合物。限域效应对纳米受限空间内的甲烷分子和水分子的有序度和物性的改变是造成多次二次形成的内在结构原因。在273.15 K以下甲烷水合物的分解均存在分解后的二次形成过程,温度越低纳米孔隙内甲烷水合物相平衡压力越低,二次形成越容易, 二次形成的次数越多,从而使得分解过程耗时越长。因此,273.15 K以下的纳米硅胶孔隙内甲烷水合物分解的主要控制因素是多次二次形成,而造成多次二次形成的外在因素是纳米孔隙内甲烷分子较慢的脱附速率。
3 结论
1)纳米孔隙水拉曼频率降低,水分子间的吸引力增强,削弱了OH化学键的作用。纳米孔隙水分子被圈闭在孔隙水分子构成的四面体氢键网络结构中。这种结构使硅胶孔隙水极易形成水合物,在满足相平衡条件下,可快速形成水合物。
2)纳米尺度受限空间内甲烷水合物的分解经历分解—二次形成—继续分解,直到晶体消失的过程,分解最终的产物,以水合物笼型结构的形式存在。在273.15 K以下纳米尺度受限空间内甲烷水合物的分解均存在分解后的二次形成过程,温度越低,相平衡压力越低,二次形成的次数越多,分解耗时越长。分解过程中无冰的特征峰,无自保护现象。273.15 K以下的纳米硅胶孔隙内甲烷水合物分解的主要控制因素是多次二次形成,而造成多次二次形成的控制因素是甲烷分子较慢的脱附速率。
3)纳米孔隙水的结构本身十分有利于甲烷水合物的形成,在满足相平衡条件下,可快速形成水合物,是二次形成的内在结构条件。
