大分割放疗对糖尿病患者乳腺癌根治术后肺功能及并发症的影响
2020-03-21李晓慧陈春建
李晓慧,陈春建
(河南省通许县人民医院 肿瘤内科,河南 开封 475400)
乳腺癌是女性常见恶性肿瘤,其发病率仅次于子宫癌,死亡率居于第一位[1]。手术治疗是乳腺癌主要治疗手段,放疗、化疗是乳腺癌术后患者不可缺少的辅助治疗方案,其中放疗能显著降低患者复发风险及死亡率。临床常规放疗执行的剂量标准为50 Gy/25 F,需要患者治疗5~7周,较长时间的住院治疗不仅增加患者放射性损伤并发症发生,同时对患者身心及经济造成压力,因此,需要一种短时间放疗方案来缩短患者疗程,减少放射性损并发症发生,减轻患者经济压力及负担[2-3]。大分割放疗是近年来专家学者提出的不同于常规分割放疗新型模式,本研究旨在分析大分割放疗对乳腺癌术后患者肺功能及并发症的影响。
1 资料与方法
1.1 一般资料
纳入2014年3月至2016年3月本院接诊的83例乳腺癌术后患者作为本次研究对象,掷币法分组。纳入标准:所有患者经本院相关检查结合病理学确诊[4],患者均存在3年以上的糖尿病史,血糖水平为:空腹血糖高于7.0 mmol/L或餐后血糖高于11.1 mmol/L,患者生命体征平稳,KPS评分≥70分,经本院伦理委员会批准,患者及家属知情同意。排除标准:严重肝、肾、心、肺功能不全者;凝血功能、造血功能障碍者;重度低蛋白血症,生命体征不平稳者;难以耐受放疗过程者等。对照组41例,年龄42~63岁,平均(61.35±5.80)岁;平均病程(2.69±0.73)年;Stage分期:Ⅱ期5例,Ⅲ期30例,Ⅳ期6例。观察组42例,年龄45~61岁,平均(60.87±5.42)岁;平均病程(2.80±0.61)年;Stage分期:Ⅱ期8例,Ⅲ期29例,Ⅳ期5例。两组患者性别、年龄、病程及Stage分期分布比较差异无统计学意义(P>0.05),具有可比性。
1.2 方法
两组患者均接受乳腺癌根治术,术后接受逆向调强放疗(intensity modulated radiation therapy,IMRT),仰卧于乳腺托架上,外展双臂,采用铅丝标记手术瘢痕,CT模拟定位,放射范围包括锁骨上淋巴结、胸壁,观察组接受大分割放疗:42Gy/15F,瘤床加量9 Gy/3 F,5 F/周,2.8 Gy/F。对照组接受常规分割放疗:50 Gy/25 F,瘤床加量10 Gy/5 F,5 F/周,2 Gy/F。
1.3 观察指标
①放射性肺炎 依据美国肿瘤放射治疗组(Radiation Therapy Oncology Group,RTOG)放射性肺损伤分级标准,观察两组放疗3个月内急性肺损伤发生情况。0级:无异常变化;1级:轻微症状的干咳,用力时呼吸困难;2级:咳嗽成持续性,需镇咳药治疗,稍微用力时呼吸困难;3级:咳嗽加重,麻醉类镇咳药治疗无效,静息时呼吸困难,需配合间断吸氧或激素治疗;4级:呼吸功能不全,持续吸氧或者辅助通气;5级:致死。②肺纤维化 依据美国RTOG放射性肺损伤标准分级观察两组放疗3个月后发生的晚期慢性肺损伤,1级:存在轻微放射变化及轻微咳嗽;2级:存在中度肺纤维化,严重咳嗽、发热等症状,放射学变化呈片状改变;3级:重度肺纤维化,放射学变化呈致密影;4级:严重呼吸功能障碍,持续吸氧,辅助通气;5级:致死。③肺功能 治疗前后两组均进行肺功能检查,检测用力肺活量(forced vital capacity,FVC)、第1秒用力呼气容积(forced expiratory volume in 1 second,FEV1)。
1.4 统计学方法
采用SPSS 21.0软件对文中所得数据进行分析处理,计量资料以均数±标准差(±s)表示,采用t检验;计数资料以百分比(%)表示,采用χ2检验,等级资料采用秩和检验,P<0.05为差异有统计学意义。
2 结果
2.1 两组急性放射性肺炎及肺纤维化发生率比较
观察组急性放射性肺炎发生率低于对照组,差异有统计学意义(P<0.05),两组肺纤维化发生率比较差异无统计学意义(P>0.05)。见表1。
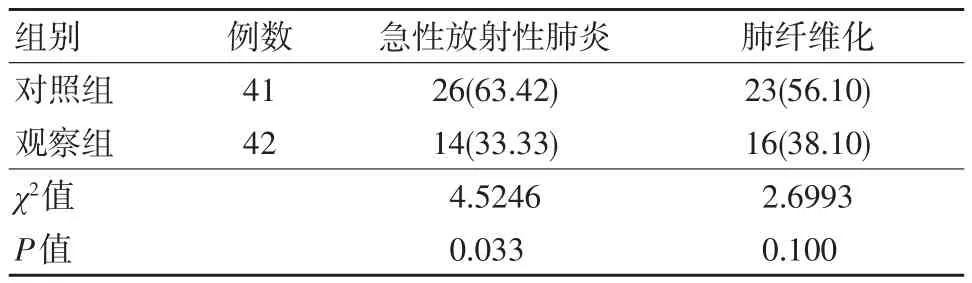
表1 两组急性放射性肺炎及肺纤维化发生率比较 例(%)
2.2 两组急性放射性肺炎分级比较
两组急性放射性肺炎严重程度分级比较,差异有统计学意义,对照组严重程度高于观察组(P<0.05)。见表 2。
2.3 两组肺纤维化严重程度分级比较
两组肺纤维化严重程度分级比较差异无统计学意义(P>0.05)。见表 3。
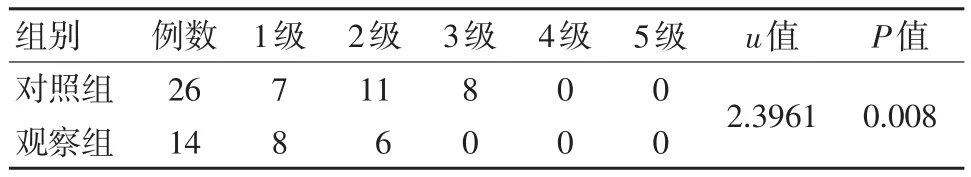
表2 两组急性放射性肺炎分级比较 例
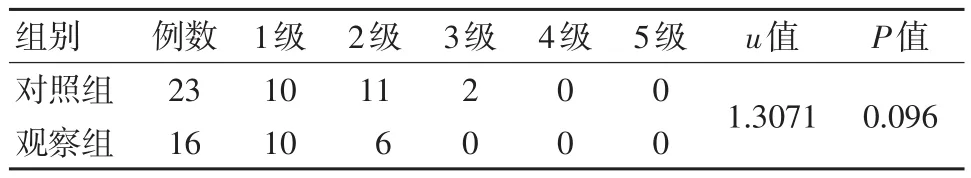
表3 两组肺纤维化严重程度分级比较 例
2.4 两组治疗前后肺功能比较
两组患者治疗前各肺功能指标比较差异无统计学意义(P>0.05),治疗后对照组FEV1、FVC显著低于观察组及治疗前,差异有统计学意义(P<0.05),观察组治疗前后肺功能比较差异无统计学意义(P>0.05)。见表 4。
表4 两组治疗前后肺功能比较 (±s,L)

表4 两组治疗前后肺功能比较 (±s,L)
注:†与对照组治疗后比较,P<0.05。
FEV1例数FVC组别41对照组
3 讨论
糖尿病是临床常见慢性病,也是乳腺癌患者最为常见基础病,糖尿病引起的血管病变并发症能增加血管通透性,促进炎症渗出,影响患者免疫功能,增加乳腺癌术后放疗患者并发症的发生,且不利于患者术后恢复[5]。乳腺癌是女性常见恶性肿瘤,具有极高发病率及病死率,近年随着医学技术的不断提升,手术已成为治疗乳腺癌最主要的方案之一,亦是临床治疗乳腺癌首选方案,而乳腺癌根治术是治疗乳腺癌的常用术式,其能最大程度切除肿瘤组织,但术后局部区域复发率较高,因此,术后需配合放疗、化疗辅助治疗以提高患者生活质量,降低死亡风险[6-7]。
放疗是利用一种或多种电离辐射对恶性肿瘤进行放射治疗,是临床治疗恶性肿瘤常见局部治疗手段,主要通过放射性同位素产生的α、β、γ射线来抑制术后残存的癌细胞生长,从而达到根治癌细胞的目的[8]。在放疗过程中,肺位于胸部左右两侧胸腔内,与乳房解剖位置最为接近,在放疗过程中不可避免会损伤肺脏,引起放射性肺损伤,现行的放疗国际标准剂量为50 Gy/25 F,需要患者治疗5~7周,长时间住院治疗可增加患者身心压力及经济负担,同时还能增加并发症发生概率,因此,需要一种短疗程的放疗方案来缩短治疗时间,减少放射性肺损伤的发生,减轻患者身心及经济压力[9]。
近年来,专家学者为缩短放疗疗程,减少并发症发生,提出了诸多不同于常规分割的放疗模式,包括加速部分乳腺照射、大分割放疗等,其中大分割放疗模式受到临床广泛关注。大分割放疗是指高于常规分割放疗2 Gy单次剂量的放疗模式,其优势在于增大单次照射剂量(>2 Gy),减少照射总次数,减少照射总剂量,从而缩短放疗时间[10]。传统理论上认为增加常规放疗分次剂量可能会增加并发症的发生,这是由于放疗后的生物学影响与正常组织接受的放疗剂量呈正比,即单次分割剂量越大,正常组织毒性越强。但实者不然,组织对放疗敏感性取决于α/β值,比值越低的组织对大分割放疗剂量敏感性越高,一项大型随机临床试验研究表明[11],乳腺癌组织α/β比值为2.88 Gy,同时确定了肿瘤潜在倍增时间为(14.4±7.8)d。由此可见,乳腺癌组织α/β比值较低,肿瘤潜在倍增时间较长,表明大分割放疗对乳腺癌杀伤力更强,效果更好,且并不增加并发症发生。
采用生物等效剂量进行换算,大分割放疗42 Gy/15 F等效常规放疗剂量50 Gy/25 F。本研究结果显示观察组急性放射性肺炎发生率低于对照组,放射性肺炎程度分级亦低于对照组,对照组肺功能指标均显著低于观察组,可见大分割放疗能显著减少急性放射性肺损伤发生,减轻已有放射性肺炎的分级程度,减少放疗对患者肺功能的影响,究其原因可能与肿瘤潜在倍增时间及基础病影响较低有关,正常组织修复能力较肿瘤组织快而完整,在下一次照射前可基本恢复到正常状态,但肿瘤组织恢复极差,大分割分次照射的过程中,正常组织及肿瘤组织的放射效应逐渐出现差异,从而达到在杀灭肿瘤细胞的同时保护正常组织的目的,同时大分割放疗疗程短,糖尿病、高血压等基础病对免疫功能影响较低[12-13]。本研究显示放疗3个月后,两组肺纤维化发生率、分级比较无显著差异,可见大分割放疗模式在抑制乳腺癌生长的同时,不增加远期放射性肺纤维化的发生。
综上所述,大分割放疗能显著降低乳腺癌合并糖尿病患者近期放射性肺炎的发生、减轻放射性肺炎严重程度,同时并不增加远期肺纤维化的发生。
