奥氮平对男性精神分裂症患者生殖功能的影响
2020-03-19冯晓薇刘婷朱倩芸
冯晓薇,刘婷,朱倩芸*
(1.武汉市优抚医院精神科,武汉 430022;2.长江航运总医院妇产科,武汉 430000)
精神分裂症是一种多因素的、慢性、重型、易复发的精神疾病,发病率约为0.6%,男性发病率约在1.0%左右[1],患者需进行长期的抗精神病药物治疗[2]。随着精神科药理学的不断进步,非典型抗精神病药物已成为抗精神病治疗的首选,与传统药物相比具有较少的锥体外系副作用,且能够有效控制精神分裂症思维贫乏、情感淡漠、意志减退、社会性退缩等阴性症状。有研究显示,此类药物作用于中枢神经系统对男性生殖功能有负面效应[3],但其对男性生殖功能的确切影响及其机制研究相关报道仍然较少。奥氮平是一种非典型抗精神病药物,具有良好的治疗效果,已经普遍应用于精神分裂症患者的治疗。除了能阻断五羟色胺(5-HT)和多巴胺D2受体,奥氮平还对胆碱能M1、组胺H1、5-HT2C、5-HT3、5-HT6、肾上腺素能α1、D1和D4受体有特异性作用,并且对5-HT的阻断作用比多巴胺受体的阻断作用强8倍[4]。本文通过比较男性精神分裂症患者给予奥氮平治疗前后生殖激素水平和精液常规参数的变化,以期探讨奥氮平对男性生育功能产生的影响。现报道如下。
一、资料与方法
1.研究对象:采用回顾性研究设计,选取2016年6月至2018年12月在我院精神科确诊为精神分裂症的男性患者47例为研究对象。纳入标准:(1)符合《精神疾病诊断与统计手册》第5版(DSM-5)中关于精神分裂症的诊断标准;(2)年龄24~45岁;(3)入组前3个月内无任何抗精神病药物使用历史;(4)已生育。排除标准:(1)既往被诊断患有其他疾病者,如:心血管疾病、肿瘤、呼吸系统疾病等;(2)患有不孕症及相关疾病者;(3)过去2周内使用了任何其他药物。
2.研究方法:(1)治疗方案:初次纳入研究对象时询问基本信息,如:年龄、身高、体重、教育程度、生育史、患病史、服药史,并进行DSM-5及阳性和阴性症状评定量表(PANSS)评估。患者均给予单一的非典型抗精神病药物奥氮平(欧兰宁,江苏豪森药业集团,规格10 mg,批准文号:H20010799)口服治疗,治疗时间为3个月。(2)观察指标:治疗前后分别评估PANSS量表,检测血清卵泡刺激素(FSH)、黄体生成素(LH)、睾酮(T)、泌乳素(PRL)、雌二醇(E2)以及精液常规、精子DNA碎片化指数(DFI)。(3)诊断及量表评估:安排2名从事精神科5年的专业医师同时对患者进行诊断及评估。PANSS的作用是总体评定精神分裂症的严重程度,以及分别评定各个精神症状的有无和严重度。PANSS的组成由阳性量表7项(P分)、阴性量表7项(N分)、一般精神病例量表16项(G分)和补充项目评定攻击危险性3项(S分)组成。PANSS每个项目都有定义和具体的评分标准,按精神病理水平递增分为“无”到“极重度”共7级,分别对应1分到7分。总分为30项的总得分,3个补充项目一般不计入总分。(4)标本采集方法:晨起空腹,抽静脉血3~8 ml,将血清及时分离之后获得血清标本。禁欲3 d,排空小便,清洗外生殖器,消毒处理后,采用手淫法收集精液标本。(5)激素检测:FSH、LH、T、PRL和E2采用化学发光法进行检测,该化学发光仪(ADVIA Centaur XP)和试剂盒由西门子公司生产和提供。(6)精液分析与DFI检测:精液液化后,按世界卫生组织(WHO)精液分析指南第5版分析各项参数指标。精子DNA碎片率检测方法为精子染色体扩散实验,严格按说明书操作。结果判断:在常规显微镜下统计约400个精子中大、中、小光晕,无光晕和退化的异常精子的百分率。DFI实际上为小光晕精子、无光晕精子和退化精子占实际精子总数的百分比。
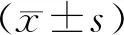
二、结果
1.治疗前后患者的一般资料及PANSS评分比较:本研究纳入患者的平均年龄(26.3±8.5)岁、体重指数(BMI)(22.4±2.2)kg/m2、受教育程度平均(12.5±3.8)年、平均病程(38.7±19.1)个月、治疗前PANSS评分(89.2±13.6)分,奥氮平使用剂量(13.9±5.0)mg。治疗过程中,有4例患者出现头晕、睡眠增多,有6例患者出现双上肢肌张力增高、双手细颤、静坐不能等锥体外系副作用,给予相应短暂的药物处理,或者将奥氮平减量,副作用均得到改善。所纳入患者中未出现停药及退出研究的患者。另外,27例患者治疗后出现不同程度的体重增加,治疗后平均BMI(25.1±2.5)kg/m2,显著高于治疗前(P<0.05)。治疗3个月后PANSS评分(56.6±14.7)分,与治疗前比较显著降低(P<0.05)。所有患者治疗期间多数时间在封闭式住院环境中,仅2例患者主动表示性欲减退、性冲动减少,未随访到明显的生殖内分泌相关改变,用药期间所纳入患者的妻子均无妊娠者。
2.所纳入患者治疗前的性激素水平情况:本研究纳入患者治疗前血清T水平为(16.8±6.0)nmol/L,显著高于检验科正常男性标准;血清E2水平为(79.4±11.6)pmol/L,显著低于检验科正常男性标准(P均<0.001);FSH水平为(5.6±2.2)U/L、LH(4.6±2.0)U/L、PRL(10.9±2.3)ng/ml,与检验科正常男性标准比较无显著性差异(P>0.05)。精液常规总活动率[(72.8±19.5)%]显著低于WHO精液检查正常参考值(P<0.001),精液量[(2.1±0.6)ml]、精子密度[(88.3±40.5)×106个/ml]、前向运动率[(54.2±7.7)%]和正常形态率[(11.1±1.2)%]与WHO精液检查正常参考值比较无显著性差异 (P>0.05)。
3.治疗前后患者血清性激素水平、精液常规参数及DFI等指标比较:与治疗前比较,所纳入患者治疗后血清T水平显著下降,PRL水平显著升高(P<0.001),FSH、LH和E2水平无显著性差异(P>0.05)。药物治疗后精子密度、前向运动率、总活动率和正常形态率均显著低于治疗前(P<0.001),精液量与治疗前比较无显著性差异(P>0.05)。药物治疗后精液DFI显著高于治疗前(P<0.001)(表1)。另外,治疗后血清T水平[(14.1±6.9) nmol/L]与检验科正常男性标准比较无显著性差异(P>0.05)。
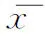
表1 治疗前后患者血清性激素水平、精液常规参数及DFI比较(±s)
注:与治疗前比较,*P<0.001
三、讨论
抗精神病药物可能影响下丘脑-垂体-性腺轴的各个环节。本研究纳入的47例男性精神分裂症患者在服用奥氮平3个月后血清T水平较治疗前显著降低(达到正常男性标准),PRL水平显著升高(P<0.001)。抗精神病药物的使用可以提高PRL水平,可能导致机体生殖内分泌轴的相关功能障碍[10];亦有文献显示奥氮平使用后PRL水平增高,导致溢乳及性功能障碍[11]。PRL升高可诱导对促性腺激素的抑制,从而抑制FSH、LH和T[12],血清T水平降低[13]。PRL可能干扰睾丸对促性腺激素的反应,导致T分泌减少,它还能抑制5-α-还原酶,而这是T转化为更具生物活性的二氢睾酮所必需的酶[14]。
奥氮平可使小鼠生精小管直径和上皮高度降低,而生精小管直径和上皮高度是精子发生活性评价的相关参数,经奥氮平治疗后小鼠生精活性降低,对精子发生产生不利影响[15]。在大鼠的动物实验中也发现,奥氮平与生精小管生殖细胞中的多巴胺受体结合,对精子发生产生直接作用[16]。提示奥氮平可通过降低T水平或直接作用于生殖细胞对精子发生产生双重影响。精子DFI可影响精子活力及活动率,DFI 越高其活力、活动率越低。本研究中,使用奥氮平治疗后的患者精子DFI升高,同时精子密度、前向运动率、总活动率及正常形态率下降,与Varghese等[17]研究一致,进一步证明奥氮平对精子质量有不利影响。
综上所述,非典型抗精神病药物奥氮平可通过影响下丘脑-垂体-性腺轴,导致患者PRL水平升高,T水平下降;同时,奥氮平可能直接或间接影响睾丸精子发生,导致精子质量下降、DFI升高,继而引起生殖能力下降。未来需要进一步研究奥氮平对男性生殖系统影响的生物学机制及其对生育力甚至子代的影响。
