芪黄疽愈方对ASOLE大鼠肝脏脂质代谢相关因子表达的影响❋
2020-03-13葛建立张敏妹何建明李晓东马云龙孙云朝楚信强白建英
张 静,葛建立,张 欣,张敏妹,何建明,李晓东,马云龙,孙云朝,楚信强,白建英
(1.河北中医学院,石家庄 050200;2.河北省中医院,石家庄 050011;3.石家庄市中医院,石家庄 050051)
下肢动脉硬化闭塞症(arteriosclerosis occlusive disease of the lower extremities,ASOLE)是动脉硬化在下肢的特殊表现[1-2]。动脉硬化发病原因及形成机制复杂[2-4],肝脏B类Ⅰ型清道夫受体(scavenger receptor class b type Ⅰ,SR-BⅠ)、过氧化物酶体增殖物激活受体(peroxisome proliferator-activated receptor,PPAR)-α、单核细胞趋化蛋白1(monocyte chemotactic protein-1,MCP-1)等对动脉硬化的形成具有重要调控作用[5-7]。课题组既往的临床研究证实[8],芪黄疽愈方能够有效改善ASOLE患者临床症状,但具体生物学机制尚不明确。本研究以ASOLE大鼠为实验对象,通过观察芪黄疽愈方对肝脏SR-BⅠ、PPAR-α、MCP-1等因子表达的影响,探讨其治疗ASOLE的分子生物学机制。
1 材料
1.1 动物
清洁级Wistar大鼠58只,9±1个月龄,体质量200±20 g,由河北医科大学实验动物中心提供,合格证号1704031,由河北中医学院实验楼喂养。饲养环境为独立的不锈钢通气笼,每笼5只,动物房温度23 ℃~25 ℃,相对湿度40%~70%,明暗光照各12 h交替进行。实验用普通全价颗粒饲料和高脂饲料均购自河北医科大学实验动物中心。本实验已通过河北中医学院实验动物伦理委员会审查。
1.2 药物
芪黄疽愈方中药饮片由红花、鸡血藤、海藻、浙贝母、鬼箭羽、虫、延胡索、黄芪、黄精、牛膝组成,由国药乐仁堂石家庄药材有限公司生产;维生素D3针剂由上海通用药业股份有限公司生产。
1.3 试剂
兔抗SR-BⅠ一抗(Abcam,货号:ab52629);山羊抗兔二抗-HRP(Easybio,货号:BE0106);ECL显色试剂盒(Thermo,货号:34094);PPAR-α酶联免疫检测试剂盒、MCP-1酶联免疫检测试剂盒,货号:ml0045637、ml0022423,购自上海纪宁实业有限公司。
1.4 仪器
Western Blot电泳仪基础电源 PowerPacTMBasic(BIO-RAD公司);近红外双色激光成像系统(Odyssey公司);HBS-1096C Pro自动酶标仪(上海珂淮仪器有限公司)。
2 方法
2.1 动物分组及造模
动物适应性喂养1周后,随机取10只作为正常组,余下大鼠采用高脂饮食加隐动脉内膜损伤的方法[9]制作ASOLE模型。1%戊苯巴比妥钠(1 ml/200 g)腹腔注射麻醉,左后肢消毒,从腹股沟中点向后肢内侧纵行切开皮肤,分离并暴露隐动脉,用动脉夹阻断隐动脉远近端约1.8±0.1 cm,取胰岛素注射器1支,沿隐动脉血管长轴由远端向近端刺入血管腔,将0.25 mL注射用无菌蒸馏水缓慢注入阻断部位血管,5 min后取下针头和动脉夹,压迫止血并缝合切口。并在实验开始时在大鼠右下肢肌肉注射维生素D3针剂(3×105u/kg),每隔30 d重复1次。采用随机数字表法将ASOLE大鼠分为模型组、芪黄疽愈方高浓度组、中浓度组、低浓度组各12只。实验期间模型组和中药组持续高脂饲料(83.5%基础饲料,5%猪油,1%胆固醇,0.5%胆酸钠及10%蛋黄粉[10])喂养,空白组普通饲料喂养,均自由饮水。
2.2 给药方法
芪黄疽愈方组成:红花12 g,鸡血藤15 g,海藻12 g,浙贝母12 g,鬼箭羽12 g,虫9 g,延胡索12 g,黄芪20 g,黄精12 g,牛膝9 g。按原方的组方比例,并根据体表面积比率折算出200 g大鼠的等效用药剂量作为其用量,另取其1/2剂量和2倍剂量作为芪黄疽愈方低浓度和芪黄疽愈方高浓度组。由河北省中医院煎药室煎制,4 ℃冰箱保存1周内使用;芪黄疽愈方中浓度组的药物最终浓度0.4 g生药/mL,低浓度组0.2 g生药/mL,高浓度组0.8 g生药/mL,实验过程中每次中药制剂均按同一标准进行。
造模后1周,模型组和中药组(芪黄疽愈方低浓度组、中浓度组、高浓度组)分别给予生理盐水(1 ml/100 g)或相应浓度中药灌胃(1 ml/100 g),每日1次,连续12周,空白组大鼠则不予处理。
2.3 标本采集及处理方法
取材前夜禁食水。10%水合氯醛溶液(0.3 ml/100 g)腹腔麻醉,剪开皮肤摘取肝脏组织,切割标本后,一部分匀浆充分后离心20 min左右(2000~3000 r/min),仔细收集上清液用于ELISA检测;一部分直接装入冻存管中,-80 ℃保存,待行Western印迹法检测。
2.4 指标检测
2.4.1 一般状态 观察大鼠的一般状态,包括精神状态、毛色、活动灵敏度、饮食、饮水及体质量。
2.4.2 Western印迹法测定肝脏SR-BⅠ表达 制备SDS-PAGE胶板,根据蛋白定量结果,加入相应体积的总蛋白样品与5×蛋白质凝胶电泳上样缓冲液混合,于95 ℃变性10 min后迅速置于冰水中冷却,依次加样。恒压电泳,恒流湿转,封闭1 h后依次与一抗(兔抗SR-BⅠ,1∶1000稀释)孵育过夜,洗涤后放入二抗(山羊抗兔)孵育1 h,曝光显色后扫描处理,所得条带吸光度值分别与对应内参计算比值获得相对吸光度值[11-12]。
2.4.3 ELISA法检测肝脏PPAR-α、MCP-1表达 根据试剂盒说明书严格操作,采用ELISA法检测肝脏PPAR-α、MCP-1表达水平。加样、加酶、温育(37 ℃,60 min)配液,洗涤、显色(37 ℃,15 min)、终止,450 nm波长检测吸光度值(OD值)[13]。
2.5 统计学方法

3 结果
3.1 大鼠一般状态
实验发现,空白组大鼠毛色光泽,活动灵敏,饮食、饮水量正常,体质量随饲养时间延长而增加;模型组、中药组大鼠在最初1个月增长迅速,后增长速度减缓,其精神萎靡,活动欠灵敏,毛色暗淡,食量相对正常组也减少。直至实验药物干预12周结束时,除模型组、中药低浓度组各死亡1只外,其余各组均无大鼠死亡。
3.2 各组大鼠肝脏组织SR-BⅠ表达水平比较
图1示,与空白组比较,模型组SR-BⅠ的表达明显降低;与模型组比较,中药各浓度组SR-BⅠ的表达明显升高,且SR-BⅠ的表达水平随中药浓度增加而升高。
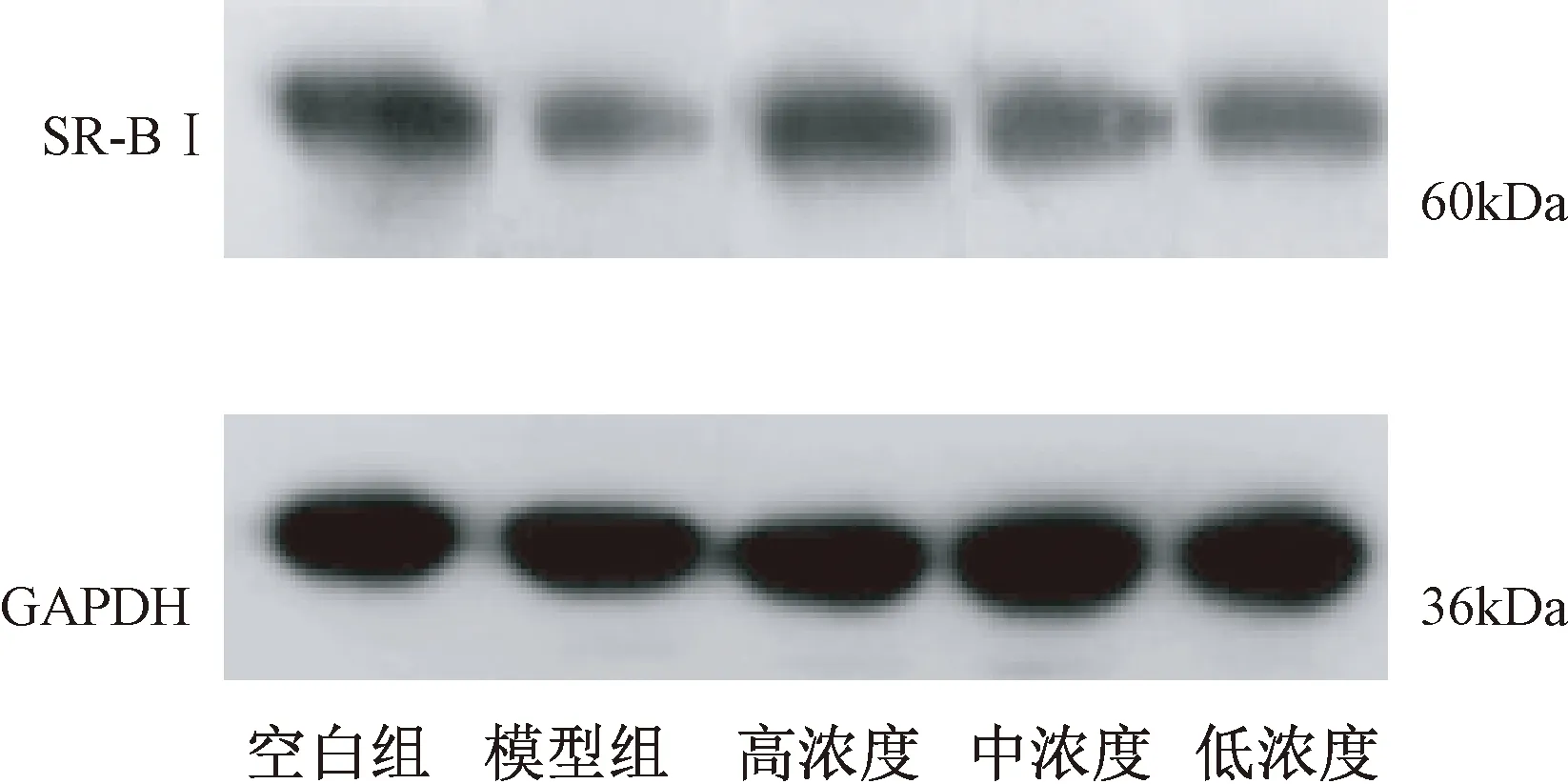
图1 各组大鼠肝脏组织SR-BⅠ蛋白免疫印迹条带图
3.3 各组大鼠肝脏组织PPAR-α、MCP-1水平比较
与空白组比较,模型组大鼠肝脏PPAR-α显著性下降(P<0.01)。中药处理有效升高大鼠肝脏PPAR-α水平,效果与药物浓度呈正相关;高、中浓度组较模型组显著性升高(P<0.01),低浓度组较模型组虽有上升但无统计学意义。
与空白组比较,模型组大鼠肝脏MCP-1显著性上升(P<0.05)。中药处理有效降低大鼠肝脏MCP-1水平,效果与药物浓度呈正相关;高浓度组较模型组显著性降低(P<0.01),中、低浓度组较模型组虽有下降但差异无统计学意义(见表1)。

表1 各组大鼠肝脏组织PPAR-α、MCP-1检测结果比较
4 讨论
脂代谢异常导致高炎症状态是动脉硬化形成的核心机制[3、14]。肝脏是机体调节血脂水平的主要脏器之一[5、15-17],通过调节血脂改变机体炎症状态是其参与动脉硬化形成、预防、治疗的重要机制[3、14、18]。肝脏SR-BⅠ、PPAR-α、MCP-1在调节血浆胆固醇、脂肪酸等血脂水平及机体炎症状态中发挥了重要作用。SR-BⅠ参与肝细胞选择性摄取血浆结合胆固醇(主要为高密度脂蛋白胆固醇),也是协助肝细胞将代谢后的胆固醇通过胆汁,经胆道、肠道排出体外的重要分子[5、17]。肝细胞内活化的PPAR-α通过调节参与脂肪酸转运、结合、活化过氧化物酶和线粒体的脂肪酸β氧化的相关基因,促进脂肪酸的摄取、利用和分解代谢[6、19]。MCP-1具有趋化单核细胞等功能[20、21]。单核-巨噬系统具有转运血脂的功能,同时也是参与炎症的重要细胞[7]。因而,肝脏SR-BⅠ、PPAR-α、MCP-1在调节血脂、降低机体炎症水平、抗动脉硬化中扮演着重要角色。
高脂饮食加隐动脉内膜损伤是目前较为成熟且被广泛接受研究ASOLE的模型方法[9]。本实验利用该模型研究芪黄疽愈方治疗ASOLE的作用机制。模型组血管壁结构破坏且显著性增厚,可见泡沫细胞浸润血管壁等,基本符合动脉硬化的病理表现,验证了此方法的有效性。进一步实验发现,芪黄疽愈方显著性升高肝细胞SR-BⅠ、PPAR-α表达,降低肝脏MCP-1水平。结合课题组既往的研究报道[22],即调节血脂参与芪黄疽愈方治疗ASOLE的机制,说明调节肝脏SR-BⅠ、PPAR-α、MCP-1表达应是其调节血脂降低机体炎症状态,治疗ASOLE的具体机制之一。
本病属于中医学“脱疽”范畴。中医认为,癥积阻络不通、气血周流受阻是导致ASO的病机关键,故治疗ASOLE需以消癥通络为基本法则。目前研究证实,活血、消癥、通络、益气的单味中药具有抗动脉硬化、促进下肢血液循环的作用。药理学研究表明,红花主要成分为羟基红花黄色素A等,可以降低胆固醇,防止动脉硬化及机体代谢紊乱[23-24]。鸡血藤醇提物有较好的调节血脂和抗脂质过氧化作用[25];浙贝母能降低全血黏度,抑制红细胞聚集[26];海藻可有效提高高密度脂蛋白水平,加速低密度脂蛋白代谢,阻止氧化低密度脂蛋白所引发的对内皮细胞的损伤[27]。“芪黄疽愈方”是本院治疗ASOLE的经典方剂,方中红花、鸡血藤活血化瘀通络,浙贝母、海藻化痰散结,四药合用消癥通络为君药;鬼箭羽、虫、延胡索协助主药增强活血化瘀之效为臣药;黄芪、黄精益气养阴固本为佐药;使以牛膝引血下行。诸药合用,标本兼治,使癥积得化,经络畅通,诸症悉除。早期临床应用“芪黄疽愈方”治疗ASOLE取得了满意疗效,但作用机理不明。课题组在前期临床研究的基础上,以“芪黄疽愈方”对ASOLE大鼠进行干预,进一步检测组方药效,探讨作用机理。结果表明,芪黄疽愈方能够有效促进SR-BⅠ蛋白表达,升高PPARα,降低MCP-1,通过调节脂质代谢、降低炎症反应,治疗ASOLE,但其深入的作用机制尚待进一步探讨。
