“多酸对维生素C光谱检测”的实验教学探究*
2020-02-09王晓红段莉梅白锁柱刘宗瑞
王 斌,王晓红,段莉梅,2,白锁柱,许 良,刘宗瑞
(1 内蒙古民族大学化学化工学院,内蒙古 通辽 028043; 2 化学国家级实验教学示范中心(内蒙古民族大学),内蒙古 通辽 028000)
多金属氧酸盐(简称多酸)是由过渡金属W、Mo、V、Nb、Ta等元素的酸式盐脱水缩合而成的金属-氧配位簇合物,具有组成元素丰富、明确的晶体结构、纳米尺度可调控(0.3~6 nm)以及可逆的氧化还原、光、电、磁等优良性质,使其在催化、能源、材料、医学等领域有广泛的应用前景[1-2]。此外,多酸在光能、电能、热能、化学能等外界刺激下会发生可逆的氧化还原性质,并伴随着颜色的可逆变化,而自身结构不发生任何改变,使其成为一类性能优异的刺激响应功能分子[3-6]。
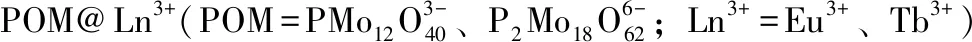
本文中以具有可逆氧化还原及可逆变色性质的Dawson型多酸(NH4)6P2Mo18O62(P2Mo18)为无机功能分子,在还原剂维生素C、氧化剂H2O2的作用下实现了多酸P2Mo18可逆的化学响应变色性质;在此基础上利用紫外-可见光谱仪对VC进行定量检测,获得维生素C检测的线性方程、检出限及检测范围,并对该检测方法的响应时间、选择性及可重复使用性进行研究。通过全面、系统的实验训练,使学生对一般无机化合物结构表征、性质研究、分析检测过程及因素考察有初步的认识;进而全面培养了学生分析问题和解决问题、实际应用、科研创新等能力。
1 实 验
1.1 实验药品及仪器
钼酸钠,维生素C(VC),H2O2(质量分数为30%),草酸,L-丙氨酸,甘氨酸,葡萄糖,D-麦芽糖,浓磷酸(质量分数为85%),氯化铵,浓硫酸(质量分数为98%),硫酸钠等均为分析纯,购买于国药集团化学试剂有限公司。实验过程中使用的纯净水由Millipore Milli-Q净化水系统处理(18.2 MΩ·cm),电化学测试用pH=1的0.5 mol/L H2SO4/Na2SO4缓冲溶液的配制过程如下:在搅拌下将0.5 mol/L H2SO4逐滴加入0.5 mol/L Na2SO4溶液中,直至混合溶液的pH=1为止。
DF-101S集热式磁力搅拌器,河南巩义市予华仪器有限责任公司;PHS-3E酸度计,上海仪电科学仪器股份有限公司;Nexus470傅里叶变换红外光谱仪,美国Nicolet仪器公司;激光拉曼光谱仪,英国Renishaw公司;UV-670紫外-可见分光光度计,上海美普达仪器有限公司;CHI660e电化学工作站(采用三电极体系玻碳为工作电极,铂丝为对电极,Ag/AgCl为参比电极),上海辰华仪器有限公司。
1.2 P2Mo18的合成
根据文献报道的方法合成了Dawson型多酸(NH4)6P2Mo18O62·11H2O[12],具体合成步骤如下:首先,将10 g Na2MoO4·2H2O溶于45 mL纯净水中,在搅拌下将1.5 mL浓磷酸、8 mL浓盐酸依次加入上述溶液中,搅拌回流2 h;然后,待反应溶液冷却至室温后,将10 g NH4Cl加入到上述溶液中便有大量黄绿色沉淀生成,经过减压过滤获得粗产物;最后,将粗产物加入20 mL 40 ℃的水中溶解,然后将溶液置于冰水浴中进行结晶,20 min后有大量黄绿色棒状晶体析出,减压过滤收集晶体产物4.86 g,产率为68.58%(以Na2MoO4·2H2O计算)。
1.3 P2Mo18的结构
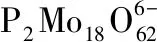
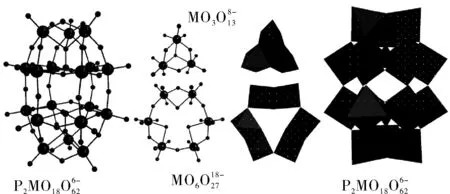
图及的球棍模型和多面体结构
2 结果与讨论
2.1 P2Mo18的红外及拉曼光谱表征
利用红外光谱及拉曼光谱对P2Mo18的结构进行表征,在红外光谱中波数为1074、998、937、902、821和762 cm-1处出现了Dawson型磷钼酸盐的特征吸收峰,分别归属于P-Oa、Mo-Od、Mo-Ob和Mo-Oc的对称或不对称伸缩振动吸收。同时,在拉曼光谱中波数为967 cm-1和703 cm-1处出现了Dawson型磷钼酸盐的特征散射峰,分别归属于Mo=Od、Mo-Ob,c-Mo的伸缩振动吸收。各特征吸收峰与文献报导一致,表明已成功合成了目标多酸化合物(NH4)6P2Mo18O62[12]。
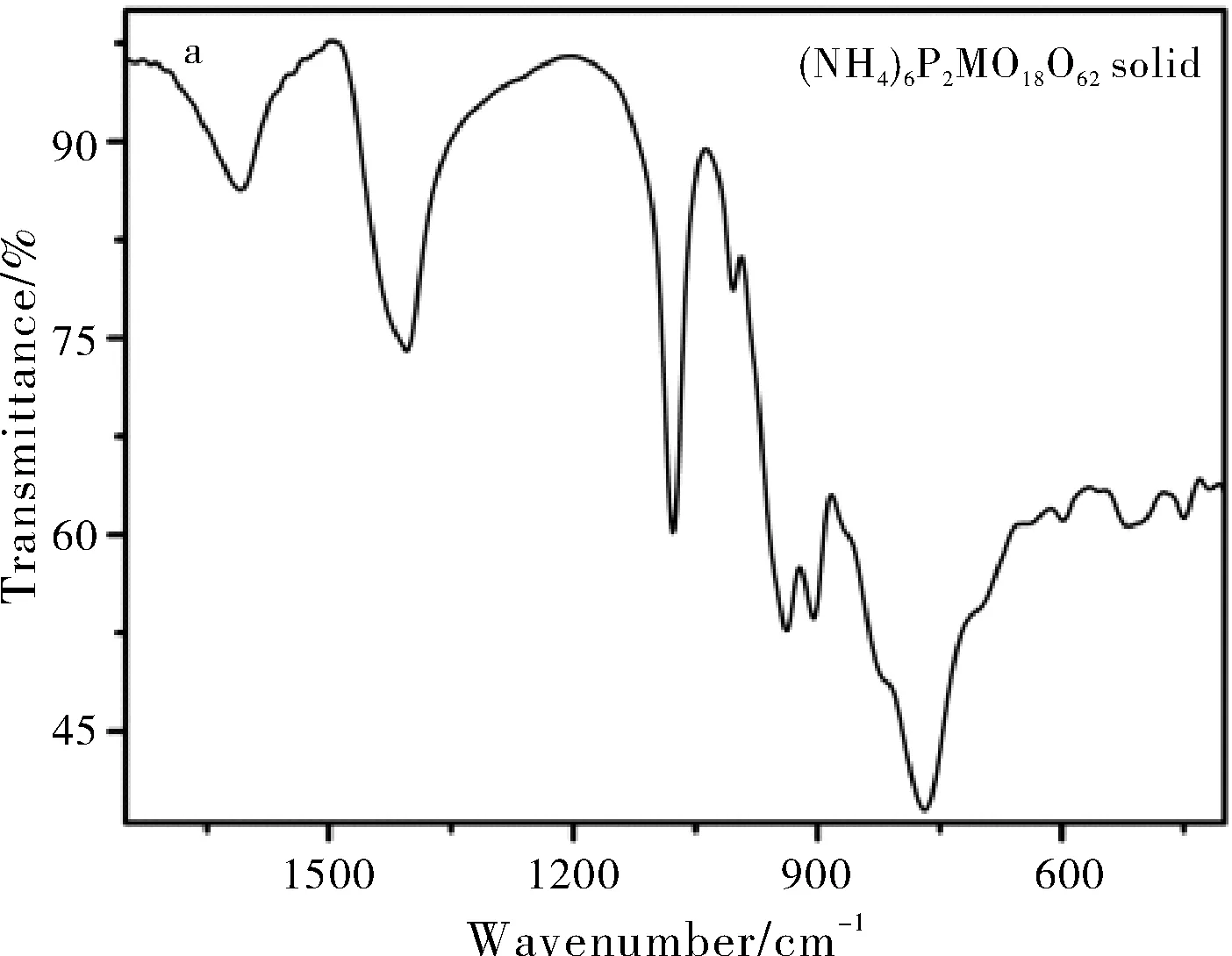
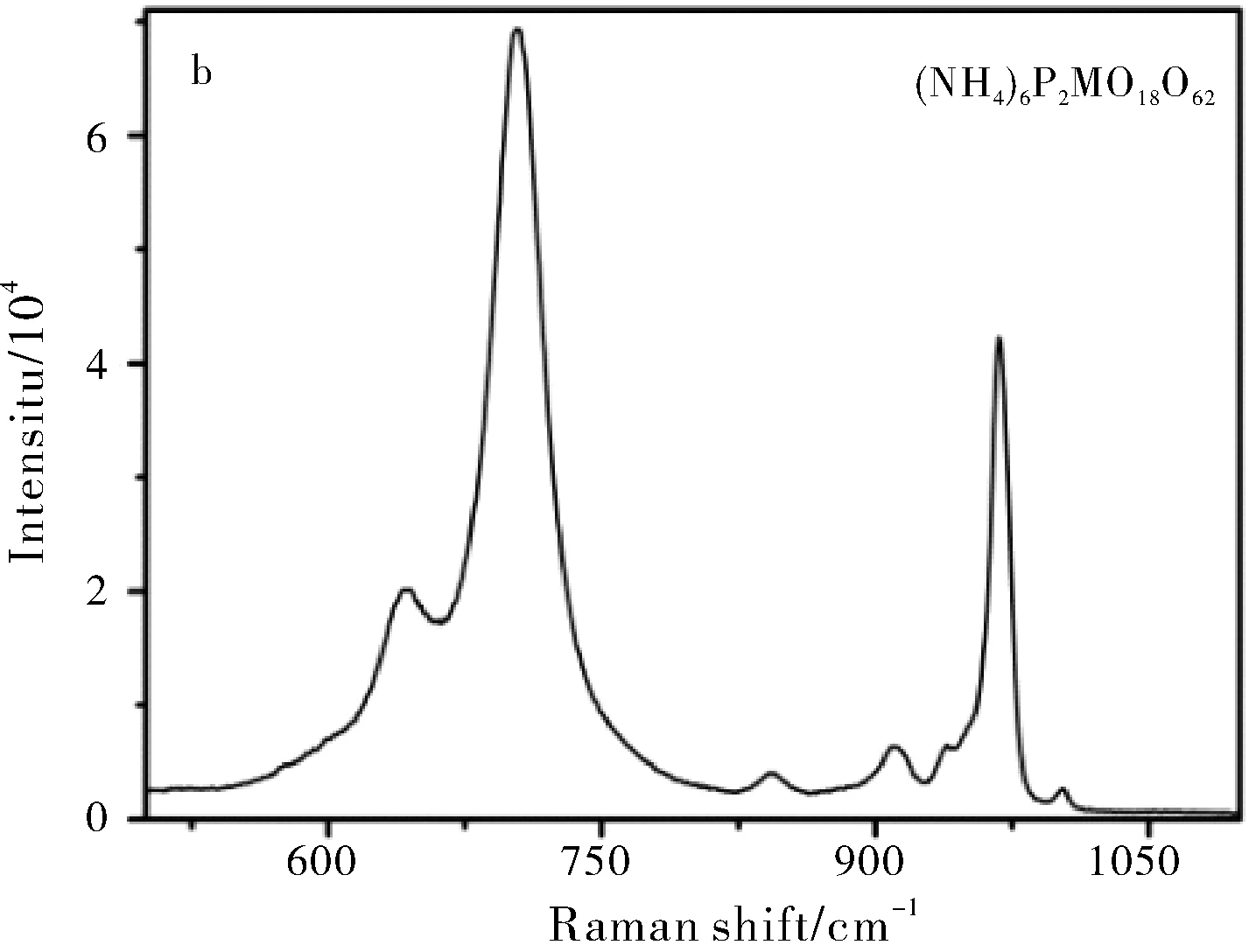
图2 P2Mo18的红外光谱(a)及拉曼光谱(b)
2.2 P2Mo18的紫外-可见光活性
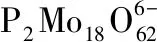
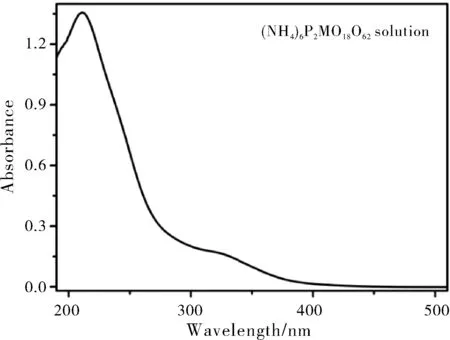
图3 P2Mo18的紫外-可见光谱
2.3 P2Mo18的电化学氧化还原性质
图4为1 mmol/L P2Mo18在pH=1,0.5 mol/L H2SO4/Na2SO4缓冲溶液中的循环伏安曲线,在E1/2=(Epa+Epc)/2为0.40 V(I-I`)、0.25 V(II-II`)、0.08 V(III-III`)、-0.22 V(IV-IV`)处呈现出4对Dawson型多酸的特征氧化还原峰(其中Epa为阳极峰电位,Epc为阴极峰电位),分别对应于P2Mo18中Mo6+/Mo5+的1 e、1 e、2 e、2 e转移过程[14],表明P2Mo18可以发生可逆的氧化还原反应。
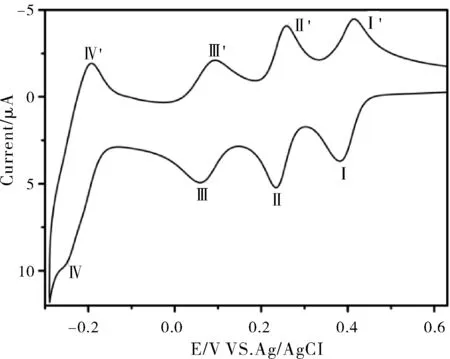
图4 P2Mo18在扫描速度为50 mV/s下的循环伏安曲线
2.4 P2Mo18溶液对维生素C的紫外-可见光谱检测
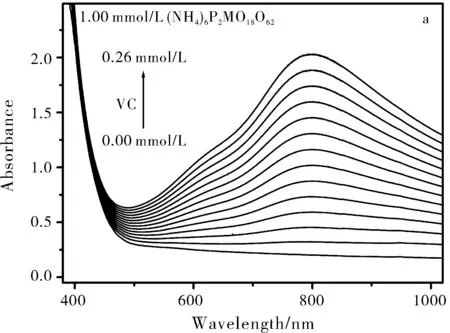
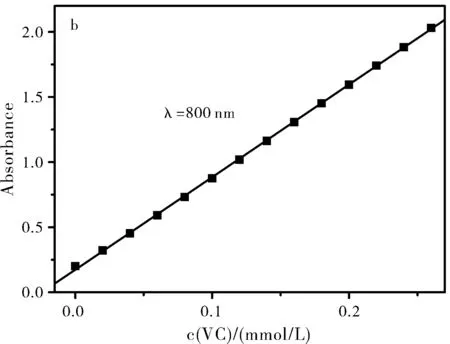
图5 不同浓度VC下P2Mo18溶液的紫外可见光谱(a)及800 nm处吸光度对VC浓度作图(b)
利用紫外-可见光谱对VC的浓度进行定量检测,向50 mL 1 mmol/L的P2Mo18溶液中依次等量加入50 μL 0.02 mol/L的VC,溶液中P2Mo18被还原由浅黄色变为蓝色,伴随着在可见区800 nm附近出现宽的吸收峰,归属于Mo6+/Mo5+分子内价电子转移吸收(Intervalence charge transfer,IVCT),随着溶液中VC浓度的增大,800 nm附近的吸收峰逐渐增强(见图5A)。以800 nm 处的吸光度对VC浓度作图,获得该方法对VC检测的线性方程A=7.1127c+0.1732(线性相关系数R2=0.9998)(见图5B),检出限CL=kSN/m=3.39×10-3μmol/L(其中置信因子k=3;标准偏差为SN=8.0753×10-6;斜率m=7.1127 L/mmol),检测范围为3.39×10-3μmol/L~0.26 mmol/L。
3 P2Mo18溶液对维生素C检测性能探讨
3.1 响应时间
利用紫外-可见动力学模式对VC检测的响应速度进行考察,监测800 nm处的吸光度随反应时间的变化,在每次等量加入0.02 mmol/L的VC时800 nm处的吸光度迅速增大,54 s后吸光度不再变化,表明反应达到平衡;同时发现反应平衡时的吸光度随着VC浓度的增大呈阶梯式等间距增大,且每次加入VC的响应时间均为54 s。该检测体系具有响应时间短,能够在较短的教学时间内完成,因此能够应用于分析检测相关的实验教学中。
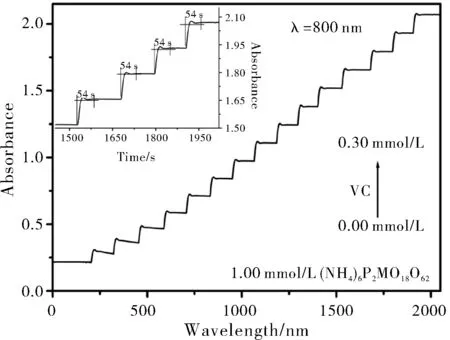
图6 不同浓度VC下P2Mo18溶液800 nm处的吸光度随时间的变化曲线
3.2 选择性

图7 VC、草酸、甘氨酸、丙氨酸、葡萄糖、麦芽糖与P2Mo18混合溶液的紫外-可见光谱
利用紫外-可见光谱对VC检测的选择性进行研究,分别将0.30 mmol/L的VC、草酸、甘氨酸、丙氨酸、葡萄糖、麦芽糖加入50 mL 1 mmol/L的P2Mo18溶液中,发现只有加入VC后800 nm附近出现宽的吸收峰,表明生物体内可能存在的草酸、甘氨酸、丙氨酸、葡萄糖、麦芽糖对VC检测没有干扰(见图7)。该方法对VC检测具有较高的选择性,可以作为分析检测实验教学过程中选择性考察的典型案例。
3.3 可重复使用性
利用紫外-可见动力学模式对VC检测的可重复使用性进行考察,向50 mL 1 mmol/L P2Mo18溶液中加入0.26 mmol/L的VC时,P2Mo18被还原溶液由浅黄色变为深蓝色、吸光度逐渐增大;相反,加入0.792 mmol/L H2O2时,P2Mo18被重新氧化溶液由深蓝色变为浅黄色、吸光度逐渐降低。在5次循环加入VC、H2O2后,溶液着色及褪色平衡时的吸光度没有明显的变化,表明该检测体系可以重复使用(见图8)。
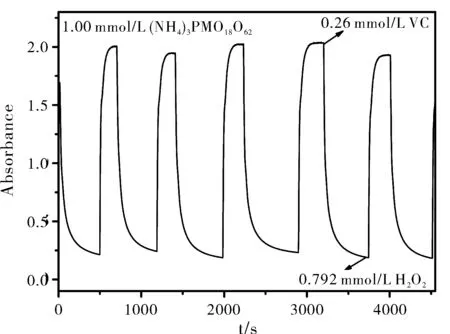
图8 在VC、H2O2循环刺激下P2Mo18溶液800 nm处吸光度随时间的变化曲线
4 结 论
通过常规水溶液合成方法及FTIR、Raman、UV-Vis、CVs等表征手段表明已成功合成了Dawson型多酸(NH4)6P2Mo18O62。基于P2Mo18可逆的氧化还原及变色性质,利用P2Mo18溶液对VC进行紫外-可见光谱检测,该方法对VC检测的线性方程为A=7.1127c+0.1732(R2=0.9998),检出限为3.39×10-3μmol/L;紫外-可见动力学结果表明该体系可重复使用、响应时间为54 s,此外该方法对VC检测具有较高的选择性。
将“多酸(NH4)6P2Mo18O62制备及其对维生素C光谱检测”用于综合实验教学中有以下优点:
(1)多酸化合物合成过程简单、产率高及仪器表征多样化,能够适用于不同高校的教学条件;
(2)基于该紫外-可见光谱法对VC检测具有检出限低、响应速度快、选择性高、可重复使用等优点,可以作为无机分析综合化学实验教学的典型案例;
(3)通过系统性的结构表征、光谱检测及数据处理,能够全面培养学生的实际应用、科学创新、分析问题和解决问题的能力。
