钠—葡萄糖协同转运蛋白-2抑制剂对2型糖尿病患者内脏脂肪面积的作用
2020-02-04黄海儒黄广龙吴志全
黄海儒 黄广龙 吴志全 冯 琨
1 佳木斯大学,黑龙江省佳木斯市 154007; 2 广东省东莞市塘厦医院; 3 黑龙江省医院
随着中国人民生活水平的提升,人群中超重和肥胖率也是逐年上升,国内外已有大量研究显示超重和肥胖是2型糖尿病(T2DM)的独立危险因素。与欧美等国家相比,我国更多的是内脏脂肪型肥胖[1]。内脏脂肪积累容易导致T2DM、高血压、高血脂、冠心病等疾病的发生发展。目前临床上兼具良好降糖减重效果且副作用少的药物稀缺。SGLT2i是一种抑制肾脏重吸收葡萄糖、增加尿糖含量、降低血糖的新机制降糖药,降糖的同时可以减轻体重[2]。因为CT或MRI扫描检查具有辐射、操作烦琐、费用高等原因,所以目前国内SGLT2i对内脏脂肪面积作用研究很少。欧姆龙HDS-2000是一种利用脂肪不导电的原理,采用生物电阻抗技术精确测量人体内脏脂肪及皮下脂肪的仪器,与以往测量方法(CT)相比,测量结果更精准,并且具有无辐射、费用低、可重复型强、操作方便等优势[3]。现在使用HDS-2000作为测量内脏脂肪面积的先进手段已逐渐被接受。本研究主要通过观察SGLT2i对T2DM患者VFA作用,并且探讨内脏脂肪与皮下脂肪等相关性,为临床工作提供参考价值。
1 对象与方法
1.1 研究对象 选取2018年9月—2019年3月在黑龙江省医院住院治疗的T2DM患者78例,其中男43例,女35例,年龄28~70岁,符合1999年WHO糖尿病诊断标准。入选标准:入院前HbA1c>6.5%,2hPBG≥10mmol/L,肾小球滤过率(eGFR)≥60ml/min。排除标准:T1DM(1型糖尿病)、GDM(妊娠糖尿病)和继发糖尿病患者;合并各种急慢泌尿系感染、手术外伤患者;合并糖尿病急性并发症,如:DKA(酮症酸中毒)、非酮症高渗状态患者;合并严重心、肝、肾功能不全患者;合并免疫系统、血液系统、恶性肿瘤患者。本研究经医院伦理委员会批准,研究对象均签署知情同意书。
1.2 研究方法
1.2.1 用药方法:所有患者经糖尿病教育,严格糖尿病饮食控制配合适当运动,原有“二甲双胍(澳大利亚艾华大药厂),500mg,tid,po”及“来得时(赛诺菲安万特制药有限公司),每天睡前皮下注射,剂量随空腹血糖值适当调整”治疗方案不变基础上,患者加用恩格列净(勃林格殷格翰制药公司),10mg,qd,清晨空腹口服,持续12周。
1.2.2 主要指标:每隔4周随访1次,分别测量第0周及4周、8周、12周后身高、体重、腰围、臀围等,每个数值测量3次取平均值。计算BMI、WHR。内脏脂肪面积及皮下脂肪面积测量:同日空腹采血后,静息,10min,平躺、用日本欧姆龙DHS-2000检测。
1.2.3 次要指标:分别检测第0周、12周FBG、2hPG、HbA1c、TC、TG、HDL-C、LDL-C、肌酐(CREA)、UA、UREA、谷丙转氨酶(ALT)、谷草转氨酶(AST)。禁食12h后于次日清晨空腹采集肘静脉血,采用美国贝克曼库尔特AU5800全自动生化分析仪检测。

2 结果
入组78例患者,完成回访62例(男35例、女27例)。其中3例因泌尿系感染停药,1例因过敏停药,12例因其他原因未完成回访。
2.1 主要指标 第12周与第0周相比,VFA减少28.82cm2(P<0.05),SFA减少8.87cm2(P<0.05),同时VFA减低幅度为22.19%明显比SFA的4%幅度大。体重减少3.46kg(P<0.05)、BMI较前减少0.91(P<0.05)、腰围减少3.66cm(P<0.05)、臀围及腰臀比差异无统计学意义(P>0.05),见表1。VFA及体重均在第0~4周变化趋势大,第4~12周变化趋势较前变小,但总趋势仍是继续下滑。SFA则是总体减低趋势(见图1)。VFA与SFA、BMI、体重具有中度正相关性,与腰围具有弱正相关性,同时与臀围、WHR无相关性(见图2)。

表1 VFA与主要指标
注:VFA:内脏脂肪面积;SFA:皮下脂肪面积;BMI:体质指数;WHR:腰围/臀围比值。
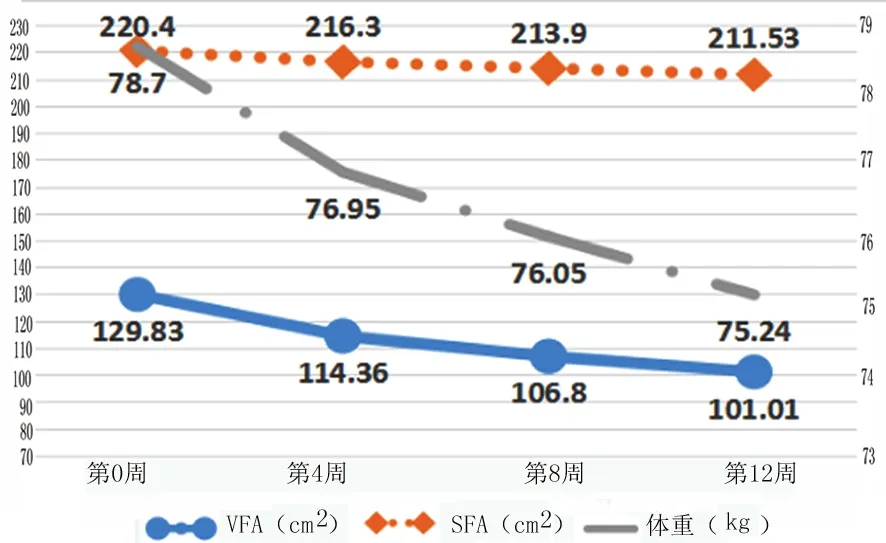
图1 VFASFA及体重变化趋势
2.2 次要指标 FBG、2hPG、HbA1c、TC、TG、UA、UREA、AST均较前显著降低(P<0.05)。HDL-C较前升高(P<0.05)。LDL-C亦较前升高,且差异无统计学意义(P=0.578>0.05)。见表2。
2.3 并发症情况 服药期间未发生低血糖、酮症酸中毒、过敏等急性并发症。3例患者发生泌尿系感染(P>0.05),停药后,经常规口服抗生素治疗后症状即可缓解。1例患者服药1周后出现皮疹伴瘙痒症状(P>0.05),停药及抗过敏治疗后症状缓解。
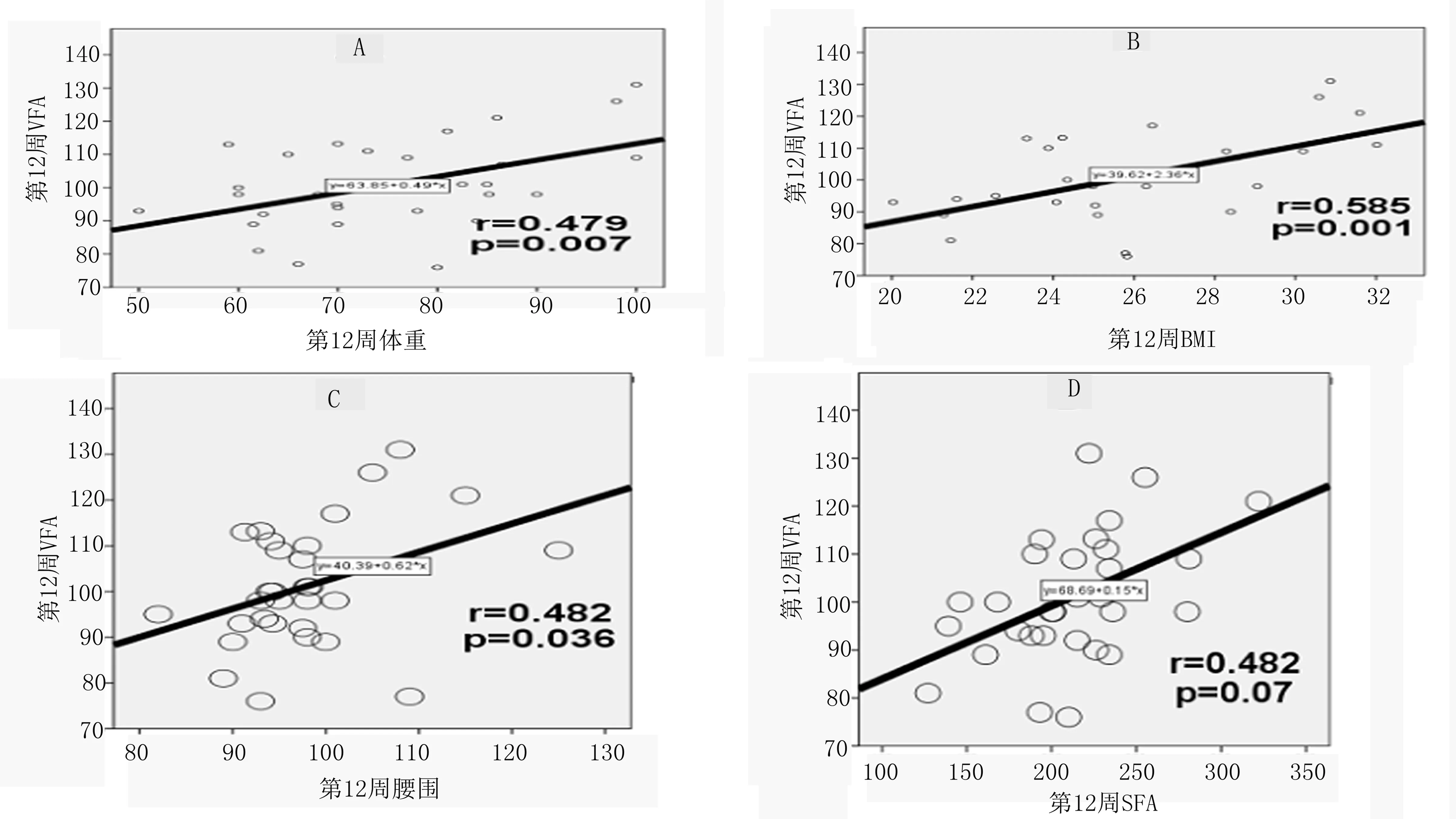
图2 VFA与各项指标相关性分析

表2 一般观察指标
3 讨论
以BMI=24为中国成人超重的界限,BMI=28为肥胖的界限;男性腰围≥90cm,女性腰围≥85cm为腹型肥胖(内脏脂肪型肥胖)。腹型肥胖是多种慢性病的最重要危险因素之一,特别是T2DM的强烈独立危险因子。前瞻性队列研究已经确定腹型肥胖与T2DM之间存在独立的正向关联,腰围每增加1cm,糖尿病发病风险增加6%[4]。换言之,减少内脏脂肪面积,不仅可以减少高血压、冠心病等疾病风险,也可以有效降低发生糖尿病风险[5-6]。
SGLT-2 抑制剂拥有独特的非胰岛素依赖性降糖机制:通过抑制近90%经过肾脏肾小管近曲小管的重吸收,增加尿液葡萄糖含量,降低血糖[7]。大量研究表明SGLT2i不仅有降糖作用,Lavalle-González等52周的双盲、随机实验表明与GLP-1受体激动剂相比,SGLT2i显著降低了体重[8]。Henry等的双盲、随机实验亦显示达格列净(Dapagliflozin)单用或与二甲双胍联合使用,与单用二甲双胍相比,不仅能降低血糖及HbA1c,而且减重效果是单用二甲双胍的2倍[9]。本研究通过分析显示在原基础治疗上加用SGLT2i后体重亦明显较基线减少3.46kg(4.3%,P<0.05),与上述研究相符。日本学者的一项24周随机、双盲、临床实验,49例T2DM患者原有胰岛素治疗基础上随机分为ipragliflozin(ipra)组和安慰剂组,结果相比安慰剂组0.22kg,ipra组体重平均减少2.78kg。值得注意的是体重的减少,其中80%是内脏脂肪的减少[10]。Yokono等认为SGLT2i能减低血糖,改善胰岛素抵抗,增强脂肪酸化产生能量,降低内脏脂肪[11]。本研究发现服用SGLT2i后BMI基线越大者,减重效果越明显。同时结果显示内脏脂肪面积基线水平越高,减少效果较前越明显,并且内脏脂肪面积减少量较皮下脂肪面积明显大。据此推测SGLT2i通过肾脏排出葡萄糖,降低血糖时,造成机体负能量平衡,根据人体能量消耗次序,优先消耗脂肪,脂肪酸化产热保持能量平衡、维持血糖稳定。中国流行病学调查显示女性肥胖率更高,女性脂肪更多堆积在臀部、大腿、腹部,形成全身性肥胖,男性则更多趋向于腹部堆积形成腹型肥胖[4-5,12]。从本研究男女性别差异性分析发现,服用SGLT2i后男性减重和内脏脂肪面积减少效果均较女性好。可能原因是与流调相比,本研究男性BMI和内脏脂肪面积更高,并且男性日常体力活动程度较高,消耗能量更多,服用SGLT2i后血糖降低,胰高血糖素分泌增加,刺激肝脏—脑—脂肪神经通路对蛋白激酶A(PKA)对蛋白质磷酸化及脂肪酸化增强,能量代谢途径改变,消耗更多脂肪供热,产热增多,维持能量平衡及血糖稳定[13]。然而值得注意的是,2例患者出现VFA不降反升现象,Ferrannini及Perkins等研究报道认为SGLT2i可以刺激能量摄入,以补偿因尿糖引起的热量损失,这足以抵消因尿中热量损失引起的体重下降[14-15]。据此推测患者初始VFA(<100cm2)并未达到肥胖标准,SGLT2i作用下损失过多能量,机体的自我保护机制,神经体液负反馈调节激活,拮抗VFA减少,保存能量维持机体生理活动,具体机制仍需完善后续研究验证。相关研究显示,SGLT2i患者初始期体重、脂肪减少是由渗透性利尿及能量损失所致,后续由脂肪逐渐减少导致体重长期缓解的减少[16]。换言之早期SGLT2i至患者早期体重快速减轻是因体内体液的快速减少,后续机体达到体液平衡,则由消耗脂肪供能,至体重减轻。本研究第4周体重、VFA减少速度较第8周、第12周快,符合上述研究结果,与之前报道一样[17],本研究FBG、2hPG、HbA1c、TC、TG、CREA、UA、UREA、AST均较前显著降低。HDL-C、LDL-C亦较前升高,具体机制未明,考虑体液丢失、机体脱水至血液浓度增加所致[16]。本研究4例泌尿系感染患者均为女性,已有报道显示与女性尿道生理解剖特点有关,并且早期尿道排出尿液含糖量高,易感染细菌[18]。
综上所述SGLT-2抑制剂可以显著减少T2DM患者内脏脂肪面积,对皮下脂肪亦有减少作用。同时对体重、FBG、2hPG、HbA1c、TC、TG、CREA、UA、UREA、AST亦有显著积极作用。
