氨基功能化介孔硅吸附剂的制备及其对铬(Ⅲ)的吸附行为
2020-01-15肖昱郭宇吴红梅姜晓庆
肖昱,郭宇,吴红梅,姜晓庆
(辽宁工业大学化学与环境工程学院,辽宁锦州121001)
铬(Ⅲ)是人体中必不可少的微量元素,它对调节糖代谢、维持体内正常的耐量起重要作用,能影响机体的脂质代谢,降低血中胆固醇和甘油三酯的含量[1-2]。然而,过多地摄入铬(Ⅲ)会引发糖尿病和动脉硬化等疾病,严重的甚至可以致癌[3-4]。近年来,随着电镀、化工、皮革、印染等工业的发展,越来越多的未处理的含铬(Ⅲ)废水被排放,致使水体受到了不同程度的污染。铬(Ⅲ)通过食物链在生物体中逐步浓缩富集,富集系数可高达几万倍,严重影响到人类的身体健康。而且,铬(Ⅲ)在一定条件下还能转化成毒性更强的铬(Ⅵ),对人体产生更大的危害[5-9]。因此,含铬(Ⅲ)重金属离子的废水处理已经迫在眉睫。目前,去除水中重金属离子的方法主要有过滤法、蒸馏法、吸附法、沉淀法和半透膜法等[10-13]。其中,吸附法因具有效率高、成本低、一般不与吸附质和介质发生化学反应和良好的力学性能等优点被广泛使用。吸附剂的种类有很多,较为常见的吸附剂有各种活性炭吸附剂、活性氧化铝、沸石分子筛、硅胶、天然黏土等[14-17]。SBA-15 作为一种介孔硅材料,不仅具有孔道结构高度有序、比表面积大、孔壁厚度可控等优点,而且合成条件要求低、水热稳定性好。这一系列的特性使其在吸附分离领域具有广泛的应用价值[18]。
SBA-15 介孔硅材料表面的硅羟基具有一定的化学反应活性,利用这一特性,可以对SBA-15介孔分子筛进行不同的官能团修饰,例如,—COOH、—SH 和—NH2等[19-22],从而提高其对重金属离子的吸附。然而,尽管各种官能团修饰的SBA-15 介孔硅材料体现出较高的吸附能力,但在铬(Ⅲ)离子吸附方面的报道较少。基于此,本论文利用3-氨丙基三甲氧基硅烷对SBA-15介孔分子筛进行氨基功能化,获得对铬(Ⅲ)离子具有良好吸附能力的氨基改性介孔硅吸附剂,详细研究其对铬(Ⅲ)离子的吸附行为,为其应用提供科学基础。
1 实验试剂和方法
1.1 实验试剂
三嵌段共聚物(P123),西格玛奥德里奇(Sigma-Aldrich)公司;正硅酸乙酯(TEOS),天津市科密欧化学试剂有限公司;盐酸(37%),沈阳试剂四厂;3-氨丙基三甲氧基硅烷(APTMS,98%),国药集团化学试剂有限公司;六水氯化铬,天津市天力化学试剂有限公司;无水乙醇,天津市科密欧化学试剂有限公司;去离子水,自制。以上均为分析纯。
1.2 氨基功能化介孔硅吸附剂的合成
称取2g 的P123,溶于62mL 盐酸(2mol/L)和8.61mL 去离子水中,在40℃下磁力搅拌使其完全溶解,然后在充分搅拌下逐滴加入4.2mL的TEOS,持续搅拌8h后放入不锈钢反应釜中,在100℃烘箱中晶化24h。取出冷却,用去离子水洗涤、抽滤至pH 为7。将得到的白色粉末在100℃下过夜干燥。将上述白色粉末在550℃下放入马弗炉中煅烧6h,去除模板剂,获得SBA-15 介孔分子筛[23]。将2g SBA-15 介孔分子筛加入盛有120mL 无水乙醇的圆底烧瓶中,在N2保护下,逐渐滴加2mL的APTMS,回流24h 后,即得到氨基功能化的介孔硅吸附剂(NH2-SBA-15)。
1.3 样品表征
采用日本日立S-4800 型扫描电子显微镜(SEM)分析样品的表面形貌。利用日本JEOL JEM 2010 型透射电子显微镜(TEM)观察介孔硅吸附剂的孔道结构。使用日本理学D/Max2400 Rigaku型X 射线衍射仪(XRD)分析样品的晶型结构。使用美国Micromeritics ASAP 2020 气体吸附仪(BET)测定样品的比表面积和孔结构参数。通过美国赛默飞ESCALAB 250Xi 型X 射线光电子能谱(XPS)和能量色散X 射线光谱仪(EDX)测定样品表面化学性质。采用美国PerkinElmer SAT8000型热重分析仪(TG)分析样品的热稳定性。
1.4 吸附性能测试
50mL 的20mg/L 的铬(Ⅲ)溶液置于放有50mg 吸附剂的锥形瓶中,在一定的温度下,水浴振荡。吸附一定时间,在转速9000r/min下离心10min,取上层清液,利用原子吸收光谱测定剩余铬(Ⅲ)的浓度,并按照式(1)和式(2)计算出对铬(Ⅲ)的吸附率R与吸附容量Q。
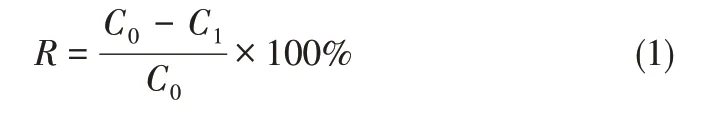
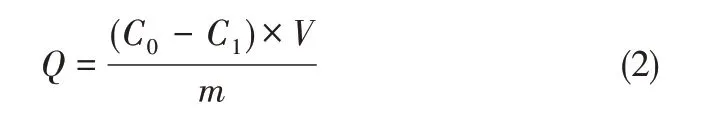
式中,C0,C1分别为吸附前后浓液的浓度,mg/L;V为体积,L;m为吸附剂质量,g。
2 实验结果与讨论
2.1 样品表征
图1(a)是NH2-SBA-15 的SEM 图片。从图1(a)可以看出,NH2-SBA-15 颗粒呈棒状,是典型的SBA-15 分子筛形貌。而且通过XRD 表征分析可知,NH2-SBA-15 在2θ<2.5°之前存在3 个明显的特征衍射峰[见图1(b)],所对应的衍射面分别为(100)、(110)和(200)晶面[24],说明所合成的NH2-SBA-15具有典型的二维六方介观结构特征衍射峰。图1(c)为NH2-SBA-15 的TEM 图。由图1(c)可见所合成的NH2-SBA-15的孔道结构规整,且排列规则有序,孔径大小约为8nm。为了确定NH2-SBA-15表面元素分布情况,利用EDX 对其进行了分析,见图1(d)。由图中可以看出样品中不仅含有C、O和Si元素,而且含有N元素,说明 NH2被成功嫁接到SBA-15 上。另外,通过BET 测试(表1)可知,SBA-15的比表面积和平均孔径分别为757m2/g和9.69nm;当表面功能化后,所获得的NH2-SBA-15 的比表面积和表面平均孔径明显变小,分别为585m2/g 和6.54nm,上述BET 分析结果同样说明了SBA-15分子筛已被氨基功能化。

表1 样品的孔结构分析
图2 是NH2-SBA-15 的XPS 谱图。由图2 中可以看出,NH2-SBA-15 表面存在的元素主要为Si、C、O 和N。在结合能为153eV、102eV、284eV 和533eV处分别出现了Si2s、Si2p、C1s和O1s的特征峰。通过XPS 谱图可知,在399.5eV 处存在N1s 的特征峰,归属于—NH2的特征峰,这与文献报道的结果一致[25-26],进一步证明了APTMS 成功嫁接到SBA-15表面。

图3 SBA-15和NH2-SBA-15的热重分析
图3(a)是SBA-15 和NH2-SBA-15 的TG 曲 线。由TG曲线可以看出,随着温度的升高,SBA-15和NH2-SBA-15 的质量均有显著降低。当温度升到800℃时,SBA-15 的质量损失为6.99%,这是由于样品脱水和脱表面羟基导致的[24]。与SBA-15 相比较可知,由于NH2-SBA-15表面官能团的损失,造成NH2-SBA-15 的质量损失明显增大,为14.62%。NH2-SBA-15的质量损失主要分为两个阶段:第一阶段(30~240℃),样品质量损失了3.82%;第二阶段(240~800℃),样品质量损失了10.80%。通过DTG曲线[图3(b)]可以看出,SBA-15的损失速率比较平缓。然而,NH2-SBA-15样品的DTG曲线出现了两个峰:1#峰在280℃,这是由于APTMS中未与羟基键结合的Si OCH3的分解;2#峰出现在530℃,是由于APTMS中与羟基键结合的 NH2CH2CH2CH2的分解。上述测试结果同样证明了APTMS 成功嫁接到SBA-15 上,与EDX 和XPS 分析结果相吻合。而且,热重测试结果说明了所合成的NH2-SBA-15具有很好的热稳定性。
2.2 吸附剂用量对吸附铬(Ⅲ)的影响
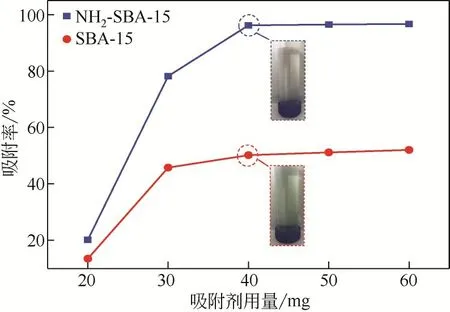
图4 吸附剂用量对吸附铬(Ⅲ)的影响
图4 是不同吸附剂用量对铬(Ⅲ)吸附性能的影响,其中铬(Ⅲ)溶液浓度20mg/L,吸附温度50℃,吸附时间6h,溶液pH为6。由图4可知,当吸附剂用量小于40mg 时,随着NH2-SBA-15 吸附剂用量的增加,铬(Ⅲ)吸附率显著提高,由20%提高至95%。这主要是由于随着吸附剂的增加,吸附位点逐渐增多,有利于铬(Ⅲ)的吸附。当继续提高吸附剂用量时,铬(Ⅲ)吸附率没有明显变化,说明此时吸附剂上的作用位点与溶液中铬(Ⅲ)含量已经达到平衡。NH2-SBA-15 对铬(Ⅲ)的吸附率(95%)远高于SBA-15(56%)。而且,经NH2-SBA-15 吸附后,铬(Ⅲ)溶液的颜色从绿色变为为无色。然而,SBA-15 吸附铬(Ⅲ)后,溶液的颜色为浅绿色,进一步说明了NH2-SBA-15 的吸附能力要高于SBA-15。不仅如此,利用EDX对吸附铬(Ⅲ)后的样品进行表面元素分析(图5),同样可以清楚地看到,NH2-SBA-15 表面所吸附的铬(Ⅲ)浓度高于SBA-15表面的铬(Ⅲ)浓度。
为了进一步分析NH2-SBA-15 对铬(Ⅲ)的吸附作用,研究吸附铬(Ⅲ)前/后NH2-SBA-15 表面的化学状态。图6(a)给出了NH2-SBA-15 吸附铬(Ⅲ)前/后样品的XPS 全谱扫描图。吸附铬(Ⅲ)后的NH2-SBA-15(Cr-NH2-SBA-15)在结合能为576.8eV和586.8eV 处出现了Cr2p1/2和Cr2p3/2谱峰,见图6(b),说明铬(Ⅲ)被NH2-SBA-15 成功吸附。图6(c)和图6(d)分别为NH2-SBA-15和Cr-NH2-SBA-15的N1s谱图。吸附铬(Ⅲ)后,N1s 结合能从399.5eV 提高至399.8eV,这主要归因于N 原子和铬(Ⅲ)配位后,N原子贡献电子给金属离子,自身电子密度降低,导致结合能增加。图6(e)和图6(f)分别为NH2-SBA-15和Cr-NH2-SBA-15 的C1s 光 谱。NH2-SBA-15 的C1s 谱图包括2 个峰,分别归属于C C(284.8eV)和C N(286.2eV)。吸附铬(Ⅲ)后,Cr-NH2-SBA-15谱图中,C C没有发生变化,而C N(285.8eV)的结合能下降。
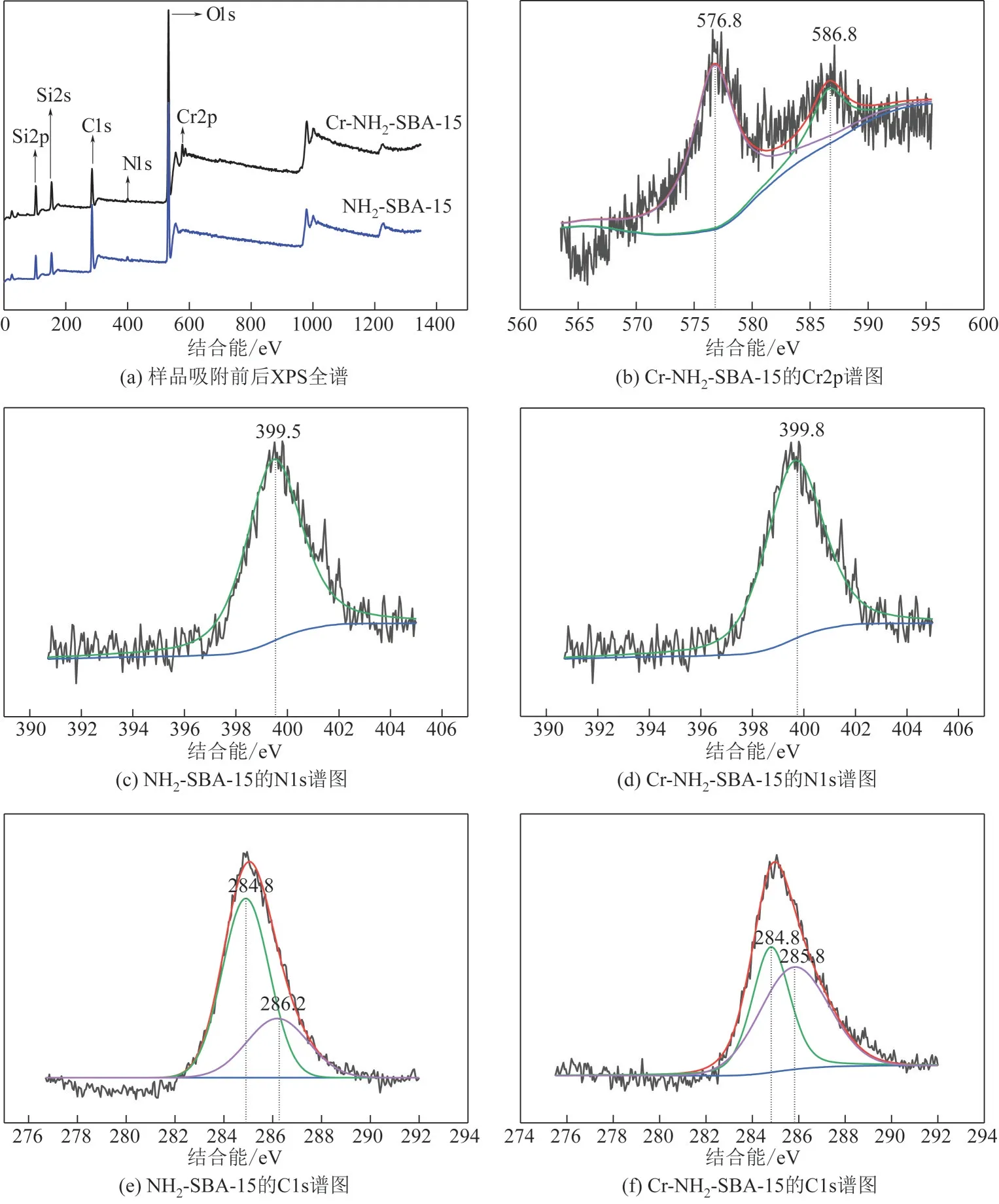
图6 NH2-SBA-15吸附铬(Ⅲ)前/后的XPS谱图
2.3 温度对吸附铬(Ⅲ)的影响
图7 是温度对NH2-SBA-15 吸附铬(Ⅲ)性能的影响,其中铬(Ⅲ)溶液浓度20mg/L,吸附剂用量为50mg,吸附时间6h,溶液pH 为6。由图中可以看出随着温度的升高,铬(Ⅲ)去除率逐渐增大。当温度达到50℃时,铬(Ⅲ)去除率达到最大。这是因为随着温度的逐渐升高,分子扩散运动越来越剧烈,铬(Ⅲ)离子更容易在分子筛孔道内扩散,从而与吸附位点发生充分反应,吸附位点逐渐被铬(Ⅲ)占据。上述结果说明,该吸附行为为吸热过程,升高温度有利于吸附。

图7 温度对吸附铬(Ⅲ)的影响
2.4 pH对吸附铬(Ⅲ)的影响
在吸附过程中,溶液pH 是影响吸附效果的重要因素之一[27-28]。图8是在溶液pH对NH2-SBA-15吸附铬(Ⅲ)性能的影响,其中铬(Ⅲ)溶液浓度20mg/L,吸附剂用量为50mg,吸附时间6h,吸附温度50℃。当pH<4 时,铬(Ⅲ)主要以Cr3+和Cr(OH)2+形式存在,溶液中存在大量的H+,由于NH2-SBA-15中 NH2的N 有1 对孤对电子而显弱碱性,能够与H+发生反应,生成—N+H3,使吸附剂表面带正电,从而与电性相同的铬(Ⅲ)离子发生排斥过程,使得吸附性能降低。当进一步提高溶液pH,NH2-SBA-15吸附剂对铬(Ⅲ)的吸附率显著提高。这是由于当4<pH<6 时,溶液中Cr3+随着pH 的升高会逐渐转变Cr(OH)2+、Cr(OH)2+的形式,溶液中阳离子所带的电荷逐渐减少,受H+影响所产生的排斥作用减弱,从而使其吸附性能提高。然而,当pH>6 时,铬(Ⅲ)溶液中开始产生Cr(OH)3沉淀,这与文献报道的一致[29]。

图8 pH对吸附铬(Ⅲ)的影响
2.5 吸附等温线
为了明确吸附机理,采用Freundlich 模型[式(3)]和Langmuir模型[式(4)]拟合吸附等温数据来描述NH2-SBA-15吸附剂在固-液体系中的吸附行为。
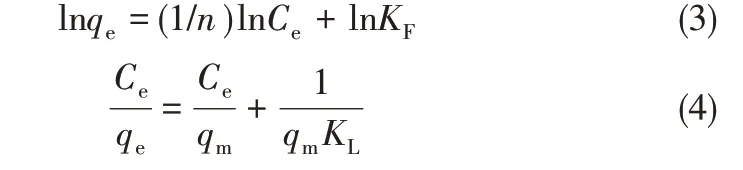
式中,Ce为平衡吸附浓度,mg/L;qe为吸附质在单位质量吸附剂的平衡吸附容量,mg/g;qm为吸附质在单位质量吸附剂的最大吸附容量, mg/g;KF为Freundlich 模型的吸附平衡常数;KL为Langmuir模型的吸附平衡常数;1/n为吸附系数。
图9 为NH2-SBA-15 的吸附等温线,相关参数见表2。由拟合参数可知,采用Langmuir 模型分析时,NH2-SBA-15 对于铬(Ⅲ)吸附拟合获得的相关性系数R2均大于0.99。而且,Langmuir方程模拟所得的最大吸附量和实际的吸附容量较为接近。然而,利用Freundlich 模型拟合时,拟合结果的相关系数较低(R2<0.9),说明吸附数据更符合Langmuir 吸附等温线模型。因此,NH2-SBA-15 吸附铬(Ⅲ)的过程属于单分子层吸附。KL通常能够揭示吸附过程的难易程度,KL>1或KL<0难吸附,KL=1线性吸附,KL<1 易吸附,KL=0 不可逆吸附。本实验吸附过程中,KL的数值都在0~1 之间,说明吸附过程属于易吸附过程[30]。
2.6 吸附热力学
为进一步研究温度对NH2-SBA-15 吸附铬(Ⅲ)的影响,通过计算吸附过程中的吉布斯自由能(ΔG)、焓变(ΔH)和熵变(ΔS)等热力学参数,分析吸附剂对铬(Ⅲ)的吸附作用力和性质,从而合理解释吸附现象。相关吸附热力学参数计算公式如式(5)~式(8)。
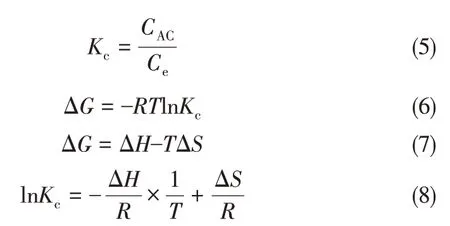
式中,Kc为浓度平衡常数;CAC和Ce分别是吸附平衡后吸附剂上与溶液中剩余的金属离子浓度;R为气体常数;T为反应热力学温度。
根据式(8)以lnKc对1/T作图可得吸附剂样品对铬(Ⅲ)的吸附热力学拟合曲线图,见图10。由拟合曲线可计算ΔH、ΔG和ΔS,计算结果如表3 所示。由计算结果可知,SBA-15 在293K、303K、313K、323K 和333K 温度下吸附铬(Ⅲ)时,ΔG均大于0,说明SBA-15 吸附铬(Ⅲ)时不能自发进行。NH2-SBA-15在不同的温度下ΔG均小于0,说明该吸附材料吸附铬(Ⅲ)是自发进行的。而且,ΔH>0 说明NH2-SBA-15 吸附铬(Ⅲ)的过程为吸热反应,升高温度有助于吸附的进行,这与图7所得出的结果一致。ΔS>0,表明在固液吸附体系中,铬(Ⅲ)吸附在NH2-SBA-15吸附剂上,自由度增加[31]。

图10 NH2-SBA-15和SBA-15对铬(Ⅲ)吸附热力学拟合曲线
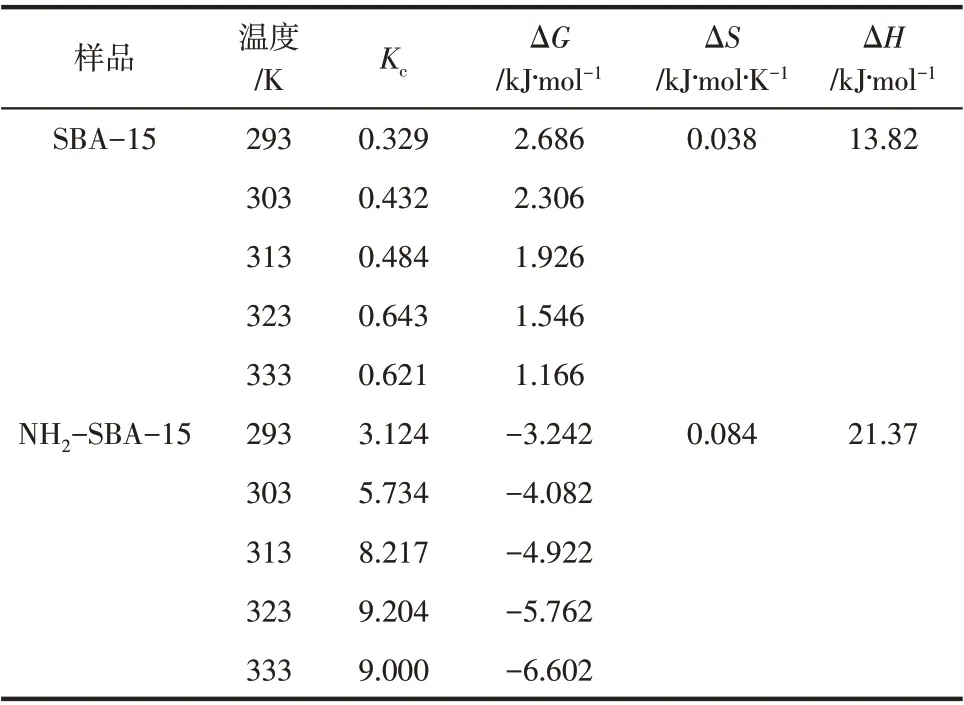
表3 吸附铬(Ⅲ)的平衡常数和热力学参数
2.7 吸附动力学
采用拟一级动力学模型方程[式(9)]、拟二级动力学方程[式(10)]对两种材料的动力学数据进行线性拟合,从而研究两种吸附剂的吸附机理和速率控制步骤。

式中,qt和qe分别为t时和平衡态时的吸附量,mg/g;K1为拟一级吸附速率常数,min-1;K2为拟二级吸附速率常数,g/(mg·min)。
图11 为吸附数据的动力学拟合结果,相关参数见表4。由图11 中可以看出,对于NH2-SBA-15,t/qt与t呈现明显的直线关系,拟二级吸附动力学方程的线性相关系数R2>0.9,高于其拟一级动力学模型。不仅如此,由表3结果可以发现,拟一级动力学模型拟合的qe与实际测定值相差较大,而拟二级动力学模型拟合的qe与实际测定值更为接近,此外,这说明NH2-SBA-15 吸附铬(Ⅲ)的过程更符合拟二级动力学模型。在NH2-SBA-15吸附铬(Ⅲ)过程中以化学吸附为主,其表面上的亚氨基中的N 作为吸附剂的吸附位点,与铬(Ⅲ)发生络合作用[32]。表5 列出了不同吸附剂对铬(Ⅲ)的吸附性能数据。对比其他吸附剂的吸附性能可知,NH2-SBA-15 吸附剂对于水溶液中铬(Ⅲ)的处理具有一定的优势。

表4 NH2-SBA-15吸附铬(Ⅲ)动力学方程回归数据
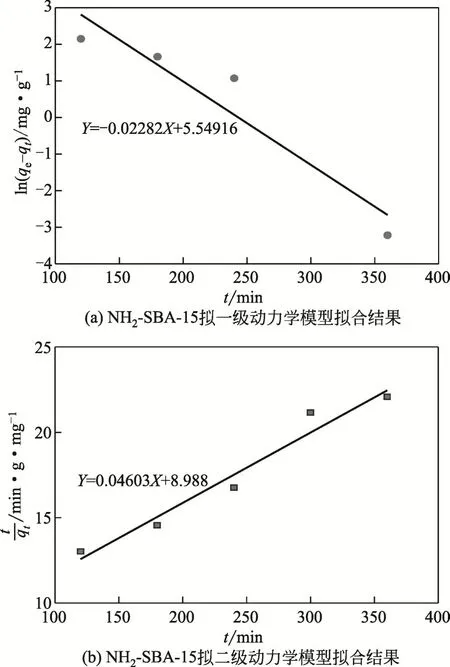
图11 样品对铬(Ⅲ)的吸附动力学分析
2.8 吸附再生性
吸附剂的再生性是吸附剂应用性能的一项重要指标。为了研究NH2-SBA-15这一特性,将吸附铬(Ⅲ)的NH2-SBA-15 置于50mL 浓度为0.1mol/L 的HNO3溶液中,室温搅拌3h,离心干燥后再吸附。
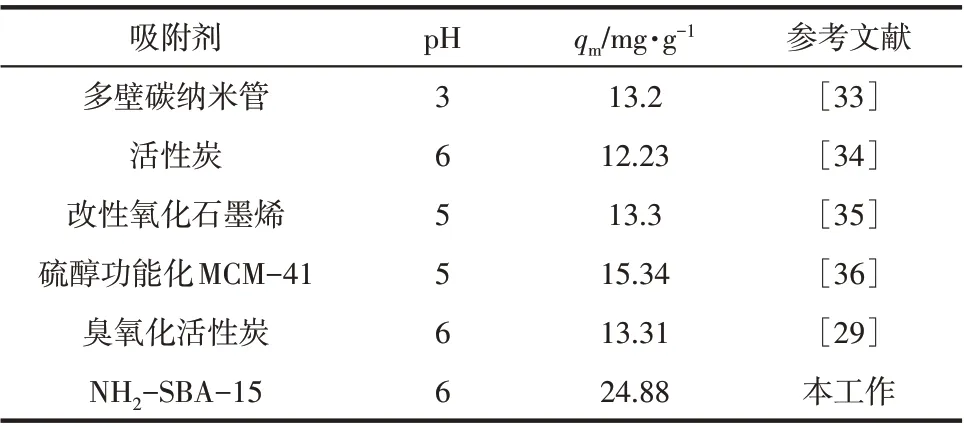
表5 各种吸附剂对铬(Ⅲ)的吸附性能数据
图12 是NH2-SBA-15 的再生性能。由测试结果可以看出,NH2-SBA-15 被重复使用5 次后,尽管其对铬(Ⅲ)的吸附率略微下降,但吸附率依然达到92.79%。这说明HNO3溶液对吸附在NH2-SBA-15 上的铬(Ⅲ)有很好的解析效果,NH2-SBA-15 具有良好的再生性能。
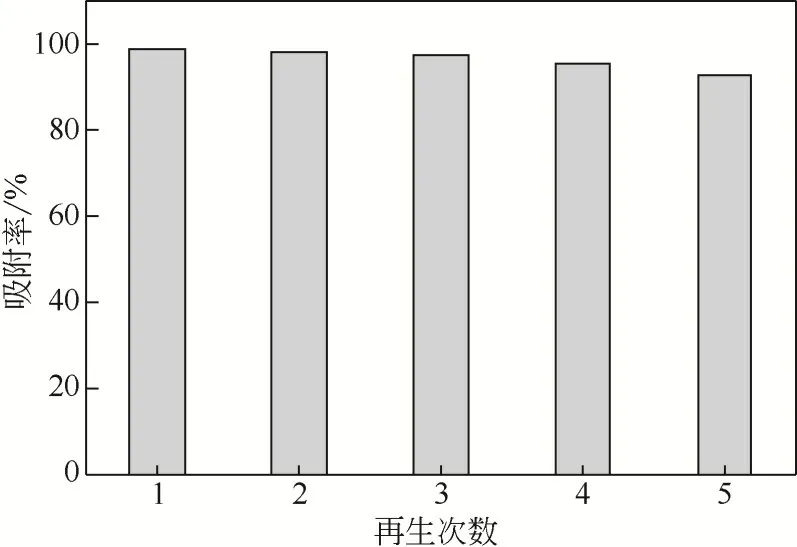
图12 NH2-SBA-15吸附剂的再生性能
3 结论
(1)APTMS 对SBA-15 实现了表面改性,使—NH2官能团成功负载到SBA-15 表面,为后续对铬(Ⅲ)的吸附提供了化学吸附位点。
(2)相比SBA-15,NH2-SBA-15 对铬(Ⅲ)的吸附能力有明显提高。NH2-SBA-15 对铬(Ⅲ)的吸附过程为吸热过程,提高温度有利于吸附;而且,溶液pH对吸附效果影响显著。
(3)Langmuir 模型能很好地描述NH2-SBA-15对铬(Ⅲ)的吸附特征,该吸附过程符合拟二级动力学模型,ΔG<0,ΔH>0,ΔS>0。
(4)利用HNO3溶液可以对NH2-SBA-15 吸附剂实现有效再生,重复使用5次后,该介孔分子筛吸附剂对铬(Ⅲ)的吸附率仍然能够达到92.79%。
