樟树籽仁油的结构和特性分析
2020-01-14冯绍贵李彦宸董春怡文学方曾哲灵
冯绍贵,李彦宸,董春怡,文学方,余 平,3,曾哲灵
(1.南昌大学资源环境与化工学院,南昌 330031; 2.南昌大学江西省药食同源植物资源高值化利用重点实验室,南昌 330031; 3.南昌大学食品科学与技术国家重点实验室,南昌 330047)
樟树(Cinnamomumcamphora(L.) Presl),又名香樟、乌樟、芳樟、樟木等,常绿高大乔木植物,属樟科樟属。我国樟树资源丰富,主要分布于长江流域及长江以南地区。樟树既是良好的绿化树种,也是价值很高的经济树种。樟树的根、茎、叶、籽皮和肉中精油含量较高,已经成为提取樟树精油的主要原料。樟树籽含樟树籽仁油40%以上,樟树籽仁油含中碳链脂肪酸95%以上,主要以癸酸(C10∶0)、月桂酸(C12∶0)为主,属于天然中碳链油脂。樟树籽仁油具有快速补充能量、显著减少体内脂肪积蓄、降低血脂血糖水平及提高胰岛素敏感性等改善体内糖脂代谢紊乱作用[1-7]。
有关樟树籽仁油甘油三酯结构研究的文献报道,至今都是依据当量碳原子数和脂肪酸组成来测定分析。本文采用高效液相色谱仪、三重串联四极杆液质联用仪,以三脂肪酸甘油酯为标样,精确测定分析樟树籽仁油的甘油三酯结构,同时测定分析樟树籽仁油的理化性质及融化结晶特性,为樟树籽仁油的后续研究开发提供理论基础。
1 材料与方法
1.1 实验材料
樟树籽,于2018年在江西省南昌市南昌大学校园内采集10个不同地点的成熟樟树籽。
乙腈、异丙醇,色谱纯,TEDIA公司;三辛酸甘油酯、三癸酸甘油酯、三月桂酸甘油酯,美国Sigma公司;盐酸、氯化钠、无水乙醚、甲醇、正己烷、无水硫酸钠,分析纯;三氟化硼甲醇溶液,德国CNW科技有限公司。
Agilent 6430三重串联四极杆液质联用仪,配自动进样系统、自动脱气系统和DAD检测器;Agilent 1260高效液相色谱仪,配蒸发光散射检测器和C.01.03 安捷伦化学工作站;Agilent 7890B 气相色谱仪;DH-50立式榨油机,乐龄市道行实业有限公司;BS223S型电子分析天平,德国赛多利斯有限公司;电热恒温水浴锅;DHG-9101-2SA电热恒温鼓风干燥箱。
1.2 实验方法
1.2.1 精炼樟树籽仁油的制备
将樟树籽去除果皮和果肉,在(40±1)℃烘至恒重,采用脱壳机脱壳得到樟树籽仁,在120~130℃下采用榨油机压榨得到樟树籽仁毛油。测定毛油酸价,然后将毛油加热至(60±1)℃,采用0.05 mol/L NaOH溶液碱炼脱酸,水洗除去皂脚,得到樟树籽仁脱酸油,再将油加热至(90±1)℃,加入油质量2%~3%的活性白土,搅拌脱色20 min,趁热真空过滤(真空度0.07~0.08 MPa),得到精炼樟树籽仁油。
1.2.2 樟树籽仁油脂肪酸组成的测定
樟树籽仁油脂肪酸甲酯化采用GB 5009.168—2016并改进方法[8]。称取30 mg油样于15 mL容量瓶中,加入3 mL 0.5 mol/L的氢氧化钠甲醇溶液,放入65℃的水浴中保持35 min,之后取出自然冷却,加入3 mL 0.5 mol/L三氟化硼甲醇溶液,随即放入70℃水浴中保持5 min,取出并自然冷却,加入3 mL正己烷,振荡1 min,最后加入6 mL饱和氯化钠溶液,取上层有机相,加入无水硫酸钠除水,用1 mL注射器吸取后过0.22 μm有机滤膜,待气相色谱分析。
sn-2位和sn-1,3位脂肪酸组成分析采用胰脂肪酶酶解法[9]。准确称量10 mg油样,加入10 mL 1 mol/L Tris-HCl缓冲液(pH 8)、2 mL 0.05%胆酸钠溶液、1 mL 2%氯化钙溶液以及15 mg胰脂肪酶,混合振荡均匀后于37℃水浴中反应7 min,之后加入5 mL无水乙醚混合均匀,静置分层后吸取乙醚层过无水硫酸钠柱,滤液用氮气吹干,用毛细管点于硅胶板上进行薄层色谱分析,展开剂为正己烷-无水乙醚-乙酸(体积比70∶30∶1)。干燥后用0.2% 2,7-二氯荧光黄甲醇溶液喷涂并置于紫外灯下观察,刮下2-单甘酯条带和其他条带,分别置于离心管中并加入4 mL无水乙醚溶解,过无水硫酸钠柱并用氮气吹干浓缩,然后再进行甲酯化,待气相色谱分析。
气相色谱条件[10]:色谱柱为DB-23熔融石英毛细管柱(30 m ×0.25 mm×0.25 μm);氢火焰离子化检测器(FID);载气为氮气,燃烧气为氢气和空气;进样口温度250℃,压力34 439.3 Pa;检测器温度280℃;进样量1 μL;不分流进样;氢气流速40 mL/min,空气流速450 mL/min,氮气流速30 mL/min;升温程序为初始柱温50℃保持1 min,25℃/min升温至175℃,3℃/min升温至230℃保持10 min。
1.2.3 樟树籽仁油甘油三酯结构的定性和定量分析[11-12]
HPLC-ELSD样品制备:称取5 mg樟树籽仁油样品于5 mL离心管中,用异丙醇稀释至5 mg/mL,旋涡振荡溶解,过0.22 μm有机滤膜,进HPLC-ELSD分析。
HPLC-MS/MS样品制备:称取50 mg樟树籽仁油样品于15 mL离心管中,加入10 mL异丙醇,旋涡振荡溶解,过0.22 μm有机滤膜后,稀释1 000倍进HPLC-MS/MS分析。
HPLC-ELSD条件: Elite C18色谱柱(4.6 mm×200 mm,5 μm);流动相A为乙腈,流动相B为异丙醇;柱温30℃;进样量5 μL;采用梯度洗脱,0 min为70%A、30%B,30 min内以0.8 mL/min变为50%A、50%B;雾化室温度45℃,氮气流速1.6 L/min;增益1。
HPLC-MS/MS条件:HPLC条件同上,MS条件为APCI离子源,正离子模式,干燥气温度300℃,干燥气流量5 L/min,雾化器压力2.07×105Pa,鞘气温度350℃,鞘气流量11 L/min,毛细管电压4.2 kV,碎裂电压150 V,碰撞能量25 V,质量扫描范围(m/z)100~1 000。
1.2.4 樟树籽仁油理化性质的测定
酸价的测定依照GB 5009.229—2016,皂化值的测定依照GB/T 5534—2008,碘值的测定依照GB/T 5532—2008,过氧化值的测定依照GB 5009.227—2016。
1.2.5 樟树籽仁油融化和结晶特性测定
通过配备冷藏冷却系统的差示扫描量热仪(DSC8000,PE Instruments)测定樟树籽仁油的熔融和结晶曲线。将样品在铝盘中称重,范围为5~10 mg。将样品以50℃/min从17℃加热至50℃,并在50℃保持10 min,然后以5℃/min降至-50℃,保持5 min,最后以5℃/min加热至50℃[13]。使用Pyris软件(Perkin-Elmer Instruments)分析温度记录图。
1.2.6 数据处理与分析
实验数据采用Excel 2016统计整理,采用SPSS 16.0进行数据分析,用OriginPro 2017进行绘图。
2 结果与讨论
2.1 樟树籽仁油的脂肪酸组成(见表1)
从表1可以看出:樟树籽仁油脂肪酸主要由中碳链脂肪酸组成,含量达96.58%,其中癸酸含量为(60.25±0.85)%、月桂酸含量为(35.88±0.63)%、辛酸含量为(0.45±0.02)%;长碳链脂肪酸主要是肉豆蔻酸、油酸、亚油酸,含量约为3%;sn-2位和sn-1,3位的脂肪酸组成有一些差异但相差不大。这表明樟树籽仁油属于天然的癸酸月桂酸型中碳链油脂,这与大豆油、玉米油、花生油、菜籽油等大宗长碳链油脂的脂肪酸组成不同。油脂的脂肪酸组成、脂肪酸在甘油分子上的位置、脂肪酸碳链长短和双键个数影响油脂的理化性质、体内吸收代谢途径和机制、生理作用[1]。中碳链脂肪酸的吸收代谢途径与长碳链脂肪酸明显不同,其消化吸收速率是长碳链脂肪酸的4倍,代谢速率则是长碳链脂肪酸的10倍。因此,长碳链油脂会因其脂肪酸在血液中吸收和代谢速率较慢容易造成过量堆积,进而引起肥胖、高血脂等脂代谢紊乱类疾病[14],中碳链油脂不会引起肥胖等脂代谢紊乱问题[1]。因此,樟树籽仁油是研发生产减肥降脂、快速供能类功能性油脂、营养补剂和特殊医疗用途食品的理想原料,具有很高的开发利用价值。
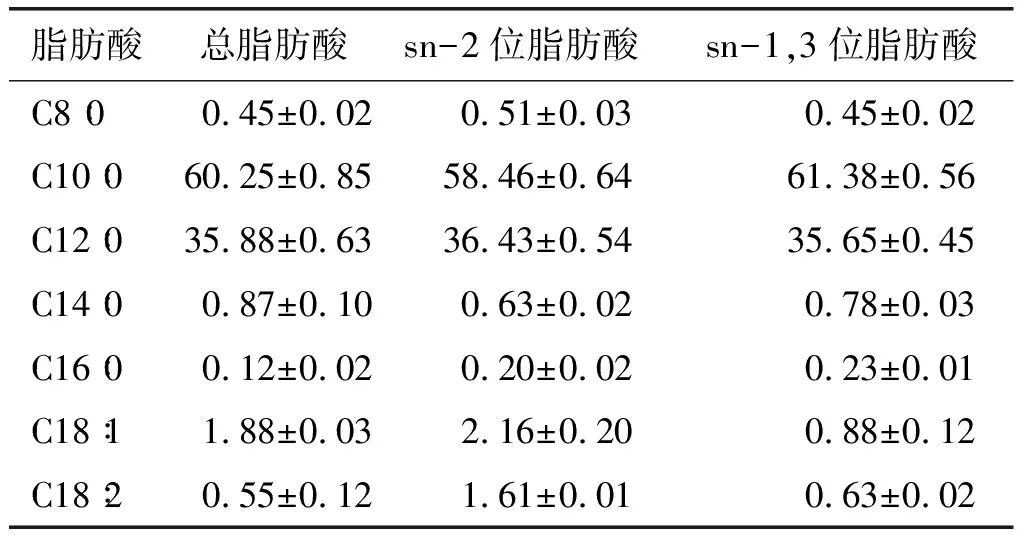
表1 樟树籽仁油的脂肪酸组成 %
2.2 樟树籽仁油的甘油三酯组成
樟树籽仁油的HPLC-MS/MS总离子流图见图1,其对应的甘油三酯质谱棒状图见图2。

图1 樟树籽仁油的HPLC-MS/MS总离子流图


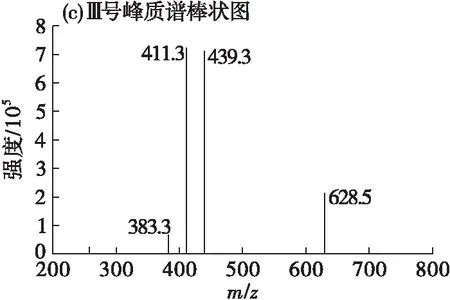
图2 樟树籽仁油HPLC-MS/MS总离子流图中3个峰的质谱棒状图
从图1可以看出,樟树籽仁油经过色谱分离后得到3个色谱峰,色谱峰的分离度较好,达到基线分离。
用大气压化学电离(APCI)源分析甘油三酯可以得到[M]+、[M+H-RCOOH]+、[M+H-RCOO-R′CO]+和[RCO]+离子,根据[DAG]+离子和丰度可以判断TAG结构或脂肪酸与甘油结合的位置[15]。sn-2位上的脂肪酸一般不容易掉落形成碎片离子[16]。碳原子当量(ECN)(也称等价碳数或当量碳数)的计算方法为甘油三酯中脂肪酸的总碳原子数减去2倍的双键数。使用反相高效液相色谱柱洗脱分离甘油三酯时,甘油三酯的保留时间与甘油三酯的 ECN、双键数成线性关系[17]。甘油三酯中双键增加会缩短其保留时间,每增1个双键就会减少约2个碳原子的保留时间[18]。 利用甘油三酯准分子离子和失去1个脂肪酸结构的碎片离子,结合3个甘油三酯标准品进行分析,鉴定出樟树籽仁油的甘油三酯组成,结果见表2。

表2 樟树籽仁油的甘油三酯组成
注:CCC.三癸酸甘油酯;CCLa.二癸酸月桂酸甘油酯;CLaLa.二月桂酸癸酸甘油酯;MCC.二癸酸肉豆蔻酸甘油酯。
由表2可知,对于Ⅰ号峰,在APCI正离子模式下,扫描模式为全扫,监测得到准分子离子m/z572.4[M1+NH4]+和1个失去脂肪酸的碎片离子m/z383.3[M1+1-癸酸]+即[CC]+,综合分析图2(a)、色谱峰保留时间及ECN,确定Ⅰ号峰为CCC。对于Ⅱ号峰,监测得到准分子离子m/z600.5[M2+NH4]+和2个失去1个脂肪酸的碎片离子m/z383.3[M2+1-癸酸]+即[CC]+、m/z411.3[M2+1-月桂酸]+即[CLa]+,综合分析图2(b)、甘油三酯裂解规律以及ECN,确定Ⅱ号峰为CCLa。对于Ⅲ号峰,监测得到准分子离子m/z628.5[M3+NH4]+和3个失去1个脂肪酸的碎片离子m/z383.3[M2+1-癸酸]+即[CC]+、m/z411.3[M3+1-月桂酸]+即[CLa]+或[M3+1-癸酸]+即[MC]+、m/z439.3[M3+1-癸酸]+即[LaLa]+,综合分析图2(c)、裂解规律、相对分子质量以及ECN,确定Ⅲ号峰为MCC和CLaLa的混合物。
2.3 樟树籽仁油中不同甘油三酯的含量
樟树籽仁油中甘油三酯的HPLC-ELSD色谱图如图3所示,采用面积归一化法计算各色谱峰面积对应甘油三酯的含量。结果表明,樟树籽仁油中CCLa含量为56.38%,CLaLa和MCC含量为20.36%,CCC含量为12.55%。

图3 樟树籽仁油中甘油三酯的HPLC-ELSD色谱图
2.4 樟树籽仁油的理化性质(见表3)

表3 樟树籽仁油的理化性质
由表3可知:樟树籽仁油的酸价(KOH)为0.32 mg/g,说明精炼樟树籽仁油中游离脂肪酸含量非常少;碘值(I)为5.70 g/100 g,表明樟树籽仁油中饱和脂肪酸含量较高,这符合脂肪酸组成测定结果;皂化值(KOH)为267.30 mg/g,表明樟树籽仁油中脂肪酸相对分子质量较小,亦符合脂肪酸组成和甘油三酯结构测定结果;过氧化值为0.03 g/100 g,表明樟树籽仁油不易被氧化。精炼樟树籽仁油的理化性质达到国家食用植物油标准(GB 2716—2018)。
2.5 樟树籽仁油的融化和结晶特性
甘油三酯的融化和结晶行为受其脂肪酸组成和分布的影响,甘油三酯含有的脂肪酸种类越多,甘油三酯的DSC曲线上出现的熔融和结晶峰越多。樟树籽仁油的融化和结晶曲线见图4。

图4 樟树籽仁油的DSC特性图
从图4可以看出:樟树籽仁油在-4.27~5.16℃范围内出现结晶峰Ⅰ,且结晶温度为1.54℃;樟树籽仁油在15.34~22.56℃范围内出现吸热峰Ⅱ,熔融温度为21.63℃。樟树籽仁油的熔融温度为21.63℃,比人体体温低15℃以上,樟树籽仁油在室温下可保持液态,可开发为功能食用油脂及营养补剂等产品。
3 结 论
樟树籽仁油中碳链脂肪酸含量高达95%以上,属天然中碳链油脂。樟树籽仁油中的甘油三酯结构较简单,主要含CCLa(56.38%)、CLaLa和MCC(20.36%)、CCC(12.55%)。精炼樟树籽仁油的理化性质达到国家食用植物油标准(GB 2716—2018),室温下为液态,是研发、生产功能食用油脂、营养补剂及特殊医学用途配方食品等产品的理想原料。
