化疗联合射频消融术或阿帕替尼对中晚期非小细胞肺癌的疗效研究
2020-01-11曹达魁王海琴
曹达魁 王海琴
[摘要] 目的 通過三种不同方案进行对比研究化疗联合射频消融术或阿帕替尼对中晚期非小细胞肺癌的疗效。 方法 选择本院经病理确诊且临床分期为ⅢB~ⅣB期90例非小细胞肺癌患者,将其分为化疗组、化疗联合阿帕替尼组及化疗联合射频组,每组各30例。化疗组采用PP(顺铂+培美曲塞)方案,化疗联合阿帕替尼组在PP方案化疗后3 d口服甲磺酸阿帕替尼,化疗联合射频组予PP方案化疗结束后3 d行射频消融术。比较各组肿瘤控制率、不良反应、无进展生存期及生存时间。 结果 (1)肿瘤控制率:化疗组与化疗联合射频组比较,差异有统计学意义(P<0.05);(2)不良反应:化疗组、化疗联合阿帕替尼组及化疗联合射频组比较,差异无统计学意义(P>0.05);(3)无进展生存期:化疗联合阿帕替尼组与化疗联合射频组比较,差异无统计学意义(P>0.05),化疗组分别与化疗联合阿帕替尼组及化疗联合射频组比较,差异有统计学意义(P<0.05);(4)生存时间:化疗组分别与化疗联合射频组及化疗组同化疗联合阿帕替尼组比较,差异有统计学意义(P<0.05),化疗联合阿帕替尼组与化疗联合射频组比较,差异无统计学意义(P>0.05)。 结论 中晚期非小细胞癌采用化疗联合射频消融或阿帕替尼治疗,相对于单一化疗而言,疗效确切,有效率高,生存时间久,为中晚期非小细胞肺癌患者提供更多治疗方案。
[关键词] 射频消融术;化疗;中晚期非小细胞肺癌;阿帕替尼
[中图分类号] R734.2 [文献标识码] B [文章编号] 1673-9701(2020)31-0084-04
[Abstract] Objective To compare the effects of chemotherapy combined with radiofrequency ablation or apatinib on advanced non-small cell lung cancer through three different programs. Methods A total of 90 non-small cell lung cancer patients diagnosed by pathology with clinical stage ⅢB-ⅣB in our hospital were selected and divided into chemotherapy group, chemotherapy combined with apatinib group and chemotherapy combined with radiofrequency group, with 30 cases in each group. The chemotherapy group used PP(Cisplatin+Pemetrexed) regimen, the chemotherapy combined with apatinib group received orally apatinib mesylate 3 days after PP regimen chemotherapy. The chemotherapy combined with radiofrequency group received radiofrequency ablation 3 days after the end of the PP regimen chemotherapy. Results(1)Tumor control rate:The difference between chemotherapy group and chemotherapy combined with radiofrequency group was statistically significant. (2)Adverse reactions:There was no statistically significant difference between the chemotherapy group, chemotherapy combined with apatinib group and chemotherapy combined with radiofrequency group. (3)Progression-free survival: There was no statistically significant difference between the chemotherapy combined with apatinib group and the chemotherapy combined with radiofrequency group. Compared with the chemotherapy combined with apatinib group and the chemotherapy combined with radiofrequency group, and the chemotherapy group had statistically significant difference. (4)Survival time: Compared with the chemotherapy combined with radiofrequency group and the chemotherapy combined with apatinib group, the chemotherapy group had statistically significant difference. There was no significant difference between the chemotherapy combined with apatinib group and the chemotherapy combined with radiofrequency group. Conclusion Compared with single chemotherapy, chemotherapy combined with radiofrequency ablation or apatinib for intermediate-advanced non-small cell carcinoma has definite curative effect, higher effective rate and longer survival time, providing more treatment solutions for patients with intermediate-advanced non-small cell lung cancer.
[Key words] Radiofrequency ablation; Chemotherapy; Advanced non-small cell lung cancer; Apatinib
肺癌目前占我国的恶性肿瘤发病率和死亡率的第一位,肺也是转移性恶性疾病最常见的部位之一,通常预后较差[1-2],约3/4为非小细胞肺癌(Non-small cell lung cancer,NSCLC)。因早期無特异性表现,约75%患者发现时已处于中晚期,丧失手术机会。其高发病率及死亡率使其成为全球关注的公共健康问题。以化疗为主的综合方案仍是目前晚期非小细胞肺癌患者的一线治疗方案,因对化疗耐药,致使诸多患者更换治疗方案。CT引导下肺癌射频消融术是针对局部实体瘤的微创治疗,联合化疗或许可以给予中晚期非小细胞肺癌患者新的治疗方案。甲磺酸阿帕替尼是我国自主研发的新型口服抗血管药物,主要作用机制为抑制血管内皮生长因子受体2(Vascular endothelial growth factor receptor 2,VEGFR-2),破坏肿瘤微血管生成而起到抗肿瘤作用,目前在非小细胞肺癌的治疗中多有研究。本研究联合对比三种方法治疗90例中晚期非小细胞肺癌患者的疗效,现报道如下。
1 资料与方法
1.1 一般资料
选取2015年4月~2018年3月在我院经病理学确诊为非小细胞肺癌,且分期为ⅢB~ⅣB的患者,随机分为化疗组、化疗联合阿帕替尼组和化疗联合射频组,每组各30例。化疗组男12例,女18例,平均年龄(67.53±14.62)岁,肿瘤大小(41.54±9.84)mm;化疗联合阿帕替尼组男14例,女16例,平均年龄(64.58±11.23)岁,肿瘤大小(45.07±14.80)mm;化疗联合射频组男16例,女14例,平均年龄(68.36±12.50)岁,肿瘤大小(43.37±11.80)mm。三组性别、年龄、肿瘤大小等比较,差异无统计学意义(P>0.05),具有可比性。经医院医学伦理委员会审批后,所有患者及家属均需签署研究知情同意书。纳入标准:入组患者无明显重要脏器功能衰竭,临床查凝血功能、肝肾功能无明显异常,Karnofsky评分>60分,预计生存期>3个月;胸部CT下有可测量的病灶,短期内无心肌梗死、中枢神经系统疾病及活动性心脏病等疾病[3]。排除标准:妊娠;年龄<18岁或>80岁;KPS评分<60分;预计生存期<3个月;合并其他原发恶性肿瘤;严重的肝、肾、心、肺等疾病[3]。
1.2 方法
1.2.1 化疗组 化疗采用PP方案(顺铂75 mg/m2+培美曲塞500 mg/m2,D1),化疗21 d为一个疗程,持续时间为6个月(约8.5个疗程)。其中顺铂(江苏豪森药业集团有限公司,批准文号:国药准字H20040812, 30 mg/支),培美曲塞(江苏豪森药业集团有限公司,批准文号:国药准字H2005 1288,0.2 g/支)。
1.2.2 化疗联合阿帕替尼组 化疗方案同化疗组。结束3 d后口服甲磺酸阿帕替尼(江苏盛迪医药有限公司,批准文号:国药准字H20140102,250 mg/片)1片/次,2次/d,早晚餐后半小时用药,持续时间6个月。
1.2.3 化疗联合射频组 化疗方案同化疗组。结束3 d后行CT引导下肺癌射频消融治疗。采用单针(肿瘤直径<3 cm时)或多针(肿瘤直径≥3 cm时)射频消融。射频范围比肿瘤区多0.5~1.0 cm的正常非瘤组织。
1.3 观察指标
1.3.1 肿瘤控制情况 采用胸部CT测定瘤体大小(双径测量),按WHO实体肿瘤疗效标准分为完全缓解(Complete remission,CR):所有靶病灶消失,全部病理淋巴结(包括靶结节和非靶结节)短直径必须减少10 mm;部分缓解(Partial remission,PR):靶病灶直径之和比基线水平减少至少30%;疾病稳定(Stable disease,SD):靶病灶减小的程度没达到PR,增加的程度也没达到PD水平,介于两者之间;疾病进展(Progressive disease,PD):靶病灶直径之和相对增加至少20%(如果基线测量值最小就以基线值为参考),除此之外必须满足直径和的绝对值增加至少5 mm(出现一个或多个新病灶也视为疾病进展)。客观缓解率(Objective response rate,ORR)=(CR+PR)例数/总例数×100%,疾病控制率(Disease control rate,DCR)=(CR+PR+SD)例数/总例数×100%[4]。
1.3.2 不良反应 以美国国立癌症研究所不良事件常用术语标准(Common toxicity criteria for adverse events,CTCAE)分级:0级表示没有;1级为轻度,不需要干预;2级为中度,需要极少或非侵入性干预,在日常生活中限制适于年龄的活动;3级为严重,有重要意义但不会立即危及生命;4级为危及生命,需要紧急治疗[5]。
1.3.3 生存情况 无进展生存期(Progression-free survival,PFS)为患者自治疗开始至PD时间,总生存期(Overall survival,OS)为患者治疗开始至死亡或末次随访时间。
1.4 统计学方法
采用SPSS 22.0 统计学软件进行分析,计量资料以均数±标准差(x±s)表示,组间比较采用t检验;计数资料以[n(%)] 表示,组间比较采用χ2检验,生存时间采用Kaplan-Meier检验。α=0.05为显著性检验水准,P<0.05为差异有统计学意义。
2 结果
2.1 三组肿瘤控制情况比较
化疗组CR 1例,PR 8例,ORR为30%;化疗联合阿帕替尼组CR 2例,PR13例,ORR为50%;化疗联合射频组CR 1例,PR 14例,ORR为50%。三组组间比较,差异有统计学意义(P<0.05)。
2.2 三组不良反应比较
A组有3例出现不良反应,CTCAE分级均为1级;B组有5例出现不良反应,CTCAE分级均为1级;C组有4例出现不良反应,CTCAE分级均为1级。三组比较,差異无统计学意义(P>0.05)。
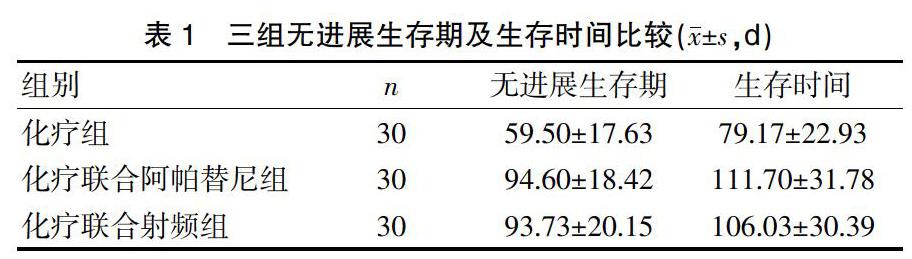
2.3 三组无进展生存期比较
化疗组无进展生存期为(59.50±17.63)d,化疗联合阿帕替尼组为(94.60±18.42)d,化疗联合射频组为(93.73±20.15)d。三组比较,差异有统计学意义(P<0.05)。而化疗联合阿帕替尼组与化疗联合射频组比较,差异无统计学意义(P>0.05),见表1。
2.4 三组生存时间比较
化疗组生存时间为(79.17±22.93)d,化疗联合阿帕替尼组为(111.70±31.78)d,化疗联合射频组为(106.03±30.39)d。三组组间比较,差异有统计学意义(P<0.05)。而化疗联合阿帕替尼组与化疗联合射频组比较,差异无统计学意义(P>0.05),见表1、 封三图3。
3 讨论
肺癌早期手术仍是其最佳治疗方案[6],但中晚期肺癌患者大多在确诊时已丧失手术条件,目前以化疗为主的综合治疗方案仍是一线治疗方案,但反复化疗常致耐药,导致化疗陷入瓶颈。
射频消融治疗是在瘤体组织内插入电极针释放出射频电流,导致组织粒子高速震荡摩擦产热,致使肿瘤细胞发生坏死,造成病变组织凝固性坏死,进一步形成液化病灶或纤维化组织,中断肿瘤的血供及转移,达到肿瘤的局部消融目的[7]。肺部肿瘤的周围组织存在大量气体,可导致绝缘效果,从而较实体瘤更适合RFA,故肺肿瘤更适合采用射频消融治疗。目前已用于临床治疗多年,是安全有效且微创的,特别是用于晚期肺癌的治疗[8]。气胸目前是RFA技术最常见的并发症,发生率为4.5%~61.1%,但气胸可自行吸收。
本研究结果显示,化疗联合射频组肿瘤控制情况较化疗组高,化疗组ORR为30%,化疗联合射频组ORR为50%,对无进展生存期及生存时间而言,化疗联合射频组均高于化疗组。与Shiono等[9]研究结果相近。考虑RFA能毁损肿瘤结构及组织,破坏残留细胞的生存微环境,使肿瘤转为单一或独立的细胞或细胞团,化疗更加有效,而且杀灭大量肿瘤细胞,极大地降低了耐药细胞的克隆,使患者生存时间延长[10-11]。故联合化疗可改善肿瘤患者的临床症状,提高患者生存质量,延长患者临床生存时间。
据研究显示,VEGF及其受体(VEGFR)在多种肿瘤血管内皮有高表达,为肿瘤的治疗提供了新的靶点。VEGFR-2是VEGF介导的血管生成通路的主要介质,能导致肿瘤的血管生成、细胞增殖和转移。甲磺酸阿帕替尼是一种新型小分子口服靶向抗血管药物,对VEGFR-2亲和性较高,通过减少肿瘤微血管密度,抑制肿瘤细胞组织周围血管的形成,从而使肿瘤细胞失去滋养而发生凋亡[12-13]。据报道,超过50%的肺癌有VEGF过表达,与预后不良相关[14]。阿帕替尼可以高度选择性地竞争细胞内VEGFR-2的ATP结合位点并阻断其下游信号转导,从而通过强烈抑制肿瘤血管生成发挥抗肿瘤作用[15]。阿帕替尼还可以促进肿瘤细胞自噬、凋亡,从而减少机体的肿瘤负荷[16]。
本研究结果显示,化疗联合阿帕替尼治疗相对于单一化疗而言,患者无进展生存期及生存时间明显延长,治疗ORR也高于单一化疗,与郭运杰等[17]研究报道一致。Li等[18]对40例晚期肺鳞癌患者单独给予阿帕替尼或联合化疗方案,结果发现DCR为72.5%,中位PFS为3.7个月。Wu等[19]对28例二、三线药物化疗进展的晚期非鳞状NSCLC予阿帕替尼口服治疗,中位 PFS为3个月,OS 为 7.4 个月,提示阿帕替尼对晚期非鳞状 NSCLC 患者具有一定的治疗作用。
有研究[18]显示,阿帕替尼在晚期非鳞状非小细胞肺癌中显示出疗效。单独使用阿帕替尼或与化疗联合使用具有良好的反应率和良好的疗效。阿帕替尼不仅能减少肿瘤细胞对化疗的耐药,逆转化疗耐药性,而且机体对化疗的敏感性增加,故而联合化疗后效果更佳。另有研究[20]显示,阿帕替尼在二线及二线治疗后失败的晚期NSCLC患者中,患者的中位PFS为4.8个月,ORR和DCR分别为13.8%和83.3%,疗效显著。
综上所述,中晚期NSCLC患者可通过化疗联合射频消融术或阿帕替尼治疗,可以更好地改善患者的生存质量,延长生存期,值得临床进一步推广和使用。但总体样本量仍有限,需进一步大样本多中心研究证实。
[参考文献]
[1] Bray F. Global cancer statistics 2018:GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries[J]. Cancer J Clin,2018,68(6):394-424.
[2] Stella GM. Lung-seeking metastases[J]. Cancers (Basel),2019,11(7):1010.
[3] 韩宝惠 高树根. 中华医学会肺癌临床诊疗指南2018版[J].中华肿瘤杂志,2018,40(12):944-951.
[4] Eisenhauer EA,Verweij J. New response evaluation criteria in solid tumors:Recist Guideline Version 1.1[J]. EJC Supplements,2009,7(2):5.
[5] 皋文君,刘砚燕. 国际肿瘤化疗不良反应评价系统-通用不良反应术语标准4.0版[J]. 肿瘤,2012,32(2):143.
[6] Aokage K, Yoshida J, Hishida T, et al. Limited resection for early-stage non-small cell lung cancer as function-preserving radical surgery:A review[J]. Jpn J Clin Oncol,2017,47:7-11.
[7] Hartley-Blossom ZJ,Healey TT. Percutaneous thermal ablation for lung cancer:An update[J]. Surg Technol Int,2019,34:359-364.
[8] Chi J,Ding M,Shi Y,et al. Comparison study of computed tomography-guided radiofrequency and microwave ablation for pulmonary tumors:A retrospective case-controlled observational study[J]. Thorac Cancer,2018,9:1241-1248.
[9] Shiono S,Okumura T,Boku N,et al. Outcomes of segmentectomy and wedge resection for pulmonary metastases from colorectal cancer[J]. Eur J Cardiothorac Surg,2017,51(3):504-510.
[10] Vogl TJ. Microwave ablation(MWA)of pulmonary neoplasms:Clinical performance of high-frequency MWA with spatial energy control versus conventional low-frequency MWA[J]. AJR,2019,213:1388-1396.
[11] Nahum Jiang B. Efficacy and safety of thermal ablation of lung malignancies:A Network meta-analysis[J]. Ann Thorac Med,2018,13(4):243-250.
[12] Xie L,Guo W,Wang Y,et al. Apatinib for advanced sarcoma:Results from multiple institutions' off-label use in China[J]. BMC Cancer,2018,18:396.
[13] Yang C,Feng W,Wu D. Apatinib for advanced non-small cell lung cancer:A retrospective case series analysis[J]. J Cancer Res Ther,2018,14:159-162.
[14] Deng Y,Yang Y,Yao B,et al. Paracrine signaling by VEGF-C promotes non-small cell lung cancer cell metastasis via recruitment of tumor-associated macrophages[J]. Exp Cell Res,2018,364:208-216.
[15] Zhang Y,Chen Y,Zhang D,et al. Discovery of novel potent VEGFR-2 inhibitors exerting significant antiproliferative activity against cancer cell lines[J]. J Med Chem,2018,61:140-157.
[16] Liu K,Ren T,Huang Y,et al. Apatinib promotes autophagy andapoptosis through VEGFR2 /STAT3/BCL-2 signaling in osteosarcoma[J].Cell Death and Disease,2017, 8(8):e3015.
[17] 郭運杰,井小会. 多西他赛联合阿帕替尼二线治疗非鳞癌非小细胞肺癌的有效性及安全性分析[J]. 中国肿瘤临床,2017,44(11):544-546.
[18] Li X,Le L,Han L,et al. Short-term efficacy and safety of apatinib in advanced squamous cell carcinoma of the lung[J]. Indian J Cancer,2017,54(3):547-549.
[19] Wu D,Liang L,Nie L,et al. Efficacy,safety and predictive indicators of apatinib after multilines treatment in advanced nonsquamous non-small cell lung cancer:Apatinib treatment in nonsquamous NSCLC[J]. Asia Pac J Clin Oncol,2018,14(6):446-452.
[20] 石明伟,王升晔,徐振武,等. 阿帕替尼治疗晚期非小细胞肺癌的疗[J]. 临床与病理杂志,2017,37(9):1880-1886.
(收稿日期:2020-05-28)
