超声造影引导下经皮腹膜后占位性病变穿刺活检的价值
2020-01-09谢琉嘉徐亚丹闻捷先季正标王文平
谢琉嘉 ,徐亚丹,闻捷先,季正标,王文平
1.复旦大学附属中山医院超声科,上海 200032;
2.福建中医药大学附属第二人民医院超声科,福州 350003
腹膜后占位性病变以原发性肿瘤居多,其组织学类型多,生长部位深,与腹膜后重要脏器和血管关系紧密,临床表现隐秘而缺乏特异性,诊断困难,多数在体检时发现,发现时肿块往往较大[1]。其辅助检查主要是超声、CT、磁共振成像(magnetic resonance imaging,MRI)等影像学检查,诊断价值有限[2],术前病理学诊断显得尤为重要,能够为腹膜后肿瘤个体化治疗提供重要参考[3]。常规超声引导下经皮穿刺技术具有微创、简便、灵活、安全及无辐射的特点,已在临床广泛应用。本研究对80例患者拟行穿刺的腹膜后病灶进行常规超声和超声造影(contrastenhanced ultrasound,CEUS)检查,探讨CEUS引导下经皮腹膜后占位性病变穿刺活检的价值。
1 资料和方法
1.1 一般资料
收集2015年5月—2018年12月于复旦大学附属中山医院经影像学检查发现腹膜后占位性病变的患者80例,包括性质待定或治疗后复发的肿块,患者拟行CEUS引导下穿刺活检,其中男性43例,女性37例,年龄17~83岁,平均年龄(52.4±15.1)岁,病灶最大径34~200 mm,平均(112.4±43.2)mm。术前常规检查凝血功能,患者均已签署知情同意书。
1.2 仪器与方法
选用荷兰Philips公司HD15、中国迈瑞医疗国际股份有限公司DC-8和意大利Esaote公司MyLab Twice超声诊断仪,探头频率1~5 MHz,均配备低机械指数CEUS技术,造影剂使用意大利Bracco公司的SonoVue,将5 mL的0.9% NaCl溶液注入24.98 mg冻干粉剂瓶中,用力振荡数秒,直至混匀形成乳白色混悬液备用。
患者取仰卧位或侧卧位,先行常规超声观察病灶的部位、大小、回声、边界形态、肿块内部及周围的血流分布,再调至造影模式,经肘部浅静脉快速团注SonoVue混悬液2.0 mL,用5 mL的0.9% NaCl溶液冲管,注射后立即开始计时,连续实时观察病灶增强减退过程及造影剂分布区域。
常规消毒、铺巾,超声探头外套无菌探头套,超声实时引导下,用2%利多卡因局部麻醉至肿块表面,然后采用16 G BARD自动弹射式活检枪,切割长度调至22 mm档,选取CEUS增强区,避开脏器及肿块内部大血管,进针至目标区域,击发活检枪,迅速拔针。用无菌滤纸取下组织条,观察其外观及长度。根据取材的完整性及临床病理学要求决定穿刺次数,通常穿刺2~3次,置于4%中性甲醛溶液标本瓶中固定,送病理学检查。
术后患者卧床休息,并观察有无出血、腹痛等并发症。
1.3 统计学处理
将常规超声显示的无回声区且未见彩色血流的区域视为液化坏死区,将CEUS检查中始终未增强区定为液化坏死区,比较两者的显示率。以标本相对完整、达到病理科诊断要求为取材满意,计算取材满意率。穿刺病理诊断中,如有手术者,与术后病理学检查结果相符为诊断正确;对于未手术者,如穿刺病理诊断考虑恶性可确诊,反之考虑为良性或描述性诊断需参考其他影像学检查及随访6个月以上确定诊断;另外,因取材组织过少或几乎为坏死组织而病理学检查无结果的为无法诊断,由此计算病理诊断率。
2 结 果
2.1 病理诊断率
80例患者行CEUS检查后,3例因CEUS显示几乎无造影剂增强,分别考虑为肿块内大部分坏死、血肿及脓肿而取消穿刺,并经CT、MRI等其他影像学检查及后期随访证实(图1)。其余77例穿刺后均获得病理学诊断结果:淋巴瘤24例,纤维源性肿瘤12例,胃肠道间质瘤9例,转移瘤6例,平滑肌源性肿瘤5例,无法分类的肉瘤5例,脂肪肉瘤2例,神经源性肿瘤2例,间皮瘤2例,血管周上皮样细胞肿瘤2例,滑膜肉瘤1例,神经内分泌肿瘤1例,未分类的小圆细胞肿瘤2例,未分类的小梭形细胞恶性肿瘤1例,炎性病变2例,IgG4相关硬化性疾病1例。病理诊断率为100.0%(77/77)。
2.2 坏死灶显示率
80例患者中对于病灶的液化坏死区,CEUS的显示率为62.5%(50/80),明显高于常规超声的显示率15.0%(12/80),差异有统计学意义(P<0.01),并且CEUS显示坏死区与活性区的界限更加分明(图2~3)。CEUS显示相对常见的淋巴瘤、肉瘤(包括脂肪肉瘤、平滑肌肉瘤、纤维肉瘤、滑膜肉瘤、恶性神经鞘膜瘤等)、纤维源性肿瘤及胃肠道间质瘤的坏死率分别为20.8%(5/24)、93.8%(15/16)、50.0%(6/12)及88.9%(8/9)。肉瘤和胃肠道间质瘤出现坏死的比例明显高于淋巴瘤和纤维性肿瘤,差异有统计学意义(P<0.05),其他病种因例数较少不具可比性(表1)。对于这些易出现坏死的病种,CEUS在引导穿刺中起到重要作用。
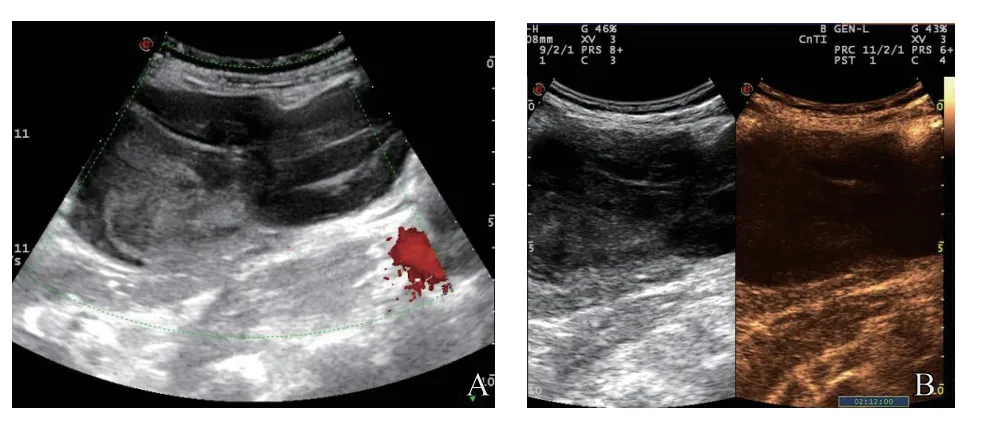
图1 典型病例1(男性,66岁)的彩色多普勒血流显像及CEUS图像

表1 不同病种CEUS显示的坏死情况

图2 典型病例2(男性,34岁,腹腔单发肿块)的超声表现及病理学观察
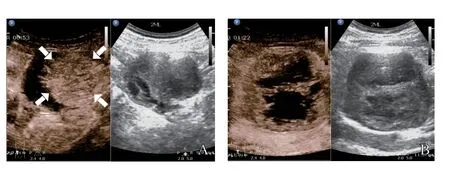
图3 典型病例3(男性,58岁,腹腔混合回声团块)CEUS图像
另外,本研究患者中出现肿块包绕血管的有11例,其中10例为淋巴瘤,占淋巴瘤总例数的41.7%(10/24)。可能是淋巴瘤较常出现包绕血管,在腹膜后肿瘤中出现包绕血管生长的肿块很大程度上提示淋巴瘤,在穿刺时应注意避开肿块包绕的大血管(图4)。
2.3 取材满意率
77例接受穿刺的患者中,65例取材2次(组织条10~20 mm),12例取材3次(组织条5~20 mm),组织条的长度和完整性与肿块组织细胞成分有直接关系,取材次数很大程度上取决于组织条的性状及临床病理要求。77例患者穿刺活检均达到病理科诊断要求,取材满意率为100.0%。
2.4 并发症情况
本研究接受CEUS引导下穿刺活检的患者术后卧床6~8 h,并绑腹带加压,均未出现明显的腹腔出血和难以忍受的腹痛等并发症。

图4 典型病例4(男性,61岁,腹腔多个低回声团块融合)超声表现及病理学观察
2.5 治疗方案
本研究行穿刺活检的77例患者中,手术切除12例,术后病理学检查结果与穿刺病理学检查结果相符合。化疗29例,放疗4例,经动脉栓塞治疗4例,靶向药物治疗4例,高能聚焦超声刀治疗1例;上述中有部分患者采取多种方法联合治疗。有17例患者因肿块为转移性、难以根治切除、预后差、合并其他系统严重疾病或处于肿瘤终末期等情况,无手术指征亦未随访到其他针对性治疗;4例拒绝治疗或后续无治疗记录;2例因穿刺病理学检查结果与既往手术病理学检查结果符合,考虑术后复发;4例经腹腔镜或剖腹探查肿块活检,其中2例只获取肿块表面组织,与穿刺病理学检查结果不符,但临床表现及影像学检查均支持穿刺结果。
3 讨 论
腹膜后占位性病变是一组少见疾病,以肿瘤性病变为主,分原发性和继发性,腹膜后原发性肿瘤约占所有肿瘤构成的0.2%,其中恶性占80.0%[1]。其组织类型复杂,治疗方案多样,需根据不同的病理学分型采取不同治疗方案,故明确组织亚型是诊断的一个重要方面,决定了治疗方案及预后[4]。目前尚无任何影像学技术能预测组织学亚型[5],经皮穿刺活检是获取组织病理学证据最有效的方法,对于尚未明确诊断的病变,或者怀疑复发的病灶需穿刺活检明确诊断[6]。超声的多平面功能使操作者能够灵活选择穿刺路径,避开血管、脏器,如不可避免地需经肝穿刺肿块也是可行的[7],与CT引导相比,超声能实时显示活检针及其尖端,可重复性高,成本更低,也避免了电离辐射和碘造影剂的肾毒性[8-9]。
近些年随着CEUS技术的逐渐成熟,CEUS与介入性超声相结合,在临床上的应用日益广泛[10]。本研究利用CEUS引导下经皮腹膜后占位性病变穿刺活检。超声造影剂SonoVue是血池显像剂,不会渗透到血管外,能够显示病灶内的血流灌注情况,描绘微血管及新生血管的分布情况[11]。CEUS对坏死区的显示率明显高于常规超声,而且能清晰显示病灶边界,界定活性区与坏死区,因此可以更好地规划穿刺路径和定位最具代表性的采样区[12]。相关研究[13-14]显示与常规超声相比,CEUS引导穿刺的组织条获取的病理学结果与手术病理学检查结果更加吻合[13-14]。实践表明,取材组织过少或大部分为坏死组织而无法确诊是穿刺失败的主要原因,避开坏死区穿刺是提高病理学诊断成功率的关键[15-16]。
本研究还发现不同肿瘤之间的坏死率和生长方式存在差异,不同肿瘤的组织条质地有所不同,良恶性病灶的造影增强模式有一定区别,这与腹膜后肿瘤的多种组织来源及不同病理分型有关[17]。例如:肉瘤及胃肠道间质瘤大多有坏死;胃肠道间质瘤通常质地软,组织条易碎;纤维来源的肿瘤质硬,组织条致密;淋巴瘤增强较均匀,很少出现坏死,常包绕血管生长(图4);恶性肿瘤血供较丰富,多呈浸润性生长。这些特点对于肿块的初步判断有一定的参考价值,对穿刺途径及取材要求有相应的指导意义,但这些或更多的特点还需大样本量的研究来证实和发现。
CEUS引导下的穿刺活检可以取到肿块深部的活性组织,不仅创伤极小,而且有时候诊断性甚至优于手术局部活检。如图4患者先行腹腔镜下肿块活检,病理学检查考虑侵袭性纤维瘤可能,但是临床与影像学均怀疑淋巴瘤,遂行CEUS引导下穿刺活检,病理学检查诊断为淋巴瘤,后予化疗有效,证实诊断,推测可能因为腹腔镜下活检取材于肿块表面组织,难以代表肿块全貌,从而影响病理学诊断结果。
超声引导下经皮穿刺活检的并发症发生率很低,如疼痛、出血、意外的器官损伤,以及可能沿针道播散肿瘤[7],CEUS引导下穿刺有利于避免以上并发症发生。出血是最常见的并发症,本研究中患者无一例出现明显出血并发症,CEUS能清晰地显示肿块周边和内部的血管,穿刺过程中可有效避开这些血管(图4),以减少出血的可能,当然肿块位置、操作者经验也与穿刺的并发症有一定关系。另外,腹膜后占位性病变由于位置较深,前方常有肠管遮挡,穿刺时可适当加压推开肠管,以免误穿肠管。针道恶性播散罕见,有研究者[7]提出为了将风险降到最低,针道数量应尽可能少。CEUS可明显提高取材成功率,减少穿刺次数,降低肿瘤针道种植的可能,CEUS还能识别常规超声无法分辨的活动性出血,以便及时指导治疗[18-19]。
综上所述,CEUS引导下经皮腹膜后占位性病变穿刺活检,可提高坏死区的检出率,并准确区分活性区和坏死区,实时准确地引导穿刺针对活性区取材,获得满意的取材率和病理诊断率,从而指导治疗方案的选择,有较高的临床应用价值。
