超声引导下骶管阻滞时加用右美托咪定对小儿发育性髋脱位矫形术术后镇痛效果的影响
2020-01-07赵聪聪郑少强
朱 丰,赵聪聪,覃 倩,种 皓,郑少强,周 雁※,王 庚
(北京积水潭医院 a.麻醉科,b.小儿骨科,北京 100035)
发育性髋关节脱位(developmental dysplasia of the hip,DDH)是较常见的小儿骨科疾病,发病率为1.1‰~3.8‰,多见于女性儿童。对于闭合复位失败者,一般需要行截骨矫形手术治疗,主要包括髋关节切开复位、股骨短缩旋转截骨钢板内固定、髋臼周围截骨内固定、自体髂骨移植、单髋人字石膏固定等,手术范围累及广泛的肌肉软组织、骨膜和骨骼组织,术中及术后疼痛剧烈[1]。骶管阻滞现已广泛用于腹部、肛门会阴区及下肢手术的麻醉和术后镇痛,已被广泛应用于小儿DDH矫形术的术中及术后镇痛[2]。研究证实,超声引导下骶管阻滞的麻醉和镇痛效果较明确,可实时观察局部麻醉药物的扩散情况,最大限度地避免不良反应的发生,可在小儿DDH矫形术术后有效镇痛至少18 h[3]。进一步延长单次骶管阻滞的镇痛时间是目前研究的热点。有研究证实,α2受体激动剂可以延长硬膜外阻滞的镇痛时间[4]。右美托咪定作为一种高选择性α2受体激动剂,用于鞘内注射、硬膜外阻滞、周围神经阻滞和静脉输注均可延长局部麻醉药的镇痛时间[5]。本研究主要观察超声引导下罗哌卡因联合右美托咪定骶管阻滞用于小儿DDH矫形术的安全性及术后镇痛效果。
1 资料与方法
1.1一般资料 选取2016年5月至2018年12月在北京积水潭医院小儿骨科行择期DDH矫形术的患儿46例,所有患儿均采用股骨上端旋转截骨、髋臼截骨矫形内固定、髋关节复位、单髋人字石膏固定术治疗。排除标准:①存在骶管阻滞禁忌证;②存在解剖异常;③对试验所用药物过敏;④同期参与其他研究者;⑤体质指数>30 kg/m2;⑥患儿家属拒绝者。上述患儿依据随机数字法分为试验组和对照组,各23例。本研究获得北京积水潭医院医学伦理委员会批准,患儿家属签署知情同意书。
1.2麻醉方法
1.2.1麻醉准备 两组患儿均无术前用药。使用Datex-Ohmeda S/5监护仪监测患儿基本生命体征,包括无创血压、心电图、脉搏血氧饱和度,使用Aspect A-1000TM脑电双频指数(bispectral index,BIS)监测仪(Aspect Medical System公司,美国)连续监测患儿BIS值。
1.2.2麻醉诱导 根据患儿配合度选择是否需要诱导麻醉,如患儿配合度较差,则需要行七氟烷吸入诱导麻醉后建立外周静脉通路,停用吸入麻醉后再予以静脉诱导;如患儿配合良好,可在开放上肢静脉后直接进行静脉诱导麻醉。静脉诱导给药依次为3 μg/kg芬太尼、1.5 mg/kg异丙酚、0.7 mg/kg罗库溴铵,待患儿入睡且BIS值<60,下颌完全松弛后置入喉罩,确定喉罩位置正确后,连接麻醉机行机械通气,调整压力设定值及呼吸频率,监测呼气末二氧化碳分压,将其维持在30~40 mmHg(1 mmHg=0.133 kPa)。
1.2.3超声引导下骶管阻滞操作 喉罩位置固定后,患儿取侧卧位,并行超声引导下骶管阻滞,体表定位标记为双侧骶角中点,使用双侧髂后上棘连线向骶尾侧描迹等边三角形修订骶管位置(等边三角形三个点分别为双侧髂后上棘及骶管阻滞进针点),之后使用超声图像再次确定骶管位置并引导进针。首先将超声探头垂直脊柱放置获取骶管的短轴影像,图像中两个高亮凸起之后声影脱失结构为双侧骶骨角,其间凹陷的暗性区域为骶裂孔,暗性区域内可识别上下两条高回声线,浅层为骶尾背侧韧带,深层为骶骨骨面(青蛙征),在骶椎椎体(小儿未融合)和骶尾背韧带之间的黑色区域为骶管腔。之后将探头旋转90°获取骶管结构的长轴影像,探头长轴与骶骨正中线一致,超声图像中显示为高亮线性凸起即骶岬和深部的骶椎骨面(台阶征),骶管硬膜外腔为高亮的骶尾背韧带与骶骨上方的黑色区域,穿刺目标点选择在两侧骶骨角之间骶管腔最宽部位。穿刺点确定后,选取骶管的长轴影像采用平面内技术进行穿刺注药,将21G注射器针头作为穿刺针,与装有局部麻醉药物的注射器通过泵用注射导线连接。超声图像显示,针尖刺破骶尾背韧带并进入骶管腔,回抽注射器,确定无血及脑脊液后注药,注药过程可见骶管腔增宽,且注射时骶尾背侧韧带抬起,停药后复位。对照组单纯使用0.20%罗哌卡因1 mL/kg[6];试验组使用0.20%罗哌卡因+右美托咪定混合液,右美托咪定使用剂量为1 μg/kg,混合液使用容量为1 mL/kg[2]。
1.2.4麻醉维持 术中使用静脉吸入复合麻醉维持,将七氟烷呼气末浓度维持在0.7 MAC(最低肺泡有效浓度),术中静脉泵注丙泊酚并调整持续输注剂量,维持BIS值40~60,根据肌电图监测情况间断追加罗库溴铵维持肌松。手术至少在骶管阻滞完成后30 min开始,若血压和心率升高大于基础值的20%,静脉滴注枸橼酸芬太尼注射液0.5~1 μg/kg,以减少手术引起的应激反应。皮肤缝合完成后停止七氟烷吸入麻醉,单纯使用丙泊酚静脉泵注维持麻醉,石膏固定完成后停止泵注。待患儿自主呼吸恢复,潮气量>7 mL/kg,呼吸频率维持在16~25 次/min,吸入空气时脉搏血氧饱和度维持在0.95以上时,将其送入麻醉后恢复室,根据拔管指征适时拔出喉罩。如患儿完全清醒、生命体征平稳、改良面部表情评分(the modified faces,legs,activity,cry and consolability scale,FLACC)≤2分时,可将其送回普通病房。
1.2.5术后镇痛 所有患儿术后均未连接静脉镇痛泵,若FLACC评分≥4分,给予口服对乙酰氨基酚(泰诺林)1.5 mg/kg,30 min后再次行FLACC评分,若FLACC评分≥4分,则予肌内注射盐酸哌替啶1 mg/kg。盐酸哌替啶单次注射最大剂量不超过50 mg,对乙酰氨基酚最小服药间隔为6 h,若服药间隔出现爆发性疼痛,则予盐酸哌替啶肌内注射[3]。
1.3监测指标 记录两组患儿骶管注药前、骶管注药后5、10、20、30、60、120、180 min的心率和平均动脉压(mean arterial pressure,MAP)以及术中丙泊酚和芬太尼的使用剂量。由不知分组情况的麻醉医师对两组患儿术后情况进行评估,测定指标为:①分别记录患儿术后2、4、6、12、24、36、48 h的FLACC评分[3]。②记录患儿术后首次服用对乙酰氨基酚的时间,记录盐酸哌替啶注射液的使用时间及剂量。③拔管即刻、术后回病房即刻及回病房2 h后采用Ramsay评分法评估患儿镇静程度,评分标准参见文献[3]的研究。④记录两组患儿围手术期恶心、呕吐、尿潴留、低血压、心动过缓、心律失常、呼吸抑制的发生情况。相关并发症的诊断和处理办法如下:a.当患儿发生恶心或呕吐时,静脉给予0.1 mg/kg昂丹司琼;b.患儿术后12 h后仍无法自主排尿,则予以单次导尿,并诊断尿潴留;c.收缩压低于基线值的30%诊断低血压,采用0.1 mg/kg麻黄碱和5 mL/kg乳酸钠林格液静脉注射治疗,并可根据需要重复;d.心率<50 次/min或心率较基线降低20%或更多(以最低者为准)诊断为心动过缓,使用阿托品0.01 mg/kg静脉注射治疗;e.呼吸频率<8 次/min或吸气时氧饱和度<0.90诊断呼吸抑制,给予吸氧,必要时予以呼吸支持治疗。⑤使用0~10的分级评分法(0分为不满意,10分为非常满意)评估患儿家属对术后镇痛效果的满意度。

2 结 果
2.1两组一般情况以及麻醉分级和手术时间比较 两组患儿性别、年龄等一般情况比较差异无统计学意义(P>0.05),见表1。两组患儿骶管阻滞操作顺利,无相关并发症(穿刺部位出血感染、血肿形成、局部麻醉药物全身中毒反应、脑脊液漏、全脊髓麻醉等)发生。所有患儿均按设计完成了研究。
2.2两组循环变化情况比较 试验组患儿注药后10、20、30、60 min心率低于对照组(P<0.05),两组患儿各时点间MAP比较差异无统计学意义(P>0.05)。两组心率组间、时点间、组间和时点间交互作用比较差异有统计学意义(P<0.05),两组MAP不同时点间差异有统计学意义(P<0.05),组间、组间和时点间交互作用差异无统计学意义(P>0.05)。见表2。
2.3两组术中和术后镇痛效果比较 采用相同七氟烷最低肺泡有效浓度吸入麻醉并维持相同BIS值时,试验组患儿术中丙泊酚用量明显少于对照组(P<0.05);而两组患儿术中芬太尼用量比较差异无统计学意义(P>0.05);试验组患儿术后对乙酰氨基酚的首次觅求时间明显晚于对照组(P<0.05),见表3。试验组患儿术后12、24 h的FLACC评分低于对照组(P<0.05);术后两组术后2、4、6、36、48 h的FLACC评分比较差异均无统计学意义(P>0.05);两组术后12、24、36、48 h的FLACC评分均高于术后2、4、6 h(P<0.05),两组间、时点间、组间和时点间交互作用比较差异有统计学意义(P<0.05),见表4。两组所有患儿术后均未采用肌内注射盐酸哌替啶镇痛。

表1 两组患儿一般情况以及麻醉分级和手术时间比较
对照组:单纯罗哌卡因骶管阻滞;试验组:罗哌卡因+右美托咪定混合液骶管阻滞;a为χ2值,b为t值

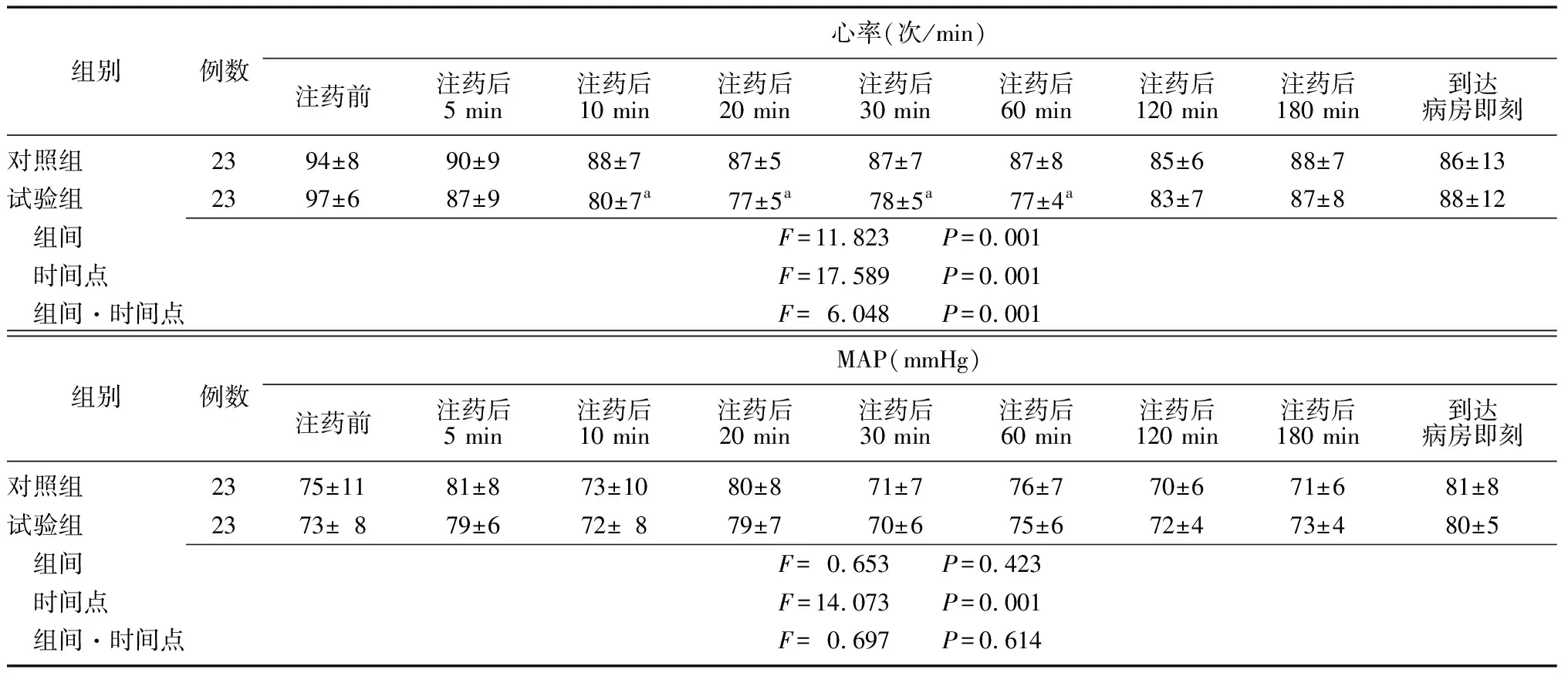
组别例数心率(次/min)注药前注药后5 min注药后10 min注药后20 min注药后30 min注药后60 min注药后120 min注药后180 min到达病房即刻对照组2394±890±988±787±587±787±885±688±786±13试验组2397±687±980±7a77±5a78±5a77±4a83±787±888±12 组间F=11.823 P=0.001 时间点F=17.589 P=0.001 组间·时间点F=6.048 P=0.001组别例数MAP(mmHg)注药前注药后5 min注药后10 min注药后20 min注药后30 min注药后60 min注药后120 min注药后180 min到达病房即刻对照组2375±1181±873±1080±871±776±770±671±681±8试验组2373±879±672±879±770±675±6 72±473±480±5 组间F=0.653 P=0.423 时间点F=14.073 P=0.001 组间·时间点F=0.697 P=0.614
MAP:平均动脉压;对照组:单纯罗哌卡因骶管阻滞;试验组:罗哌卡因+右美托咪定混合液骶管阻滞;1 mmHg=0.133 kPa;a与对照组比较,P<0.05
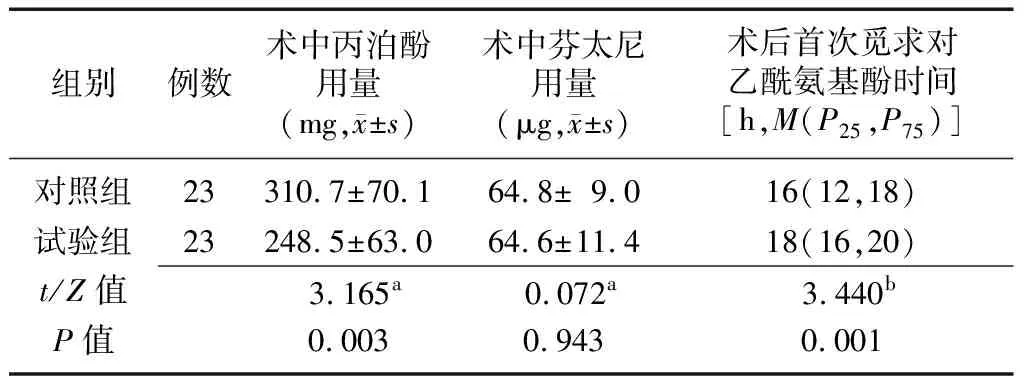
表3 两组术中丙泊酚、芬太尼使用剂量以及术后首次觅求对乙酰氨基酚时间比较
对照组:单纯罗哌卡因骶管阻滞;试验组:罗哌卡因+右美托咪定混合液骶管阻滞;a为t值,b为Z值
2.4两组麻醉镇痛药物相关不良反应的发生情况和家属满意度比较 试验组心动过缓发生率高于对照组(P<0.05),两组患儿其他并发症发生率比较差异无统计学意义(P>0.05)。试验组患儿拔管后即刻镇静评分高于对照组(P<0.05);两组术后其他时点间镇静评分比较差异无统计学意义(P>0.05);两组患儿均未出现过度镇静;两组患儿家属对术后镇痛的满意度评分均较高,比较差异无统计学意义(P>0.05),见表5。
3 讨 论
在现代加速康复外科理念中,围手术期疼痛控制是决定患者术后康复质量的重要环节,加速康复外科理念的终极目标是实现“无痛无风险的手术”,有助于患者早日康复出院[7]。加速康复外科理念主张实施多模式镇痛,且多模式镇痛的各种疼痛控制模式不应孤立存在,而应针对特定患者、特定手术制订个体化的疼痛控制措施,确保达到最佳的镇痛效果,并使不良反应最小化[8]。由此可见,围手术期小儿患者镇痛方式的选择尤为重要。
区域阻滞(包括椎管内阻滞、周围神经阻滞、局部浸润麻醉等)是常用的麻醉及镇痛方法。超声引导下骶管阻滞已在小儿DDH矫形术中成功应用[9]。区域阻滞的术中及术后镇痛效果明确,但其麻醉消退后的疼痛反跳现象仍不可避免,应用局麻药辅助剂是改善麻醉消退后疼痛反跳现象的方法之一[10-11]。局麻药辅助剂可缩短麻醉起效时间、改善阻滞效果、减少局部麻醉药物用量、减少局部麻醉药物所致毒性反应的发生,并可延长麻醉作用时间、改善麻醉消退后疼痛反跳现象。目前常用的局部麻醉药物辅助剂包括肾上腺素、阿片类药物、可乐定、右美托咪定、地塞米松、咪达唑仑、新斯的明、透明质酸酶、氯胺酮等。与单纯局部麻醉药物相比,局部麻醉药物辅助剂除具有确切的增强麻醉效果证据外,选择应用时还需要满足以下条件:①应充分了解所用药物的作用机制,很多局部麻醉药物辅助剂的协同作用机制尚不明确,但应合理使用;②不含防腐剂;③与单纯使用局部麻醉药物相比,加用局部麻醉药物辅助剂并不会引起严重不良反应;④选用经临床试验和Meta分析证实有效且常规使用的局部麻醉药物辅助剂。

表4 两组术后不同时间点FLACC评分比较 (分,
FLACC:改良面部表情评分;对照组:单纯罗哌卡因骶管阻滞;试验组:罗哌卡因+右美托咪定混合液骶管阻滞;a与术后2 h比较,P<0.05;b与术后4 h比较,P<0.05;c与术后6 h比较,P<0.05;d与术后12 h比较,P<0.05;e与术后24 h比较,P<0.05;f与术后36 h,P<0.05

表5 两组麻醉镇痛相关不良反应发生情况及家属满意度比较
对照组:单纯罗哌卡因骶管阻滞;试验组:罗哌卡因+右美托咪定混合液骶管阻滞;a为χ2值;b为Z值
对临床常用椎管内阻滞局部麻醉药物辅助剂的药物毒性的研究显示,行椎管内阻滞时,不含防腐剂的吗啡和可乐定对患者无害,但氯胺酮可引起脊髓神经元凋亡增加[12]。Meta分析显示,可乐定和右美托咪定作为骶管阻滞和持续硬膜外麻醉的辅助剂具有积极作用。但另有研究证实,不含防腐剂的氯胺酮可增强骶管阻滞的麻醉效果,较可乐定延长术后镇痛时间的效果更好[13]。由于使用安全性尚不明确,且受到药物制作工艺的限制,我国并未将氯胺酮作为椎管内阻滞辅助剂应用;肾上腺素可增加神经缺血和损伤的发生风险,故不推荐用于小儿骶管及硬膜外阻滞[6]。目前应用的椎管内阻滞辅助剂为骶管神经阻滞时,可乐定和右美托咪定可改善术后镇痛,不加防腐剂的氯胺酮也可改善麻醉和镇痛效果,但氯胺酮具有引起脊髓神经元凋亡的潜在风险,故新生儿和婴幼儿应避免使用氯胺酮;硬膜外麻醉时,不加防腐剂的吗啡、可乐定和右美托咪定可提高术后镇痛效果;蛛网膜下腔麻醉时,不加防腐剂的吗啡、合成的阿片类药物和可乐定的联合使用可延长鞘内阻滞的持续时间,提高镇痛效果[6]。因此,骶管阻滞时加用右美托咪定是安全、有效、可行的镇痛方式,且具有循证基础。
本研究中,骶管阻滞时加用右美托咪定可改善小儿DDH矫形术患儿术后12 h和术后24 h的镇痛效果,并明显延长术后首次觅求镇痛药物的时间。Al-Mustafa等[14]在泌尿外科手术中鞘内注射右美托咪定5 μg和10 μg联合布比卡因作用的研究发现,右美托咪定可呈剂量依赖性地延长椎管内麻醉的持续时间。Shukla等[15]将右美托咪定与硫酸镁作为局部麻醉药物辅助剂与布比卡因联合应用于下腹部和下肢手术的研究指出,与硫酸镁相比,右美托咪定组起效迅速,且作用持续时间延长。Mohamed等[16]发现,鞘内注射5 μg右美托咪定可改善术后镇痛质量和持续时间,可为接受腹部大手术患者提供长时间的镇痛作用。对外周神经阻滞的研究证实,右美托咪定可延长周围神经阻滞作用时间,并改善术后镇痛效果[17-18]。
目前,右美托咪定延长区域阻滞镇痛时间的具体机制尚无定论,可能与其镇痛作用有关。研究证实,α2受体激动剂(可乐定、右美托咪定)作为局部麻醉药物辅助剂用于区域阻滞麻醉均具有明确的镇痛作用,但镇痛机制尚未完全阐明[19]。右美托咪定是一种咪唑类化合物,是美托咪定的右旋异构体,具有特异性的选择性α2肾上腺素能受体激动作用。有研究认为,α2受体激动剂通过内向整流的G1-蛋白质门控钾离子通道的激活,可使细胞膜超极化,从而降低中枢神经系统可兴奋细胞的放电速率,被认为是α2肾上腺素能受体激动剂的抑制性神经元作用的重要机制[20]。此外,α2肾上腺素能受体还可降低细胞内钙传导,从而抑制神经递质的释放。α2肾上腺素能受体的两种机制代表了两种截然不同的镇痛方式,第一种是阻止神经冲动的发放,第二种是阻止冲动信号向相邻神经元传导[20]。α2肾上腺素能受体激动剂还可通过抑制C类神经纤维递质释放和超极化突触后背角神经元来产生镇痛作用[21]。
右美托咪定在脊髓内的镇痛作用机制还包括:①激动脊髓后角细胞上的α2受体,抑制感觉神经递质(如致痛物质)的释放;②激动α受体的α2c亚型,与阿片类药物产生协同作用;③与胆碱能、嘌呤及5-羟色胺介导的疼痛传导系统相互作用。既往研究表明,右美托咪定具有镇痛和减轻应激反应的作用,且无明显呼吸抑制[22]。本研究中,两组患儿术中芬太尼用量比较差异无统计学意义,可见无论是否加用右美托咪定,骶管阻滞均可为DDH畸形矫正手术提供满意的术中镇痛,但0.2%罗哌卡因+右美托咪定可明显延长骶管阻滞的作用时间,达到长时间的术后镇痛效果。
本研究中,两组患儿在骶管硬膜外注药前后所有时间点及到达病房时MAP之间差异无统计学意义,与Al-Ghanem等[23]和Mohamed等[16]的研究结果一致。但有研究指出,右美托咪定用于椎管内阻滞有造成剂量相关低血压的可能,其降压作用通过兴奋脑干髓质缩血管中枢(网状核)α2抑制神经元引起,导致去甲肾上腺素释放减少以及交感神经向外周组织的传导下降,但本研究未观察到两组患儿的血压差异[24]。本研究中,试验组注药后10、20、30、60 min的心率较对照组显著降低;两组患儿注药后120 min的心率差异无统计学意义(P>0.05)。两组患儿心率的差异可能与右美托咪定全身吸收及硬膜外头侧扩散引起副交感神经流出导致中枢刺激引起迷走神经张力增加以及交感神经活性下降共同引起心动过缓有关[25]。两组患儿骶管阻滞后的心率和MAP较注药前变化显著,表明无论是否加用右美托咪定,骶管阻滞均可对循环产生影响。骶管阻滞后循环改变可能由多种因素参与,包括诱导时药物的作用时间、补液量、骶管阻滞时的体位改变、硬膜外麻醉时局部麻醉药物导致的血管扩张、手术出血等因素,但无严重循环障碍发生,表明在合理麻醉管理的前提下,无论是否加用右美托咪定,骶管阻滞对于小儿DDH矫形术均安全有效。
本研究采用相同七氟烷最低肺泡有效浓度吸入麻醉并维持相同BIS值前提下,试验组患儿术中丙泊酚用量少于对照组;术后两组患儿均出现过度镇静;试验组术后拔管即刻的镇静评分高于对照组;两组术后回病房即刻以及回病房2 h后的镇静评分比较差异无统计学意义,可见无论通过骶管局部吸收还是通过硬膜外向中枢神经系统扩散,右美托咪定均具有镇静催眠作用。药理学基础相关研究显示,右美托咪定与蓝斑处的α2受体结合可激活脑桥-脊髓的去甲肾上腺素能下行控制系统,并增加脊髓背角细胞抑制性突触的传递,进而减少伤害性信息的上行传递和体内儿茶酚胺类物质的释放,并降低手术等伤害性刺激引起的应激反应,可更好地保持血流动力学的相对稳定,减少其他全身麻醉和镇痛药物的使用[26]。研究证实,右美托咪定具有镇静催眠作用,可引起自然动眼睡眠,但不会引起过度镇静[27]。本研究两组患儿术后发生恶心、呕吐、尿潴留的发生率比较差异无统计学意义,且两组患儿家属对术后镇痛的满意度均较高。本研究也存在一定的局限性,如样本量较小,术后随访时间较短,未来仍需大样本量及长时间随访研究(术后24 h后)以明确右美托咪定的术后镇痛效果及其对阿片类药物消耗情况的影响。
综上所述,除全身麻醉外,接受DDH矫形术患儿采用0.20%罗哌卡因联合1 μg/kg右美托咪定骶管阻滞的术中及术后镇痛效果,与单独使用罗哌卡因相比,其术后首次觅求镇痛药物的时间延后,并可改善术后12 h和24 h时镇痛评分,且无严重不良反应发生。
