MIL-101(Cr)-NH2/CaCl2复合材料的热化学蓄热性能研究*
2020-01-02朱艳青时伟娜钟柳文肖秀娣徐雪青
朱艳青,时伟娜,沈 聪,钟柳文,肖秀娣,徐雪青,徐 刚†
(1.中国科学院广州能源研究所,中国科学院可再生能源重点实验室,广东省新能源和可再生能源研究开发与应用重点实验室,广州 510640;2.中国科学院大学,北京 100049)
0 引 言
在过去几十年中,化石能源面临着资源日渐枯竭和环境污染的双重压力,发展新型清洁和可再生能源技术的需求愈发紧迫。太阳能由于分布广泛、清洁、储量巨大等优点受到了研究人员的青睐[1]。但太阳能受季节、天气等因素影响严重,限制了太阳能的高效和广泛应用。蓄热技术是解决太阳能在空间和时间上分布不均的有效手段,传统蓄热技术一般分为显热蓄热[2]、潜热蓄热[3]和热化学蓄热[4]。相比于显热蓄热和潜热蓄热,热化学蓄热的蓄热密度有数倍的提升,并且其能量在储存过程中几乎无损失,有利于长期蓄热。
在热化学蓄热材料中,无机水合盐被认为是太阳能蓄热和空间加热等应用的最佳相变储能材料[5]。而基于纯无机盐的蓄热系统容易面临过度水合、潮解、水合速率慢和腐蚀性等问题,这极大地限制了无机盐在实际工程中的应用。在2002年,ARISTOV等[6]将无机盐(CaCl2和LiBr)浸渍到硅胶中形成复合材料,利用硅胶的多孔结构避免了纯无机盐的潮解和结块现象,加速了传热传质的速率。WHITING等[7]采用沸石作为多孔基质来改善硫酸镁的蓄热性能,蓄热密度达到了1 090 kJ/kg。TOKAREV等[8]研究了CaCl2/MCM-41(CaCl2质量分数为37.7%)分子筛复合材料,提高了 CaCl2的蓄热密度和吸附能力,MCM-41分子筛还可以克服结晶和腐蚀问题。此外,ARISTOV等[9]研究了膨胀石墨/氯化钙复合材料的吸水性能,并发现膨胀石墨可以提高氯化钙在低湿度下的吸水能力。多孔材料的高比表面积和大孔容有利于提高复合材料的含盐量并加快传热传质过程,而金属有机骨架由于具有极高的比表面积及灵活可变的结构受到了研究人员的广泛关注[10]。
在众多的金属有机骨架材料中,MIL-101(Cr) 是水热稳定性和化学稳定性较高的一种,且具有很大的比表面积和孔容,被认为是目前有希望应用于热化学蓄热的多孔材料之一[11]。表1列出了MIL-101(Cr)与其他多孔材料的比表面积,可以看出MIL-101(Cr)具有绝对优势[12]。但 MIL-101(Cr) 本身为疏水性材料,因此在半干旱或干旱的沙漠等低相对湿度条件下的吸水能力有限。对此,本文提出在MIL-101(Cr)中引入亲水性基团 -NH2来提高其在低相对湿度下的吸水能力,并将具有高吸水能力的吸湿盐 CaCl2与其复合,制备具有高吸水能力和高蓄热密度的MIL-101(Cr)- NH2/CaCl2复合材料。

表1 不同多孔材料的比表面积对比Table 1 Comparison of specific surface area of different porous materials
1 实验部分
1.1 样品的制备
MIL-101(Cr)-NH2的合成方法是在 LIN等[13]所提出的直接合成法基础上改进的,采用一步合成法,具体制备过程如下:
(1)将 2.40 g Cr(NO3)3·9H2O、1.08 g 2-氨基对苯二甲酸和0.6 g NaOH均匀地分散在盛有45 mL去离子水白大口瓶中,将瓶口用封口膜封住并超声处理30 min;
(2)将上述混合溶液转移至具有特氟龙衬底的高压反应釜中,反应温度设置为 150℃,反应总时长共12 h。反应完成后停止加热,使其温度逐渐降至室温;
(3)将反应产物离心获得沉淀物,并在室温下用热的N,N-二甲基甲酰胺(DMF,80℃)回流洗涤除去沉淀物表面未反应完全的2-氨基对苯二甲酸;
(4)将沉淀物在高压釜中用热乙醇(100℃)洗涤24 h以置换出孔道中的DMF,通过离心获得沉淀物;
(5)最后将反应产物在 100℃的真空干燥箱中干燥12 h,最终获得MIL-101(Cr)-NH2成品。
MIL-101(Cr)-NH2/CaCl2复合材料的制备过程:先取一定量的 MIL-101(Cr)-NH2与无水 CaCl2在100℃和 150℃的烘箱中干燥 3 h,以确保没有水分残留;称取一定量干燥后的 MIL-101(Cr)-NH2样品放置于密封的烧瓶中,外接真空泵抽取真空1 ~ 2 h;抽完真空后,将配制好的一定质量浓度的 CaCl2水溶液用注射器注入到 MIL-101(Cr)-NH2中,在智能磁力加热搅拌器内机械搅拌5 ~ 6 h;最后,离心去除多余的CaCl2水溶液获得沉淀,并在100℃烘箱内干燥过夜,所得样品即为 MIL-101(Cr)-NH2/CaCl2复合材料。
1.2 样品表征
MIL-101(Cr)-NH2和 MIL-101(Cr)-NH2/CaCl2复合材料的X射线衍射(XRD)图谱如图1所示。由图1可以看出,MIL-101(Cr)-NH2的 XRD图谱与MIIL-101(Cr) 相比,其衍射峰出现了一定的展宽,这是由于 MIL-101(Cr)-NH2本身是比较小的纳米粒子造成的[13],其纳米结构可以从后面的扫描电镜(SEM)图中得到验证。而 MIL-101(Cr)-NH2在与CaCl2复合后,其XRD图谱的小角度峰基本消失,一方面是由于 MIL-101(Cr)-NH2在复合材料中的含量较低,另一方面是由于CaCl2在MIL-101(Cr)-NH2孔内高度无序的分布进一步减低了其衍射峰强度[14]。
MIL-101(Cr)-NH2和 MIL-101(Cr)-NH2/CaCl2复合材料的 SEM 图见图2。可知 MIL-101(Cr)-NH2晶体尺寸较小,且没有明显的正八面体结构,这与XRD的测试结果一致,说明其结晶度较低。而MIL-101(Cr)-NH2在与 CaCl2复合后仍旧保留了原有的微观形貌,说明CaCl2与MIL-101(Cr)-NH2复合不会破坏其晶体结构。此外,采用X射线能谱(EDS)分析了样品的元素比例,其中Ca与Cr的质量比为1.77,由此可以计算出MIL-101(Cr)-NH2/CaCl2复合材料中CaCl2的含量约为49%。为了进一步确认复合材料中的盐含量,利用电感耦合等离子发射光谱(ICP-OES)测试了复合材料中的元素比例,其中Ca与 Cr的原子比为 1.49,进而可以计算出MIL-101(Cr)-NH2/CaCl2复合材料中 CaCl2的含量约为46%。对比这两种方法可以看出,二者的计算结果差别不大,均能得到复合材料中的盐含量。
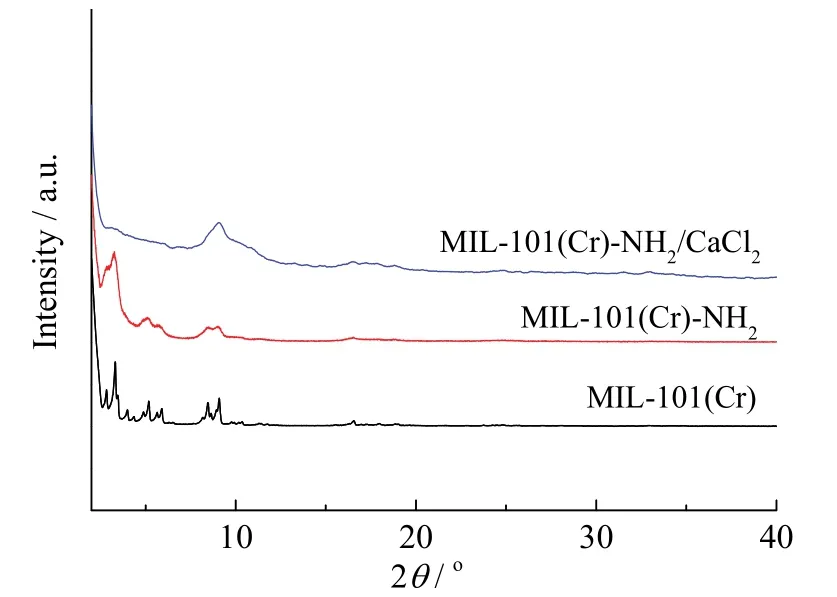
图1 MIL-101(Cr)-NH2/CaCl2复合材料、MIL-101(Cr)-NH2和MIL-101(Cr)的XRD谱图Fig.1 XRD spectra of MIL-101(Cr)-NH2/CaCl2 composite,MIL-101(Cr)-NH2 and MIL-101(Cr)

图2 MIL-101(Cr)-NH2(a)和 MIL-101(Cr)-NH2/CaCl2复合材料(b)的SEM图Fig.2 SEM diagrams of MIL-101(Cr)-NH2 (a) and MIL-101(Cr)-NH2/CaCl2 composite (b)
采用傅里叶红外光谱仪测试了MIL-101(Cr)-NH2与 MIL-101(Cr)-NH2/CaCl2复合材料的傅里叶红外光谱,结果如图3所示。可以看到,复合后的MIL-101(Cr)-NH2/CaCl2材料的FTIR光谱上依旧存在着3 443 cm−1和1 620 cm−1处的吸收带,这两个吸收带均由 -NH2中化学键的振动所引起[15],证明复合后的样品中依旧存在着 -NH2官能团,而1 259 cm−1处 C—N化学键的伸缩振动证明了官能团 -NH2依旧结合在复合后的样品骨架上,没有影响本身的结构,保留了MIL-101(Cr)-NH2本身的亲水性。
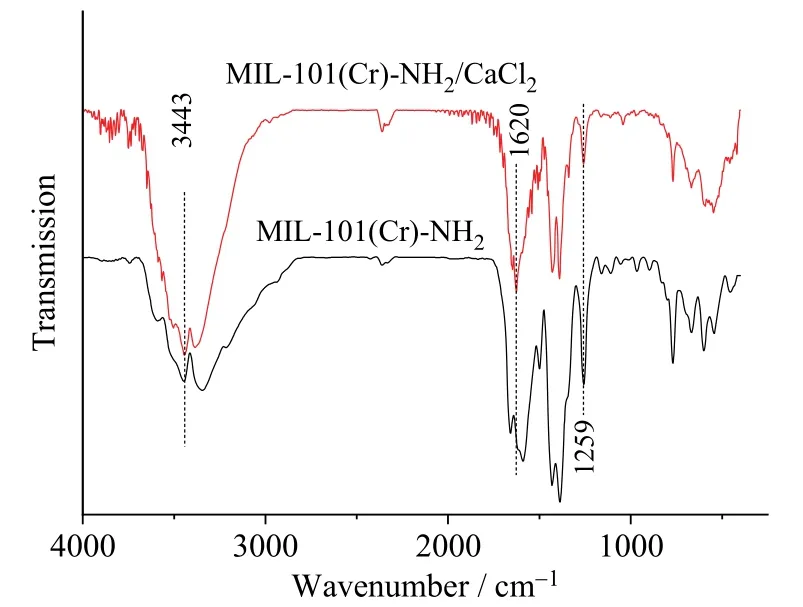
图3 MIL-101(Cr)-NH2与MIL-101(Cr)-NH2/CaCl2复合材料的傅里叶红外光谱Fig.3 FTIR spectra of MIL-101(Cr)-NH2 and MIL-101(Cr)-NH2/CaCl2 composite
为了进一步验证MIL-101(Cr)-NH2的稳定性,将复合材料MIL-101(Cr)-NH2/CaCl2中的CaCl2清洗掉,并重新进行了XRD测试,结果如图4所示。当金属有机骨架孔道内的CaCl2被洗掉之后,其X射线衍射图谱中的衍射峰因CaCl2的浸渍而略有下降,但是仍然存在,说明复合后的MIL-101(Cr)-NH2/CaCl2复合材料仍保持MIL-101(Cr)-NH2原有的骨架结构。同时,XRD结果证明复合后MIL-101(Cr)-NH2/CaCl2样品的XRD曲线中小角度衍射峰强度的降低确实是由于孔道内填充了CaCl2所致。

图4 MIL-101(Cr)-NH2与MIL-101(Cr)-NH2/CaCl2清洗后的XRD图谱Fig.4 XRD patterns of MIL-101(Cr)-NH2 and MIL-100(Cr)-NH2/CaCl2 composite after washing
此外,采用氮气吸附−脱附测试获得了MIL-101(Cr)-NH2与 MIL-101(Cr)-NH2/CaCl2复合材料的氮气吸附−脱附曲线,如图5所示。根据氮气吸附−脱附曲线,计算出了 MIL-101(Cr)-NH2与MIL-101(Cr)-NH2/CaCl2复合材料的 BET比表面积和总孔容,如表2所示。可以看到,MIL-101(Cr)-NH2的比表面积在与CaCl2复合后由1 900 m2/g降到了137 m2/g,总孔容也由2.49 cm3/g减少到0.37 cm3/g,这是由于 MIL-101(Cr)-NH2的孔道被 CaCl2部分填充所导致。另外,MIL-101(Cr)-NH2/CaCl2复合材料的氮气吸附−脱附曲线的滞后环出现了明显的展宽和拖尾,这是由于CaCl2在MIL-101(Cr)-NH2的孔道内形成了多孔塞所引起的[16-17],这也证明了 CaCl2存在于MIL-101(Cr)-NH2的孔道内。
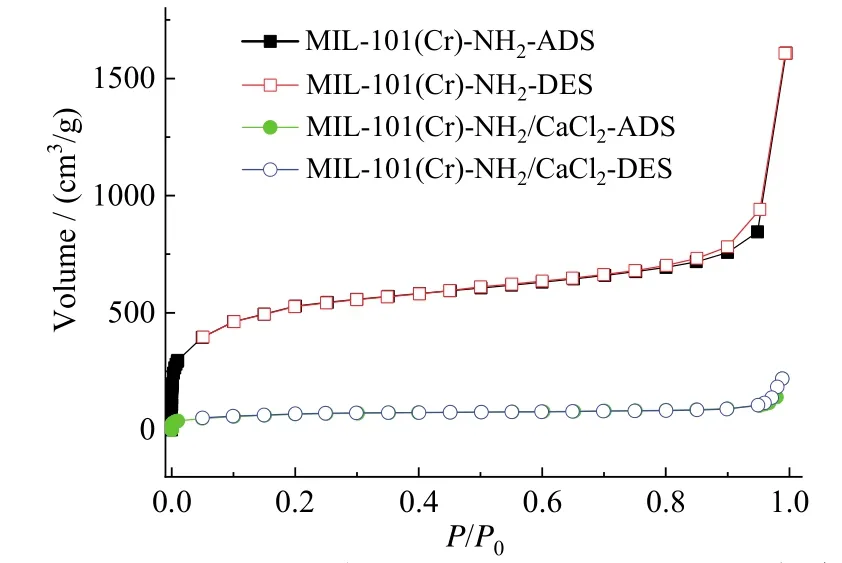
图5 MIL-101(Cr)-NH2与MIL-101(Cr)-NH2/CaCl2复合材料的氮气吸附−脱附曲线Fig.5 N2 adsorption-desorption isotherms of MIL-101(Cr)-NH2 and MIL-101(Cr)-NH2/CaCl2 composite

表2 MIL-101(Cr)-NH2与MIL-101(Cr)-NH2/CaCl2复合材料的BET比表面积和孔容Table 2 BET surface areas and pore size distributions of MIL-101(Cr)-NH2与MIL-101(Cr)-NH2/CaCl2 composite
2 MIL-101(Cr)-NH2/CaCl2复合材料的吸附性能测试
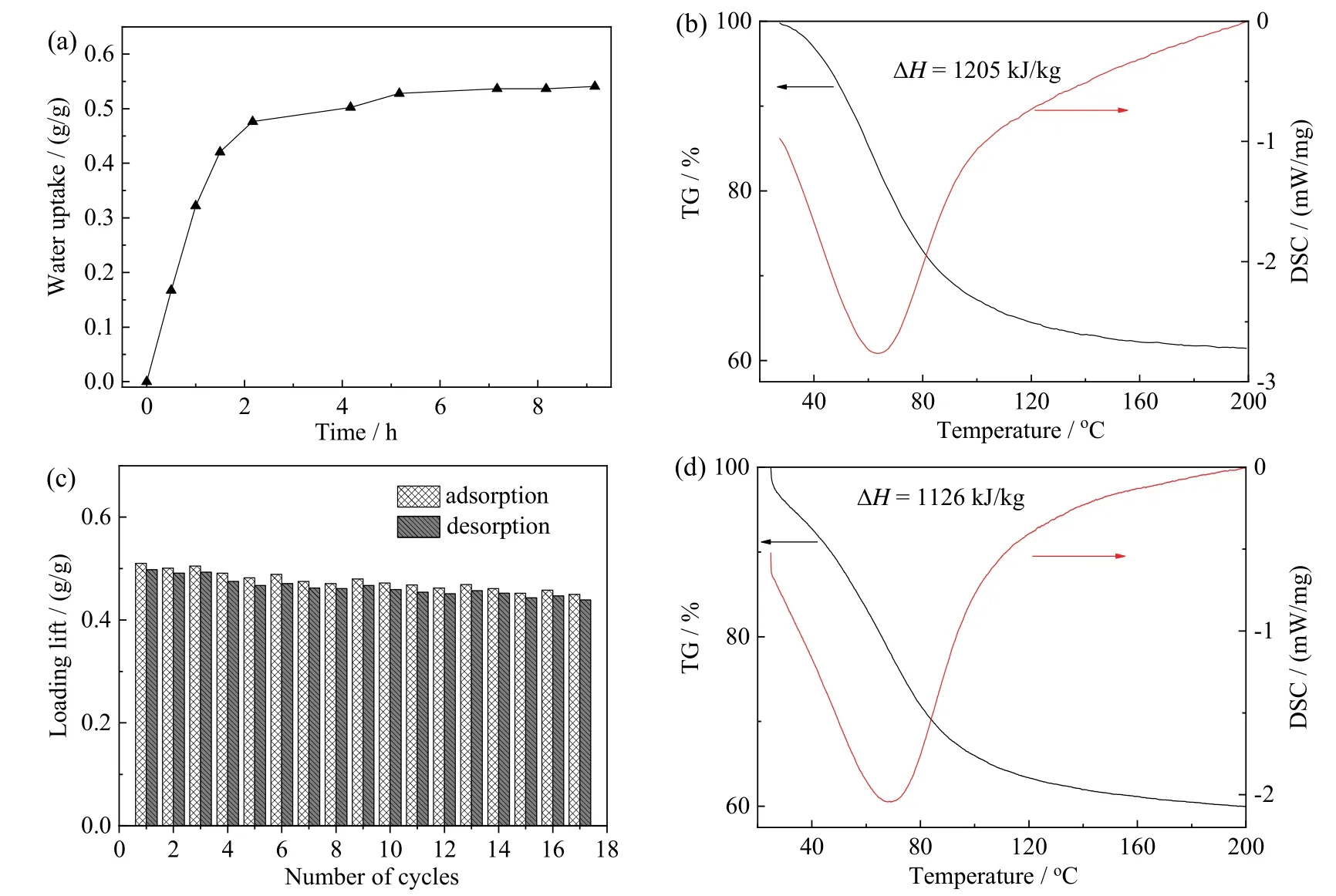
图6 MIL-101(Cr)-NH2/CaCl2复合材料的水合曲线(a)、TG-DSC曲线(b)、循环负载量(c)及循环后的TG-DSC曲线(d)Fig.6 Water adsorption curve (a), TG-DSC curves (b), stability of the cycle loading lift (c) and TG-DSC curves after cycle loading lift (d) of MIL-101(Cr)-NH2/CaCl2 composite
利用自主搭建的恒温恒湿系统对复合材料MIL-101(Cr)-NH2/CaCl2进行了水合能力测试。将50 g MIL-101(Cr)-NH2/CaCl2复合材料在 30℃和 32%相对湿度的条件下水合9 h,其水合过程的吸水量如图6a所示,最大吸水量达到了0.54 g(H2O)/g(样品)。随后测试了 MIL-101(Cr)-NH2/CaCl2复合材料的热重−差热扫描量热(TG-DSC)曲线,如图6b所示。其解吸过程中的蓄热密度为1 204 kJ/kg,解吸的峰值温度为 70℃。为了研究 MIL-101(Cr)-NH2/CaCl2复合材料的循环稳定性,对其进行了17次连续的吸附−脱附循环测试,循环次数要高于PERMYAKOVA等[18]报道的 11次循环,所测试的循环负载量如图6c所示。循环时吸附条件为30℃和32%相对湿度下吸附8 h,解吸条件为120℃下解吸4 h。循环后的TG-DSC曲线如图6d所示,其蓄热密度为1 126 kJ/kg,相比于循环前只下降了6.5%,表现出了优异的循环稳定性。
3 结 论
采用金属有机骨架 MIL-101(Cr)-NH2作为多孔基质材料、CaCl2作为吸湿盐,制备了具有高吸水能力高蓄热密度的复合材料MIL-101(Cr)-NH2/CaCl2。采用XRD、SEM、EDS和TG-DSC等多种表征手段测试了其微观结构和吸附性能。MIL-101(Cr)-NH2/CaCl2复合材料在低温低湿环境下(30℃、32%相对湿度)的吸水量可达0.54 g(H2O)/g(样品),蓄热密度达到了1 204 kJ/kg,并且在经历了17次吸附−解吸循环后,其蓄热密度仅降低了6.5%,表现出优异的循环稳定性。这一新型复合材料在太阳能蓄热领域具有广阔的应用前景。
