不同诱因噬血细胞综合征患者的临床特征及预后分析
2019-12-27杨学兵陆雯萍余先球施小凤丁宏胜陆益龙
杨学兵,陆雯萍,余先球,施小凤,丁宏胜, 陆益龙
(1. 南通大学附属海安医院重症医学科,江苏 海安 226600; 2. 江苏大学附属医院血液科,江苏 镇江 212001)
噬血细胞综合征(hemophagocytic syndrome, HPS)是一种严重威胁生命的免疫功能紊乱性疾病,临床主要表现为高热,肝、脾、淋巴结肿大,黄疸,进行性全血细胞减少。HPS分原发性和继发性,成人以继发性为主,多因不同病因致患者体内炎症因子高表达并激活单核-巨噬细胞系统致多脏器损害。该类疾病早期诊断难、病情发展迅速,临床预后差。本研究回顾性分析35例HPS患者临床资料及病情发展规律,为该类患者早诊、早治,改善患者预后提供参考依据。
1 资料与方法
1.1 临床资料
收集2013年1月至2018年12月我院及江苏大学附属医院诊治的35例HPS患者,其中男16例,女 19 例,年龄30~80岁,中位年龄61岁。根据HPS患者原发疾病分为EB病毒感染组(12例)、肿瘤相关组(13例)和免疫疾病组(10例)。将EB病毒感染组患者HPS相关临床特征在2周内全面表现者设为早期表现组(5例),>2周者设为迟发表现组(7例)。EB病毒感染组及肿瘤相关组HPS患者中,对确诊并行干预性治疗120 d内死亡者设为近期死亡组,超过120 d死亡、包括长期存活者为非近期死亡组。参照2004年HPS诊断标准: ① 发热:体温>38.5°C,持续>7 d; ② 脾脏肿大; ③ 血细胞减少(累及外周血两系或三系):血红蛋白<90 g/L,血小板计数<100×109/L,中性粒细胞<1.0×109/L且非骨髓造血功能减低所致; ④ 高三酰甘油血症和(或)低纤维蛋白原血症:三酰甘油>3 mmol/L; ⑤ 骨髓、脾脏、肝脏或淋巴结穿刺可见噬血细胞; ⑥ 血清铁蛋白≥500 μg/L; ⑦ NK细胞活性降低或缺如; ⑧ sCD25升高。符合以上8条指标中5条者确诊。
1.2 方法
入院患者当日抽取静脉血检测以下指标:外周血象(血细胞分析仪);肝肾功能、血脂及肌酶谱(全自动生化分析仪);EB病毒-DNA(EB病毒核酸扩增荧光定量检测法);淋巴细胞免疫分型(流式细胞仪);肿瘤指标(AFP、CEA、CA125、CA199、CA50)及血清铁蛋白(同位素法);凝血指标(凝固法);自身抗体(酶标法)等指标检测。并通过胸腹部CT平扫、B超定位明确患者有无肝、脾、浅表淋巴结肿大及是否合并有肺部感染。血片、骨髓穿刺涂片检查通过光学显微镜进行人工观察分析。
1.3 临床治疗
EB病毒感染组及免疫相关组患者均采用HPS(2004)方案治疗。初始治疗8周:地塞米松10 mg/(m2·d) 2周 、5 mg/(m2·d)2周、2.5mg/(m2·d)2周、1.25 mg/(m2·d)2周。VP16每次 150 mg/m2,2次/周、共 2周;1次/周,共6周。环孢素A 6 mg/(kg·d),口服,1周后监测血药浓度,后每月监测1次,维持环孢素A血药浓度在200 mg/L左右。HPS发病过程中有神经系统症状者,行脑脊液检查,脑脊液检查异常者予甲氨蝶呤、地塞米松二联鞘注,从第3周开始,每周1次,共4次。维持治疗(9~40周):地塞米松10 mg/(m2·d),3 d/2周;VP16每次150 mg/m2,1次/2周;环孢素A同初始治疗,直到40周后。肿瘤相关组HPS依据患者原发性疾病予以相应化疗方案治疗。
1.4 统计学分析

2 结果
2.1 HPS患者临床特征比较
HPS患者均以发热、脾肿大、外周血象变化、高乳酸脱氢酶、低纤维蛋白原、高血清铁蛋白、骨髓中见噬血细胞为主要临床特征。骨髓涂片检查结果显示,35例HPS患者中,骨髓有核细胞增生明显活跃22例,增生活跃13例。所有病例骨髓涂片中均可见吞噬细胞,其形态特征为细胞胞质量丰富、并可见细颗粒、空泡及吞噬的幼红细胞、粒细胞、血小板及细胞碎片,核不规则型多见,核染色质紧密,核仁不明显,该类细胞在骨髓涂片中有核细胞占比为3%~7.5%,EB病毒感染组为(4.61±1.25)%、肿瘤相关组为(4.22±0.93)%和免疫疾病组为(3.51±0.58)%,3组噬血细胞占比差异无统计学意义(F=0.715,P>0.05)。
2.2 不同诱因HPS患者临床各指标比较
EB病毒感染组谷草转氨酶、乳酸脱氢酶水平较肿瘤相关组明显升高,差异有统计学意义(P<0.05),免疫疾病组血小板计数较肿瘤相关组和EB病毒感染组升高,差异均有统计学意义(P<0.05),免疫疾病组谷丙转氨酶、谷草转氨酶和乳酸脱氢酶较EB病毒感染组均明显降低,差异均有统计学意义(P<0.05)。见表1。
2.3 EB病毒感染HPS患者诊断时期及治疗对患者预后影响
结果表明,迟发表现组患者血清白蛋白水平明显低于早期表现组,差异有统计学意义(P<0.01);谷丙转氨酶、谷草转氨酶、乳酸脱氢酶水平显著高于早期表现组。见表2。早期表现组血清铁蛋白>20 000 ng/L患者数3例、迟发表现组为7例,迟发表现组患者高血清铁蛋白患者比例显著高于早期表现组(χ2=4.278,P<0.05);迟发表现组近期死亡患者数(4例)明显高于早期表现组(0例)(χ2=12,P<0.05)。

表1 肿瘤相关组、EB病毒感染组、免疫疾病组HPS患者各指标比较
a:与肿瘤相关组比较,P<0.05;b:与EB病毒感染组比较,P<0.05
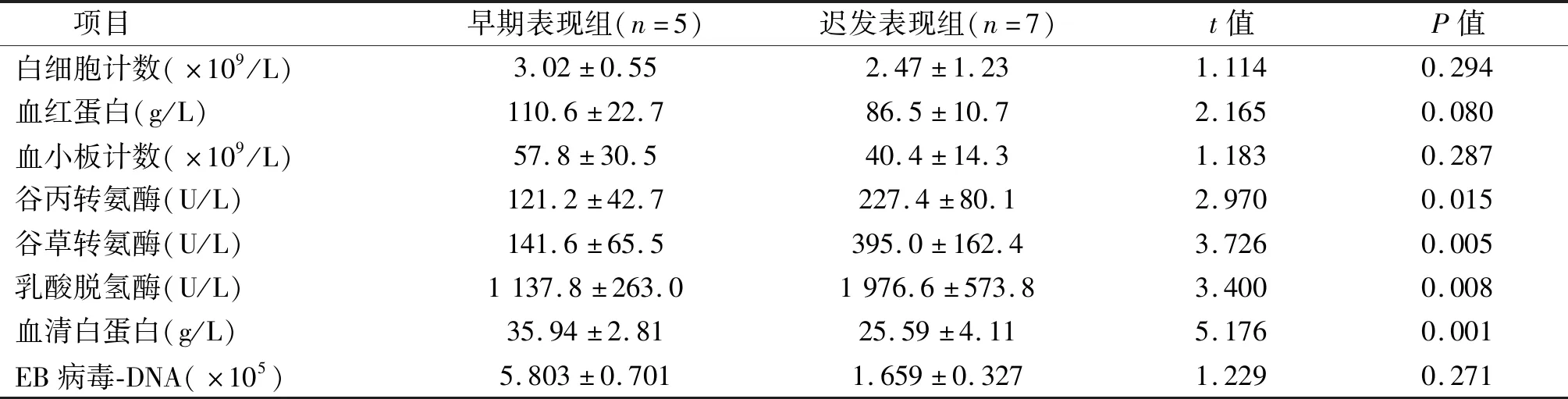
表2 EB病毒感染相关HPS早期表现组与迟发表现组各指标比较
2.4 近期死亡组与非近期死亡组各指标水平比较
比较结果显示,近期死亡组患者谷丙转氨酶、谷草转氨酶、乳酸脱氢酶水平显著高于非近期死亡组患者,而血红蛋白水平明显降低。见表3。近期死亡组及非近期死亡组患者中,血清铁蛋白>20 000 ng/L的患者数分别为6例和8例,近期死亡组高血清铁蛋白患者比例显著高于非近期死亡组(χ2=25.0,P<0.05)。
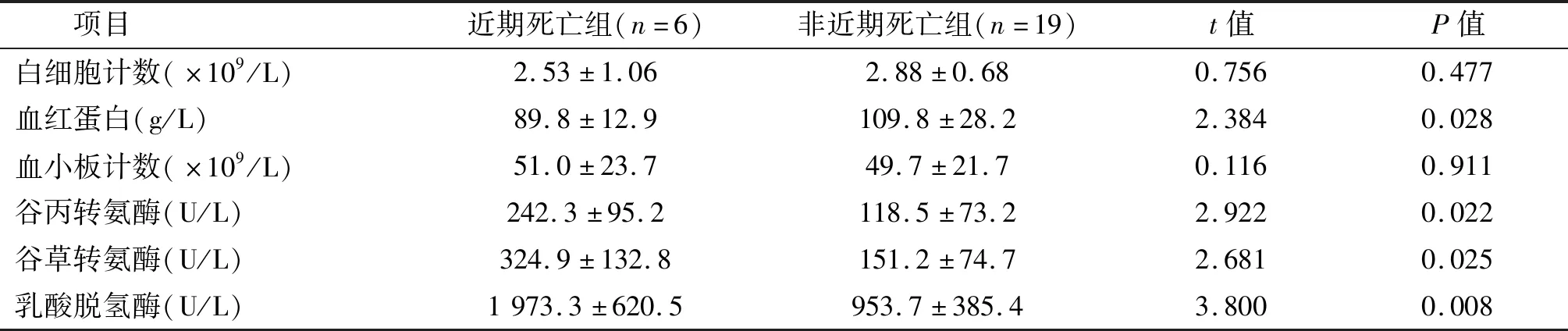
表3 近期死亡组与非近期死亡组各指标水平比较
2.5 HPS患者预后比较
EB病毒感染组患者近期死亡率(33.3%,4/12例)明显高于肿瘤相关组(15.4%,2/13例),差异有统计学意义(χ2=25.0,P<0.05)。EB病毒感染组患者死亡原因为感染并多脏器功能衰竭,肿瘤相关组患者死亡原因为严重低蛋白血症并多脏器功能衰竭。EB病毒感染组患者中有2例分别于26个月、32个月后并发急性髓系白血病,1例18个月后并发T细胞淋巴瘤,现仍接受治疗,另3例无病生存。
3 讨论
HPS属于单核细胞巨噬细胞系统的过度反应疾病,早期诊断较难,目前普遍认为继发性HPS以感染、免疫性疾病及继发肿瘤者多见[1]。该类疾病发生多表现为多脏器损害,这与HPS发病过程中患者体内CD8+T细胞、巨噬细胞过度活化并进而降低细胞毒性T细胞(CTL)对抗原提呈细胞的清除,导致患者体内持续存在CD8+T细胞慢性刺激有关[2]。HPS患者临床表现为血清谷丙转氨酶、谷草转氨酶、乳酸脱氢酶升高,全血细胞减少及血清白蛋白降低。三组HPS患者中,发热、脾肿大、外周血象变化明显,EB病毒感染相关HPS患者上述临床特征表现更为明显。程艳丽等[3]对28例EB病毒感染相关HPS患者临床资料采用 Logistic回归分析,显示EB病毒感染、CD4/CD8比例倒置是HPS 死亡的高危因素。本研究表明,EB病毒感染相关HPS患者肝、脾、淋巴结肿大,多浆膜腔积液的发生率高于肿瘤相关组和免疫疾病组患者,且EB病毒感染组患者死亡率最高。
乳酸脱氢酶为胞内酶,体内组织细胞出现损伤、破坏增多时会明显升高[4],且乳酸脱氢酶升高的水平及持续的时间反映了组织损伤的程度[5]。本资料显示三组HPS患者乳酸脱氢酶水平均明显升高,EB病毒感染相关HPS患者乳酸脱氢酶升高更为显著。有资料显示[6]:NK/T 淋巴瘤相关HPS诊断与死亡(最后一次接触)时间间隔为4~701 d,中位时间间隔为15 d。乳酸脱氢酶在HPS、低纤维蛋白原血症和脾肿大与较差的生存率显著相关。高乳酸脱氢酶与HPS患者预后直接相关[7]。另有文献报道:初诊3周内HPS患者血清铁蛋白>11 000 μg/L者的死亡率是<11 000 μg/L患者死亡率的5.6倍[8]。本组病例中,EB病毒相关HPS迟发表现组患者高死亡率及近期死亡HPS患者血清乳酸脱氢酶及铁蛋白均显著升高同样说明这一点。有研究报道,低蛋白血症会减少患者体内自由基中和作用,降低治疗中的药物作用[10],因此严重低蛋白血症也是EB病毒相关HPS患者近期高死亡率原因之一。
综上所述,HPS患者病情发展迅速,死亡率高,尤其是EB病毒感染HPS患者。早期明确诊断、尽早干预治疗是HPS治疗成功的关键。因此,临床上对发热原因不明,合并有白细胞、血小板计数减少,谷丙转氨酶、谷草转氨酶及乳酸脱氢酶升高的迟发表现HPS患者应及早进行EB病毒筛查及多部位骨髓穿刺涂片检查,可尽早明确EB病毒感染相关HPS诊断并能得到早期有效治疗、提高该类HPS患者治疗效果。
