重组人内皮抑制素联合同步放化疗对局部晚期非小细胞肺癌的疗效及安全性分析
2019-12-20徐海玲吕冬青王碧云王苗孟胤男周超王微杨海华
徐海玲 吕冬青 王碧云 王苗 孟胤男 周超 王微 杨海华
非小细胞肺癌(non-small-cell lung cancer,NSCLC)是肺癌的主要病理类型,占80%~85%。对于局部晚期NSCLC,同步放化疗是目前的标准治疗方案。相关研究结果表明,同步放化疗对NSCLC的效果优于贯序放化疗[1-2]。近年来发现,抗血管生成抑制剂对晚期NSCLC也有很好的临床疗效。其中重组人血管内皮抑制素具有诱导凋亡、肿瘤血管正常化、放疗增敏等特点且不良反应较少,目前被广泛用于肿瘤治疗[3-4]。对于初治或复发的NSCLC患者,重组人内皮抑制素联合化疗(顺铂及长春瑞滨)能提高患者生存,被推荐为一线治疗方案[5-7]。但在局部晚期NSCLC患者中,同步放化疗联合抗血管生成药物的治疗效果仍未明确。如关于贝伐单抗联合放化疗对局部晚期肺癌患者的疗效尚有争议,在肺鳞癌患者中甚至会增加大出血的风险[8-9]。而最新HELPER研究表明,重组人内皮抑制素联合同步放化疗(化疗方案为依托泊苷及顺铂)治疗不可手术的Ⅲ期NSCLC患者,其无进展生存期(PFS)和总生存期(OS)分别达到13.3、34.7个月,且不增加不良反应[10]。相对于单纯化疗或重组人内皮抑制素联合化疗方案,重组人内皮抑制素联合其他同步放化疗(化疗方案为多西他赛联合顺铂、依托泊苷联合顺铂等)的临床试验结果也取得了较好的生存效益[11-12]。因此,本研究对重组人内皮抑制素联合同步放化疗(化疗方案为长春瑞滨联合卡铂)治疗局部晚期NSCLC患者的临床疗效及安全性作一探讨,现将结果报道如下。
1 对象和方法
1.1 对象 选取2008年12月至2017年12月本院收治且经组织学或细胞学病理确诊为晚期NSCLC的122例患者,其中接受同步放化疗(单纯治疗组)76例,接受重组人内皮抑制素联合同步放化疗(联合治疗组)46例。两组患者性别、年龄、吸烟史、病理类型、TNM分期比较,差异均无统计学意义(均P>0.05);两组患者卡氏功能状态(KPS)评分比较,差异有统计学意义(P<0.05),见表1。本研究经浙江省台州医院伦理委员会审核通过,相关治疗及操作前所有患者均对本研究知情同意并签署知情同意书。

表1 两组患者一般资料比较(例)
1.2 治疗方法 (1)单纯治疗:仅予同步放化疗,共6个周期。化疗方案:酒石酸长春瑞滨注射液(江苏豪森药业集团有限公司,商品名:盖诺,每支1ml∶10mg,国药准字 H19990278),12.5mg/m2,静脉滴注,1 次/周;卡铂注射液(齐鲁制药有限公司,商品名:波贝,每支10ml∶100mg,国药准字 20020180),AUC=2,静脉滴注,1 次/周。胸腔放疗方案:采用三维适性放射治疗,总剂量60Gy。剂量限制:脊髓 Vmax<45Gy;肺 V5<65.0%,V20<30.0%,平均肺剂量<18.0Gy,心脏 V40<40.0%。(2)联合治疗:予重组人内皮抑制素联合同步放化疗。其中重组人内皮抑制素注射液(山东先声生物制药有限公司,商品名:恩度,每支 3ml∶15mg,国药准字 S20050088),7.5mg/m2,连续静脉滴注(第1~14天),休息1周,共2个周期;放化疗方案与单纯治疗组相同,共6个周期。
1.3 疗效评价 患者治疗1个月后进行胸部CT检查,以评估肿瘤病灶大小及消退情况,并根据实体瘤疗效评价标准(RECIST v1.1)评定结果,包括完全缓解(CR)、部分缓解(PR)、疾病稳定(SD)和疾病进展(PD)[13]。疾病客观缓解率(ORR)指经治疗后获得缓解(CR+PR)的病例数占所有可评价病例数的百分比。疾病控制率(DCR)是指经治疗后获得缓解(CR+PR)和SD的病例数占所有可评价病例数的百分比。每次随访复查血常规、肿瘤指标、肝肾功能等,记录放射性肺炎、放射性食管炎、骨髓抑制及恶心呕吐等不良反应发生情况,并根据不良反应CTCVE 5.0评定标准分级(0~5级)。
1.4 统计学处理 应用SPSS 20.0统计软件。不符合正态分布的计量资料用中位数表示;计数资料用率表示,组间比较采用χ2检验。采用Kaplan-Meier法绘制生存曲线,计算中位PFS及OS,生存率的比较采用log-rank法。P<0.05为差异有统计学意义。
2 结果
2.1 两组患者近期疗效比较 单纯治疗组CR 7例,PR 59例,SD 4例,PD 6例;ORR为86.8%,DCR为92.1%。联合治疗组CR 2例,PR 35例,SD 5例,PD 4例;ORR为80.4%,DCR为91.3%。两组患者ORR及DCR比较,差异均无统计学意义(均P>0.05)。
2.2 两组患者生存情况比较 本研究随访1~85个月,中位随访时间为19.9个月。单纯治疗组与联合治疗组中位PFS分别为9.3、14.5个月,差异有统计学意义(P<0.05);中位OS分别为15.0、21.5个月,差异亦有统计学意义(P<0.05),见图1。进一步作病理类型亚组分析,结果显示肺腺癌患者单纯治疗组与联合治疗组中位PFS分别为9.0、19.0个月,差异有统计学意义(P<0.05);中位OS分别为15.5、23.7个月,差异无统计学意义(P>0.05),见图2。肺鳞癌患者单纯治疗组与联合治疗组中位PFS分别为9.6、14.2个月,中位OS分别为15.0、21.1个月,两组比较差异均无统计学意义(均P>0.05),见图3。

图1 两组NSCLC患者PFS及OS曲线

图2 两肺腺癌亚组患者PFS及OS曲线
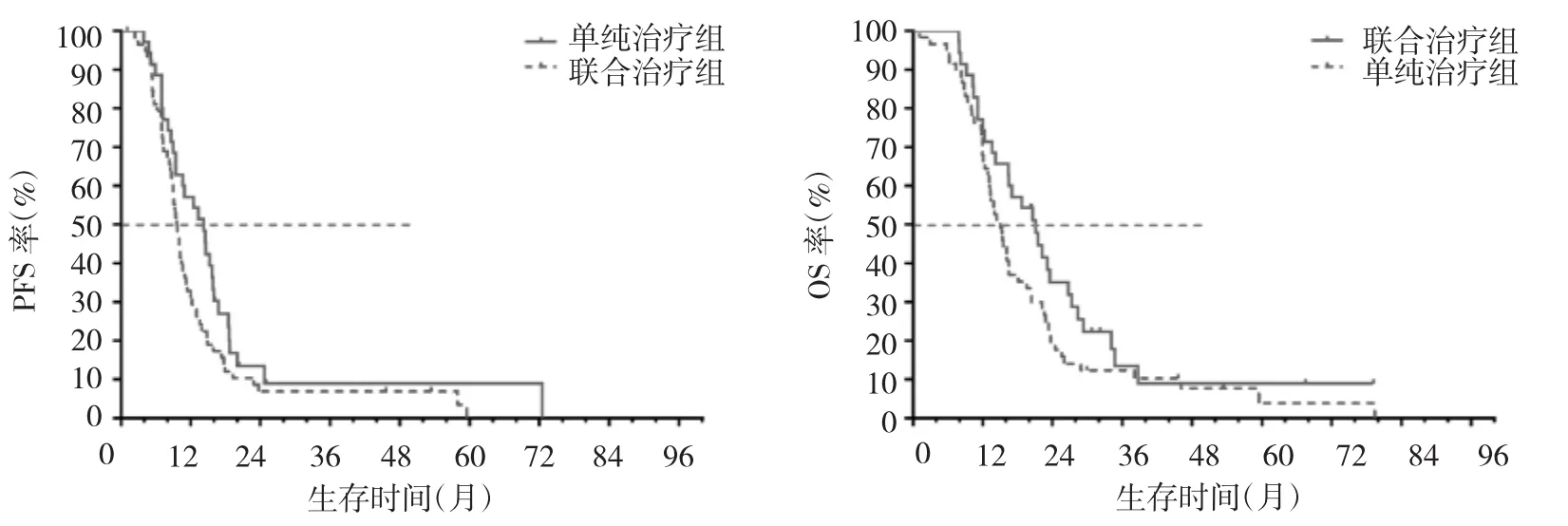
图3 两肺鳞癌亚组患者PFS及OS曲线
2.3 两组患者不良反应比较 两组患者恶心呕吐、放射性肺炎发生率比较,差异均有统计学意义(均P<0.05);骨髓抑制、放射性食管炎发生率比较,差异均无统计学意义(均P>0.05)。两组患者3级以上不良反应有骨髓抑制、放射性肺炎,见表2。

表2 两组患者不良反应比较(例)
3 讨论
重组人血管内皮抑素是一种重要的抗血管生成抑制剂,可通过促进血管内皮凋亡、诱导肿瘤血管正常化、改善肿瘤乏氧情况等多种机制发挥抗肿瘤的作用[14]。研究表明,重组人内皮抑制素可以诱导肿瘤血管出现“窗口期”,大约出现在药物使用后第4~10天。此阶段肿瘤血管正常化、局部血流灌注增加、乏氧情况改善,因此放化疗的效果更明显。体内外试验也证实重组人内皮抑制素联合其他治疗可明显改善肿瘤患者的ORR。同时,在许多临床试验中证实重组人内皮抑制素联合同步放化疗(包括长春瑞滨、多西他赛、依托泊苷及紫杉醇等双药化疗)能使晚期NSCLC患者生存获益。最近HELPER试验结果表明,与同步放化疗相比,重组人内皮抑制素联合同步放化疗能降低肿瘤远处转移率,延长患者OS,但其局部肿瘤控制效果仍无断论,需要更多研究来验证[10]。
本研究结果显示,单纯治疗组与联合治疗组患者中位PFS和OS比较,差异均有统计学意义;这说明重组人内皮抑制素联合同步放化疗能改善局部晚期NSCLC的生存情况。此外,亚组分析结果显示,肺腺癌患者联合治疗组中位PFS较单纯治疗组明显延长,而两组中位OS比较差异无统计学意义;肺鳞癌患者两组中位PFS及OS比较,差异均无统计学意义。以上结果表明,重组人内皮抑制素联合同步放化疗能使晚期肺腺癌患者的生存获益更多。虽然两组肺鳞癌患者生存比较差异无统计学意义,但是我们也能看到重组人内皮抑制素联合同步放化疗可以延长肺鳞癌患者的PFS及OS(5~6个月)。因此,对于肺鳞癌患者,重组人内皮抑制素联合同步放化疗的疗效需要进一步分层分析,或探索预测指标以更好地指导临床应用。
相对于重组人内皮抑制素单独联合化疗或放疗的不良反应,三联治疗是否增加不良反应也是本研究的重点。据统计,重组人内皮抑制素联合治疗最常见的不良反应为出血、骨髓抑制、放射性肺炎、放射性食管炎、高血压、心律失常等。因此,本研究也对上述不良反应进行了观察。在本研究中,最常见的3级以上不良反应为骨髓抑制,但两组差异无统计学意义。两组患者恶心呕吐及放射性肺炎发生率比较,差异均有统计学意义;但两组3级以上放射性肺炎发生率比较差异无统计学意义。这说明在重组人内皮抑制素联合化疗的基础上加用放疗,获得晚期肺癌患者的生存效益时并不增加严重的不良反应。相关研究表明,较贝伐单抗等抗血管生成药物,重组人内皮抑制素治疗NSCLC患者出现出血等不良反应更少,适用范围更广[8]。
综上所述,重组人内皮抑制素联合同步放化疗(长春瑞滨联合卡铂)方案能明显延长局部晚期NSCLC患者的PFS和OS,且不增加严重的不良反应,尤其是对晚期肺腺癌患者的生存情况改善明显。
