胰腺内副脾伴表皮样囊肿误诊误治分析
2019-12-18王少健陈娇丁忠祥张治邦干兴平
王少健 陈娇 丁忠祥 张治邦 干兴平
1浙江天台县人民医院放射科,天台 317200;2浙江省人民医院放射科,杭州 310014
副脾是存在于正常脾脏以外,与脾脏结构相似、功能相同的异位脾组织。胰腺内副脾表皮样囊肿(epidermoid cyst in intrapancreatic accessory spleen, ECIPAS)是副脾发生于胰腺尾部并伴表皮样囊肿形成,临床中极为罕见,易被误诊为胰腺肿瘤性病变而进行不必要的手术治疗。本研究回顾性分析8例被误诊为胰腺肿瘤的ECIPAS患者的临床和影像学资料,分析误诊误治的原因,以期提高对ECIPAS影像学特征的认识。
资料和方法
一、临床资料
收集2008年6月至2018年2月间天台县人民医院初诊后转至浙江省人民医院诊治并经病理证实的8例ECIPAS患者的临床、病理及影像学资料。8例中男性1例,女性7例;年龄32~59岁,平均年龄48岁。1例因体检发现血清CA19-9升高就诊,7例因体检发现胰腺占位就诊。8例患者均无腹痛、腹泻、黄疸或体重减轻等症状,既往无腹部外伤、手术或急、慢性胰腺炎等病史。
二、影像学检查方法
1.CT检查方法:8例患者中6例行CT检查。检查前常规禁食8 h,扫描前30 min、扫描前即刻分别口服2.5%甘露醇500 ml。CT检查使用SOMATOM Definition AS 40 X线计算机断层扫描装置,采用常规平扫和3期增强扫描。扫描范围自胰腺上1 cm向下至十二指肠水平段。先行常规轴位扫描,层厚10 mm;再行多平面重建,层厚2 mm。对比剂为碘海醇(总量100 ml,350 mg I/ml),用高压注射器注入,注射速率为3 ml/s。
2.MRI检查方法:4例患者行MRI检查,其中2例同时行CT检查。MRI检查使用MAGNETOM Avanto 1.5T磁共振扫描仪。T1WI序列参数:重复时间(repetition time,TR) 150 ms,回波时间(echo time,TE)4.8 ms;T2WI序列参数:TR 1 400 ms,TE 96.0 ms,层厚5 mm;增强扫描T1WI序列参数:TR 4.7 ms,TE 2.4 ms,层厚3 mm。对比剂为钆喷酸葡胺,剂量0.10 mmol/kg体重,用高压注射器注入,注射速率为2~2.5 ml/s。
3.影像学分析:明确病灶的位置、大小、形态,寻找病灶的实性部分并观察实性部分的形态、密度或信号、强化方式,将实性部分平扫同脾脏密度或信号比较。增强扫描则分别与胰腺和脾脏比较。
结 果
一、影像学表现
8例患者病灶均位于胰腺尾部,边缘超过胰腺尾部尖端,直径为22~50 mm,平均35 mm。病灶呈囊实性,3例为单房,5例为多房。3例以囊性为主,囊壁呈线状,厚薄均匀,增强后轻度强化,由于实性部分太小而不能观察,因此难以与脾脏进行比较。5例观察到实性成分,其中1例实性形态不规则。实性部分密度或信号与脾脏相似,CT呈等密度,MRI示T1WI呈等或稍低信号,T2WI呈等或稍高信号(图1A),弥散加权成像(duffusion weighted imaging, DWI)呈高信号,表观扩散系数呈低信号;囊性部分CT值接近水密度,MRI示T1WI呈低信号、T2WI呈高信号。动态增强扫描示1例患者实性部分形态不规则,动脉期呈不均匀强化,与脾脏“花斑样”强化方式及程度相似;其余4例病灶实性部分动脉期均匀强化且强化程度高于胰腺(图1B),门静脉期均匀强化且与脾脏强化程度一致(图1C)。
二、诊断和治疗
5例患者血清CA19-9轻度升高,3例CA19-9正常。术前诊断胰腺囊腺癌1例,实性假乳头状瘤1例,胰腺囊性肿瘤1例,囊腺瘤5例。8例患者均行手术治疗,其中4例行胰腺远端联合脾切除术、4例行保留脾脏的胰腺远端切除术。1例术后出现胰瘘和胰周坏死物包裹。术前CA19-9升高的5例患者术后复查CA19-9均恢复正常。所有病例术后病理均证实为ECIAPS(图1D)。术后随访为半年至5年,均未见复发迹象。
讨 论
副脾是一种脾脏常见的先天性变异,与脾脏结构相似、功能相同[1]。副脾发生率为10%~30%,80%位于脾门附近,17%位于胰尾,称胰腺内副脾,多为单发,有包膜包裹,部分包膜不完整[2]。胰腺内副脾伴发表皮样囊肿极为罕见,ECIPAS与脾的表皮样囊肿起源相同,属于真性囊肿,发生率仅为1.7%[3]。ECIPAS一般无明显的临床表现,多在体检或检查其他病变时偶然发现。实验室检查多在正常范围,部分ECIPAS患者血清CA19-9升高[3]。本组8例患者中5例血清CA19-9升高,术后复查均降至正常水平。
影像学上,ECIPAS表现为胰腺尾部囊实性肿块,以囊性为主,单房或多房[3],基本位于胰腺尾部尖端或接近尖端处。本组资料显示ECIPAS实性部分CT密度或MR信号及强化方式与脾脏相似,与文献报道一致[4-6],因此寻找囊肿周围副脾组织是诊断的关键。副脾组织增强扫描动脉期均匀或不均匀强化且强化程度高于胰腺,门静脉期均匀强化且与脾脏强化程度一致[7-8]。当副脾组织较少时,难以与脾脏进行宏观比较。
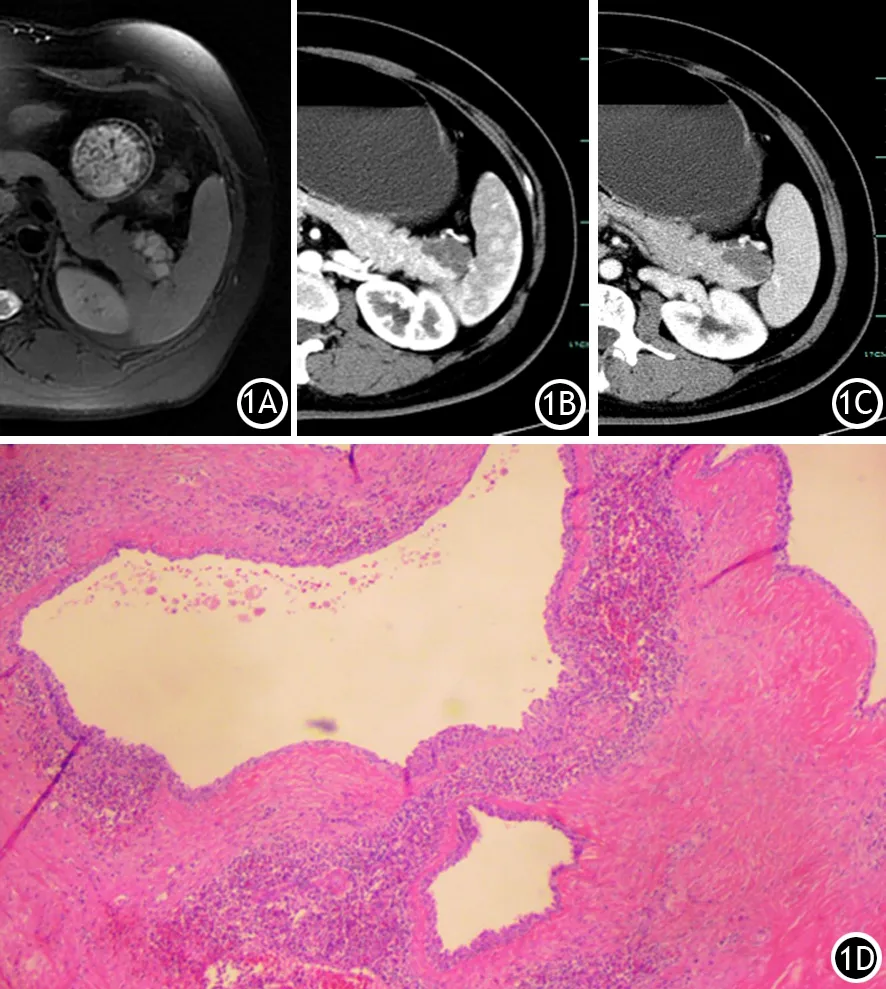
图1 胰腺尾部囊实性肿块,实性部分T2WI信号与脾脏相似(1A);增强后动脉期实性部分及囊壁强化,强化程度高于胰腺(1B)、门静脉期均匀强化且与脾脏强化程度一致(1C)。病理检查为ECIPAS(1D,HE ×100)
ECIPAS常被误诊为胰腺其他囊性或囊实性肿瘤性病变,误诊率高达95.2%[9]。当胰腺尾部出现囊实性肿块,实性部分CT密度或MR信号及动态增强扫描强化程度和强化方式与脾脏相似时,需考虑ECIPAS可能。Kwak等[10]认为DWI有助于鉴别ECIPAS与其他胰腺囊性或囊实性肿瘤。Motosugi等[11]认为超顺磁性氧化铁增强MRI扫描有助于ECIPAS诊断。
本组8例ECIPAS患者术前5例诊断为囊腺瘤、1例诊断为胰腺囊腺癌、1例诊断为胰腺囊性肿瘤、1例诊断为实性假乳头状瘤。胰腺囊腺瘤分浆液性囊腺瘤和黏液性囊腺瘤,浆液性囊腺瘤以胰头多见,由蜂窝状多个水样密度或信号的小囊构成,典型特征为中央纤维瘢痕和日光放射状钙化;黏液性囊腺瘤或囊腺癌以胰腺体尾部多见,为多发大囊或囊实性肿物,囊壁厚薄不均,囊内可有分隔和壁结节,增强扫描后实性成分较明显强化[12]。实性假乳头状瘤可发生于胰尾,多见于年轻女性,肿瘤常较大,有完整包膜,存在不同程度的出血、坏死、囊变、胆固醇结晶沉积等继发改变。实性成分较少的ECIPAS需与胰腺假性囊肿鉴别,胰腺假性囊肿常有胰腺炎病史,伴肾前筋膜增厚等改变。
ECIPAS临床极其罕见,部分放射科医师主观上对其认识不足,将胰腺囊实性肿块首先考虑囊腺瘤或囊腺癌。部分病例病灶实性部分较少,难以观察,给诊断带来困难。主脾切除后,病灶实性部分缺乏对照亦会给诊断带来难度。
总之,对ECIPAS有足够的认识并认真阅片是正确诊断的必要条件。当影像学上发现胰尾囊实性病变的实性成分信号、强化程度及强化方式与脾脏相似时需高度怀疑ECIPAS。ECIPAS患者若术前明确诊断且无其他并发症,建议每半年复查1次。本组资料的不足之处在于未进行内镜超声检查,当ECIPAS副脾组织较少、无法明确诊断时可以尝试行内镜超声下活组织检查以求明确诊断,以避免不必要的手术。
利益冲突所有作者均声明不存在利益冲突
