支架置入食管癌患者放疗时锥形束CT图像与定位CT图像不同融合配准方式摆位的误差
2019-12-17吴承骏孙凌飞温翠侠
吴承骏,孙凌飞,温翠侠
(徐州市中心医院,江苏徐州221000)
放射治疗在食管癌的综合治疗中占有重要的地位,图像引导放疗(IGRT)通过实时获取患者影像信息,可减少摆位误差,实现精确放疗。文献[1]报道,15%~31%的患者放疗时需要KV级锥形束CT(KV-CBCT)来校正摆位误差。
KV-CBCT是IGRT的重要设备,通过加速器机载的千伏级X射线源产生的锥形束射线扫描,采集的图像经重建后与定位CT图像进行融合配准,获得患者放疗时在三维方向上的误差[2]。不同的融合配准方式可能导致不同的摆位误差结果[3]。医师手动配准一般精确度较高,但花费时间较长;骨配准在保证精确度的情况下用时短,临床应用最为广泛;灰度配准适用于远离骨结构的肿瘤组织。在CBCT图像中,由于分辨率相对较低,肿瘤靶区不能良好的显示,如果常规按照肿瘤组织进行手动配准往往难度较大。食管癌患者由于进食梗阻症状往往选择支架置入,而支架多为金属材质,无论在定位CT还是CBCT上均有清晰的显示,由于支架直接反映了肿瘤的位置,这时利用基于金属支架的手动配准可能较常规手动配准更为精确。但具体哪种配准方式更好目前临床尚无定论,本研究比较了三种不同的CBCT图像及定位CT图像融合配准方式下食管癌患者的摆位误差,为临床选择合适的融合配准方式提供理论依据。
1.1 临床资料 2018年7月~2019年3月在徐州市中心医院放疗科行放疗的支架(镍钛金属合金支架)置入后食管癌患者18例,其中男14例、女4例,中位年龄63岁。肿瘤部位位于胸上段4例,胸中段9例,胸下段5例(分段参考2010年AJCC标准)。患者均因严重进食困难预先行支架置入扩张,后行肿瘤放疗,均完善相关检查,除外肝、骨等远处转移患者。
1.2 CBCT图像及定位CT图像数据收集、融合配准 患者入院后每周一次行CBCT,收集其CBCT图像,并导入计划系统内与定位CT图像融合配准。分别采用自动灰度匹配(直线加速器系统自带工具,将软组织作为参照自动匹配)、自动骨匹配(直线加速器系统自带工具,将骨性组织作为参照自动匹配)、基于支架上缘的手动匹配(将支架作为目标参照,手动对比摆位误差)进行融合配准,得到X(左右)、Y(前后)、Z(头脚)三个方向上的摆位误差,将得到的摆位误差输入治疗床进行误差校正,然后对患者进行放疗。
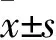
2 结果
自动灰度匹配融合配准方式下,X、Y、Z轴方向上食管癌患者放疗摆位误差分别为(0.40±0.09)、(0.39±0.26)、(0.44±0.12)cm,自动骨匹配融合配准方式下分别为(0.38±0.25)、(0.35±0.08)、(0.40±0.22)cm,支架手动匹配融合配准方式下分别为(0.37±0.19)、(0.33±0.20)、(0.35±0.18)cm。自动骨匹配与支架手动匹配方式相比较,P均>0.05;自动灰度匹配与支架手动匹配比较:在X轴及Z轴上比较,t分别为2.47、2.21,P<0.05;在Y轴上比较,P>0.05。
3 讨论
放射治疗是食管癌治疗的重要手段之一,各种误差的存在是影响精确放疗的因素,分次间的摆位误差主要来源于固定设备的不可靠性、激光灯、模拟机和治疗床的差别等,而分次内的误差则受患者蠕动、呼吸运动、咳嗽等因素的影响[4]。摆位误差是放疗分次间器官移位的主要原因,也是重要的不确定因素[5]。IGRT在常规放疗基础上引入了CBCT技术,通过对摆位误差的纠正提高了放疗的精确度。
Liliana等[6]比较了平面KV级CT与CBCT对食管癌患者放疗摆位误差的影响,认为所选择的模式会影响到所观察到的误差修正。尚凯等[7]研究发现,胸段食管癌IGRT时骨性及灰度匹配在X、Z轴上有差异,考虑纵隔内全为软组织,位置相对固定,建议采用灰度配准。吴建亭等[8]比较了不同配准方式对食管癌摆位误差的影响,发现自动灰度配准、自动灰度+手动配准、自动骨性配准、自动骨性+手动配准在X方向上的误差分别为(2.70±2.20)、(3.04±2.36)、(2.76±2.24)、(3.04±2.45)mm,在Y方向上的误差分别为(2.82±2.15)、(2.95±2.31)、(2.74±1.78)、(2.66±1.82)mm,在Z方向上的误差分别为(2.42±1.91)、(2.49±2.02)、(3.07±2.16)、(2.67±2.02)mm,建议对于食管癌的图像配准,加上手动配准是有必要的,自动骨性+手动配准的精确度最好。车少敏等[9]建议对颈段及胸上段食管癌以骨性配准为首选,必要时结合手动微调更好。本研究发现,自动灰度匹配与支架手动匹配相比较,在X轴及Z轴上有统计学差异,在Y轴上无统计学差异。由于人体非刚性结构,单纯自动匹配可能造成肿瘤部位的偏差,因此,我们认为在系统自动匹配之后加上手动调整是很有必要的。
Melanie等[10]通过预先对食管癌植入基准标记物,然后行放疗和CBCT扫描,探讨了不同配准方式对摆位误差的影响,认为通过外在标记物进行配准是完全可行的。de Blanck等[11]利用内镜将一种不透明标记物标记在食管肿瘤的边缘,发现其改善了放疗的精确定位,且没有显著不良反应。Liu等[12]针对胃食管交界处肿瘤植入放射不透明基准作为肿瘤替代物,而后进行呼吸门控放疗,发现植入的基准物与肿瘤体积的运动有很好的相关性,而门控降低了肿瘤在治疗过程中的移动,不过不同患者间的变异较大。Chandran等[13]对26例患者共植入92个标记物,发现标记物的放置改善了放疗的定位,有助于IGRT放疗,且没有明显不良事件的发生。在我们的研究中,由于患者严重进食困难而预先行支架置入,由于支架的金属特性本身就是一种很好的参照物,在IGRT摆位中是一种合适的配准参照。自动骨匹配与支架手动匹配相比较,左右前后及头脚三个方向上均没有统计学差异,提示两者具有等效性,而由于支架的位置直接反映了肿瘤的部位,较常规手动配准用来评估摆位误差更为准确。
总之,支架置入后放疗的食管癌患者CBCT图像与定位CT图像通过自动骨匹配与支架手动匹配进行融合配准的摆位误差相似,均优于自动灰度匹配。目前临床上多应用CBCT来纠正放疗前的摆位误差,而放疗分次内的误差同样不容忽视。黄大钡等[14]研究发现,放疗分次内的误差随着治疗时间的延长而增大,下一步我们将评估放疗前后分次内不同融合配准方式对患者放疗误差的影响。CBCT扫描的是一段时间内的容积图像,显示的是完整的呼吸心跳周期内的图像,而定位CT扫描的是瞬时图像,显示的是某一特定时间的图像,两者匹配时本身就会产生误差,进一步的研究可采用呼吸门控或4DCT来辅助解决这个问题。
