耳内镜下鼓膜大穿孔鼓室成形术及其临床疗效分析
2019-12-17张春林李春雷林季珍刘兆辉
张春林,邓 原,龙 丹,2,孙 强,2,李春雷,林季珍,刘兆辉
(遵义医科大学1.附属医院耳鼻咽喉头颈外科;2.研究生院,贵州遵义 563000)
鼓室成形术是耳显微外科的常规手术,鼓膜大穿孔的修补相对困难,对于手术方法的选择,一直是临床医生探讨的热点。显微镜下的鼓室成形术已取得了良好的临床效果,但是对于鼓膜大穿孔,由于显微镜柱状视野的特点,往往需要耳后或耳内切口才能保证手术顺利完成,创伤相对较大[1-2]。而耳内镜下的鼓室成形在临床上应用越来越广泛[3-4],但是由于耳内镜手术单手操作的特点,在处理鼓室复杂病变时,可能增加操作难度及手术风险。此外,鼓膜大穿孔鼓室成形术对修补材料要求较高,常用的修复鼓膜的材料包括颞肌筋膜、耳屏软骨或软骨膜、脱细胞真皮等,筋膜抗负压能力差,术后易塌陷及粘连[5],耳屏软骨由于较强的支撑作用及抗感染能力,具有一定的优势,但是厚度过大可能影响新生鼓膜的振动,从而影响术后听力水平[6-7]。既往观点认为,咽鼓管功能不良是鼓室成形术是预后不良的一个重要因素,对于此类患者需要谨慎进行鼓室成形术及同期听骨链重建[8-9]。我科采用耳屏软骨-软骨膜复合体在慢性化脓性中耳炎鼓膜大穿孔鼓室成形术中进行修复,并对咽鼓管功能不良的患者同期进行咽鼓管球囊扩张术(balloon eustachian tuboplasty,BET),取得良好的效果,现报道如下。
1 材料与方法
1.1 入组标准
符合纳入标准:①诊断符合《中耳炎临床分类和手术分型指南(2012)》[10];②耳镜评估为鼓膜大穿孔(鼓膜穿孔直径大于5 mm);③中耳炎症控制良好,鼓室无持续性流脓的患者。并排除:①镫骨固定,不能同期行听骨链重建的患者;②合并霉菌性外耳道炎,且术前未完全控制;③松弛部穿孔或者合并上鼓室胆脂瘤的患者;④术中探查发现咽鼓管明显堵塞或闭锁,需咽鼓管成形的患者;⑤合并乳突病变,需开放性鼓室成形的患者;⑥术后不能按时换药、随访的患者。本研究经遵义医科大学附属医院伦理委员会批准,并经患者知情同意。所有病例手术均由同一具有高级职称的术者完成。
1.2 临床资料
分析2017 年5 月至2019 年1 月间于我科手术的慢性化脓性中耳炎的患者,共110 例(115 耳)患者符合纳入标准,其中男60 例(63 耳),女50 例(52 耳);年龄6~69 岁,平均(34.1±14.8)岁,病程1 年至36 年,平均(21.4±7.6)年;右侧66 耳(占57.4%),左侧49耳(42.6%)。所有患者术前常规行颞骨薄层CT 平扫及听骨链重建、纯音听阈测定、声阻抗鼓室压力图及正-负压平衡试验、咽鼓管滴药实验。以纯音听阈语言频率(0.5、1.0、2.0 kHz)的平均值作为平均气导听阈(pure tone threshold average,PTA),所有患者术前PTA为(41.3±15.4)dB HL,气骨导差(air-bone gap,ABG)为(28.2±12.3)dB HL。以正-负压平衡试验显示咽鼓管通气功能不良且咽鼓管滴药实验时间超过10 min 评定为咽鼓管功能不良,并根据咽鼓管功能检查结果进行分组分析,评估为咽鼓管功能不良29 耳(25.2%),咽鼓管通畅且功能良好86 耳(74.8%),两组患者年龄、性别、术前PTA及ABG比较无统计学差异(均P>0.05,表1)。BET组鼓室成形术分型的构成为Ⅰ型22 耳,Ⅱ型5 耳,Ⅲ型2 耳,与未行BET的患者相比,构成比无统计学差异(P=0.649)。
1.2 手术方法
1.2.1 耳屏软骨-软骨膜复合体的制备 于同侧耳屏软骨外侧缘下方2 mm 处纵行切开耳屏软骨,保留外侧部分耳屏软骨以防耳屏变形,分离并去除软骨前面的软骨膜,剔除后方软骨膜周围软骨,制备成耳屏软骨-软骨膜复合体,并修剪成适当大小备用。如果锤骨柄完整,则剔除部分软骨并做一楔形缺口放置于锤骨柄上。如果锤骨柄缺如,则直接使用耳屏软骨-软骨膜复合体修补鼓膜(图1)。
表1 患者一般临床资料及听力水平Table 1 Clinical characteristics and hearing level in all patients [n(%),]

表1 患者一般临床资料及听力水平Table 1 Clinical characteristics and hearing level in all patients [n(%),]
ET:eustachian tube;PTA:pure tone threshold average;ABG:air-bone gap
1.2.2 鼓室成形术 耳内镜下制作移植床,若无残余鼓膜,则需搔刮鼓环或鼓室外侧壁骨质黏膜,制作外耳道皮肤鼓膜瓣,去除鼓室内的肉芽及钙化灶,清理听骨链周围病变,开放鼓室通气引流通道,内置法修补鼓膜,回复外耳道皮瓣覆盖于软骨-软骨膜复合体,明胶海绵鼓室填塞支撑,鼓膜表面及外耳道填塞明胶海绵及氧氟沙星眼膏,耳道口填塞碘仿纱条。根据《中耳炎临床分类和手术分型指南(2012)》[10],听骨链完整且活动好,行鼓室成形术Ⅰ型;若锤砧骨破坏或固定,而镫骨完整且活动好,则植入部分人工听骨(PORP)行鼓室成形术Ⅱ型重建;若镫骨上结构缺如,而镫骨足板活动好,则植入全部人工听骨(TORP)行鼓室成形术Ⅲ型重建。
我们将常规的距鼓环5 mm 处做耳道后壁弧形切口外移至距鼓环8~10 mm,且超过外耳道2/3周,制作蒂在下方的外耳道皮肤鼓膜瓣,回复皮瓣时可将其向鼓膜中心方面移动,使皮瓣更大面积的覆盖鼓膜移植物。此外,对于前方仅残余鼓环的鼓膜穿孔,则适度剥离前方纤维鼓环及与之相连的鼓室黏膜并向内侧分离,移植物放置于鼓环下方,可以达到移植物与外耳道皮肤鼓膜瓣之间更紧密的贴合(图1)。
1.2.3 咽鼓管球囊扩张术 对于评估为咽鼓管功能不良的患者,同期行咽鼓管球囊扩张术(balloon eustachian tuboplasty,BET)。常规选用经鼻BET,收缩鼻腔黏膜,鼻内镜直视下用咽鼓管球囊扩张器将咽鼓管扩张导管推送入咽鼓管内,打水囊至10 Bar,维持2 min,水泵减压,吸至负压,退出球囊及导丝,吸除咽鼓管周分泌物。
1.3 术后换药及随访
术后常规抗生素治疗,术后2~3 d 出院,2 周后门诊拔除外耳道内碘仿纱条,吸除外耳道残留的填塞材料及渗液,并检查鼓膜生长情况。术后1、2、3 月复查鼓膜生长情况,术后3 个月进行纯音听阈检查。
1.4 统计学分析
使用SPSS 17.0 统计软件进行数据处理,计量资料符合正态分布用均值±标准差表示,偏态分布则用中位数(四分位间距)表示。符合正态分布、方差齐性的数据采用t检验或单因素方差分析;非正态分布或方差不齐的数据采用Kruskal-WallisH检验,当差异存在统计学意义时,使用Bonferroni 检验进一步两两比较。计量资料的比较使用χ2检验或者χ2校正检验及Fisher′s 精确概率法检验。双侧检验,取α=0.05,P<0.05 为差异具有统计学意义。
2 结果
2.1 耳道皮瓣及鼓膜生长情况
术后2 周抽除外耳道口填塞碘仿纱条,耳内镜下清理耳道内未吸收的填塞材料及分泌物,外耳道皮瓣均于术后1 个月内完全愈合,无外耳道骨质裸露;3 例患者取出耳道填塞物后外耳道皮瓣贴合欠佳,复位后完全愈合;1 例患者外耳道皮瓣发生坏死,清理换药后愈合。动态观察鼓膜移植物生长情况,术后2 周时,移植软骨表面有纤维素性分泌物附着,新生血管开始生长,1 个月后新生鼓膜开始重塑,新生血管减少,术后3 个月时,鼓膜进一步塑形,鼓膜变薄。

图1 耳屏软骨-软骨膜复合体修补鼓膜大穿孔术中及术后形态Fig.1 Intraoperative and postoperative displayof myringoplasty with cartilage and perichondrium complex
115 耳均随访超过3 个月,一期鼓膜愈合率为95.7%。共5 耳鼓膜未能一期愈合,其中3 耳在术后1 个月时穿孔边缘与鼓膜移植物之间出现小裂隙(2 耳为前方,1 耳为下方),且均为鼓室成形术Ⅰ型的患者,予以换药时制作新鲜创面,明胶海绵覆盖,后愈合。1 耳术后合并感染,移植物坏死脱落而遗留穿孔(Ⅱ型);1 耳在术后2 月时合并霉菌感染,移植物坏死,鼓膜穿孔未愈合(Ⅰ型)。根据术前咽鼓管功能的评估,对是否同期行BET 进行亚组比较,结果显示同期BET 的亚组鼓膜一期愈合率96.6%,未行BET 的亚组鼓膜一期愈合率为95.3%,差异无统计学意义(P=0.801;表2)。此外,根据鼓室成形术分型进行亚组比较,结果显示各亚组的鼓膜愈合率分别为95.0%,96.3%,100%,差异无统计学意义(P=0.790;表2)。
2.2 术后听力情况
所有患者(115 耳)术后3 个月时PTA 和ABG分别为(25.7±11.8)dB HL 和(13.8±6.9)dB HL,术后PTA 降低了13(9~23)dB HL,ABG 缩小了12(7~22)dB HL,差异有统计学意义(Z=9.184,P<0.001;Z=9.158,P<0.001)。术后骨导听阈与术前相比,差异无统计学意义(Z=1.855,P=0.064)。
根据是否同期行BET 术进行分组分析,同期BET 组(29 耳)术后PTA 和ABG 与未行BET 的患者(86 耳)相比,差异无统计学意义(P=0.961,P=0.809;表2)。
根据鼓室成形术分型进行听力重建效果的亚组分析,三亚组患者术后PTA 较术前分别降低了(13.3±7.8)dB HL,(20.8±11.4)dB HL,(22.1±13.7)dB HL,差异均有统计学意义(P<0.001,P<0.001,P=0.018;表2);三亚组患者术后ABG较术前分别缩小(11.9±8.2)dB HL,(19.0±12.3)dB HL,(23.8±14.2)dB HL,差异均有统计学意义(P<0.001,P<0.001,P=0.002,表2)。亚组间术后PTA及ABG组间比较,差异均有统计学意义(均P<0.001;表2),鼓室成形术分型与术后患者听力重建效果相关。
表2 各亚组术前术后纯音听阈测定结果比较Table 2 The comparison of graft take rate and the hearinglevel between subgroups pre-andpost-surgery (,%)
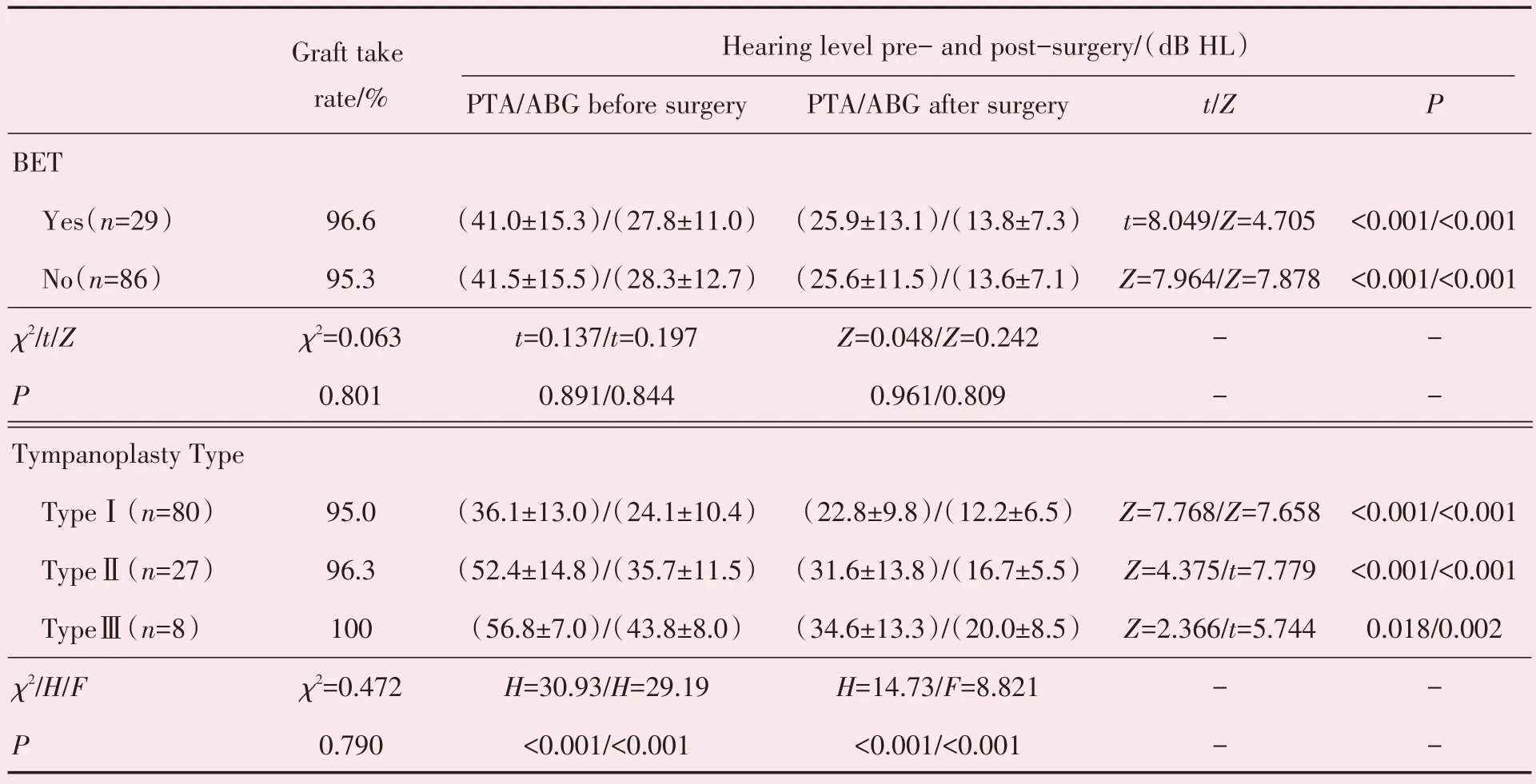
表2 各亚组术前术后纯音听阈测定结果比较Table 2 The comparison of graft take rate and the hearinglevel between subgroups pre-andpost-surgery (,%)
BET:balloon eustachian tuboplasty;PTA:Pure Tone threshold average;ABG:air-bone gap
3 讨论
近年来,耳内镜外科处于快速发展阶段[1-4],Tseng[2]和Lee[11]均通过荟萃分析耳内镜下鼓室成形术的临床疗效,发现其鼓膜愈合率与显微镜下无明显差别,但是耳内镜手术在切口并发症以及手术时间,住院时间方面具有明显的优势。而该优势在鼓膜大穿孔的患者尤为明显,本研究115 耳病例均于全耳内镜下完成手术,所有患者只需做耳道内切口,均不需耳道成形而完成手术,而相关研究报道发现显微镜下鼓室成形术耳道成形术比例高达30%[12]。此外,在探查听骨链及鼓室病变时,借助角度镜,可以避免凿除过多的鼓室盾板,不仅微创,减少了术后住院时间,也保证了术后鼓膜形态的相对稳定,提高了鼓膜一期愈合率。
耳屏软骨是近些年被推广应用的鼓膜修补材料,取材方便,具有良好的抗感染和抗负压能力[5-7],能有效对抗术后因鼓室填塞而造成的短暂咽鼓管通气不足及鼓室负压,减少再穿孔和鼓室粘连的发生可能。对于保留锤骨柄的鼓膜大穿孔,我们在耳屏软骨-软骨膜复合体上做一个楔形缺口,不仅减少了移植物的质量,且利于术后维持鼓膜的锥形形态,对于放置人工听骨的病例,由于无需另外放置软骨,从而避免了术后软骨片移位、听骨裸露,鼓膜再发穿孔的风险。本研究发现鼓膜的一期愈合率达到95.7%,与以往报道一致,高于颞肌筋膜的愈合率[5,13]。但是,较少的文献同期对比分析不同鼓室成形术分型之间鼓膜一期成活率,本研究发现,应用耳屏软骨-软骨膜复合体进行鼓膜修补,鼓膜一期成活率与是否同期行人工听骨植入并无关系,可以应用于不同的鼓室成形术中。
对于鼓膜大穿孔的修复,外耳道皮肤鼓膜瓣的制作及回复也是影响鼓膜愈合率的重要因素。本组病例中3 例术后新生鼓膜周围残留小裂隙穿孔,可能术后皮瓣和移植物瘢痕收缩有关。为此,我们增加切口至鼓环的距离,并且切口超过耳道2/3 周,术后适当将外耳道皮瓣向内侧移位从而增加与鼓膜移植物的接触面积,从而避免了术后残留穿孔,而术后2 w 换药时因皮瓣内移而裸露的外耳道骨质部分均已有新生上皮覆盖。此外,对于前方仅残余鼓环的穿孔,则适度剥离前方纤维鼓环及与之相连的鼓室黏膜并向内侧分离,从而减少了鼓膜移植物与纤维鼓环之间的张力,在保证复合体中软骨大小的前提下,通过增加软骨周围软骨膜与鼓室外侧壁的接触面积,达到外耳道皮肤鼓膜瓣之间更紧密的贴合,提高了鼓膜的一期愈合率。
术后听力水平是评判鼓室成形术效果的一个指标,有学者对耳屏软骨传音进行研究,当软骨厚度为0.5 mm 时,不仅能维持移植物的稳定,并且传导声音的功能较好[14],而国人的耳屏软骨厚度约为0.7~1.0 mm[7],使用全厚层耳屏软骨会对声音传到产生损耗,影响术后听力恢复。为此,本研究把耳屏软骨制备成耳屏软骨-软骨膜复合体,剔除部分软骨,即保留移植物的稳定性和支撑作用,又减少因全层软骨过厚而致影响术后听力提高。本研究术后连续性随访发现,术后3 个月时新生鼓膜的形态基本正常,随着时间的推移,耳屏软骨会进一步的变软及塑形,听力会进一步提高。此外,本研究发现鼓室成形Ⅰ型的患者术后听力最佳,这也提示我们,在保证听骨链活动的前提下,需尽量保留听骨链,不仅有利于维持新生鼓膜的稳定性,保留听骨链的杠杆效应也利于听力提高,而由于耳内镜的优势,借助角度镜可以无死角探查鼓室及清理听骨链周围病变,开放鼓室通气引流系统,所以提高了听骨链的保留率以及术后听力提高。
既往认为,咽鼓管功能良好是鼓室成形术的一个前提条件[15],陈阳[8]等回顾性分析121 例鼓室成形术的患者,发现术前咽鼓管功能不良者术后听力改善率低于咽鼓管功能良好者,但术后鼓膜穿孔率明显低于功能良好者,Choi 等[9]报道咽鼓管功能良好的患者鼓室成形术后ABG 小于咽鼓管功能不良的患者。由于耳屏软骨的抗负压能力,虽然术后短期内弥补咽鼓管功能不足的影响,但由于无法从根本上解决咽鼓管功能障碍,随着时间的推移,重建的软骨会被周围组织吸收,甚至溶解,逐渐变薄、内陷。本研究发现,对于术前评估咽鼓管功能不良的患者,同期咽鼓管球囊扩张,改善咽鼓管功能,术后鼓膜一期愈合率以及听力重建效果良好,与咽鼓管功能良好的患者并无明显差别。所以,同期行咽鼓管球囊扩张术,是合并咽鼓管功能不良患者的可行治疗方式。
综上所述,耳内镜下鼓室成形术操作微创,耳屏软骨-软骨膜复合体是鼓膜大穿孔时鼓室成形术后可靠的修复材料,术后疗效可靠,具有一定的优势,值得临床上推广应用。
