血清TLR4在COPD患者中的表达及其与肺功能、mMRC分级及CAT评分的相关性研究
2019-12-11何士杰景卫革韦海燕
孙 印 何士杰 景卫革 韦海燕
河北省承德市中心医院呼吸内科 067000
慢性阻塞性肺疾病(COPD)患者存在持续呼吸道症状及气流受限[1],多数患者病情随病程延长而逐渐加重,给患者家庭和社会造成极大的负担,导致患者生命质量下降,预期寿命缩短。目前,医生多根据肺功能、临床症状、急性加重风险综合评估患者病情。肺功能是诊断COPD的必备条件,并且能够评估COPD患者气流受限的严重程度。目前用于评估COPD患者症状的问卷有:改良英国医学研究委员会呼吸困难问卷(mMRC分级)、COPD评估测试问卷(CAT评分)、圣乔治呼吸问卷(SGRQ)、慢性呼吸问卷(CRQ)等,其中mMRC问卷及CAT评分临床应用最多。
COPD是一种慢性气道炎症性疾病,炎症反应还可以介导免疫应答。因此,通过测定COPD患者血清中部分炎症因子水平及免疫指标,可以在一定程度上反映患者体内炎症免疫功能状态及病情严重程度。TLR4是一种天然免疫模式识别受体,是联系天然免疫和获得性免疫的桥梁[2]。TLR4在对抗革兰氏阴性杆菌所引起的炎症反应中发挥关键作用[3],还能够启动固有免疫应答。目前国内外有研究显示TLR4参与了COPD的发病过程,但迄今为止,尚未见到在COPD患者血清中TLR4与肺功能指标、mMRC评分、CAT评分相关性的研究,本研究进行相关探讨。
1 资料与方法
1.1 临床资料 选取2016年12月—2017年12月于我院呼吸科门诊就诊的吸烟COPD稳定期患者60例为COPD稳定期组(简称COPD组),均符合中华医学会COPD的诊断标准[4],且患者近3个月气短、咳嗽、咳痰等呼吸系统症状稳定或症状轻微,无急性加重;且患者有吸烟史,每天吸烟5~20支;近3个月无应用抗生素、口服或静脉糖皮质激素病史。健康吸烟组及健康非吸烟组入选标准:同期于我院体检中心行健康体检者,肺功能检查无持续气流受限,其中吸烟者45例,每天吸烟5~20支,为健康吸烟组,非吸烟者45例为健康非吸烟组。三组受试对象均无呼吸系统其他疾病,无肺功能检查禁忌证。
1.2 观察指标及监测方法 基线资料:包括年龄、性别、吸烟指数、体重指数(BMI)及肺功能(德国耶格品牌);COPD患者测定mMRC分级及CAT评分。通过ELISA法检测三组受试对象血清中TLR4的表达水平。
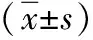
2 结果
2.1 各组一般资料 三组受试者在年龄、性别构成、BMI方面的差异均无统计学意义(P均>0.05)。COPD组与健康吸烟组吸烟支数差异无统计学意义(P>0.05)。三组受试对象具有可比性。见表1。
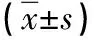
表1 三组一般资料比较
2.2 各组血清TLR4的表达水平 COPD组血清TLR4水平高于健康吸烟组及健康非吸烟组,健康非吸烟组高于健康吸烟组,差异均具有统计学意义(P<0.05)。见表2。

表2 各组血清TLR4的表达水平
注:a与健康吸烟组相比,P<0.05;b与健康非吸烟组相比,P<0.05;c与健康非吸烟组相比,P<0.05。
2.3 各组血清TLR4水平与FEV1pred%的相关性 COPD组患者血清TLR4水平与FEV1%pred呈负相关(r=-0.623,P<0.05),健康吸烟组及健康非吸烟组血清TLR4水平与FEV1%pred均无相关性(P均>0.05)。见表3。

表3 各组血清TLR4水平与FEV1pred%的相关性
2.4 血清TLR4水平与FEV1/FVC、mMRC分级、CAT评分、年龄、BMI及吸烟指数的相关性 COPD组患者血清TLR4水平与mMRC分级呈正相关(r=0.326,P<0.05),与CAT评分呈正相关(r=0.589,P<0.05),与年龄、体重指数及吸烟支数等均无明显相关性(P>0.05)。见表4。

表4 COPD组血清TLR4水平与FEV1/FVC、mMRC分级、CAT评分、年龄、BMI及吸烟支数的相关性
3 讨论
COPD是一种多因素疾病,是长期有毒颗粒及气体的暴露、基因、气道高反应性、幼年呼吸道感染、肺发育不良等多因素互相作用的结果[5]。COPD的发病率居高不下,死亡率不断增加,给各国带来巨大的经济负担和社会负担。早期正确诊断、准确评估患者病情、规范合理的治疗能够改善COPD患者的预后。肺功能FEV1% pred是评价COPD患者气流受限严重程度的经典指标,并且与患者急性加重风险及预后具有显著的相关性。另外,mMRC分级问卷、CAT评分问卷等也在COPD的病情评估中起到非常重要作用。COPD的确切发病机制尚不明确,炎症机制、氧化应激、蛋白酶—抗蛋白酶失衡是学者公认的发病机制。近几年来,炎症免疫因素成为COPD患者发病机制的研究热点[6],炎症可以诱发免疫失衡,免疫失衡导致炎症持续存在并加重,两者相互作用,最终导致COPD的发生及发展。
TLR4是最早被发现参与哺乳动物固有免疫的Toll样受体(TLRs)。TLR4主要由胞外区、跨膜区和胞内区组成[7],其胞外区能够识别病原体相关分子模式和损伤分子相关模式;胞内区与人白介素1受体(IL-1R)的胞内区具有高度同源性,故称为TLR/IL-1R受体同源区(TIR)结构域。TIR区域可以识别髓样分化蛋白88(MyD88)、肿瘤坏死因子受体活化因子6(TRAF)等信号传导分子,并向下游传导信号。TLR4几乎表达于所有的细胞系,中性粒细胞、单核细胞、巨噬细胞、未成熟树突状细胞等均有表达[8]。TLR4也分布于气道上皮细胞、气道平滑肌细胞、肺巨噬细胞及血管内皮细胞。TLR4识别的受体分为外源性配体和内源性配体,外源性配体主要是革兰阴性杆菌(G-杆菌)细胞壁成分脂多糖(LPS);内源性配体主要来源于宿主细胞(如细胞外基质及机体细胞主动分泌的介质等)。TLR4信号传导通路分为细胞外信号传导和细胞内信号传导两部分[9]。细胞外信号传导过程:TLR4在LPS存在条件下与髓样分化蛋白2(MD2)结合,形成TLR4- MD2二聚体,TLR4-MD2二聚体与LPS结合后TLR4构象发生变化,而后与胞内区TIR结构域结合进行细胞内信号传导。细胞内信号传导过程:细胞内信号传导通路主要有MyD88依赖型途径和MyD88非依赖型途径[10],通过一系列复杂的信号传导过程,MyD88依赖型途径激活核转录因子(NF-κB)和激活蛋白-1(AP1),MyD88非依赖型途径激活干扰素β相关因子3(IRF3)、晚发NF-κB及AP1,启动转录调控、炎症反应及免疫调节作用。TLR4是外源性病源分子脂多糖(LPS)最重要的识别感受器,其代表了抗感染的第一道防线。TLR4还能识别受损组织和坏死细胞释放的内源性病源分子,进而相互作用诱导强烈的促炎反应,修复机体的同时亦可能损害组织。通常来说,TLR4介导的炎症免疫反应通过复杂而协调的过程,最终使组织、细胞的完整性和功能得以恢复。但是,过度和调控不良的炎症免疫反应亦会对机体造成损伤而致病。本实验结果显示,COPD稳定期患者血清TLR4水平显著高于健康人群,而且健康非吸烟者高于健康吸烟者,差异均有统计学意义。曾晓丽等[11]研究发现,COPD患者血单核巨噬细胞表面TLR4、MyD88的mRNA及蛋白表达水平均显著高于健康对照组,而且单核巨噬细胞培养上清液中炎症因子TNF-α和IL-6含量亦显著高于健康对照组。国外研究[12-13]显示,COPD患者气道及外周血中性粒细胞表面TLR4水平明显高于健康对照组。本实验与上述研究结论一致,表明TLR4参与了COPD的免疫炎症发病机制。现有研究表明,G-杆菌是COPD最重要的病原体之一,当患者呼吸道或全身抵抗能力下降时,G-杆菌感染机会明显增加。COPD患者反复发生G-杆菌感染,LPS可诱导机体TLR4表达上调,通过MyD88依赖型途径激活NF-κB炎症通路,使炎症因子TNF-α、IL-1、IL-6、IFN-γ分泌明显增加,进而趋化中性粒细胞及巨噬细胞到达炎症部位,上述细胞活化后杀灭病原体的同时释放中性粒细胞弹性蛋白酶及金属基质蛋白酶,且氧自由基产生增加,损伤气道及肺组织,致使气道重塑、肺泡破裂融合,最终导致COPD的发生和发展。另外,本研究还显示健康非吸烟者血清TLR4水平显著高于健康吸烟者,这说明吸烟抑制血清TLR4的表达,吸烟者固有免疫功能降低,对G-杆菌等病原体的清除能力下降。
呼吸困难是COPD的标志性症状,用mMRC问卷能很好地评估患者的临床症状[14]。mMRC分级与反映COPD患者健康状况的其他指标有良好的相关性[15],并能预测患者远期死亡风险[16]。COPD评估测试(CAT评分)能够反映COPD对患者生活质量的影响程度[14]。肺功能指标FEV1%pred是诊断气流受限严重程度的良好指标,也是预测患者全因死亡率的一个独立指标。在整体人群水平,FEV1%pred是预测患者住院率、死亡率、指导非药物治疗(如肺减容或肺移植手术)的重要因素。本实验显示,COPD患者血清TLR4与mMRC分级、CAT评分呈正相关,与肺功能指标FEV1%pred呈负相关,这说明血清TLR4与COPD患者呼吸困难严重程度、生活质量及气流受限严重程度具有相关性,同时也表明血清TLR4可能与COPD患者病情的严重程度具有相关性。
综上所述,本研究表明血清中TLR4参与了COPD的炎症免疫发病机制,但是具体的炎症免疫通路仍不明确,需要在今后的研究中进一步探索。随着医疗水平的提高和对COPD研究的进一步深入,COPD的发病机制会更加明确,诊疗方面也会有更大的突破。
