糖尿病合并持续植物状态胰岛素注射患者低血糖的发生情况
2019-11-19李国英程千鹏张蕙李慧莉
李国英 程千鹏 张蕙 李慧莉

[摘要] 目的 探討糖尿病合并持续植物状态胰岛素注射患者低血糖的发生及原因。 方法 选取2017年2月~2018年3月于解放军总医院第七医学中心干部病房三科住院的糖尿病合并持续植物状态胰岛素皮内注射控制血糖的患者40例,行血糖监测。依据是否发生低血糖将患者分为低血糖组18例和无低血糖组22例。进一步根据发生低血糖次数将低血糖患者分为多发组8例和少发组10例。统计低血糖发生率及原因。比较各组性别、年龄、糖尿病病程、收缩压、舒张压、糖化血红蛋白、三酰甘油、低密度脂蛋白胆固醇水平。 结果 低血糖发生18例(占45.00%),低血糖发生次数83次,餐后低血糖发生次数49次(占59.04%),夜间低血糖发生次数34次(占40.96%)。餐后低血糖主要原因是鼻饲反流。夜间低血糖主要原因是睡前血糖偏低及胰岛素剂型。少发组的糖尿病病程短于多发组,糖化血红蛋白水平高于多发组,差异有统计学意义(P < 0.05)。 结论 病程越长、血糖控制越严格的糖尿病合并持续植物状态胰岛素注射患者更易发生低血糖,临床需关注鼻饲反流和胰岛素剂型。
[关键词] 糖尿病;持续植物状态;低血糖;胰岛素注射
[中图分类号] R587.1 [文献标识码] A [文章编号] 1673-7210(2019)09(c)-0069-04
Occurrence of hypoglycemia in insulin-injecting diabetic patients with persistent vegetative state
LI Guoying1 CHENG Qianpeng2 ZHANG Hui1 LI Huili1
1.The Third Department of Cadre Ward, the Seventh Medical Center, PLA General Hospital, Beijing 100700, China; 2.Department of Endocrinology, the Seventh Medical Center, PLA General Hospital, Beijing 100700, China
[Abstract] Objective To investigate occurrence and causes of hypoglycemia in insulin-injecting diabetic patients with persistent vegetative state. Methods A total of 40 patients with diabetes mellitus complicated with persistent vegetative state insulin intradermal injection to control blood sugar were selected from February 2017 to March 2018 in Three Departments of Cadre Ward, the Seventh Medical Center in PLA General Hospital. Blood sugar was monitored. According to occurrence of hypoglycemia, the patients were divided into hypoglycemia group (18 cases) and non-hypoglycemia group (22 cases). According to the frequency of hypoglycemia, hypoglycemia patients were divided into multiple-occurrence group (8 cases) and low-occurrence group (10 cases). The incidence and causes of hypoglycemia were counted. Gender, age, course of diabetes, systolic blood pressure, diastolic blood pressure, glycosylated hemoglobin, triglyceride and low density lipoprotein cholesterol were compared among groups. Results There were 18 cases of hypoglycemia (45.00%), 83 times of hypoglycemia, 49 times of postprandial hypoglycemia (59.04%) and 34 times of night hypoglycemia (40.96%). The main cause of postprandial hypoglycemia was nasal feeding reflux. The main causes of night hypoglycemia were hypoglycemia before bed and insulin dosage forms. The course of diabetes mellitus in low-occurrence group was shorter than that in multiple-occurrence group, and the level of glycosylated hemoglobin was higher than that in multiple-occurrence group (P < 0.05). Conclusion Insulin-injecting diabetic patients with persistent vegetative state are more likely to suffer from hypoglycemia with longer course of disease and stricter blood sugar control. Clinical attention should be paid to nasal feeding reflux and insulin dosage form.
[Key words] Diabetes mellitus; Persistent vegetative state; Hypoglycemia; Insulin injection
糖尿病合并持续植物状态,尤其是糖尿病严重脑血管并发症后导致的持续植物状态,预期寿命较短,血糖一般不需要严格控制[1]。临床观察中虽然血糖未严格控制仍有低血糖发生,尤其是皮内注射胰岛素控制血糖患者。低血糖尤其是严重低血糖的发生可导致患者死亡,应予以重视。本研究主要分析长期住院的糖尿病合并持续植物状态胰岛素注射患者的低血糖发生情况。
1 对象与方法
1.1 研究对象
选取2017年2月~2018年3月于解放军总医院第七医学中心干部病房三科住院的糖尿病合并持续植物状态且需胰岛素皮内注射控制血糖患者为研究对象。糖尿病诊断及分型依据目前国际通用的WHO(1999)标准[1],持续植物状态诊断标准[2]符合我国急诊医学会(1996)标准。共纳入患者40例,男22例,女18例,年龄75~90岁,平均(79.43±2.79)岁,病程9~32年,平均(18.00±5.90)年。将患者是否发生低血糖分为低血糖组18例和无低血糖组22例。根据患者发生低血糖次数,取均值为4.6次,故5次及以上定义为多发组(8例),5次以下定义为少发组(10例)。纳入标准:患者均为严重脑血管病后导致持续植物状态。排除标准:严重肝、肾功能损害者;肿瘤患者;血液疾病者;胰腺炎病史者。本研究方案经原陆军总医院医学伦理委员会批准。研究对象均签署知情同意书。
1.2 研究方法
1.2.1 血糖监测 患者入院后由营养科给予营养匀浆膳食,晨7:00,中午11:00,晚17:00按时胃管注入。既往胰岛素注射方案不变,并已经保持3个月,并于入院3 d后开始应用罗氏血糖仪进行血糖监测。记录三餐前后,晚22:00,凌晨3:00指血糖,共记录10 d。以血糖< 3.9 mmol/L为低血糖。夜间低血糖指晚22:00至次日晨7:00时发生的低血糖。餐后低血糖指日间进餐后到下次进餐前出现的低血糖,或晚餐后到22:00发生的低血糖。
1.2.2 低血糖原因 研究者对每次低血糖进行分析。每次记录低血糖发生原因。原因包括进食后反流、胰岛素剂量大、胰岛素剂型、餐前或睡前血糖低。记录原因时若出现低血糖前有明显反流,原因记为反流。胰岛素剂量大即餐后2 h血糖较餐前血糖下降继而导致低血糖或餐后2 h低血糖,或晨起低血糖。胰岛素剂型导致低血糖为下餐前血糖较餐后2 h波动大,或预混胰岛素夜间血糖较睡前明显下降,或凌晨3:00低血糖但既往晨起较凌晨3:00明显上升者。根据《中国2型糖尿病诊治指南2017年版》[1],对于老年认知功能障碍患者餐前血糖控制在5.6~10.0 mmol/L,睡前血糖控制在6.1~11.1 mmol/L。取中间值,定义餐前血糖< 7.8 mmol/L为低血糖,定义睡前血糖< 8.6 mmol/L为低血糖。
1.2.3 低血糖救治 监测到患者低血糖时,给予10%葡糖糖注射液静脉滴注,15 min后复测指血糖,必要时给予50%葡萄糖注射液50 mL静脉注射。
1.2.4 观察指标 记录一般资料包括患者性别、年龄、糖尿病病程、血压。糖化血红蛋白采用DiaSTAT糖化血红蛋白分析仪(美国Bio-Rad公司)测定;三酰甘油、低密度脂蛋白胆固醇采用解放军总医院第七医学中心检验科全自动生化分析仪检测。
1.3 统计学方法
采用SPSS 16.0统计软件进行统计分析。计量资料用均数±标准差(x±s)表示,组间比较采用t检验,计数资料采用χ2检验,以P < 0.05为差异有统计学意义。
2 结果
2.1 患者低血糖发生情况
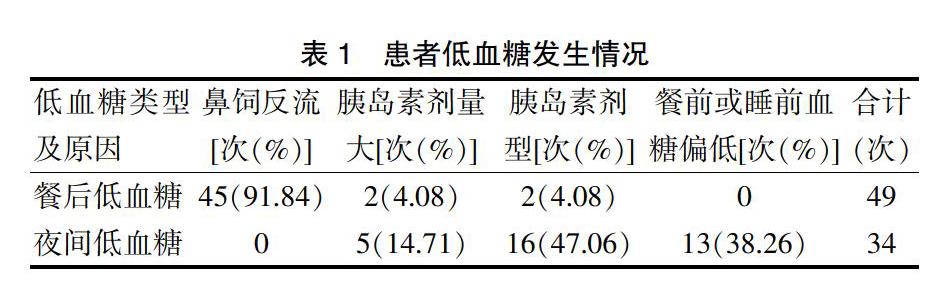
所有患者平均糖化血红蛋白为8.41%,低血糖发生18例,低血糖发生率为45.00%,低血糖发生次数83次,餐后低血糖发生次数49次,占比59.04%,夜间低血糖发生次数34次,占比40.96%。餐后低血糖的主要原因是进食反流,夜间低血糖的主要原因是睡前血糖偏低及胰岛素剂型。见表1。
2.2 低血糖危险因素分析
2.2.1 低血糖组与无低血糖组患者相关指标比较 低血糖组与无低血糖组的性别、年龄、糖尿病病程、收缩压、舒张压、糖化血红蛋白、三酰甘油、低密度脂蛋白胆固醇比较,差异无统计学意义(P > 0.05)。见表2。
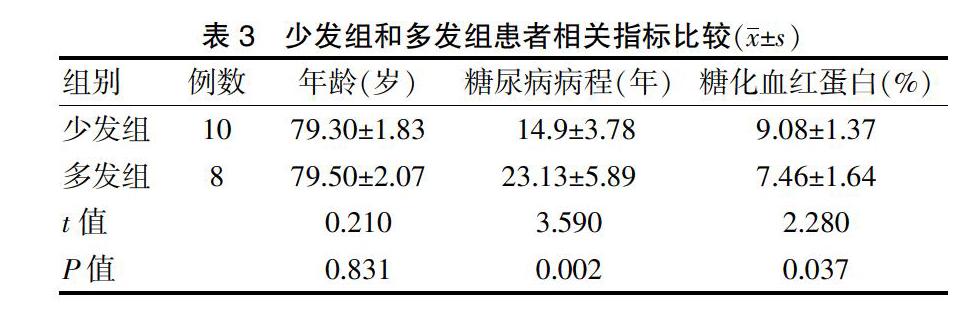
2.2.2 少发组和多发组患者相关指标比较 少发组和多发组的年龄比较,差异无统计学意义(P > 0.05)。少发组的糖尿病病程短于多发组,糖化血红蛋白水平高于多发组,差异有统计学意义(P < 0.05)。见表3。
3 讨论
糖尿病发病率持续升高,尤其应用胰岛素控制血糖,低血糖高发。低血糖是一组多种病因引起的以静脉血浆葡萄糖水平过低,导致临床上以交感神经兴奋和脑细胞缺氧为主要特点的的综合征。糖尿病患者定义血糖< 3.9 mmol/L为低血糖。低血糖通常表现为出汗、饥饿、心慌、面色苍白,严重低血糖患者可出现昏迷[3]。低血糖时目前依据患者能否自我进食缓解评价低血糖严重程度,低血糖分为[4]:①严重低血糖;血糖< 2.8 mmo1/L,或需要他人的帮助才能获取碳水化合物;②症状性低血糖,伴有典型的低血糖症状,并伴有血糖< 3.9 mmo1/L;③无症状低血糖,不伴有典型的低血糖症状,但血糖< 3.9 mmo1/L;④可疑症状性低血糖,出现典型低血糖症状,但不确定血糖< 3.9 mmo1/L。随着现代医学技术水平的不断提高,许多严重脑血管疾病患者虽经抢救挽救了生命,但其中不少患者却进入持续植物状态[5]。2001年“全国脑复苏、持续植物状态学术交流暨修订我国持续植物状态诊断和疗效标准的专家会议”会议确定了植物状态的诊断标准:①认知功能丧失,没有意识活动,不能执行指令;②能自动睁眼或刺激下睁眼;③有睡眠-觉醒周期;④可有无目的性眼球跟踪运动;⑤不能理解和表达语言;⑥保持自主呼吸和血压;⑦丘脑下部及脑干功能基本保存。植物状态持续1个月以上定义为持续植物状态。创伤性脑损伤引起的植物状态病程超过1年者、非创伤性脑损伤引起的植物状态病程超过3个月者均定为永久植物状态。他们的营养主要靠匀浆膳食鼻胃管长期定时注入维持身体能量需求。合并糖尿病患者,由于患者伴有严重并发症,预期寿命较短,不需严格血糖控制,但仍有低血糖发生,尤其注射胰岛素控制血糖患者。对于持续植物状态患者低血糖危害主要有两点:①低血糖引起交感神经兴奋,诱发血管痉挛和动脉粥样硬化斑块不稳定,從而导致急性心脑血管事件[6]。对2型糖尿病患者行动态血糖监测及动态心电图,发现低血糖时心电图有缺血性改变,但高血糖时没有发生这种改变[7]。在美国糖尿病心血管风险因素队列性研究中,强化组低血糖更常见,且低血糖发生次数与死亡风险相关[8]。②低血糖导致内脏自主神经功能受损,特别是频发低血糖,从而诱发致命性的心律失常[9-11]。低血糖导致心律失常原因主要是低血糖可影响心肌电活动。低血糖可引起心肌复极化延迟,QTQ间期延长,代偿性激活迷走神经,随后导致室性快速心律失常[12-13}。研究者对25例1型糖尿病患者分别进行24 h心电图和连续血糖监测,13次低血糖中8次有心率和心律紊乱,包括窦性心动过缓、心室异位、心房异位等[14]。
研究患者平均糖化血红蛋白8.41%,血糖控制基本达到指南要求,血糖控制可[1]。本研究显示,低血糖发生率为45.00%,与国内外老年糖尿病患者低血糖发生率相比偏高[15-17],究其原因,可能与本研究选用受试者糖尿病病程长,且均为胰岛素治疗有关,另外研究中有一个突出问题是餐后低血糖发生率高(餐后低血糖发生次数49次,占比59.04%),分析原因主要与鼻饲液反流有关,因为患者的症状无法主诉,胰岛素餐前注射,进餐时反流使进餐碳水化合物减少导致低血糖。夜间低血糖与既往报道发生率差别不大,发生低血糖原因主要是睡前血糖偏低及胰岛素剂型。从本研究可以看出,糖尿病合并持续植物状态胰岛素注射患者导致低血糖主要原因为胰岛素剂型及进餐状况。进一步根据患者发生低血糖的次数,分为少发组和多发组,少发组较多发组病程更短,糖化血红蛋白水平更高。提示病程越长、糖化血红蛋白控制越严格低血糖发生越多。既往研究提示[18],年龄也是低血糖发生危险因素,但本研究因入组患者均为高龄,年龄对低血糖的影响并未体现。英国低血糖研究和美国糖尿病控制与并发症研究均证实随着血糖更好的控制,也就是糖化血红蛋白越低,低血糖的发生率、严重低血糖的发生率均上升[19]。
血糖过于严格控制,增加低血糖的发生率。严重低血糖诱发的严重心律失常或急性心脑血管事件可导致患者死亡风险增加。在糖尿病治疗时需衡量血糖控制带来的益处及低血糖的危害,所以糖尿病的治疗应该是一个个体化的治疗,制订个体化目标、个体化方案。但某些时候,如胰岛素治疗、或促泌剂治疗,低血糖是无法避免的。因此,在这些患者的诊疗中,不仅仅关注糖化血红蛋白,更要关注有规律的大的血糖波动及有可能偶发的大的血糖波动所导致的低血糖,找到血糖波动及低血糖原因,预防严重低血糖出现。针对本研究低血糖发生原因,为预防低血糖发生,对每名患者进行个体干预[20]。主要干预措施:①先鼻胃管打匀浆膳食,根据进餐情况,餐后注射速效胰岛素类似物;②监测睡前血糖,若血糖偏低,调整晚间基础胰岛素用量;③基础胰岛素以长效胰岛素类似物为好。
综上所述,本研究发现了糖尿病合并持续植物状态胰岛素注射患者发生低血糖的特点,但未采用动态血糖监测技术作为补充,可能会漏掉部分低血糖情况;另外对于持续植物状态患者睡前安全血糖仍需进一步研究。
[参考文献]
[1] 中华医学会糖尿病学分会.中国2型糖尿病防治指南(2017年版)[J].中国糖尿病杂志,2018,10(1):4-67.
[2] 《中华医学会急诊医学学会意识障碍研究专业组》.持续性植物状态的命名、定义及诊断标准[J].现代临床医学生物工程杂志,1996,2(3):232.
[3] Feinkohl I,Aung PP,Keller M,et al. Severe hypoglycemia and cognitive decline in older people with type 2 diabetes:the Edinburgh type 2 diabetes study [J]. Diabetes Care,2014,37(2):507-515.
[4] Association AD. Foundations of care and comprehensive medical evaluation [J]. Diabetes Care,2016,39(Suppl 1):s23-s35.
[5] 趙茜,蒋利丹.医院到家庭连续护理干预对持续植物状态出院患者的效果[J].护理学杂志,2015,30(2):7-10.
[6] 张俊清.糖尿病患者低血糖的危害及预防[J].药品评价,2010,28(7):18-20.
[7] Desouza C,Salazar H,Cheong B,et al. Association of hypoglycemia and cardiac ischemia A study based on continuous monitoring [J]. Diabetes Care,2018,26(5):1485-1489.
[8] Seaquist ER,Miller ME,Bonds DE,et al. The impact of frequent and unrecognized hypoglycemia on mortality in the ACCORD study [J]. Diabetes Care,2017,35(2):409-414.
[9] 钱荣立.高度警惕老年糖尿病患者夜间无症状低血糖引发致命性心律失常的危险[J].中国糖尿病杂志,2016,24(3):198-199.
[10] Cha SA,Yun JS,Lim TS,et al. Severe hypoglycemia and ardiovascular or all-cause mortality in patients with type 2 diabetes [J]. Diabetes Metab J,2016,40(3):202-210.
[11] Pi?諭tkiewicz P,Buraczewska-Leszczyńska B,Kuczerowski R,et al. severe hypoglycemia in elderly Patients with type 2 diabetes and coexistence of cardiovascular history [J]. Kardiol Pol,2016,74(8):779-785.
[12] Tsujimoto T,Yamamoto-Honda R,Kajio H,et al. Vital signs,QT prolongation,and newly diagnosed cardiovascular disease during severe hypoglycemia in type 1 and type 2 diabetic patients [J]. Diabetes Care,2013,37(1):217-225.
[13] Reno CM,Daphna-Iken D,Chen YS,et al. Severe hypoglycemia-induced lethal cardiac arrhythmias are mediated by sympathoadrenal activation [J]. Diabetes,2013,62(10):3570-3581.
[14] Gill GV,Woodward A,Casson IF,et al. Cardiac arrhythmia and nocturnal hypoglycaemia in type 1 diabetes—the "dead in bed" syndrome revisited [J]. Diabetologia,2016, 52(1):42-45.
[15] 曹月琴,魯亚玲.老年2型糖尿病并发低血糖的原因分析及预防[J].中国热带医学,2009,9(7):1250-1251.
[16] 廖淑金,黄萍,傅明捷,等.老年2型糖尿病患者低血糖特征的临床研究[J].中国糖尿病杂志,2016,24(3):205-209.
[17] Fukuda M,Doi K,Sugawara M,et al. Survey of hypoglycemia in elderly people with type 2 diabetes mellitus in Japan [J]. J Clin Med Res,2015,7(12):967-978.
[18] Schutt M,Fach EM,Seufert J,et al. Multiple complications and frequent severe hypoglycaemia in "elderly" and "old" patients with type 1 diabetes [J]. Diabet Med,2018, 29(8):e176-e179.
[19] Brian M,Simon R. Hypoglycaemia in clinical diabetes [M]. Third Edition. John Wiley & Sons Ltd.,2014:265-283.
[20] Yong YM,Shin KM,Lee KM,et al. Intensive individualized reinforcement education is important for the prevention of hypoglycemia in patients with type 2 diabetes [J]. Diabetes Metab J,2015,39(2):154-163.
(收稿日期:2019-07-31 本文编辑:李亚聪)
