399例蛇毒类血凝酶相关药品不良反应报告分析及风险信号挖掘
2019-11-09郭代红杨鸿溢刘思源栗啸阳解放军总医院临床药学中心北京100853
齐 榛,郭代红,姚 翀,杨鸿溢,庞 宁,刘思源,栗啸阳(解放军总医院临床药学中心,北京 100853)
出血是临床上常见症状之一,蛇毒类血凝酶是一种动物来源的蛋白酶类止血药[1],目前已在国内止血药物市场中占主导地位[2]。其相关的药品不良反应(adverse drug reaction,ADR)案例多有发生,用药安全性问题受到多方关注,而相关文献报道多为个药、个案分析,且病例数较少[3-5]。因此,笔者提取解放军ADR数据库中十年间所有涉及蛇毒类血凝酶的ADR报告相关信息进行统计分析,并基于数据挖掘技术进行风险信号挖掘与评价,深入了解该类药物相关ADR发生的情况及特点,旨为临床安全合理用药提供参考依据。
1 资料与方法
1.1 资料来源
收集2009年1月- 2018年12月解放军ADR监测中心数据库中注射用尖吻蝮蛇血凝酶、注射用矛头蝮蛇血凝酶、注射用白眉蛇毒血凝酶和蛇毒血凝酶注射液(商品名称分别为:苏灵、巴曲亭/立芷雪、邦亭、速乐涓;生产厂家分别为:北京康辰药业股份有限公司、蓬莱诺康药业有限公司/瑞士素高药厂、锦州奥鸿药业有限责任公司、兆科药业有限公司)相关ADR报告,纳入标准为:第一怀疑药品为蛇毒类血凝酶,关联性评价结果为“可能”、“很可能”、“肯定”。
1.2 方法
采用回顾性研究方法,根据《WHO药品不良反应术语集》(2015版)[6]对ADR报告进行规整,对同一报告累及多个系统/器官、涉及多个临床表现的分别计算频次(ADR表现例次>ADR报告例数)。应用Excel 2016对报告中涉及药品、患者年龄及性别、ADR临床表现、累及系统/器官、发生时间、给药途径及转归情况等进行统计汇总,采用SPSS19.0软件进行统计分析,P < 0.05为差异具有统计学意义。
1.3 数据信号挖掘
重点关注蛇毒类血凝酶相关严重ADR,参考国家ADR监测中心《药品不良反应术语使用指南》(征求意见稿)[6]中相关过敏样反应的主要判断依据对数据规整后,利用比例报告比法(proportional reporting ratio,PRR)、报告比值比法(reporting odd ratio,ROR)、英国药品和保健产品管理局的综合标准法(MHRA)和贝叶斯可信区间递进神经网络法(Bayesian confidence propagation neural network,BCPNN),对蛇毒类血凝酶相关过敏性休克、过敏样反应、血浆纤维蛋白原减少进行风险信号挖掘,以IC-2SD > 0、ROR-1.96SE > 1、PRR-1.96SE > 1及(PRR ≥2,A ≥ 3,χ2≥ 4)为生成阳性信号的判定标准[7]。
2 结果
2.1 病例概况
最终纳入ADR报告399例。其中,年龄最小为新生儿1 d,最大111岁,平均年龄(46.91±17.56)岁。男性231例(57.89%),女性168例(42.11%),男女比例1.38 : 1,详见表1。78例严重报告中,患者年龄最小2个月,最大87岁,平均年龄(53.04±15.51)岁。男性57例,女性21例,男性严重的ADR发生比例(24.68%)显著高于女性(12.50%),差异有统计学意义(P = 0.002)。
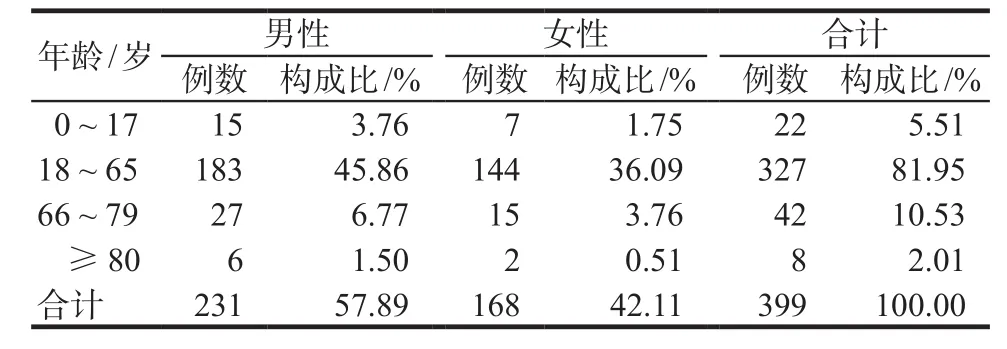
表1 患者性别、年龄段分布情况Tab 1 Gender and age distribution of patients
2.2 ADR涉及药品情况及其主要临床表现
399例报告涉及四种药品的构成情况详见表2。注射用尖吻蝮蛇血凝酶占比最多为232例(58.14%);严重报告78例(19.55%),注射用尖吻蝮蛇血凝酶为62例(79.49%)。ADR累及多个系统/器官,共计597例次,主要为全身性损害187例次(31.32%)和皮肤及附件损害136例次(22.78%)。严重报告主要为全身性损害59例次(60.83%)和血液系统损害15例次(15.46%),详见表3 ~ 4。
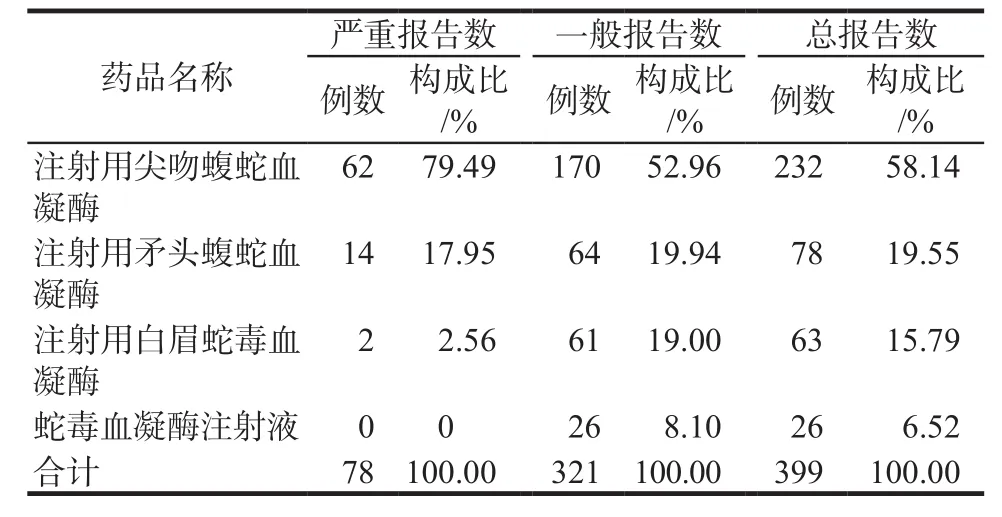
表2 ADR涉及药品情况Tab 2 Distribution of drugs involved in ADR

表3 ADR严重程度及主要临床表现Tab 3 Severity and major clinical manifestations in ADR
2.3 ADR发生时间与给药途径
399例报告中除6例ADR发生时间不详外,发生时间最短为用药后即刻发生过敏性休克。最长为用药后第12天,在患者静注注射用白眉蛇毒血凝酶后,出现凝血酶原时间延长、凝血时间延长、血浆纤维蛋白原减少的临床症状。57例(14.28%)ADR发生时间在用药1 min内/即刻,其中严重报告21例(26.92%);93例(23.31%)发生在用药2 ~ 5 min,且严重ADR最多,为28例(35.90%)。用药后60 min内发生的319例(79.95%),其中严重报告66例(84.61%),临床表现主要为过敏性休克、过敏样反应、胸闷、高热、血压下降等。用药后6 h以上发生的严重ADR多为血液系统损害,其临床主要表现为血浆纤维蛋白原减少、脑梗死、脑出血等,详见表5。
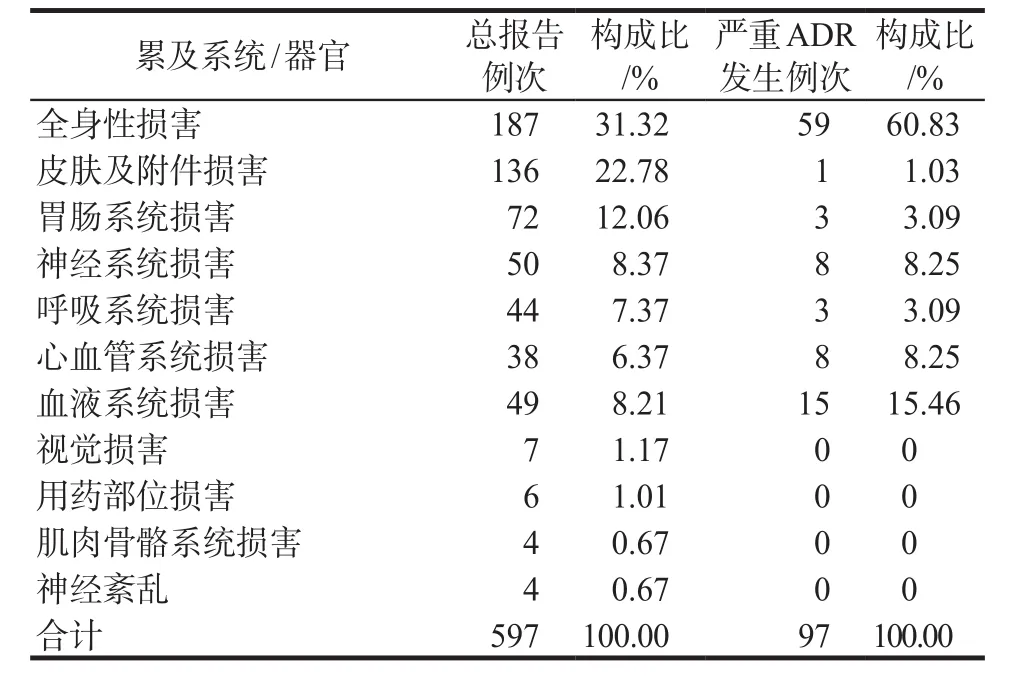
表4 ADR累及系统/器官及构成比分布情况Tab 4 Distribution of system/organ and proportion involved in ADR
2.4 ADR报告转归情况
399例ADR转归情况:除2例(0.50%)患者不详外,245例(61.40%)痊愈、149例(37.35%)好转、2例(0.50%)持续,1例(0.25%)死亡病例,为使用注射用白眉蛇毒血凝酶后出现颅内静脉窦血栓形成、急性脑梗塞并脑出血、蛛网膜下腔出血、脑水肿等症状,经抢救无效后死亡。
2.5 风险信号挖掘
鉴于上述严重报告中排名前三位的临床表现为过敏性休克(34例,43.59%)、过敏样反应(18例,23.07%)、血浆纤维蛋白原减少(8例,10.26%),因此参考国家ADR监测中心《药品不良反应术语使用指南》(征求意见稿)[6]中相关过敏样反应的主要判断依据对数据进行规整后,得到蛇毒类血凝酶ADR的分布特征,详见表6。继之对上述3项ADR进行风险信号挖掘,所得结果详见表7 ~ 9。ROR法、PRR法、MHPA法、BCPNN法均检测出注射用尖吻蝮蛇血凝酶相关过敏性休克、注射用白眉蛇毒血凝酶相关血浆纤维蛋白原减少的异常风险信号,MHPA法检测出注射用尖吻蝮蛇血凝酶相关血浆纤维蛋白原减少的异常风险信号。
3 讨论
3.1 发生ADR的患者年龄与性别因素
本研究显示患者发生ADR年龄跨度较大,可能与该类药物适应证广泛有关。报告主要集中于18 ~65岁(81.95%)。男女比例为1.38 : 1,严重报告中,男女比例为2.71 : 1,与国内相关研究结果一致[8-10],这可能与该类药物主要用于减少出血或止血的各种医疗情况,且部队医院收治患者男性多于女性有关。值得注意的是,研究中有11例报告的患者年龄在10岁以下,4种药物均有分布,而其说明书中关于儿童用药方面均无可靠参考文献。儿童的肝肾功能尚不完全,药物代谢率低,耐受性差,个体差异大[11],虽然有血凝酶用于治疗新生儿肺出血的相关报道[12],但临床使用时仍须慎重,应取得家长的知情同意,并注意风险监测。
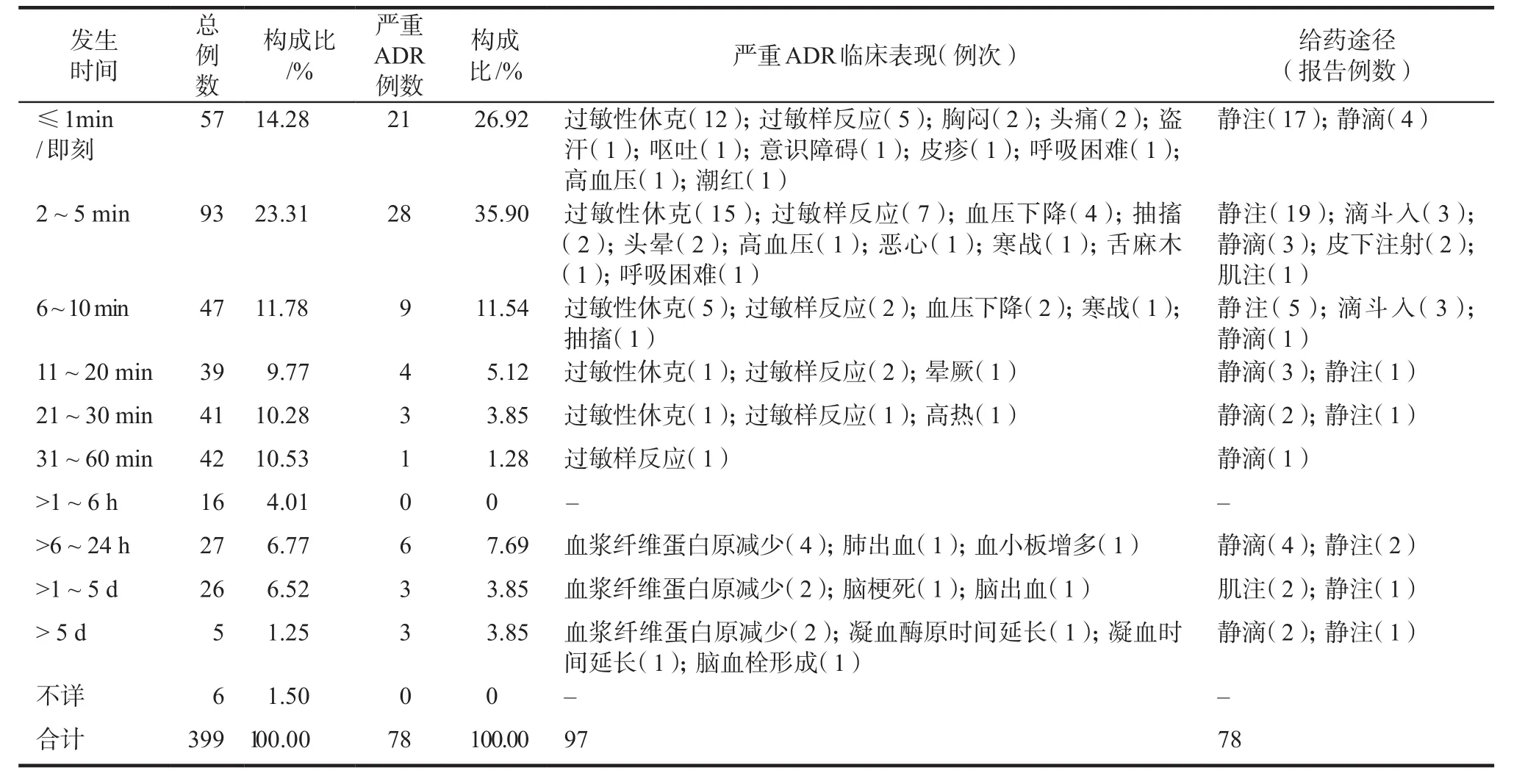
表5 ADR相关发生时间与给药途径Tab 5 The occurrence time and administration route involved in ADR
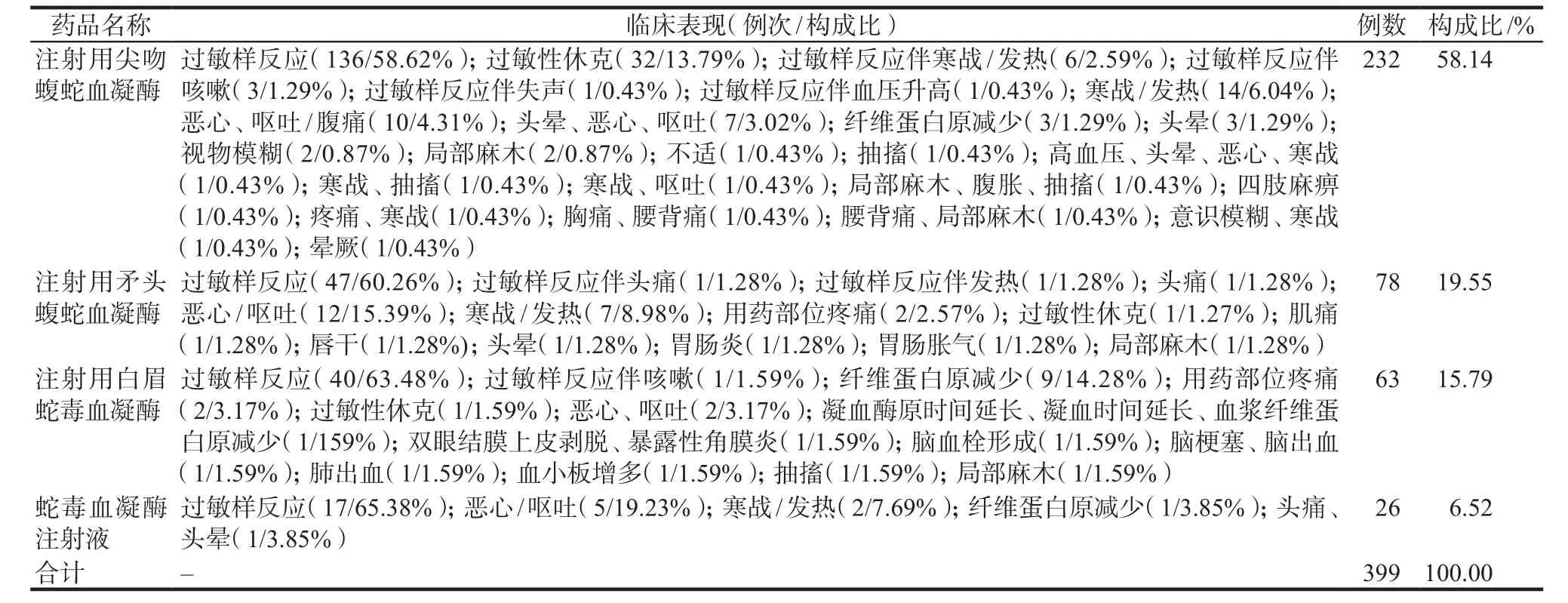
表6 蛇毒类血凝酶相关ADR临床表现分布特征Tab 6 Distribution of clinical manifestations involved in hemocoagulase-related ADR
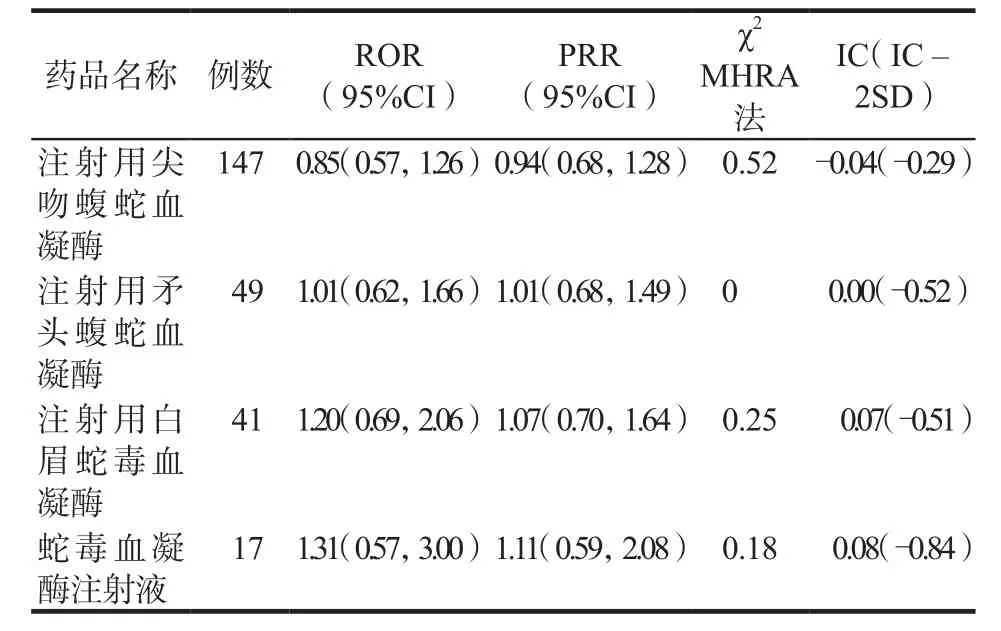
表8 过敏样反应异常信号检测结果Tab 8 Abnormal signal detection results of anaphylactoid reaction
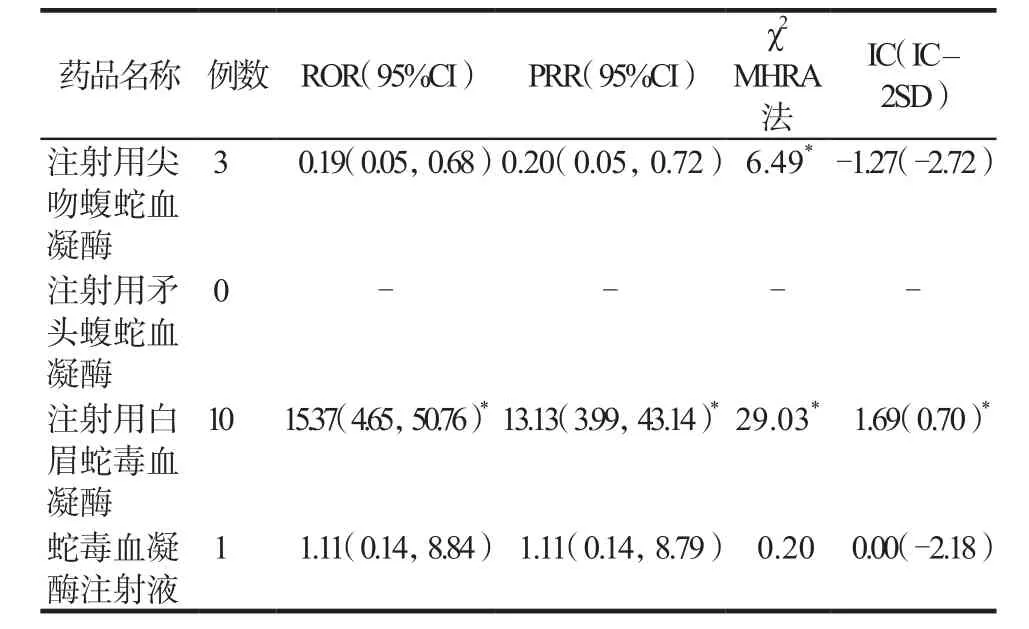
表9 血浆纤维蛋白原减少异常信号检测结果Tab 9 Abnormal signal detection results of plasma fibrinogen reduction
3.2 ADR的临床表现分析
过敏样反应可表现为累及皮肤黏膜、呼吸、心血管、神经、消化等多个系统/器官的损害[6],本研究所得蛇毒类血凝酶相关ADR与其基本一致,一般表现为胸闷、皮疹、恶心、寒战等,严重则表现为过敏性休克、过敏样反应、血浆纤维蛋白原减少等。4个品种的说明书中均示ADR发生率较低,为偶见/非常罕见过敏样反应,但过敏性休克可能危及生命,因此临床应用时需配备好抢救药材和设备,以备突发情况的发生。
3.3 ADR的发生时间及其与给药途径的关系
399例报告中,49.37%ADR和74.36%严重ADR发生在10 min以内,其临床表现主要为过敏性休克、过敏样反应等,提示为速发型过敏反应。69.42% ADR、83.33%严重ADR发生在用药后30 min之内,与相关文献报道结果一致[13-14]。发生严重过敏样反应用药时间最长的为60 min,提示临床用药后60 min内均应注意监测,尤其是有药物过敏史的患者。而用药后较长时间(> 6 h)发生的严重ADR多为血液系统损害,主要表现为血浆纤维蛋白原减少、脑梗死等。给药途径中,静脉滴注最多,为181例(45.36%),以静脉注射、滴斗入、静脉滴注、肌肉注射给药途径所引起的ADR,其中位发生时间分别为5、7.5、30、60 min。在用药10 min内引发严重ADR的给药途径中,静脉注射、静脉滴注、滴斗入各占41、8、6例;在用药11 ~ 60 min内引发严重ADR的给药途径中,静脉注射、静脉滴注各占2、6例。表明给药速度与ADR的发生时间可能相关,严重ADR表现更显著。以上均提示临床可视给药途径及用药后相应的时间段对患者加强监管,以期尽早发现ADR并采取相应治疗措施。注射用尖吻蝮蛇血凝酶说明书中仅推荐静脉注射给药,而临床上有以滴斗入方式替代,这可减慢给药速度,操作时只要注意使用纯溶媒,也不失为一种针对性的风险防控措施。
3.4 风险信号挖掘结果分析
4种信号挖掘方法均检出注射用尖吻蝮蛇血凝酶相关过敏性休克、注射用白眉蛇毒血凝酶相关血浆纤维蛋白原减少的异常风险信号。注射用尖吻蝮蛇血凝酶引发过敏性休克的原因可能有两方面因素:药物方面,蛇毒类血凝酶本身就是具有抗原性的异性蛋白[15],其辅料中的小分子右旋糖酐也可以通过免疫机制触发全身性过敏性反应[16];机体方面,手术及麻醉均可诱发机体产生急性期反应,导致机体在应激状态下的药物过敏反应增强[17],尤其对于过敏体质患者。注射用白眉蛇毒血凝酶相关血浆纤维蛋白原减少在说明书中虽有提示,但指的是大剂量(50 ~ 100 KU·次-1)时具有较强的去纤维蛋白原作用,能明显降低血液中的纤维蛋白原,使血液黏度及凝血性下降。而本研究结果显示常规剂量也可发生该ADR,这与国内相关文献报道结果相一致[18-19]。提示临床用药尤其是在外科手术中出现流血、渗血不止时,应谨慎、及时处理,切不可盲目大量用药,以避免严重ADR发生。张英等[20]人通过对白眉蛇毒血凝酶治疗食管胃静脉曲张破裂出血致严重低纤维蛋白原血症的相关因素研究发现,治疗3 ~ 10 d,累计严重低纤维蛋白原血症的发生率可达6.5%,治疗时间是其独立影响因素。国内相关共识[21]也指出,不推荐较长时间使用血凝酶,连续使用> 5 d需监测纤维蛋白原水平。
综上,本研究对蛇毒类血凝酶ADR自发报告的描述性分析,鉴于蛇毒类血凝酶相关ADR较多且严重,临床使用时应密切关注患者生理状态,连续使用该药> 5 d应注意监测患者凝血功能,提前做好应对措施。有条件时应开展注射用尖吻蝮蛇血凝酶相关过敏性休克、注射用白眉蛇毒血凝酶相关血浆纤维蛋白原减少的风险信号主动监测,以进一步验证蛇毒类血凝酶的临床安全性,减少用药风险。
