两种提取方法对辣木叶挥发油化学成分及抗氧化活性的影响研究
2019-11-04李国明李守岭张丽萍李秀林
李国明,李守岭*,张丽萍,李秀林
1云南省德宏热带农业科学研究所;2瑞丽海关综合技术中心,瑞丽 678600
辣木(MoringaoleiferaLam.)又称鼓槌树,为辣木科(Moringaceae)辣木属(Moringa)多年生落叶乔木植物[1,2]。研究表明,辣木富含纤维素、黄酮类[3,4]、维生素、蛋白质[5]、多糖类[6]、酚类及其苷[7,8]、生物碱类等营养性和功能性化学物质[9],具有免疫调节,抗癌,止痉挛、利尿、调节血压和胆固醇,降血糖,抗氧化,抗炎、抗溃疡,抗菌等生理活性[10-14]。
对辣木挥发性化学成分的研究中,采用水蒸气蒸馏法来提取辣木挥发油并以GC-MS法分析挥发油的化学成分的报道较多,该方法分析得到的辣木挥发油化学成分主要为脂肪酸类、烷烃类、醛类、烯烃类、甾体类、酮类、醇类、酯类、杂环类、萜类、胺类和芳香类等化合物[15-20]。而采用其它方法提取辣木挥发油并对比不同方法对化学成分种类及含量的研究鲜有报道。
本研究采用索氏提取法和超声波提取法提取非洲种、缅甸种和印度种三个品种的辣木叶挥发油,利用气相色谱-质谱联用仪研究两种提取方法对辣木叶挥发油化学成分类型及含量的影响。以DPPH自由基的清除能力作为评价指标,通过测定两种方法提取的三个品种的辣木叶挥发油对DPPH自由基的清除率和半数清除率IC50,研究三个品种辣木叶挥发油的抗氧化活性,为采用合适方法提取辣木挥发油并对挥发油品质评价提供科学依据。
1 材料与方法
1.1 材料
1.1.1 材料与试剂
本实验所用辣木叶为云南省德宏热带农业科学研究所辣木标椎化生产示范园种植的非洲辣木、缅甸辣木和印度辣木3个辣木品种。
试剂:石油醚(分析纯,沸程:30~60 ℃,成都市科隆化学品有限公司);正己烷(色谱纯,sigma-aldrich西格玛奥德里奇(上海)贸易有限公司);
1.1.2 仪器与设备
电子天平(型号:ML4002E,梅特勒-托利多仪器上海有限公司);电热鼓风干燥箱(型号:GZX-9140MBE,上海博讯实业有限公司医疗设备厂);索氏提取仪(型号:BSXT-06,上海豫明仪器有限公司);超声波双频清洗仪(型号:SB25-12DTS,宁波新芝生物科技股份有限公司);气相色谱—质谱联用仪(型号:Trace ISQ,美国Thermo Fisher公司);毛细管色谱柱(型号:TG-1701MS,30 m×0.25 mm×0.25 μm);循环水机(型号:CCA-1111)-真空旋转蒸发仪(型号:N-1200B)(上海泉杰科学仪器有限公司);中药材粉碎机(型号:DG160,浙江瑞安春海药材器械厂)。
1.2 方法
1.2.1 辣木叶样品制备
将采集的辣木叶样品,在电热鼓风干燥箱中60 ℃恒温烘干,粉碎后过60目样品筛,收集样品,干燥保存待用。
1.2.2 辣木叶挥发油提取
准确称取两份3个不同品种的辣木叶样品1.50 g,其中一份置于索氏提取器中,以30.0 mL石油醚,控制提取温度为40 ℃,加热回流提取1.5 h。另外一份置于250 mL具塞锥形瓶中,加入30.0 mL正己烷,在超声波清洗仪温度为30 ℃,功率为40.0 KHz,功率比为95.0%的条件下超声提取1.5 h。将两种方法收集的提取液经真空旋转蒸发仪浓缩,得到的略带特殊气味的淡黄色液体即为辣木叶挥发油。用色谱纯正己烷将辣木叶挥发油溶解后,转移至10.0 mL容量瓶,定容至刻度,摇匀静置后,密封保存待用。
1.2.3 辣木叶挥发油供测试溶液的配制
准确移取辣木叶挥发油0.5 mL于5.0 mL容量瓶中,以正己烷定容至刻度,采用旋涡混合器混匀静置后,移取1.0 mL挥发油待测液至进样瓶中,密封待测试。
1.2.4 气相色谱—质谱联用仪(GC-MS)分析条件
气相色谱条件:TG-1701MS毛细管色谱柱(30 m×0.25 mm×0.25 μm),程序升温(初始温度为60.0 ℃保持1.0 min,以10.0 ℃/min的升温速率升至250.0 ℃保持30.0 min),载气为高纯He,恒流模式,柱流量为1.0 mL/min,平均线速度为37 cm/s,进样量1.0 μL,进样口温度250.0 ℃,分流比100∶1。
质谱条件:EI电离模式,电子倍增管电压1 917.0 V,电子能量70.0 eV,离子传输管温度250.0 ℃,离子源温度250.0 ℃,扫描质量范围m/z为30~550 amu。
1.2.5 成分分析
按上述分析条件,对辣木叶挥发油待测溶液进样测试,得到辣木叶挥发油总离子流图。总离子流图中各色谱峰由质谱工作站Xcalibur 3.0结合NIST08标准质谱图数据库,进行综合分析得到挥发性化学成分的组成及质量分数。采用主成分分析法,对辣木叶挥发油化学成分中含量>1.00%的化学成分进行主成分分析。
1.2.6 辣木叶挥发油抗氧化活性测定
将3个不同品种的辣木叶挥发油以正己烷定容于5.0 mL容量瓶中,摇匀静置后,分别取挥发油待测液0.2、0.4、0.6、0.8、1.0 mL,以无水乙醇定容至10.0 mL。移取不同浓度待测液2.0 mL及2.0 mL DPPH溶液(0.1 mmol/L)于具塞比色管中,摇匀静置,30.0 min后,采用紫外/可见分光光度计,以无水乙醇为参比,在517 nm波长处测定吸光度Ai,同时测定2.0 mL DPPH溶液(0.1 mmol/L)与2.0 mL无水乙醇混合液的吸光度Ao,2.0 mL不同浓度待测液与2.0 mL无水乙醇混合液的吸光度Aj。用相同浓度的抗坏血酸水溶液(Vc)为阳性对照品,通过如下公式计算DPPH自由基的清除率。
清除率(%)=[1-(Ai-Aj)/Ao]×100%
以溶液质量浓度为横坐标,DPPH自由基清除率为纵坐标,绘制DPPH自由基清除率与质量浓度变化曲线。
1.3 数据处理
通过质谱工作站软件Xcalibur 3.0对采集得到的辣木叶挥发油总离子流图中各个色谱峰进行定性分析,结合NIST08标准质谱图数据库对各色谱峰对应的化合物进行综合分析鉴定,以峰面积归一化法计算各挥发性化合物的质量分数,采用 SPSS 17.0 统计软件,应用主成分分析法对辣木叶挥发油数据进行统计分析。
2 结果与分析
2.1 两种方法提取的辣木叶挥发油总离子流色谱图
辣木叶挥发油的总离子流色谱图经质谱工作站Xcalibur 3.0结合NIST08标准质谱图数据库进行谱库检索及综合分析,得到挥发油的化学成分组成及质量分数。索氏提取法提取的非洲种、缅甸种、印度种挥发油分别鉴定出74种(图1)、72种(图2)、62种(图3)化合物;超声波提取法提取的非洲种、缅甸种、印度种挥发油分别鉴定出63种(图4)、63种(图5)、57种(图6)化合物。

图1 索氏提取法提取的非洲辣木叶挥发油GC-MS总离子流色谱图Fig.1 GC-MS total ion flow chromatography of volatile oils extracted from leaves of Moringa oleifera of Africa by soxhlet extraction
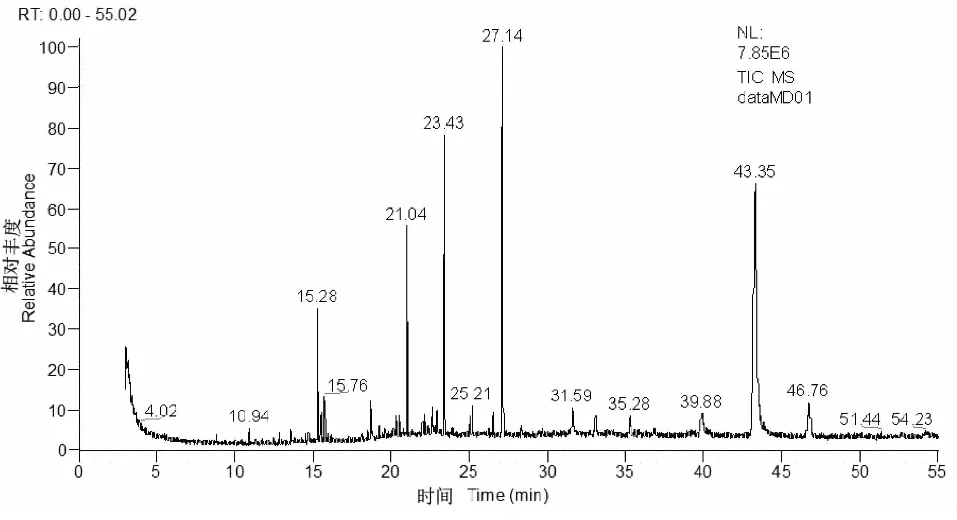
图2 索氏提取法提取的缅甸辣木叶挥发油GC-MS总离子流色谱图Fig.2 GC-MS total ion flow chromatography of volatile oils extracted from leaves of Moringa oleifera of Myanmar by soxhlet extraction

图3 索氏提取法提取的印度辣木叶挥发油GC-MS总离子流色谱图Fig.3 GC-MS total ion flow chromatography of volatile oils extracted from leaves of Moringa oleifera of India by soxhlet extraction

图4 超声波提取法提取的非洲辣木叶挥发油GC-MS总离子流色谱图Fig.4 GC-MS total ion flow chromatography of volatile oils extracted from leaves of Moringa oleifera of Africa by ultrasound extraction

图5 超声波提取法提取的缅甸辣木叶挥发油GC-MS总离子流色谱图Fig.5 GC-MS total ion flow chromatography of volatile oils extracted from leaves of Moringa oleifera of Myanmar by ultrasound extraction
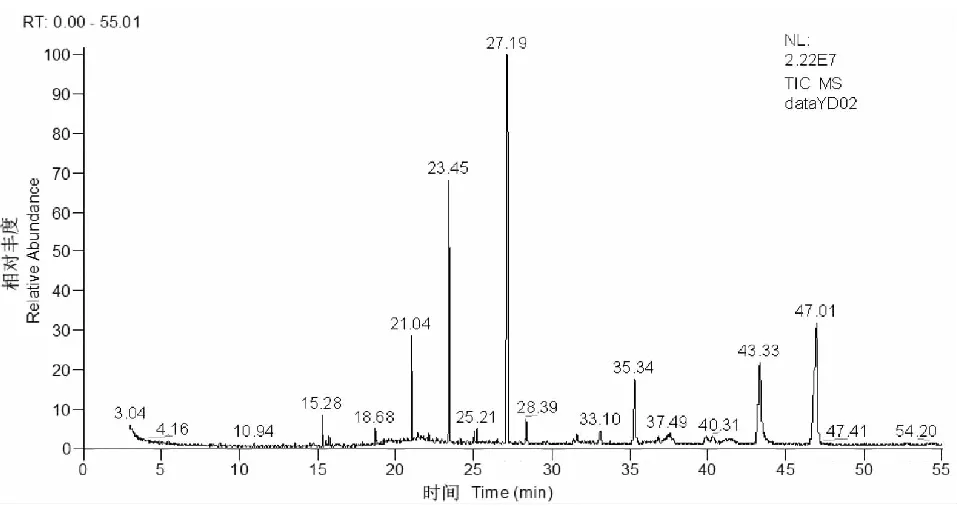
图6 超声波提取法提取的印度辣木叶挥发油GC-MS总离子流色谱图Fig.6 GC-MS total ion flow chromatography of volatile oils extracted from leaves of Moringa oleifera of India by ultrasound extraction
2.2 两种方法提取的辣木叶挥发油化学成分分析结果
辣木叶挥发油总离子流图中各色谱峰通过质谱工作站Xcalibur 3.0结合NIST08标准质谱图数据库进行成分分析鉴定,采用峰面积归一化法计算各挥发性化学成分的相对质量分数,鉴定出的化学成分及其质量分数结果见表1 。

表1 两种方法提取的辣木叶挥发油化学成分分析结果
续表1(Continued Tab.1)
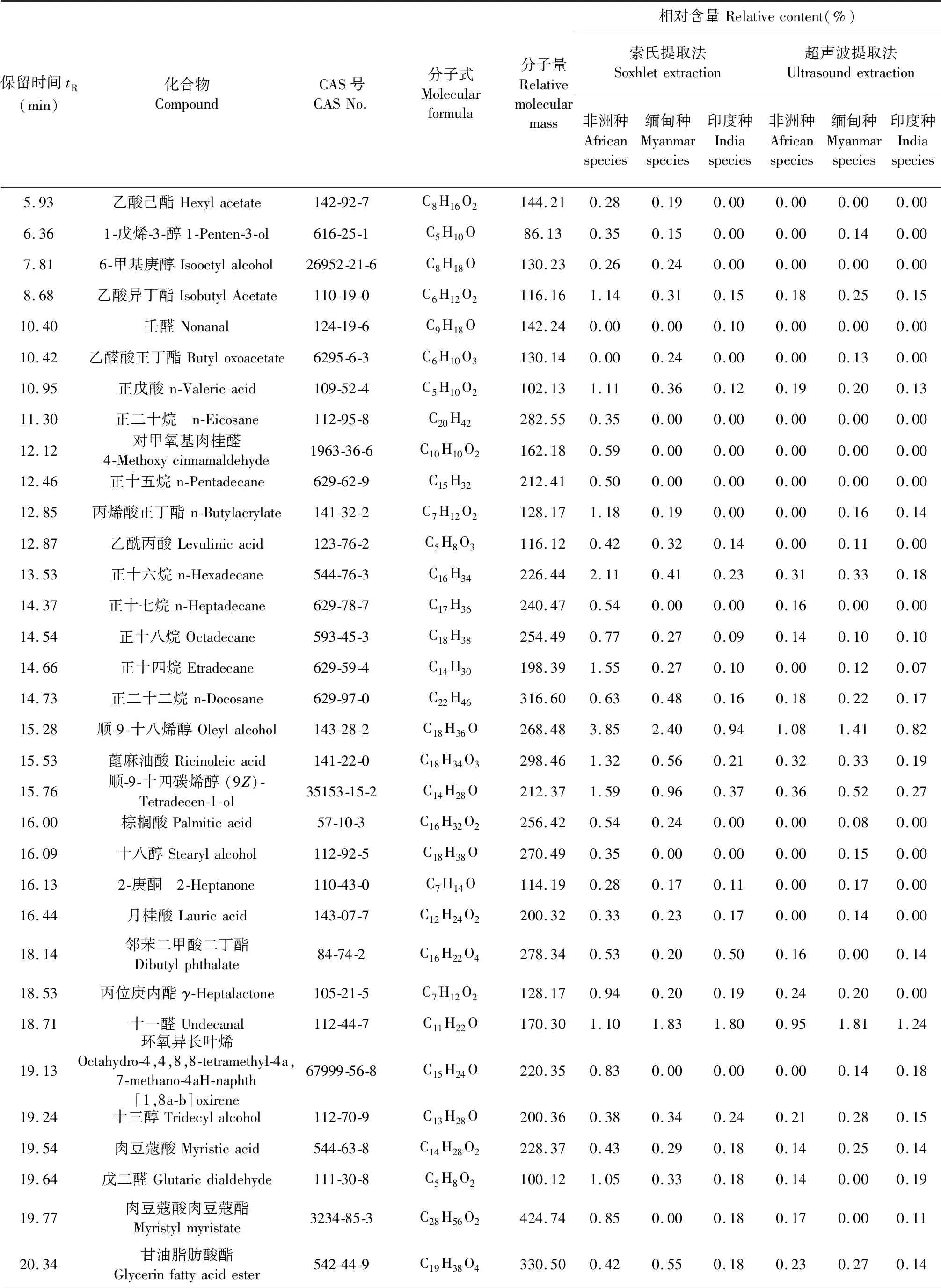
保留时间tR(min)化合物CompoundCAS号CASNo.分子式Molecularformula分子量Relativemolecularmass相对含量Relativecontent(%)索氏提取法Soxhletextraction超声波提取法Ultrasoundextraction非洲种Africanspecies缅甸种Myanmarspecies印度种Indiaspecies非洲种Africanspecies缅甸种Myanmarspecies印度种Indiaspecies5.93乙酸己酯Hexylacetate142-92-7C8H16O2144.210.280.190.000.000.000.006.361-戊烯-3-醇1-Penten-3-ol616-25-1C5H10O86.130.350.150.000.000.140.007.816-甲基庚醇Isooctylalcohol26952-21-6C8H18O130.230.260.240.000.000.000.008.68乙酸异丁酯IsobutylAcetate110-19-0C6H12O2116.161.140.310.150.180.250.1510.40壬醛Nonanal124-19-6C9H18O142.240.000.000.100.000.000.0010.42乙醛酸正丁酯Butyloxoacetate6295-6-3C6H10O3130.140.000.240.000.000.130.0010.95正戊酸n-Valericacid109-52-4C5H10O2102.131.110.360.120.190.200.1311.30正二十烷 n-Eicosane112-95-8C20H42282.550.350.000.000.000.000.0012.12对甲氧基肉桂醛4-Methoxycinnamaldehyde1963-36-6C10H10O2162.180.590.000.000.000.000.0012.46正十五烷n-Pentadecane629-62-9C15H32212.410.500.000.000.000.000.0012.85丙烯酸正丁酯n-Butylacrylate141-32-2C7H12O2128.171.180.190.000.000.160.1412.87乙酰丙酸Levulinicacid123-76-2C5H8O3116.120.420.320.140.000.110.0013.53正十六烷n-Hexadecane544-76-3C16H34226.442.110.410.230.310.330.1814.37正十七烷n-Heptadecane629-78-7C17H36240.470.540.000.000.160.000.0014.54正十八烷Octadecane593-45-3C18H38254.490.770.270.090.140.100.1014.66正十四烷Etradecane629-59-4C14H30198.391.550.270.100.000.120.0714.73正二十二烷n-Docosane629-97-0C22H46316.600.630.480.160.180.220.1715.28顺-9-十八烯醇Oleylalcohol143-28-2C18H36O268.483.852.400.941.081.410.8215.53蓖麻油酸Ricinoleicacid141-22-0C18H34O3298.461.320.560.210.320.330.1915.76顺-9-十四碳烯醇(9Z)-Tetradecen-1-ol35153-15-2C14H28O212.371.590.960.370.360.520.2716.00棕榈酸Palmiticacid57-10-3C16H32O2256.420.540.240.000.000.080.0016.09十八醇Stearylalcohol112-92-5C18H38O270.490.350.000.000.000.150.0016.132-庚酮 2-Heptanone110-43-0C7H14O114.190.280.170.110.000.170.0016.44月桂酸Lauricacid143-07-7C12H24O2200.320.330.230.170.000.140.0018.14邻苯二甲酸二丁酯Dibutylphthalate84-74-2C16H22O4278.340.530.200.500.160.000.1418.53丙位庚内酯γ-Heptalactone105-21-5C7H12O2128.170.940.200.190.240.200.0018.71十一醛Undecanal112-44-7C11H22O170.301.101.831.800.951.811.2419.13环氧异长叶烯Octahydro-4,4,8,8-tetramethyl-4a,7-methano-4aH-naphth[1,8a-b]oxirene67999-56-8C15H24O220.350.830.000.000.000.140.1819.24十三醇Tridecylalcohol112-70-9C13H28O200.360.380.340.240.210.280.1519.54肉豆蔻酸Myristicacid544-63-8C14H28O2228.370.430.290.180.140.250.1419.64戊二醛Glutaricdialdehyde111-30-8C5H8O2100.121.050.330.180.140.000.1919.77肉豆蔻酸肉豆蔻酯Myristylmyristate3234-85-3C28H56O2424.740.850.000.180.170.000.1120.34甘油脂肪酸酯Glycerinfattyacidester542-44-9C19H38O4330.500.420.550.180.230.270.14
续表1(Continued Tab.1)

保留时间tR(min)化合物CompoundCAS号CASNo.分子式Molecularformula分子量Relativemolecularmass相对含量Relativecontent(%)索氏提取法Soxhletextraction超声波提取法Ultrasoundextraction非洲种Africanspecies缅甸种Myanmarspecies印度种Indiaspecies非洲种Africanspecies缅甸种Myanmarspecies印度种Indiaspecies20.48正十五酸n-Pentadecanoicacid1002-84-2C15H30O2242.402.440.730.220.410.610.2120.75正庚基丙烯酸酯n-Heptylacrylate2499-58-3C10H18O2170.250.000.330.000.000.000.0020.78正庚酸Heptanoicacid111-14-8C7H14O2130.180.920.170.000.140.000.1821.06正二十四烷Tetracosane646-31-1C24H50338.653.094.694.803.163.703.3821.73异长叶烯酮Isolongifolenone23747-14-0C15H22O218.330.780.210.310.220.290.4021.76十八碳酸甲酯Methyloctadecanoate112-61-8C19H38O2298.510.000.000.170.150.290.2822.01十三酸Tridecanoicacid638-53-9C13H26O2214.341.040.390.210.150.230.2322.14肉豆蔻醇Tetradecylalcohol112-72-1C14H30O214.391.110.630.460.420.420.3622.211-十九碳烯1-Nonadecene18435-45-5C19H38266.510.390.270.410.370.280.2522.32十三碳二酸二甲酯Dimethylbrassylate1472-87-3C15H28O4272.380.210.430.240.180.660.0022.662-(4-甲基-3-环己烯基)丙醛2-(4-Methyl-cyclohex-3-enyl)-propionaldehyde29548-14-9C10H16O152.231.361.060.350.650.970.4522.78棕榈酸异丙酯Palmiticacidisopropylester142-91-8C19H38O2298.500.290.000.000.220.270.0022.96萜品油烯Terpinolene586-62-9C10H16136.200.580.880.220.620.790.2323.26十五醇1-Pentadecanol629-76-5C15H32O228.410.280.250.180.000.270.0023.45正二十八烷Octacosane630-02-4C28H58394.767.249.7716.9110.898.4611.9523.922,6-二叔丁基苯醌2,6-Di-tert-butyl-p-benzoquinone719-22-2C14H20O2220.311.130.450.210.140.000.0023.99γ-十二内酯4-Dodecanolide2305-5-7C12H22O2198.300.000.240.180.220.200.1624.14椰子醛Gamma-Nonanolactone104-61-0C9H16O2156.220.000.220.200.240.250.2825.15正二十六烷Hexacosane630-01-3C26H54366.710.740.790.980.750.630.7225.25油酸甲酯Methyloleate112-62-9C19H36O2296.490.951.451.121.021.200.8726.01二十烷酸甲酯Methyleicosanoate1120-28-1C21H42O2326.560.000.000.000.000.190.2226.27异长叶烷酮Isolongifolanone23787-90-8C15H24O220.350.850.480.230.270.000.0026.592-长松针烯2-Carene554-61-0C10H16136.230.251.390.400.400.760.3526.99肉豆蔻酸十二酯Dodecanylmyristate2040-64-4C26H52O2396.690.320.160.000.250.000.0027.14正二十一烷n-Heneicosane629-94-7C21H44296.5710.0219.6936.6118.5617.5927.6528.39环十五烷酰Cyclopentadecanol4727-17-7C15H30O226.400.501.100.551.672.621.7629.47丙烯酸乙酯Ethylacrylate140-88-5C5H8O2100.120.000.390.170.000.000.1429.52棕榈酸丁酯Hexadecanoicacid,butylester111-06-8C20H40O2312.530.790.000.280.220.000.1729.73正十二烷n-Dodecane112-40-3C12H26170.330.000.290.350.000.000.0029.76十九烷酸Nonadecanoicacid646-30-0C19H38O2298.500.000.200.000.320.360.3230.413-己醇3-Hexanol623-37-0C6H14O102.180.330.360.170.170.230.0031.391-十三烯1-Tridecene2437-56-1C13H26182.350.000.240.000.130.460.36
续表1(Continued Tab.1)

保留时间tR(min)化合物CompoundCAS号CASNo.分子式Molecularformula分子量Relativemolecular相对含量Relativecontent(%)索氏提取法Soxhletextraction超声波提取法Ultrasoundextraction非洲种Africanspecies缅甸种Myanmarspecies印度种Indiaspecies非洲种Africanspecies缅甸种Myanmarspecies印度种Indiaspecies31.609,10-十四烯-1-醇9,10-Tetradecenol52957-16-1C14H28O212.370.000.181.240.320.890.8731.6410-十一羧酸甲酯10-Undecenoicacid,methylester111-81-9C12H22O2198.300.901.720.001.100.000.0033.12正十九烷 Nonadecane629-92-5C19H40268.521.071.261.551.600.961.1133.982-壬酮2-Nonanone821-55-6C9H18O142.240.420.230.160.000.000.0035.29(Z)-11-十六碳烯-1-醇(Z)-Hexadec-11-en-1-ol56683-54-6C16H32O240.420.471.641.527.023.156.9435.331-十七醇Heptadecan-1-ol1454-85-9C17H36O256.470.400.260.000.003.060.0035.90对薄荷烷-1,8-二醇P-menthane-1,8-diol80-53-5C10H20O2172.260.000.480.000.000.140.0036.82顺-2-戊烯-1-醇Cis-2-Penten-1-ol1576-95-0C5H10O86.130.420.000.000.000.000.0036.842-十三烷酮2-Tridecanone593-08-8C13H26O198.350.000.460.890.760.370.5937.52十一醇1-Undecanol112-42-5C11H24O172.310.960.000.280.210.540.6937.54Z-9-十六碳稀-1-醇(9Z)-9-Hexadecen-1-ol10378-01-5C16H32O240.431.200.000.610.190.891.2039.88香草乙酮Acetovanillone498-02-2C9H10O3166.170.001.040.560.000.990.9139.89异香兰素3-Hydroxy-4-methoxybenzaldehyde621-59-0C8H8O3152.150.000.000.960.400.000.0039.97香芹酚Carvacrol499-75-2C10H14O150.220.000.960.000.350.000.0040.033,4-二甲基苯甲酸3,4-Dimethylbenzoicacid619-04-5C9H10O2150.170.330.550.000.000.210.0040.3410-十一烯酸Undecenoicacid112-38-9C11H20O2184.280.470.000.280.570.900.4740.414-叔丁基苯酚P-tert-butylphenol98-54-4C10H14O150.220.560.230.000.000.230.4541.44十八碳烷酸Octadecanoicacid57-11-4C18H36O2284.480.370.210.220.230.160.0043.25乙酸丁香酚酯1-Acetoxy-2-methoxy-4-93-28-7C12H14O3206.245.4115.3111.0710.4314.408.95allylbenzene1,3,4-Eugenolacetate46.72月桂醛Lauraldehyde112-54-9C12H24O184.320.763.963.6825.4818.8519.7
由分析结果可知,非洲种辣木叶挥发油化学成分中,超声波提取法分析得到了月桂醛、油酸甲酯和(Z)-11-十六碳烯-1-醇三种化合物,索氏提取法分析得到了蓖麻油酸和肉豆蔻醇两种影响挥发油品质的化合物;缅甸种辣木叶挥发油化学成分中,索氏提取法得到的正二十四烷、正二十八烷、正二十一烷和乙酸丁香酚酯4个化合物的质量分数较高,超声波提取法月桂醛含量较高;印度种辣木叶挥发油化学成分中,索氏提取法得到的正二十四烷、正二十八烷、正二十一烷和乙酸丁香酚酯4个化合物的质量分数较高,超声波提取法月桂醛含量较高。
2.3 两种方法提取的辣木叶挥发油化学成分主成分分析
选择两种方法提取的辣木叶挥发油化学成分中含量>1.00%的33种化学成分作为分析对象,依次编号为F1~F33。计算化学成分F1~F33的均值,采用最大方差法旋转因子及标准化全部的F1~F33值,计算协方差矩阵的特征值与特征向量,所得成分的方差即为相应的特征值,计算的方差累积贡献率>85%的成分即为主成分。从辣木叶挥发油碎石图(图7),可以看出PCA的特征值变化趋势,保留前5个主成分可以概括辣木叶挥发油化学成分的绝大部分信息,前5个主成分的特征值分别为:λ1=18.000,λ2=6.733,λ3=3.981,λ4=3.182,λ5=1.104,数值均大于1。分析贡献率数值可知,提取的前5个主成分总的累计贡献率为100.00%>85%,表明前5个主成分包含了原来33个化合物的几乎全部信息。辣木叶挥发油的碎石图中每一个碎石的特征值作为特征数量值的基础,决定了主成分需要被保留的数目。
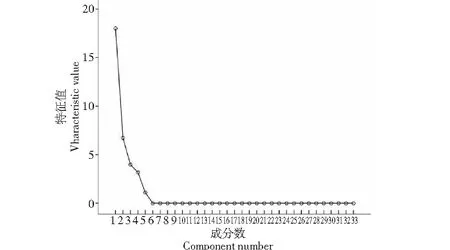
图7 两种方法提取的辣木叶挥发油碎石图(成分>1.00%)Fig.7 Scree graph of volatile oils extracted by two methods from leaves of Moringa oleifera (composition>1.00%)
对辣木叶挥发油化学成分进行主成分分析,提取了5个主成分,第一主成分(PC1)的特征值为18.000,贡献率为54.55%,对应的特征向量依次以乙酸异丁酯、正戊酸、丙烯酸正丁酯、正十六烷、正十四烷、顺-9-十八烯醇、蓖麻油酸、顺-9-十四碳烯醇、戊二醛、正十五酸、十三酸、肉豆蔻醇、2-(4-甲基-3-环己烯基)丙醛、2,6-二叔丁基苯醌等14种化合物较大,第一主成分受这些成分的影响比较大;第二主成分(PC2)的特征值为6.733,贡献率为20.40%,对应的特征向量依次以γ-戊内酯、(E)-2-己烯-1-醇、环戊醇、2-蒈烯、10-十一羧酸甲酯等5种化合物较大,第二主成分受这些成分的影响比较大;第三主成分(PC3)的特征值为3.981,贡献率为12.06%,对应的特征向量依次以十一醛、正二十四烷、油酸甲酯、乙酸丁香酚酯等4种化合物较大,第三主成分受这些成分的影响比较大;第四主成分(PC4)的特征值为3.182,贡献率为9.64%,对应的特征向量依次以环十五烷酰、1-十七醇、月桂醛等3种化合物较大,第四主成分受这些成分的影响比较大;第五主成分(PC5)的特征值为1.104,贡献率为3.35%,对应的特征向量以Z-9-十六碳稀-1-醇和香草乙酮较大,第五主成分受其影响比较大。
2.4 两种提取方法对辣木叶挥发油化学成分的影响分析
通过对两种方法提取的三个品种辣木叶挥发油化学成分的分析可知,辣木叶挥发油的化学成分类别的质量分数(见表2)和数量(见表3)均有显著差异。

表2 两种提取方法对辣木叶挥发油化学成分类别质量分数的影响
由表2可知,三个品种的辣木叶挥发油化学成分主要属于酯类、醇类、烷烃类、酮类、醛类、羧酸类、烯烃类、醌类、酰类和酚类等10类化合物,两种提取方法均得到了含量较高的烷烃类、酯类、醇类、醛类等5类共同化合物。
由表3可知,两种方法提取的挥发油化学成分中数量较多的为酯类、醇类、烷烃类、酮类、醛类、羧酸类和烯烃类等7类化合物。索氏提取法得到的三个品种种辣木叶酯类、醇类、烷烃类、酮类和羧酸类等5类化合物数量较多,超声波提取法得到的醛类和烯烃类化合物数量较多。

表3 两种提取方法对辣木叶挥发油化学成分类别数量的影响
2.5 辣木叶挥发油抗氧化活性分析
本实验采用DPPH自由基,在517 nm波长处对两种方法提取的三个品种的辣木叶挥发油抗氧化活性进行了定量分析,各实验样品对DPPH自由基的清除能力曲线见图8~13。由DPPH自由基的清除能力曲线图可知,辣木叶挥发油对DPPH自由基的清除率均随着挥发油质量浓度的增加而增大,并具有一定的量效关系。质量浓度(x)与清除率(y)之间的量效关系,半数清除率IC50,相关系数r及量效范围见表4。
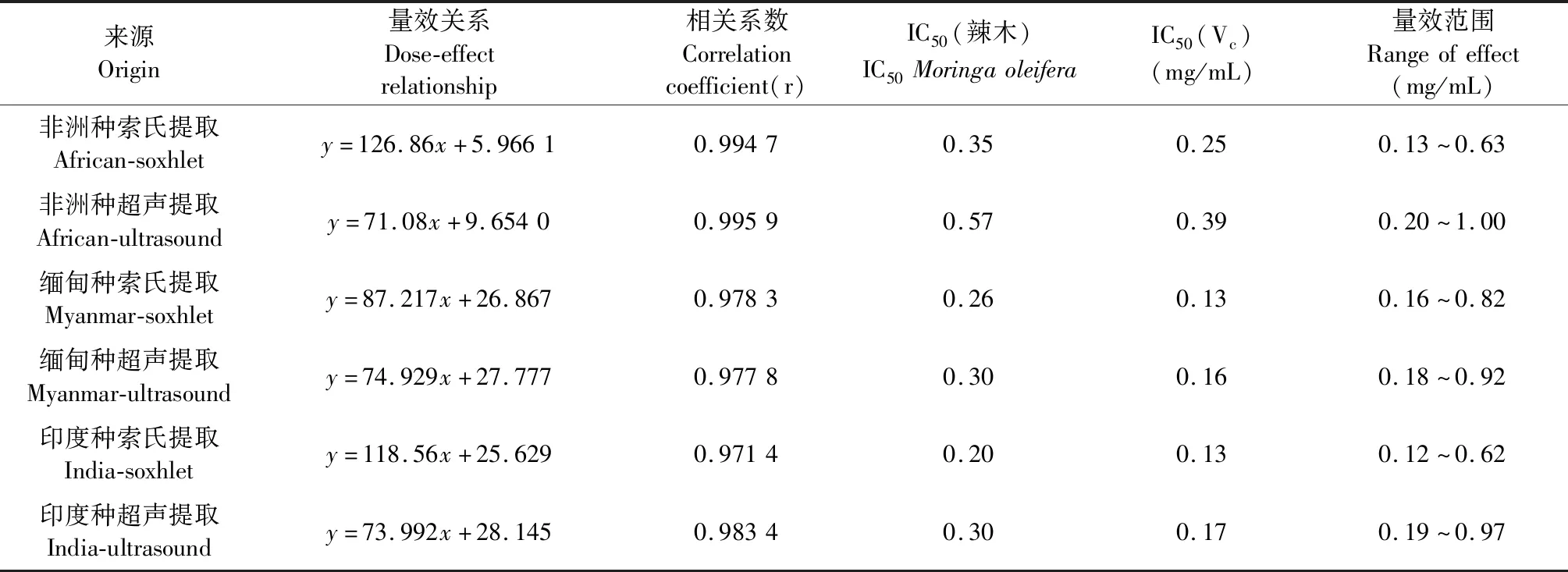
表4 两种方法提取的辣木叶挥发油抗氧化能力测定
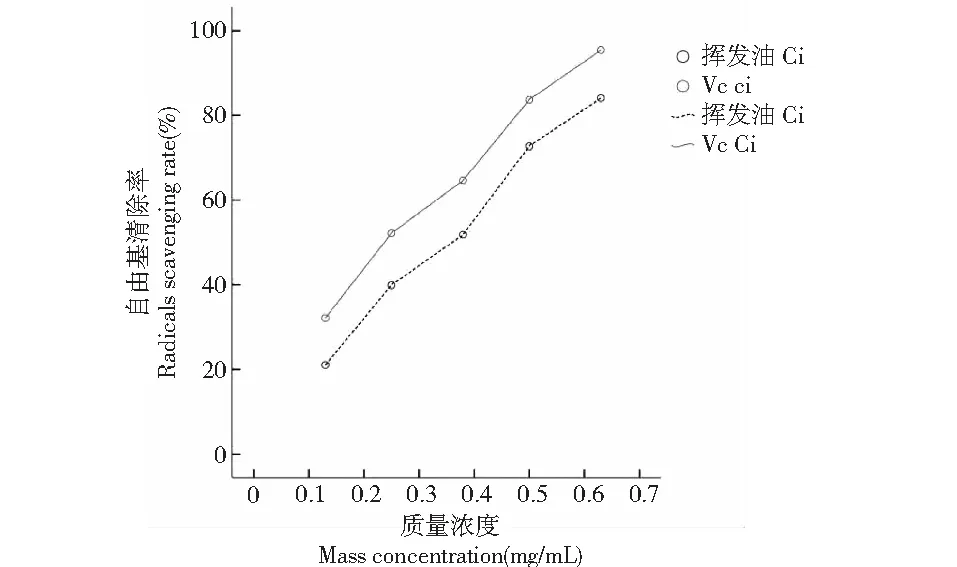
图8 索氏提取法提取的非洲辣木叶挥发油对DPPH自由基的清除能力Fig.8 DPPH free radicals scavenging capacity of volatile oils extracted from leaves of Moringa oleifera of Africa by soxhlet extraction
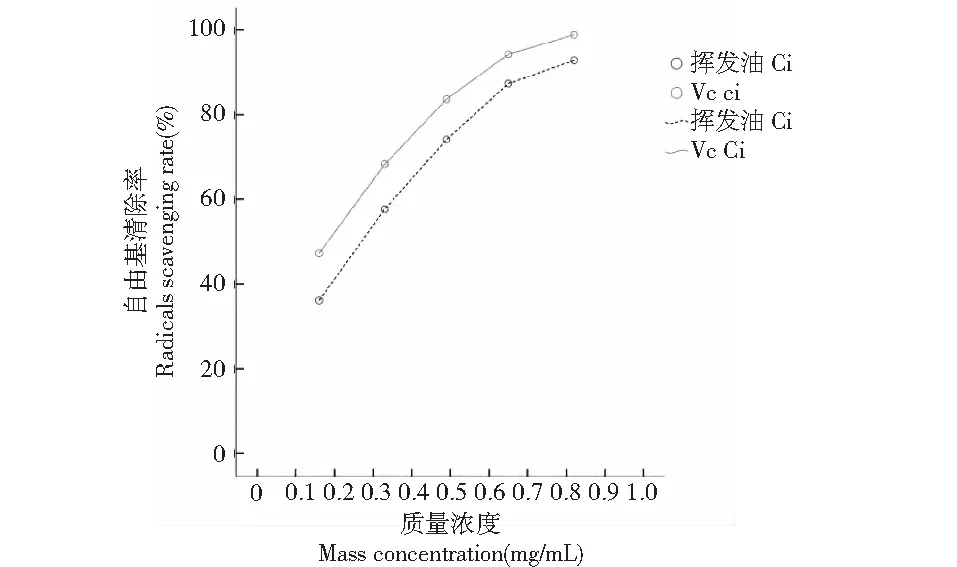
图10 索氏提取法提取的缅甸辣木叶挥发油对DPPH自由基的清除能力Fig.10 DPPH free radicals scavenging capacity of volatile oils extracted from leaves of Moringa oleifera of Myanmar by soxhlet extraction
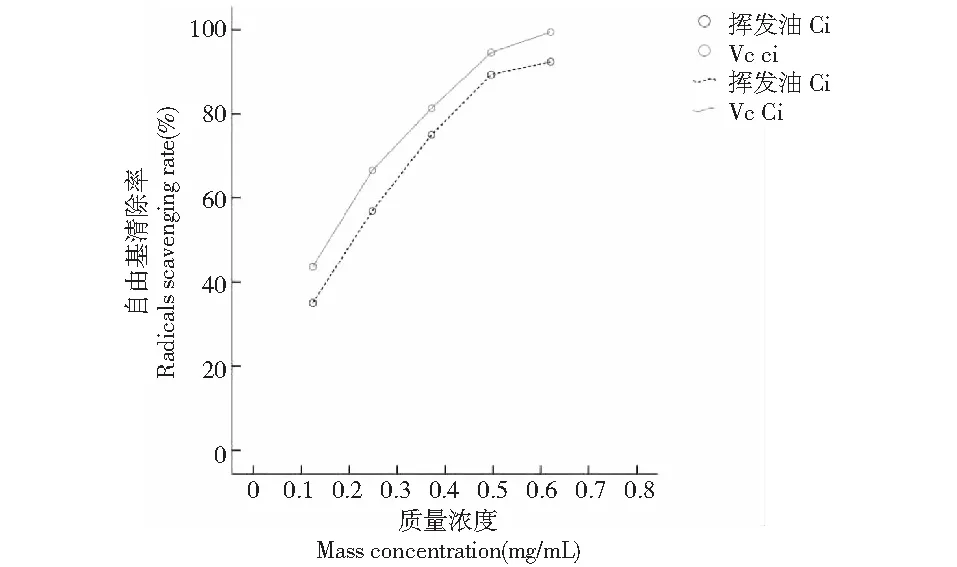
图12 索氏提取法提取的印度辣木叶挥发油对DPPH自由基的清除能力Fig.12 DPPH free radicals scavenging capacity of volatile oils extracted from leaves of Moringa oleifera of India by soxhlet extraction
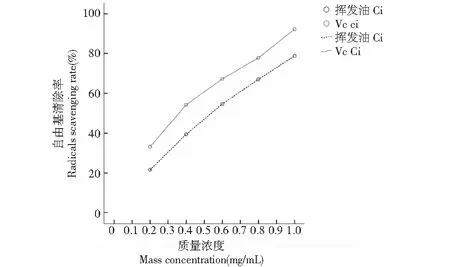
图9 超声波提取法提取的非洲辣木叶挥发油对DPPH自由基的清除能力Fig.9 DPPH free radicals scavenging capacity of volatile oils extracted from leaves of Moringa oleifera of Africa by ultrasound extraction

图11 超声波提取法提取的缅甸辣木叶挥发油对DPPH自由基的清除能力Fig.11 DPPH free radicals scavenging capacity of volatile oils extracted from leaves of Moringa oleifera of Myanmar by ultrasound extraction
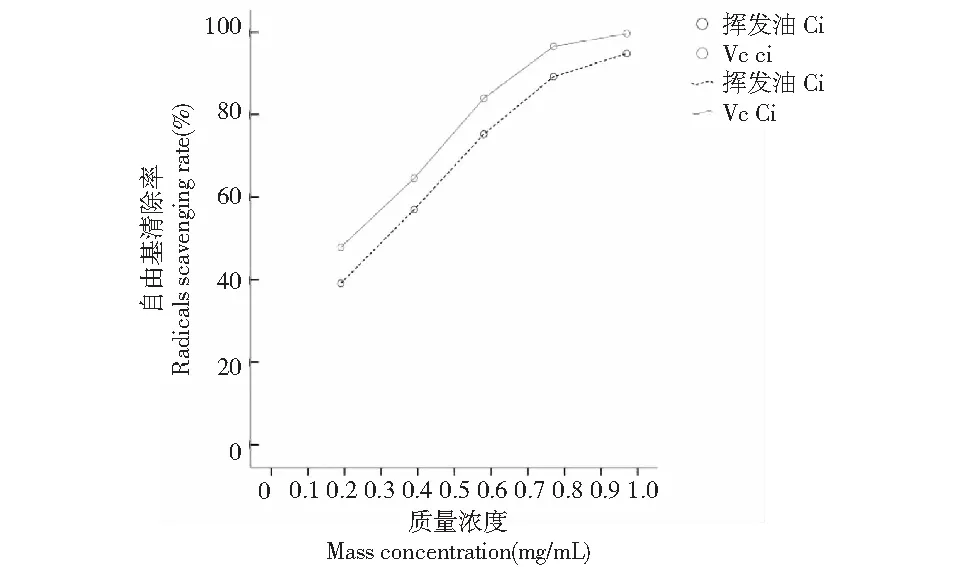
图13 超声波提取法提取的印度辣木叶挥发油对DPPH自由基的清除能力Fig.13 DPPH free radicals scavenging capacity of volatile oils extracted from leaves of Moringa oleifera of India by ultrasound extraction
3 结论
本研究采用索氏提取法和超声波提取法提取非洲种、缅甸种和印度种三个品种的辣木叶挥发油,以气相色谱质谱联用仪(GC-MS)对辣木叶挥发油化学成分及其含量进行分析。通过分析可知,三个品种的辣木叶挥发油化学成分属于酯类、醇类、烷烃类、酮类、羧酸类、醛类、烯烃类、醌类、酰类、酚类等10类化合物。索氏提取法得到的印度种挥发油未分析鉴定出酚类化合物,超声波提取法得到的缅甸种和印度种挥发油未分析鉴定出醌类化合物。索氏提取法得到的挥发油酯类含量较高,超声波提取法得到的醛类的含量较高,且缅甸种挥发油酯类含量均比其它两个品种高。索氏提取法得到的非洲种挥发油酯类、醇类、酮类、羧酸类、烯烃类、醌类和酚类含量较高,超声波提取法得到的挥发油烷烃类、醛类和酰类含量较高;索氏提取法得到的缅甸种挥发油酯类、烷烃类、酮类、羧酸类、烯烃类、醌类和酚类含量较高,超声波提取法得到的挥发油醇类、醛类和酰类含量较高;索氏提取法得到的印度种挥发油酯类、烷烃类、酮类和醌类含量较高,超声波提取法得到的挥发油醇类、醛类、羧酸类、烯烃类、酰类和酚类含量较高。通过测定DPPH自由基的清除率,证实辣木叶挥发油均具有一定的抗氧化活性,且挥发油的质量浓度与DPPH自由基清除率之间存在一定的量效关系。索氏提取法得到的挥发油半数清除率IC50值分别为0.35 mg/mL (非洲种)、0.26 mg/mL(缅甸种)、0.20 mg/mL(印度种);超声波提取法得到的挥发油半数清除率IC50值分别为0.50 mg/mL(非洲种)、0.30 mg/mL(缅甸种)、0.30 mg/mL(印度种)。实验结果表明,三个品种的辣木叶挥发油均具有一定的抗氧化活性,具有作为天然抗氧化剂的应用潜质。
