不同原料血浆制备的冷沉淀对凝血因子Ⅷ及纤维蛋白原的影响 杨
2019-10-30颜菁王艳清谢冬梅龚嘉聪
颜菁 王艳清 谢冬梅 龚嘉聪
[摘要]目的 分析由四種原料新鲜冰冻血浆制备的冷沉淀所含凝血因子Ⅷ(FⅧ)及纤维蛋白原(Fg)含量,为临床提供优质安全的冷沉淀制剂。方法 随机抽取2015年4月我站采集的20袋(ACD-B配方)全血,在6 h内按照成分制备标准操作规程制备四种新鲜冰冻血浆[新鲜冰冻血浆(FFP)、滤白冰冻血浆、灭活冰冻血浆、滤白灭活冰冻血浆]并速冻;1周后将制备的FFP在低温水浴箱(4±2)℃融化后,用虹吸法原理制备出四种冷沉淀(冰冻血浆冷沉淀、滤白冷沉淀、灭活冷沉淀、滤白灭活冷沉淀)并速冻;冰冻1周后在37℃水浴箱融化后检测凝血因子FⅧ含量及Fg含量。结果 FFP冷沉淀、滤白冷沉淀、灭活冷沉淀、滤白灭活冷沉淀的FⅧ及Fg含量依次为(1.506±0.351)、(1.352±0.217)、(1.184±0.235)、(0.724±0.281)IU/ml和(3.055±0.474)、(2.801±0.313)、(1.671±0.215)、(1.552±0.162)g/L,不同冷沉淀间的FⅧ及Fg含量比较,差异有统计学差异(P<0.05)。FFP冷沉淀、滤白冷沉淀、灭活冷沉淀、滤白灭活冷沉淀的FⅧ及Fg回收率依次为100.0%、89.7%、78.6%、48.1%和100.0%、91.7%、54.7%、50.8%,不同冷沉淀的回收率比较,差异有统计学差异(P<0.05)。结论 采用不同原料、不同方法制备出的冷沉淀FⅧ及Fg含量有所差别,FFP冷沉淀、滤白冷沉淀、灭活冷沉淀的FⅧ及Fg含量较高且符合国家标准。
[关键词]新鲜冰冻血浆;凝血因子;纤维蛋白原;冷沉淀
[中图分类号] R943 [文献标识码] A [文章编号] 1674-4721(2019)8(c)-0041-03
[Abstract] Objective To analyze the content of clotting factor Ⅷ (FⅧ) and fibrinogen (Fg) in cold precipitation prepared from fresh frozen plasma of four kinds of raw materials and provide high quality and safe cold precipitation preparations for clinical use. Methods A total of 20 bags of whole blood (ACD-B formula) collected by our station in April 2015 were randomly sampled, four kinds of fresh frozen plasma (cryoprecipitation of frozen plasm [FFP], filtered frozen plasma, inactivated cold precipitation, filtering inactivated frozen plasm) were prepared and quick freezing in 6 hours according to the standard operating procedures for preparation. Four kinds of fresh frozen plasma prepared after one week were melted in a low temperature water between(4±2)℃, four kinds of cold precipitates were prepared by siphon method, and quick freezing. The content of FⅧ and Fg were detected after thawing in 37℃ water bath after 1 week of freezing. Results FFP cryoprecipitate, filtered white cold precipitate, inactivated cryoprecipitate, filtered white inactivated cryoprecipitate FⅧ and Fg content were (1.506±0.351), (1.352±0.217), (1.184±0.235), (0.724±0.281) IU/ml and (3.055±0.474), (2.801±0.313), (1.671±0.215), (1.552±0.162) g/L, there were statistically significant differences in FⅧ and Fg content between different cryoprecipitates (P<0.05). The FⅧ and Fg recovery rates of FFP cryoprecipitate, filtered white cold precipitation, inactivated cryoprecipitate and whitening inactivated cryoprecipitate were 100.0% and 89.7%, respectively. 78.6%, 48.1% and 100.0%, 91.7%, 54.7%, 50.8%, the recovery rates of different cryoprecipitates were statistically different (P<0.05). Concluison The contents of FⅧ and fibrinogen in cold precipitation, filter white cold precipitation and inactivated cold precipitation of FP are higher and meet the national standards.
[Key words] Fresh frozen plasma; Clotting factor; Fibrinogen; Cold precipitation
冷沉淀是采用特定的提取方法,将冰冻血浆在低温条件下(一般为4℃)融化后的一些不溶性物质所提取出来的,这些不溶性物质中含有凝血过程物质,如纤维蛋白原(Fg)、凝血因子Ⅷ(FⅧ)等。在临床工作中,由于血浆制品的缺乏,冷沉淀被广泛用于那些由凝血功能障碍导致的疾病[1-3]。目前在血液中心工作中,制备冷沉淀时主要有新鲜冰冻血浆(FFP)、新鲜病毒灭活冰冻血浆(灭活FFP)、新鲜滤白冰冻血浆(滤白FFP)、新鲜滤白病毒灭活冰冻血浆(滤白灭活FFP),而据以往临床研究报道,不同的方法制备出的冷沉淀其质量不同,而反应冷沉淀质量的两个重要指标即是FⅧ及Fg含量[3-4],本研究探讨这四种冷沉淀制备方法所制备出的冷沉淀FⅧ及Fg的差异,现报道如下。
1材料与方法
1.1标本来源
随机抽取2015年4月我站采集的(ACD-B配方)400 ml全血20袋,所有血液来源均有记录,且这些血源的献血者和血液质量均符合国家相关规定的要求[5-6],这些血制品保存于2~6℃条件下,并在6 h内制成冰冻血浆制品。本研究经我中心医学伦理委员会审核批准。
1.2方法
血浆及冷沉淀制备方法及过程。将400 ml全血分成2份,每份200 ml,1份接驳5联袋,另1份接驳滤白血袋。将接驳五联袋的200 ml全血离心制备100 ml新鲜血浆,平均分成2份,1份为新鲜血浆,另1份进行用MB-P病毒灭活制备成灭活新鲜血浆。接驳滤白血袋的200 ml全血经滤白后以同样的方法离心制备成滤白新鲜血浆和滤白灭活新鲜血浆。将4种新鲜血浆各接驳一空袋,并各留取5 ml样本,将血浆和样本速冻后放入低温冰箱冰冻保存。4种血浆冰冻1周后取出,采用虹吸法制备冷沉淀,剩余血浆即为GRP,再放入冰箱冰冻保存。1周后取出上述4种FFP样本和4种CRP血浆在37℃水浴箱融化后进行检测。
1.3检测指标
采用凝固法检测FⅧ和Fg含量。
1.3.1试剂材料 凝血因子试剂盒购于南京建成生物工程公司,操作流程均按照说明书进行;其余一次性使用血袋等制品均取用我站统一购买的一次性物品。
1.3.2仪器设备 大容量低温离心机;血浆速冻机;病毒灭活机;医用低温冰箱;分光光度计;全自动血凝仪;无菌接管机。以上仪器均由我站设备科提供安装,检测时这些仪器均处于正常工作状态,保证测量值的准确。
1.4统计学方法
采用SPSS 17.0统计学软件进行数据处理,计量资料以均数±标准差(x±s)表示,多组间比较采用F检验,两组间比较采用LSD-t检验;计数资料以率表示,采用χ2检验,以P<0.05为差异有统计学意义。
2结果
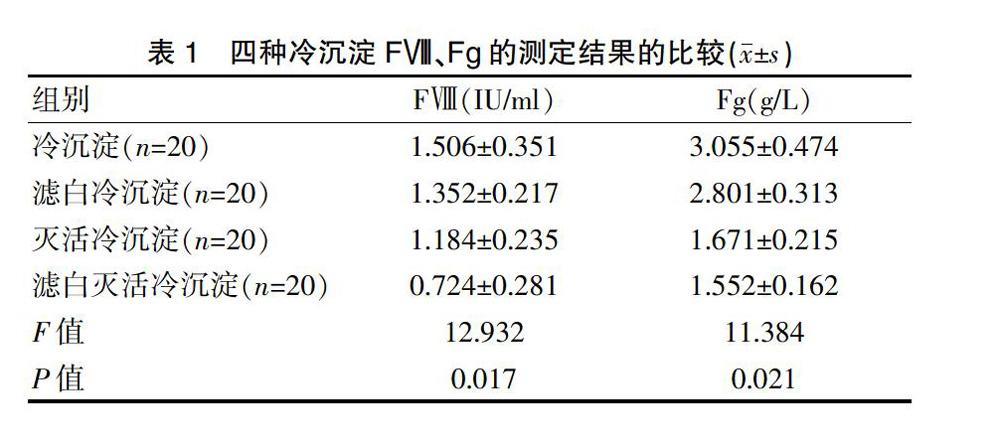
2.1四种冷沉淀FⅧ、Fg测定结果的比较
FFP冷沉淀、滤白冷沉淀、灭活冷沉淀、滤白灭活冷沉淀的FⅧ及Fg含量比较,差异有统计学意义(P<0.05)(表1)。
2.2四种冷沉淀FⅧ、Fg回收结果的比较
本试验检测出FFP冷沉淀、滤白冷沉淀、灭活冷沉淀、滤白灭活冷沉淀的FⅧ及Fg回收率依次为100.0%、89.7%、78.6%、48.1%和100.0%、91.7%、54.7%、50.8%。滤白灭活冷沉淀Ⅷ及Fg损失率接近50.0%。各种冷沉淀的FⅧ及Fg回收率比较,差异有统计学意义(P<0.05)。
3讨论
冷沉淀是冰冻血浆在4℃左右产生的不溶性白色沉淀物。冷沉淀是采用特定的提取方法,将冰冻血浆在低温条件下(一般为4℃)融化后的一些不溶性物质所提取出来的,这些不溶性物质中含有凝血过程物质,如纤维蛋白原、凝血因子等。在临床工作中,由于血浆制品的缺乏,冷沉淀被广泛用于那些由凝血功能障碍导致的疾病。同时,目前对冷沉淀的制作主要有FFP、灭活FFP、滤白FFP、滤白灭活FFP,受具体血站条件限制,其选择的制作方法有所不同[7-8]。大部分血站为了保障冷沉淀的质量,通常对血浆不做病毒灭活处理或滤除白细胞制作冷沉淀[9]。由于输血可引起血源性疾病的传播和同种免疫反应,对所有的血液制剂来说风险较高的是输注冷沉淀,更容易使病毒传染[10-11]。
国内的研究[7-8]已经证明,针对冷沉淀的制作,采用亚甲蓝光化学灭活冷沉淀中的病毒被认为对于冷沉淀是一种高效、安全的灭活方式,目前在我国仅有此法被批准应用于冷沉淀的灭活。亚甲蓝光化学灭活技术的原理主要是利用亚甲蓝与病毒的含有磷酸双分子层的模型结构相结合,其后在可见光的照射下发生作用而使得病毒无法复制和生存,以此达到灭活的目的[12-13]。虽然亚甲蓝光化学灭活法对病毒的灭活十分有效,但是此法仅仅对游离在胞质外的病毒有效,而对在采集血液前已经寄生于细胞中的病毒却无效。由于冷沉淀中含有的细胞多数为白细胞,所以如何除去白细胞中的病毒或直接除去白细胞成为广大临床输血者共同关注的热点问题,由于白细胞比冷沉淀的有效成分-凝血因子的直径更大,所以对冷沉淀采用特制的滤过膜能有效的将白细胞去除[14-15]。
白细胞过滤器可降低非溶血性输血发热反应的发生率,降低输血后移植物抗宿主病(GVHD)的发生率,防止部分输血相关病毒的传染,预防HLA同种异体免疫反应引起的血小板输注无效,降低了输血风险[16-17]。目前,国外采用的滤白冷沉淀制备方法在国内已被各个供血机构广泛采用,而增加滤白冷沉淀的工序无疑会对冷沉淀的成分產生影响[18]。而我国现行冷沉淀质量控制标准中,明确规定了在200 ml冷沉淀中,FⅧ的含量应>80 IU,而对Fg的水平并未做明确规定。而经过本次检测,采用滤白冰冻血浆制备的冷沉淀达到了质量控制标准因此可在临床推广应用。另一方面,对冰冻血浆进行灭活处理也能达到降低血液输注风险的目的,因为灭活处理技术使得各种病毒失去活性,丧失了感染能力,可降低输注风险,研究结果显示采用灭活新鲜冰冻血浆制备的冷沉淀中的FⅧ的含量达到质量控制标准因此可在临床应用。而滤白细胞和病毒灭活同时进行制备的滤白灭活冷沉淀,其Ⅷ及Fg含量均未达到国家标准,暂不能用于临床使用。
本研究结果提示,单采用新鲜冰冻血浆制备的冷沉淀,虽然FⅧ的含量达到了质量控制标准,但其由于献血人员健康状况不确定、未经病毒灭活处理及可能因白细胞存在而发生异体免疫反应,使得它的应用受到较大限制;而采用了滤白和灭活两道工序的滤白灭活冷沉淀,未能达到质量控制标准不能使用。滤白冷沉淀和灭活冷沉淀由于避免了上述风险且质量达标,故可推广使用。
[参考文献]
[1]项军,周静宇,王泰瑞.病毒灭活血浆制备时间对FⅧ活性的影响[J].临床血液学杂志,2012,25(1):95-96.
[2]邱颖婕,徐忠,徐蓓,等.病毒灭活冷沉淀制备过程中滤除亚甲蓝对凝血因子的影响[J].临床输血与检验,2014,16(4):413-415.
[3]陈菊芬,沈磁石,叶有玩,等.不同时间制备的血浆及冷沉淀的质量比较[J].中国输血杂志,2013,26(5):454-456.
[4]李慧,刘春燕,张锡敏,等.两种制备冷沉淀方法的应用与评价[J].临床血液学杂志,2014,27(3):496-497.
[5]中华人民共和国卫生部.献血者健康检查要求[S].2012.
[6]中华人民共和国卫生部和中国国际标准委员会.GB18469-2012中华人民共和国标准:全血及成分血质量要求[S].北京标准出版社,2012.
[7]Spence RK.Clinical use of plasma and plasma fractions[J].Best Pract Res Clin Haematol,2006,19(1):83-96.
[8]王莉,杜家成,刘金嫔,等.经白细胞过滤和病毒灭活新鲜冰冻血浆制备冷沉淀的可行性探讨[J].临床输血与检验,2015,17(2):149-150.
[9]Scott E,Puac K,Heraly J,et al.Evaluation and comparison of coagulation factor activity in fresh-frozen plasma and 24-hour plasma at thaw and after 120 hours of 1 to 6℃ storage[J].Transfusion,2009,49(8):1584-1591.
[10]张坤连,李晓丰,吕延中,等.滤白FFP与滤白CRP中部分凝血因子活性及蛋白含量的研究[J].中国输血杂志,2012,25(10):987-989.
[11]刘仁强,秦艳红.亚甲蓝光化学法对FFP中凝血因子及总蛋白含量的影响[J].中国输血杂志,2010,23(6):436-438.
[12]涂娟,何华庆,尤榕,等.病毒灭活新鲜冰冻血浆制备冷沉淀的制备研究[J].实验与检验医学,2015,33(5):574-575.
[13]林昂.去冷沉淀血浆部分凝血因子及蛋白含量研究[J].临床输血与检验,2011,13(2):149-150.
[14]黄翠霞,陈惠民.不同方法处理对冷沉淀纤维蛋白原(FIB)和Ⅷ因子测量值影响的比较[J].医学理论与实践,2016, 29(22):3123-3125.
[15]王惟.新鲜冰冻血浆与普通冰冻血浆制备冷沉淀的质量分析[J].中国当代医药,2012,19(8):80-82.
[16]孙振秀,李秋华,许雷,等.白细胞滤除前后血浆多种成分变化研究[J].中国输血杂志,2008,21(1):35-36.
[17]陈镇周,肖明星,陳湘屏,等.亚甲蓝光化学法病毒灭活对血浆质量的影响[J].中国输血杂志,2011,24(6):490-492.
[18]冯国基,刘鹏,杜学丽,等.滤除白细胞与MB-P法病毒灭活对血浆凝血因子的影响[J].临床输血与检验,2010, 12(1):39-41.
(收稿日期:2019-05-20 本文编辑:崔建中)
