热环境下黄羽肉鸡心脏MCEE基因表达分析
2019-10-25张权罗毅康张柏海
张权 罗毅康 张柏海

摘要:为研究热应激对黄羽肉鸡生长性能的影响,对新广黄公鸡和怀乡公鸡进行热应激处理,分析其对黄羽肉鸡体质量、心脏相对质量和心脏MCEE基因表达的影响。试验随机选取新广黄公鸡和怀乡公鸡各60羽,每个品种随机分6组,每组10羽。每个品种的前3组于22~28日龄时,每天进行热处理[(38±1 )℃,8 h/d,7 d,试验组];每个品种的后3组于22~28日龄时处于室温[(25±1 )℃,对照组]。分别测定新广黄公鸡和怀乡公鸡21、28日龄体质量。于28日龄时随机抽取每组公鸡各2羽,每个品种试验组和对照组各6羽,测定心脏绝对质量并采集心脏左心室组织用于提取总RNA。MCEE基因相对表达量采用2-ΔΔCT法,利用单因素方差分析其显著性;双因素方差分析黄羽肉鸡体质量和心脏相对质量显著性。结果表明,新广黄公鸡和怀乡公鸡21、28日龄体质量以及28日龄心脏绝对质量显著高于怀乡公鸡(P<0.05),心脏相对质量差异不显著(P>0.05)。热环境处理7 d后,28日龄新广黄公鸡体质量试验组显著低于对照组(P<0.05),而28日龄怀乡公鸡试验组与对照组差异不显著(P>0.05);心脏相对质量差异不显著(P>0.05)。新广黄公鸡心脏MCEE基因相对表达量显著高于怀乡公鸡(P<0.05)。热环境显著降低新广黄公鸡心脏MCEE基因相对表达量(P<0.05),而对怀乡公鸡心脏MCEE基因相对表达量影响不显著(P>0.05)。初步研究说明,热环境显著降低新广黄公鸡体质量及心脏MCEE基因表达水平,而对怀兴公鸡无显著影响(P>0.05)。MCEE基因表达与黄羽肉鸡生长速度相关,在黄羽肉鸡其他组织器官的表达有待进一步研究。
关键词:黄羽肉鸡;热应激;心脏相对质量;MCEE基因表达
中图分类号: S831.1 文献标志码: A 文章编号:1002-1302(2019)13-0049-03
全球气候变暖正在影响全球肉鸡业[1]。在过去的几十年中,通过遗传选择,肉鸡的生产性能,特别是在生长率方面得到了显著改善[2]。然而,与生长缓慢的肉鸡相比,高环境温度对生长迅速的肉鸡的不利影响更大[3-5],尤其是这些快大型肉鸡的体质量[6]。黄羽肉鸡是亚洲特别是我国很受欢迎的家禽品种,其生长速度慢于商品肉仔鸡,具有独特的肉味。以往对鸡的研究表明,快速生长的肉鸡会出现左心室损伤的症状[7],而左心室衰竭会导致抽血功能丧失[8]。鸟类有一个有效的心血管系统,提供营养和热量的代谢需求。然而,迄今为止,黄羽肉鸡对热应激反应的研究还很有限。
MCEE基因是丙酸代谢通路基因,编码丙二酰辅酶A表位异构酶,是丙酰辅酶A代谢为丁二酰辅酶A的重要的代谢途径,是研究人类丙酸血症的主要候选基因[9]。缺乏甲基丙二酰辅酶A导致机体组织和体液中积累甲基丙二酸,并表现出继发性代谢紊乱,如高血糖、高氨血症和间歇性低血糖[10]。丙酸代谢通路基因与模式动物代谢相关疾病的关系已被广泛研究[9,11-13],但在家禽中尚无报道。本研究从热应激反应角度出发,研究黄羽肉鸡体质量、心脏相对质量及心脏MCEE基因的表达,分析热应激对黄羽肉鸡的影响。
1 材料与方法
1.1 试验材料
新广黄公鸡和怀乡公鸡分别来自广东省佛山市新广畜牧发展有限公司和广东省信宜市盈富农业有限公司怀乡公鸡保种场,各60羽1日龄公雏。每个品种随机分6组,每组10羽,饲养管理条件一致,自由采食与饮水。每个品种的前3组于 22~28日龄时,每天进行热处理(38±1) ℃ 8 h后温度降至室溫(25±1) ℃的条件下饲养(试验组);每个品种后3组于 22~28日龄时处于室温(25±1) ℃的条件下饲养(对照组)。分别测定新广黄公鸡和怀乡公鸡21、28日龄体质量。于28日龄时随机抽取每组公鸡各2羽,每个品种试验组和对照组各共6羽,颈部放血处死,测定心脏绝对质量并采集心脏左心室组织于液氮保存,用于提取总RNA(核糖核酸)。
1.2 总RNA的提取与逆转录
鸡心脏组织总RNA提取参见Trizol试剂说明书的操作步骤进行,RNA浓度和纯度用Nanodrop紫外分光光度计检测,1.5%琼脂糖凝胶电泳检测RNA完整性,根据BeyoRTTM Ⅱ cDNA(互补脱氧核糖核酸)合成试剂盒说明书进行RNA逆转录,获得cDNA于-20 ℃用于荧光定量PCR检测。
1.3 引物的设计与合成
根据NCBI中鸡MCEE和GAPDH基因mRNA(信使RNA)序列(NM_001293217.1和NM_204305.1),采用引物在线设计软件Primer 3(http://primer3.ut.ee)设计引物,引物序列信息见表1。引物由金唯智(广州)生物科技公司合成。
1.4 荧光定量PCR
运用SYBR Green Ⅰ染料法,进行荧光定量PCR检测,以GAPDH为内参基因,检测MCEE基因表达量。荧光定量PCR反应体系:2×SYBR绿色荧光染料PCR混合液(2×SYBR Green Ⅰ PCR Mix)7.5 μL,10 μmol/L上下游引物各0.5 μL,1.0 μL 500 ng/μL cDNA,去RNA酶水(RNase-free Water)至15.0 μL。PCR反应条件为95 ℃预变性5 min;95 ℃变性10 s,60 ℃退火30 s,72 ℃延伸30 s进行40个循环。
1.5 统计分析
利用SPSS 19.0软件分析黄羽肉鸡体质量和心脏相对质量显著性。MCEE基因相对表达量采用2-ΔΔCT法计算,利用SPSS 19.0软件分析其显著性。数据采用平均值±标准差表示。
2 结果与分析
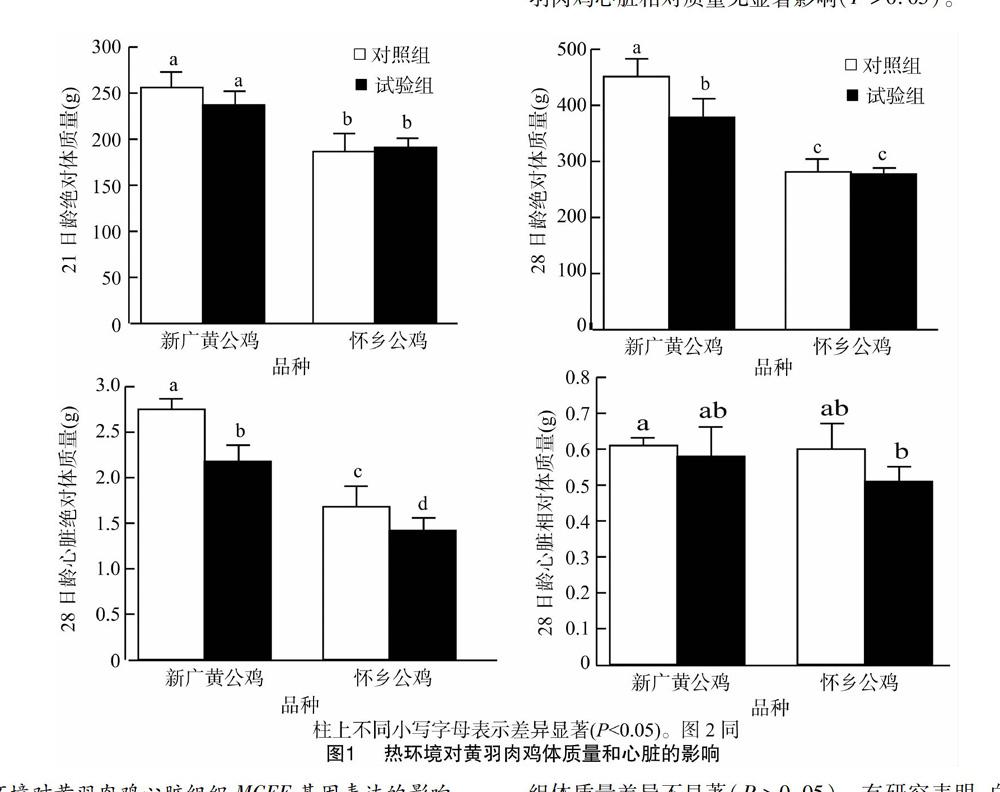
2.1 热环境对黄羽肉鸡体质量和心脏的影响
由图1可见,新广黄公鸡21、28日龄体质量以及28日龄心脏绝对质量显著高于怀乡公鸡(P<0.05),28日龄心脏相对质量差异不显著。热环境处理7 d后,28日龄新广黄公鸡绝对体质量试验组显著低于对照组(P<0.05),而28日龄怀乡公鸡试验组与对照组差异不显著(P<0.05)。试验组新广黄公鸡和怀乡公鸡心脏绝对质量均显著低于对照组(P<0.05),心脏相对质量差异不显著(P>0.05)。结果表明,高温环境显著影响快速型黄羽肉鸡(新广黄公鸡)的生长速度,对慢速型黄羽肉鸡(怀乡公鸡)影响不显著(P>0.05),对黄羽肉鸡心脏相对质量无显著影响(P>0.05)。
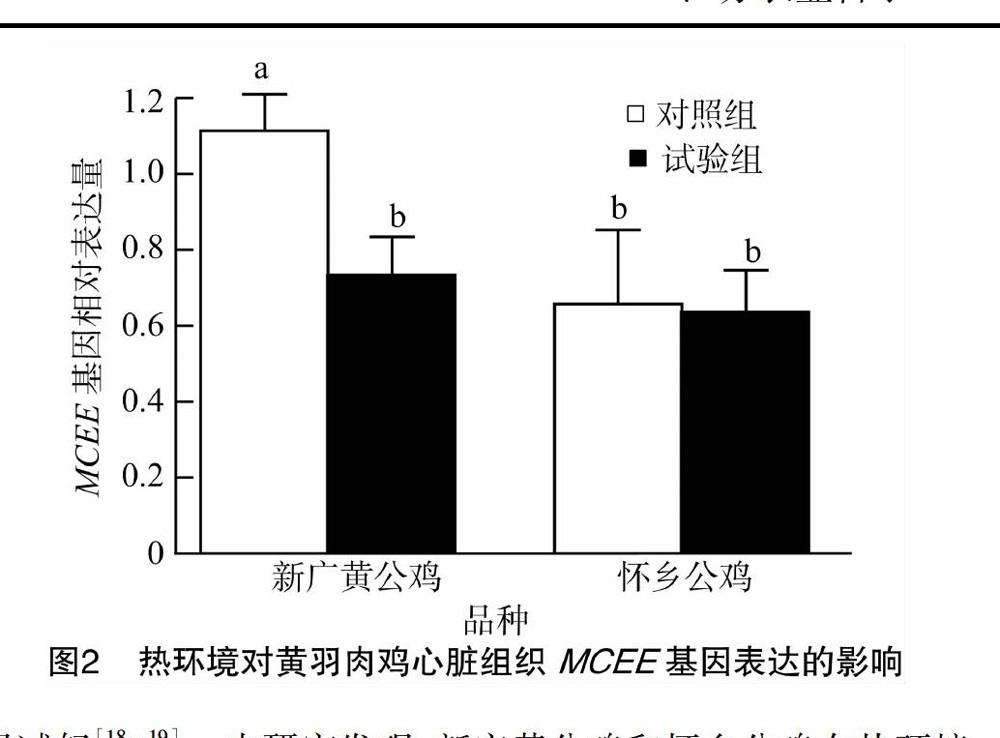
2.2 热环境对黄羽肉鸡心脏组织MCEE基因表达的影响
热环境对黄羽肉鸡心脏组织MCEE基因表达的影响结果见图2。新广黄公鸡对照组心脏MCEE基因相对表达量显著高于对照组怀乡公鸡(P<0.05)。热环境显著降低新广黄公鸡心脏MCEE基因相对表达量(P<0.05),而对怀乡公鸡心脏MCEE基因相对表达量影响不显著(P>0.05)。
3 讨论与结论
在热环境下,28日龄新广黄公鸡试验组体质量显著低于对照组体质量(P<0.05),而28日龄怀乡公鸡试验组与对照组体质量差异不显著(P>0.05)。有研究表明,白羽肉鸡在12.8%[14-15];耐热型高度近交品系[16]暴露在热环境(35 ℃、7 h/d、7 d)下时,体质量增加率为58.9%[17]。本研究中,新广黄公鸡在热环境条件下,7 d的體质量增加率约为59.7%,怀乡公鸡质量增加约为45.1%。表明黄羽肉鸡具有一定的耐热能力,且经过选育的新广黄公鸡在热环境下的增质量率较怀乡公鸡高。而热环境对怀乡公鸡的增质量率无显著影响,在黄羽肉鸡选育中,可以作为耐热型黄羽肉鸡品种。在热环境下,鸡生产性能的降低与机体组织器官的各种变化有关,这些器官变化包括肠道受损、相关免疫器官和心脏的相对质
量减轻[18-19]。本研究发现,新广黄公鸡和怀乡公鸡在热环境条件下,心脏相对质量与对照组之间差异不显著,表明在高温热环境(32 ℃,2~4周龄)条件下,28日龄体质量较室温下白羽肉鸡体质量降低约环境下,黄羽肉鸡的心脏生理发育正常[20]。
MCEE基因是丙酸代谢通路基因,编码丙二酰辅酶A表位异构酶,是丙酰辅酶A代谢为丁二酰辅酶A的重要的代谢途径。缺乏甲基丙二酰辅酶A突变酶或酶辅因子腺苷钴胺的患者,在其组织和体液中积累甲基丙二酸,并表现出继发性代谢紊乱,如高血糖、高氨血症和间歇性低血糖[10]。丙酸代谢通路基因与模式动物代谢相关疾病的关系已被广泛研究[9,11-13],但在家禽中尚无报道。本研究中,心脏MCEE基因表达与黄羽肉鸡生长速度呈正相关,且差异显著。快速型黄羽肉鸡心脏MCEE基因表达受热环境影响显著下降而导致生长速度减慢;慢速型黄羽肉鸡心脏MCEE基因表达受热环境影响及其生长速度差异不显著。
热环境显著降低新广黄公鸡体质量及心脏MCEE基因表达水平,而对怀兴公鸡无显著影响。初步表明MCEE基因表达水平与黄羽肉鸡生长速度相关,在黄羽肉鸡其他组织器官的表达有待进一步研究。
参考文献:
[1]Windhorst H W. Changes in poultry production and trade worldwide[J]. Worlds Poultry Science Journal,2006,62(4):585-602.
[2]Deeb N,Cahaner A. Genotype-by-environment interaction with broiler genotypes differing in growth rate. 3. Growth rate and water consumption of broiler progeny from weight-selected versus nonselected parents under normal and high ambient temperatures[J]. Poultry Science,2002,81(3):293-301.
[3]Cahaner A. Effects of temperature on growth and efficiency of male and female broilers from lines selected for high weight gain,favorable feed conversion,and higher low fat content[J]. Poultry Science,1992,71(8):1237-1250.
[4]Lu Q,Wen J,Zhang H. Effect of chronic heat exposure on fat deposition and meat quality in two genetic types of chicken[J]. Poultry Science,2007,86(6):1059-1064.
[5]Cheng C Y,Tu W L,Chen C J,et al. Functional genomics study of acute heat stress response in the small yellow follicles of layer-type chickens[J]. Scientific Reports,2018,8(1):1320.
[6]Sohail M U,Hume M E,Byrd J A,et al. Effect of supplementation of prebiotic mannan-oligosaccharides and probiotic mixture on growth performance of broilers subjected to chronic heat stress[J]. Poultry Science,2012,91(9):2235-2240.
[7]Olkowski A A. Pathophysiology of heart failure in broiler chickens:Structural,biochemical,and molecular characteristics[J]. Poultry Science,2007,86(5):999-1005.
[8]Baghbanzadeh A,Decuypere E. Ascites syndrome in broilers:physiological and nutritional perspectives[J]. Avian Pathology,2008,37(2):117-126.
[9]Chandler R J,Aswani V,Tsai M S,et al. Propionyl-CoA and adenosylcobalamin metabolism in Caenorhabditis elegans:evidence for a role of methylmalonyl-CoA epimerase in intermediary metabolism[J]. Molecular Genetics and Metabolism,2006,89(1/2):64-73.
[10]Chalmers R A,Lawson A M. Disorders of propionate and methylmalonate metabolism[M]//Organic acids in man. Dordrecht:Springer,1982:296-331.
[11]Carrozzo R,Dionisi-Vici C,Steuerwald U A,et al. SUCLA2 mutations are associated with mild methylmalonic aciduria,leigh-like encephalomyopathy,dystonia and deafness[J]. Brain,2007,130(3):862-874.
[12]Sakamoto O,Ohura T,Murayama K,et al. Neonatal lactic acidosis with methylmalonic aciduria due to novel mutations in the SUCLG1 gene[J]. Pediatrics International,2011,53(6):921-925.
[13]杨 帆,王瓊萍,何 侃,等. 丙酸通路基因多态性与猪肉质及胴体性状的关联分析[J]. 遗传,2012,34(7):81-87.
[14]Geraert P A,Padilha J C F,Guillaumin S. Metabolic and endocrine changes induced by chronic heatexposure in broiler chickens:growth performance,body composition and energy retention[J]. British Journal of Nutrition,1996,75(2):195-204.
[15]Yalcin S,zkan S,Türkmut L,et al. Responses to heat stress in commercial and local broiler stocks. 1. Performance traits[J]. British Poultry Science,2001,42(2):149-152.
[16]Deeb N. Genetic architecture of growth and body composition in unique chicken populations[J]. Journal of Heredity,2002,93(2):107-118.
[17]Van Goor A,Bolek K J,Ashwell C M,et al. Identification of quantitative trait loci for body temperature,body weight,breast yield,and digestibility in an advanced intercross line of chickens under heat stress[J]. Genetics Selection Evolution,2015,47(1):96.
[18]Quinteiro-Filho W M,Ribeiro A,Ferraz-de-Paula V,et al. Heat stress impairs performance parameters,induces intestinal injury,and decreases macrophage activity in broiler chickens[J]. Poultry Science,2010,89(9):1905-1914.
[19]Zhang J,Schmidt C J,Lamont S J. Transcriptome analysis reveals potential mechanisms underlying differential heart development in fast-and slow-growing broilers under heat stress[J]. BMC Genomics,2017,18(1):295.
[20]van de Ven L J F,van Wagenberg A V,Decuypere E,et al. Perinatal broiler physiology between hatching and chick collection in 2 hatching systems[J]. Poultry Science,2013,92(4):1050-1061.
