GeneXpert MTB/RIF技术诊断肺结核及 利福平耐药性的价值
2019-10-18吴海燕叶志坚王霞芳虞忻吴妹英
吴海燕 叶志坚 王霞芳 虞忻 吴妹英
肺结核是由结核分枝杆菌(MTB)引起的肺部慢性传染性疾病,是危害人类生命健康的主要疾病之一,已成为全世界公共卫生面临的重大威胁。我国是全球结核病高发国家之一,据2018年WHO[1]报告的最新数据显示,2017年估算我国新发肺结核患者89.5万例,位居全球第二位;耐药结核病的发病率为7.1%,疫情依然严峻。减少肺结核及耐药结核病的传播,提高肺结核及耐药结核病的诊断率,对结核病的防控有着十分重要的意义。由于肺结核临床症状隐匿,早期发现及诊断活动性肺结核及耐药肺结核已成为临床工作者需要迫切解决的问题。
传统病原学检测方法有两种,一是染色涂片法,是临床上最便捷快速的诊断方法[2],但因受制于痰液中分枝杆菌数量,此方法仅能检出少部分活动性结核病患者,漏检率很高,且无法区别MTB和非结核分支杆菌(NTM)。二是MTB培养、MTB药物敏感性试验(简称“药敏试验”),不仅能取得病原学结果,还能进行耐药性检测,但实验室方法繁琐,耗时长,无法满足快速诊断及开展有效抗结核治疗的临床需求。GeneXpert MTB/RIF(简称“GeneXpert法”)是目前国际上比较流行的检测方法,主要用于检测临床标本结核分枝杆菌复合菌群DNA和利福平耐药相关的ropB基因突变,一般2 h内即可出结果。因其速度快,方法简单,操作便捷,具有较高敏感度、特异度,得到广泛关注与认可[3-4]。
本研究对苏州大学附属传染病医院(苏州市第五人民医院)收治的981例疑似肺结核患者进行痰及BALF两种标本的检测,包括涂片抗酸染色镜检(简称“涂片法”)、GeneXpert法、BACTEC MGIT 960(简称“MGIT 960法”)及固体药敏比例法药敏试验(简称“药敏试验”)的检测结果,同时比较3种方法对痰标本和BALF标本的检出阳性率,探讨 GeneXpert法检测在诊断肺结核及其耐药性方面的临床价值。
资料和方法
一、研究对象
搜集苏州大学附属传染病医院(苏州市第五人民医院)结核病科2017年8月至2018年11月因疑似肺结核收治住院的981例患者为研究对象,经临床诊断最终确诊结核病患者862例,男581例,女281例,年龄11~85岁,中位年龄54岁;非结核病患者119例,男77例,女42例,年龄18~74岁,中位年龄55岁;包括肺部感染84例,肺部肿瘤11例,慢性阻塞性肺病24例。
二、 纳入和排除标准
纳入标准:(1)纳入患者均为初次来我院就诊者。胸部CT检查符合肺结核影像学表现,可有或无咳嗽、咯血等呼吸道症状。(2)所有患者具有完整临床资料及影像学资料。(3)抗结核药物治疗前均取3个合格的痰标本。(4)所有患者均行电子气管镜检查,获得3个合格的肺泡灌洗液标本。(5)所有患者完成2个月随访。肺结核诊断标准:根据患者是否有密切的肺结核患者接触史,结合临床表现及相应的必要实验室检查,最终诊断依据病原学检查结果(细菌学阳性),如无细菌学依据,则按2017年中华人民共和国国家卫生和计划生育委员会颁布的《WS 288—2017结核病诊断》中临床诊断的新标准[5]。
排除标准:(1)HIV感染者。(2)既往曾行抗结核药物治疗的患者。
三、检测方法
1.标本的采集:(1)每例入选患者均收集即时痰、夜间痰及晨痰标本3份(每份样品量在3~5 ml)。分别进行痰涂片、MGIT 960和GeneXpert检测,若MGIT 960培养阳性,则进行固体比例法药敏试验。(2)肺泡灌洗液(BALF)标本留取:每例入选的患者均行电子支气管镜检查(电子支气管镜型号Olympus BF-290),用20 ml注射器于活检孔快速注入36 ℃灭菌生理盐水100 ml,立即用负压吸引回收共计60 ml左右BALF,其中有40 ml分成3份,分别行痰涂片、MGIT 960培养和GeneXpert检测,若MGIT 960培养阳性,则进行固体比例法药敏试验。
2.涂片抗酸染色:痰涂片按照文献[6]中相关要求进行涂片、染色、镜检并报告结果。即取标本进行涂片后,在火焰上加热固定,加石炭酸复红溶液,再次加热至蒸汽出现,约5 min后用水洗,加入脱色剂,轻摇玻片至无红色脱落,再次水洗,加入复染液,再次染色约1 min;晾干玻片,最后放置在显微镜油镜下进行观察。结果判断:①阴性为连续观察300个不同视野,未发现抗酸杆菌;②阳性为找抗酸杆菌菌数1~8条/300个视野;③阳性(+):3~9条/100视野,连续观察300个视野;④阳性(++):1~9条/10个视野,连续观察100个视野;⑤阳性(+++):1~9条/1个视野;⑥阳性(++++):≥10条/1个视野。
3. MGIT 960培养:按照《分枝杆菌分离培养标准化操作程序及质量保证手册》[7]中的相关要求进行。具体步骤一:制备培养基。从冰箱中取出培养基,将温度恢复到室温,并在培养管上编制序列号,并写上患者姓名、培养日期、痰涂片编号。步骤二:标本前去污染处理。取2 ml痰标本,并在预处理管中加4%NaOH,加入量是痰标本的1~2倍,于振荡器上振荡30~60 s,并室温放置10~15 min(不得超过20 min)。步骤三:接种。取0.1 ml前处理液,通过无菌操作接种在培养基的斜面上,每份标本均需同时接种在2支酸性改良罗氏培养基上,并在37 ℃温箱中培养。步骤四:孵育。接种后3、7 d每周观察1次直至8周并记录菌落生长情况,对于生长的菌落需经抗酸染色确认是否为分枝杆菌。结果判读:阴性为斜面无分枝杆菌菌落生长;阳性(+):菌落占斜面面积1/4;分枝杆菌培养阳性(++):菌落占斜面面积1/2;阳性(+++):菌落占斜面面积3/4;阳性(++++):菌落占满整个斜面。
4.固体比例法药敏试验(简称“比例法药敏试验”):按照《结核分枝杆菌药物敏感性试验标准化操作程序及质量保证手册》[8]中的相关要求,使用接种环刮取生长旺盛的菌落置于加有少许缓冲液的磨菌管底部,充分研磨成乳酪样均匀菌液,用比浊管比浊配成1 mg/ml菌液,稀释配比,最终制成10-2mg/ml和10-4mg/ml细菌液。使用标准接种环(22 SWG)蘸取1环(即0.01 ml)细菌液,通过划线法(分别对照及接种)均匀接种至培养基表面,应尽可能的使菌液均匀分散于培养基的斜面。将其置于37 ℃温箱中培养,4周报告结果。
5.GeneXpert 法:实验操作严格按照GeneXpert MTB/RIF试剂盒说明书进行,将样本加入1~2倍体积的4%NaOH溶液混合,振荡15~30 s,充分液化后,室温静置15 min,用专用无菌吸管吸取2 ml处理好的标本转移到样本反应盒中,然后将反应盒放置到GeneXpert MTB/RIF系统仪器中,仪器开始自动化检测,约2 h反应结束后,系统依照探针的循环阈值(Ct)自动判断检测样本中是否存在MTB,若存在MTB,则判断是否有利福平耐药。
四、仪器及主要试剂
金胺O染色液购于杭州创新生物检控技术有限公司。MTB染色液、酸性和中性罗氏培养基、药敏试验培养基及对硝基苯甲酸(PNB)培养基,均购于美国BD公司。GeneXpert MTB/RIF检测系统及配套试剂购于美国Cepheid公司。
五、统计学处理
采用Excel表格录入数据,应用SPSS 25.0统计软件进行数据统计分析。计数资料以“率(%)”表示,两组间比较采用χ2检验,以P<0.05为差异有统计学意义;以临床诊断为标准,计算各方法的检测效能指标。
结 果
一、三种检测方法对初诊疑似肺结核患者痰标本的检测效能
以临床诊断为标准,涂片、MGIT 960培养、GeneXpert 法检测肺结核患者痰标本的敏感度和特异度分别为32.02%(276/862)、100.00%(119/119);53.25%(459/862)、100.00%(119/119);53.02%(457/862)、96.64%(115/119)。见表1。
二、三种检测方法对初诊疑似肺结核患者BALF标本的检测效能
以临床诊断为标准,涂片镜检、BACTEC MGIT 960培养、GeneXpert MTB/RIF检测肺结核患者BALF标本的敏感度和特异度分别为31.32%(270/862)、100.00%(119/119);69.37%(598/862)、100.00%(119/119);72.97%(629/862)、96.64%(115/119)。见表2。
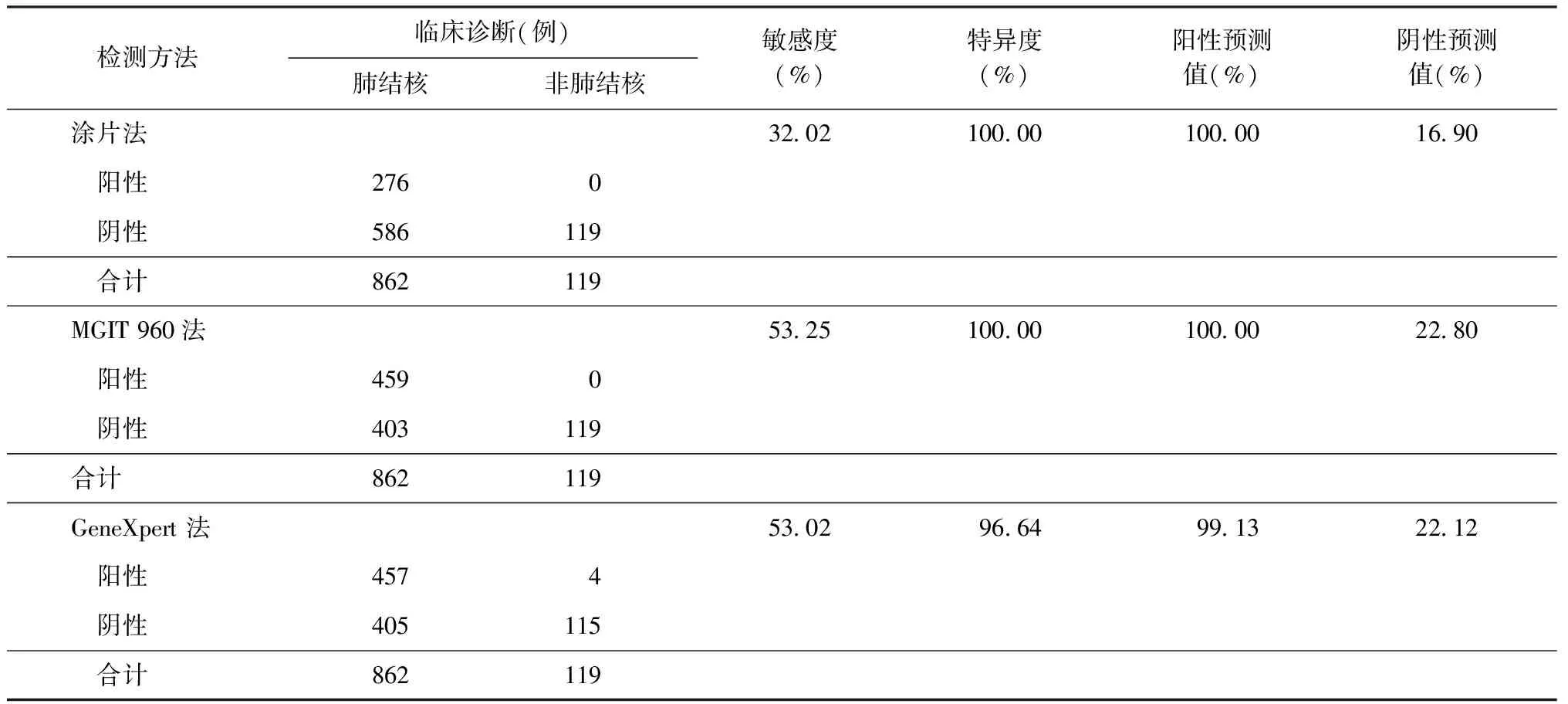
表1 以临床诊断为参考标准,3种方法对肺结核患者痰标本的检测效能
注敏感度=真阳性例数/(真阳性例数+假阴性例数)×100%;特异度=真阴性例数/(真阴性例数+假阳性例数)×100%;阳性预测值=真阳性例数/(真阳性例数+假阳性例数)×100%;阴性预测值=真阴性例数/(真阴性例数+假阴性例数)×100%
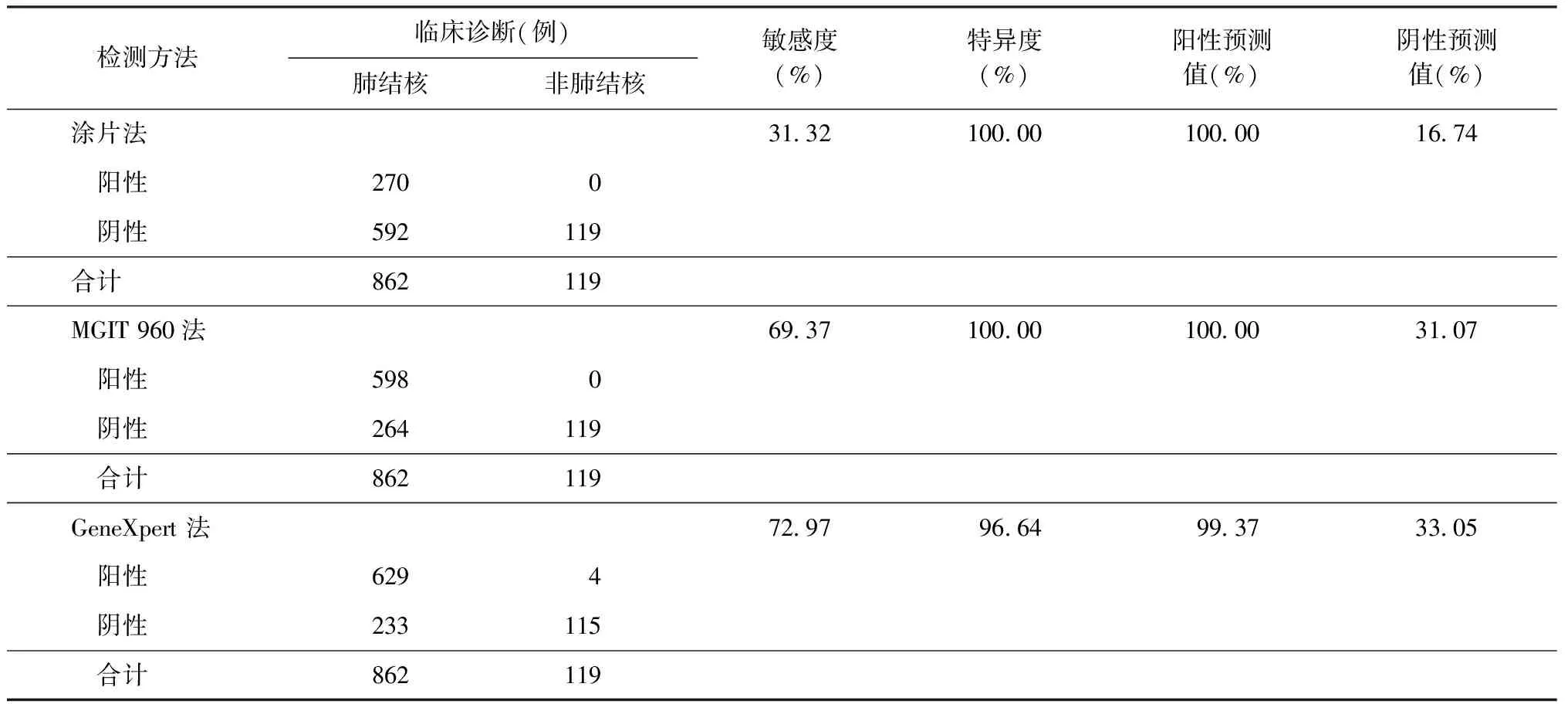
表2 以临床诊断为参考标准3种方法对肺结核患者BALF标本的检测效能
注敏感度=真阳性例数/(真阳性例数+假阴性例数)×100%;特异度=真阴性例数/(真阴性例数+假阳性例数)×100%;阳性预测值=真阳性例数/(真阳性例数+假阳性例数)×100%;阴性预测值=真阴性例数/(真阴性例数+假阴性例数)×100%
三、关于 GeneXpert法检测利福平耐药性的结果分析
在MGIT 960培养和GeneXpert 法检测均阳性的527例肺结核患者中,比例法药敏试验检测出对利福平耐药者28例,而GeneXpert 法检测结果对利福平耐药者26例,其余2例提示敏感。比例法药敏试验检测结果对利福平敏感者共有499例,GeneXpert法检测结果为敏感者497例,其余2例提示耐药。追踪2例传统药敏试验敏感但GeneXpert法检测对利福平耐药的患者,对发现上述不一致菌株的ropB基因核心区域进行测序,1例测序结果为耐药,1例测序结果为敏感(GeneXpert 法检测结果均为极低)。对GeneXpert和MGIT 960法进行Kappa检验,Kappa=0.612,P<0.001,两种检测方法具有较好一致性。以固体比例法药敏试验为金标准,GeneXpert 法对利福平耐药检测的敏感度为92.86%(26/28),特异度为99.60%(497/499)。
讨 论
我国近年来结核病发病率控制缓慢,据2010年全国结核病流行病学调查[9]及2018年WHO报告数据显示,我国结核病,包括耐药结核病疫情依然相当严峻。早期快速及精确的诊断肺结核及发现耐药结核病患者,是控制及减少结核病及耐药结核病传播的关键,对于结核病的防治有着十分重要的意义。肺结核诊断较为困难,既往传统标本找抗酸杆菌涂片、结核分枝杆菌培养为诊断肺结核常用的实验室指标,痰涂片虽然便捷迅速,但敏感度低,漏检率高,传统的罗氏培养技术是检测MTB的“金标准”,虽然敏感度相对于痰涂片有所提高,但实验室方法繁琐,对实验室的生物安全设施及操作人员的技术水平要求高,且耗时长,需1~2个月出结果,无法满足快速诊断的临床需求。
随着结核病分子诊断技术的提高,自2010年12月WHO批准了GeneXpert技术可应用于肺结核的诊断,整个流程仅需2.5 h。2017年卫生部颁布的《WS 288—2017结核病诊断》已将分子诊断技术GeneXpert列为诊断肺结核的金标准。赵冰等[10]、Bajrami等[11]均有文献提出GeneXpert MTB/RIF可快速诊断肺结核,特异度强,敏感度高,同时还可检测是否有利福平耐药,优于传统细菌学方法。在标本选择上,取痰液标本为最简便、快捷的方法,但常常受到气道、口腔等污染,阳性率低,且部分患者痰量少无法行此检查。而支气管镜灌洗标本是直接经支气管内灌洗后取出,能显著减少标本污染,进而可提高检测和诊断的准确性[12]。
笔者通过研究981例疑似肺结核患者痰标本,对3种检测方法的检测效能进行评价,发现痰标本GeneXpert检测的敏感度明显高于涂片,与MGIT 960法检测结果相当,这与王蔚等[13]学者的研究结果相同。表明GeneXpert临床应用价值优于其他2种检查方法,可提高肺结核诊断的阳性率。另外,本次研究中还对比痰及BALF两种标本进行3种不同检测方法的敏感度,发现除了涂片找抗酸杆菌,BALF标本其他2种实验室结果的敏感度均明显高于痰标本。这与刘旭辉等[14]研究结果相近,进而证实了BALF标本临床应用价值高于传统痰标本,可在痰标本基础之上再次提高肺结核病原学检查阳性率。对于BALF标本中找抗酸杆菌涂片结果低于痰标本,分析原因与行气管镜检查前已有部分痰标本病原学检查阳性的患者接受抗结核药物治疗,导致结核分枝杆菌菌量减少有关。
以固体比例法药敏试验结果为金标准,GeneXpert法检测利福平耐药性的敏感度为92.86%,特异度为99.60%。这与韩丹等[15]和Weyer等[16]研究的结果接近。经上述研究发现,GeneXpert 法检测是否耐利福平的敏感度及特异度均较高。且其检测结果与固体比例法药敏试验具有较好一致性,故真实可靠,可高效地提高早期耐利福平肺结核的发现率,为耐药肺结核早期诊断及个体化治疗提供用药指导。追踪2例固体比例法药敏试验敏感但GeneXpert 法检测对利福平耐药的患者,对发现不一致菌株进行ropB基因核心区域测序,结果1例测序报告为耐药,1例测序报告为敏感(GeneXpert法检测结果均为极低),故对待GeneXpert 法检测结果弱阳性,提示利福平耐药的患者需谨慎对待,需结合固体比例法药敏试验检测结果进一步明确[17]。因本研究人群中未统计复治肺结核和未行电子气管镜检查的初发初治的肺结核患者,故对利福平耐药的检出率较低,不能代表全国耐药结核病的发病水平。
综上所述,GeneXpert法具有早期、快速、准确的诊断肺结核等优点,临床应用价值优于涂片及MGIT 960培养及固体比例法药敏试验,在早期诊断肺结核及耐利福平肺结核方面有着较好的应用前景。同时还证明了气管镜灌洗液标本临床应用价值高于传统痰标本,可在痰标本基础上再次提高肺结核病原学检查的阳性率。故在疾病早期,特别是痰标本病原学检查均为阴性的患者,因尽早行电子支气管镜检查,可明显提高肺结核,特别是菌阴肺结核的病原学检出率。
