替诺福韦酯与恩替卡韦治疗慢性乙型肝炎肾安全性Meta分析
2019-10-17高卫真
苏 培 ,高卫真
(1.天津医科大学基础医学院药理学系,天津300070;2.天津市第三中心医院分院,天津300250)
世界上大约三分之一的人群都在某种程度上感染了乙型肝炎病毒(HBV),3.5到4亿人口是慢性HBV表面抗原携带者。在上述患者中,恩替卡韦(entecavir,ETV)和替诺福韦酯(tenofovir disoproxil,TDF)因为其效价和最小的耐受性成为首选[1]。
替诺福韦酯和恩替卡韦是口服抗病毒药物,由于二者均通过肾脏排泄的,所以肾毒性是潜在的不良反应之一。ETV和TDF产生肾毒性机制不同,包括肾小管损伤、凋亡和线粒体毒性等[2]。以前的研究还报告慢性乙型肝炎(Chronic Patitis B,CHB)和慢性肾脏疾病(CKD)之间的关联[3]。尤其是肾小球疾病,例如膜性肾病和肾小球系膜细胞增殖性肾小球肾炎可能是CHB患者肾功能不全的根本原因[4]。此外,除了核苷(酸)类药物用药史以外,糖尿病或高血压的疾病状态,开始应用核苷(酸)类药物前的基线(BL)及肾功能均可能影响因ETV或TDF引起的潜在肾毒性。因此,在选择合适的治疗CHB的核苷(酸)类药物时,肾安全性是一个需要重点考虑的因素,因为上述药物以原型通过肾脏消除,对于已经存在肾损伤或处于肾损伤风险之中的患者尤为重要。本文Meta分析研究目的是在HBV慢性感染患者中,评估使用ETV和TDF时相关的潜在肾毒性,并提供上述两种药物用于CHB治疗的临床观点。
1 资料与方法
1.1 文献纳入与排除标准 纳入标准:(1)临床前瞻性、回顾性队列研究,观察性研究,横断面研究。(2)TDF和ETV单药治疗,TDF剂量为300 mg/d,ETV剂量为0.5 mg/d或1 mg/d。(3)试验前TDF组和ETV组患者的基线情况进行了统计学检验,证实无明显差异,以确定组间均衡性和可比性。排除标准:(1)排除其他肝炎病毒感染(A、C、D 或 E)或人体免疫缺陷病毒(HIV)感染;(2)研究对象曾使用其他核苷类抗病毒药物治疗或同时使用免疫调节剂治疗;(3)排除不能获得患者肾小球滤过率(estimating glomerular filtration rate,eGFR)、血肌酐、血磷的基线数值的文献。
1.2 检索策略 以“hepatitis B”、“entecavir”and“tenofovir”检索 PubMed、Embase、Springer、Cochrane library,用替诺福韦酯、恩替卡韦和慢性乙型肝炎检索CNKI和万方数据库,所有检索均截止于2018年6月。
1.3 文献筛选及资料提取 由2位研究者独立进行文献筛选资料提取,交叉核对纳入试验的结果,对有分歧而难以确定的试验进行讨论或由第3位研究者决定其是否纳入。资料信息包括(1)文题、作者、发表日期、文献出处和参加中心数;(2)研究对象的一般情况,各组患者的基线可比性和干预措施;(3)结果测量指标。
1.4 质量评价 非随机对照研究参照Newcastle-Ottawa Scale(NOS)进行方法学质量评价。结果10分为满分,5分以上的研究可纳入Meta分析。
1.5 统计学方法 采用Stata12.0对提取的数据进行统计分析。计算合并后的标准化均数差(SMD),95%可信区间(CI)。文献间异质性检验采用I2检验方法,当P>0.1(I2≤50%)时,表明纳入研究间无异质性,采用固定效应模型做 Meta分析;当P<0.1(I2>50%)时,表明纳入研究间有异质性,采用随机效应模型做Meta分析。考虑到协变量的影响,对入选研究以基线值为协变量,采用改良Strownman法进行Meta回归分析,分析结果用森林图表示。
2 结果
2.1 根据纳入和剔除标准共筛选出9篇文献,搜索流程图见图1。包括2 346例患者,TDF治疗组1 160例,男性占68%,合并肝硬化占39%,合并高血压占6%,合并糖尿病占5%;ETV治疗组1 186例,男性占71%,合并肝硬化占47%,合并高血压占14%,合并糖尿病占 9%。表 1可见:(1)TDF无论用于eGFR>90 mL/min/1.73m2还是慢性肾脏病二期的患者,均使患者的eGFR比基线降低,而ETV用于慢性肾脏病二期的患者时,eGFR则比基线升高。(2)在经过MDRD、CKD-EPI或Cockcroft-Gault公式修正患者的eGFR基线后,TDF用药时,eGFR均比基线有不同程度的下降。而ETV用药后,eGFR与基线相比,既有上升也有下降。(3)对于失代偿期肝硬化患者,无论使用TDF还是ETV,eGFR与基线相比,均比没有肝硬化或代偿期肝硬化患者下降的幅度大。

图1 文献筛选流程图Fig 1 Details of article retrieval

表1 TDF和ETV治疗慢性乙型肝炎eGFR变化及文献Tab 1 Change in eGFR of patients with CHB underwent TDF or ETV therapy and related research papers

续表1 TDF和ETV治疗慢性乙型肝炎eGFR变化及文献Tab 1 Change in eGFR of patients with CHB underwent TDF or ETV therapy and related research papers
2.2 TDF和ETV在治疗CHB患者12月时eGFR比较,I2=77.0%,P=0.013(异质性检验z=0.54,P=0.590),采用随机效应模型,eGRFs合并后的SMD为 0.09(95% CI:-0.25~0.44)。以基线值为协变量,采用改良Strownman法进行Meta回归分析,结果显示,组间效应对eGFR影响无统计学意义(t=-0.60,P=0.593)。治疗24月时eGFR比较,I2=58.0%,P=0.068(异质性检验 z=0.62,P=0.536);SMD 为-0.07(95% CI:-0.31~0.16)。对 eGFR 影响无统计学意义(t=2.48,P=0.056),见图 2。

图2 TDF和ETV治疗12、24个月时eGFR指标Meta分析森林图Fig 2 Forest plot for the eGFR level after treatment with TDF and ETV at 12 months and 24 months
2.3 TDF和ETV在治疗CHB患者12月时血肌酐比较,I2=77.7%,P=0.011(异质性检验 z=0.92,P=0.359),采用随机效应模型,血肌酐合并后的SMD为-0.16(95% CI:-0.51~0.19)。以基线值为协变量,采用改良Strownman法进行Meta回归分析,结果显示,组间效应对血肌酐影响无统计学意义(t=-1.27,P=0.295)。治疗 24月时血肌酐比较,I2=79.6%,P=0.002(异质性检验 z=0.92,P=0.355);SMD为-0.15(95% CI:-0.46~0.17)。对血肌酐影响无统计学意义(t=-1.98,P=0.105),见图 3。
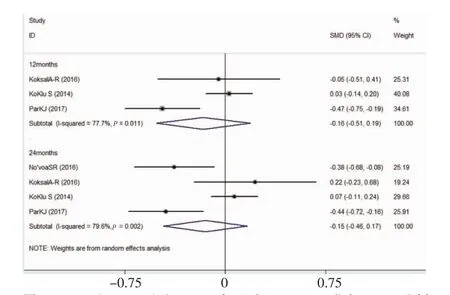
图3 TDF和ETV治疗12、24个月时Creatinine指标Meta分析森林图Fig 3 Forest plot for the Creatinine level after treatment with TDF and ETV at 12 months and 24 months
2.4 TDF和ETV在治疗CHB患者12月时血磷比较,I2=74.2%,P=0.027(z=2.64,P=0.008),采用随机效应模型,phasphate合并后的SMD为-0.43(95% CI:-0.74~-0.11)。以基线值为协变量,采用改良Trowman法进行Meta回归分析,结果显示,组间效应对phasphate影响无统计学意义(t=1.04,P=0.375)。治疗24月时血磷比较,I2=67.8%,P=0.045(z=2.46,P=0.014);SMD 为-0.37 (95% CI:-0.66~-0.08)。phasphate影响无统计学意义(t=1.41,P=0.252),见图4。

图4 TDF和ETV治疗12、24个月时Phasphate指标Meta分析森林图Fig 4 Forest plot for the Phasphate level after treatment with TDF and ETV at 12 months and 24 months
2.5 运用Egger’s检测其发表偏倚,24月时,eGFR、Creatinine、Phasphate 分别是 (t=-1.38,P=0.301)、(t=-1.36,P=0.306)、(t=-0.02,P=0.984),结果显示无发表偏倚。
3 讨论
TDF和ETV由亚太肝病协会(APASL)及美国肝病研究协会(AASLD)推荐为治疗慢性乙型肝炎的一线治疗用药[14-15]。
TDF是最强效的核苷酸类药物之一,其潜在的肾毒性仍然存在疑问。实际上,大部分肾不良事件是从暴露于TDF的HIV患者中报告的。但是,在CHB患者中,结果存在冲突。在一项737例TDF治疗的CHB患者参加的研究中,6%的患者因为eGFR恶化需要降低TDF剂量[16]。另一方面,542例CHB患者长期随访(144周)中,在少于1%的患者中检测到血肌酐恶化[17]。另一项研究也报告了非常低的肾毒性百分率。使用TDF比较ETV的一项研究表明肾功能标记物中的改变没有差异。
抗病毒药物尤其是核苷酸类似物的肾毒性是肾病的重要风险因素之一,其它风险因素还包括糖尿病,HIV合并感染,失代偿期肝硬化,控制不良的高血压,蛋白尿,活动性肾小球肾炎,同步使用肾毒性药物和实体器官移植。在搜集文献分析的因素中,使用抗病毒药物不是肾功能不全的独立风险因素。在排除了存在任意风险因素的患者时,TDF在eGFR方面的劣势与ETV相似。与接受ETV治疗的患者相比,接受TDF治疗的患者,血肌酐水平和血磷酸盐水平没有显著改变。
在本文的Meta分析中,TDF和ETV在CHB患者治疗时,均影响肾功能,但对eGFR、血肌酐、血磷酸盐的影响均无显著性差异。TDF和ETV治疗CHB患者的肾安全有相似性。但TDF无论用于eGFR>90 mL/min/1.73 m2还是慢性肾脏病二期的患者,均使患者的eGFR比基线降低,而ETV用于慢性肾脏病二期的患者时,eGFR则比基线升高。
总之,TDF和ETV治疗CHB患者时,对肾功能均有不同程度的影响,尽管临床影响较小,但在治疗CHB患者时,仍需要连续监测肾功能,包括eGFR、血肌酐和血磷酸盐[18]。对于已经存在肾脏疾患及其高危风险的CHB患者,应尽量避免应用TDF。
