制冷剂副产盐酸脱氟实验研究
2019-10-16王瑞英
王瑞英,魏 刚
(山东华安新材料有限公司,山东 淄博 255300)
制冷剂生产过程产生的副产物盐酸中含有杂质氟,含氟盐酸中氟以稀的氢氟酸形式存在,并与盐酸形成共沸物,采用蒸馏、吸附、萃取等方法很难将其有效分离开来。这种副产盐酸在出售给用户后,有可能因为用户使用方法不正确造成设备腐蚀、泄漏等安全隐患及事故;也有可能因用户利用后排放不达标含氟废水,引起周边环境氟污染[1]。因此,寻找一种既经济又有效地方法对含氟盐酸进行脱氟处理,对制冷剂副产盐酸的销售十分重要。
1 脱氟方法
目前,国内外的脱氟方法主要有沉淀法、离子交换法[1]、吸附法[2-3]、膜分离法[4]等,但是在制冷剂的生产过程中副产盐酸的氟含量往往非常高,可达100~10000mg/L,采用离子交换法、吸附法以及膜分离法在盐酸中脱去这样高浓度的氟是不现实的,只有沉淀法才有可能实现这一目标[1]。
沉淀法是选择不同的物质,与氟形成沉淀物。再比较这些沉淀物在强酸中溶解度的大小、分离难易程度等。从而找到符合工艺要求的脱氟物质,以除去盐酸中绝大部分氟化物,最终将盐酸中氟离子的质量分数控制在最小的范围内,从而达到脱氟的目的。沉淀法包括化学沉淀法和絮凝沉降法两种[5],对于高浓度含氟盐酸,一般采用钙盐沉淀法,使氟离子与钙离子生成CaF2沉淀而除去,该工艺具有方法简单、处理方便、费用低等优点,但存在处理后氟离子残留量大、泥渣沉降缓慢且脱水困难等缺点;絮凝沉淀法也存在着明显的缺点,即使用范围小,若含氟量大,絮凝剂使用量多,处理费用较大,产生污泥量多[6]。
综上所述,本文对含氟量高的盐酸先用无水氯化钙进行化学沉淀使大部分的氟离子形成CaF2沉淀,然后用絮凝剂对CaF2沉淀进行加速沉降,以此达到经济、有效脱氟的目的。
2 脱氟实验与结果分析
2.1 无水氯化钙脱氟
2.1.1 无水氯化钙用量的影响
现以氟离子浓度为1000mg/L的含氟盐酸为试验用酸,通过改变无水氯化钙的添加量观察除氟效果的变化。实验结果见表1。

表1 无水氯化钙添加量对除氟效果的影响
从表1可以看出,脱氟效果随着无水氯化钙添加量增加而提高。因此,适当过量对除氟有利,无水氯化钙用量选择为理论值过量5%左右为宜。
3.1.2 反应温度和反应时间的影响
盐酸的初始氟离子浓度为1000mg/L,搅拌转速为120r/min。研究不同温度、不同时间条件下氯化钙脱氟效果的影响,实验结果如表2所示。

表2 不同反应温度、反应时间对无水氯化钙脱氟效果的影响(以氟离子浓度记) mg/L
从表2中可以看出,随着温度的逐步升高,盐酸中氟离子浓度也逐渐升高,说明温度升高会提高盐酸的氟离子浓度,这可能是在升温的过程中,含氟有机物发生分解造成的。随着无水氯化钙脱氟时间的增加,盐酸中氟离子浓度没有出现明显的降低,说明反应时间对无水氯化钙脱氟效果影响不大。
因此,无水氯化钙脱氟的适宜温度为常温20℃即可,反应时间为30~60min。
2.2 絮凝剂脱氟
絮凝剂脱氟是往无水氯化钙脱氟后的溶液中按一定比例加入絮凝剂Ⅰ和絮凝剂Ⅱ的再脱氟过程。絮凝剂脱氟可以使已生成的CaF2沉淀加快絮凝生成沉淀,同时对盐酸中的氟离子有一定的卷扫吸附作用。
2.2.1 絮凝剂脱氟实验
按三因素(反应温度、絮凝剂Ⅰ用量、絮凝剂Ⅱ用量)四水平进行正交实验,因素水平表见表3。每次实验的条件为:搅拌转速120r/min,无水氯化钙脱氟后的盐酸溶液0.5L,反应时间1h。絮凝剂脱氟实验效果如表4所示。

表3 絮凝剂脱氟正交实验因素水平表

表4 絮凝剂脱氟实验效果
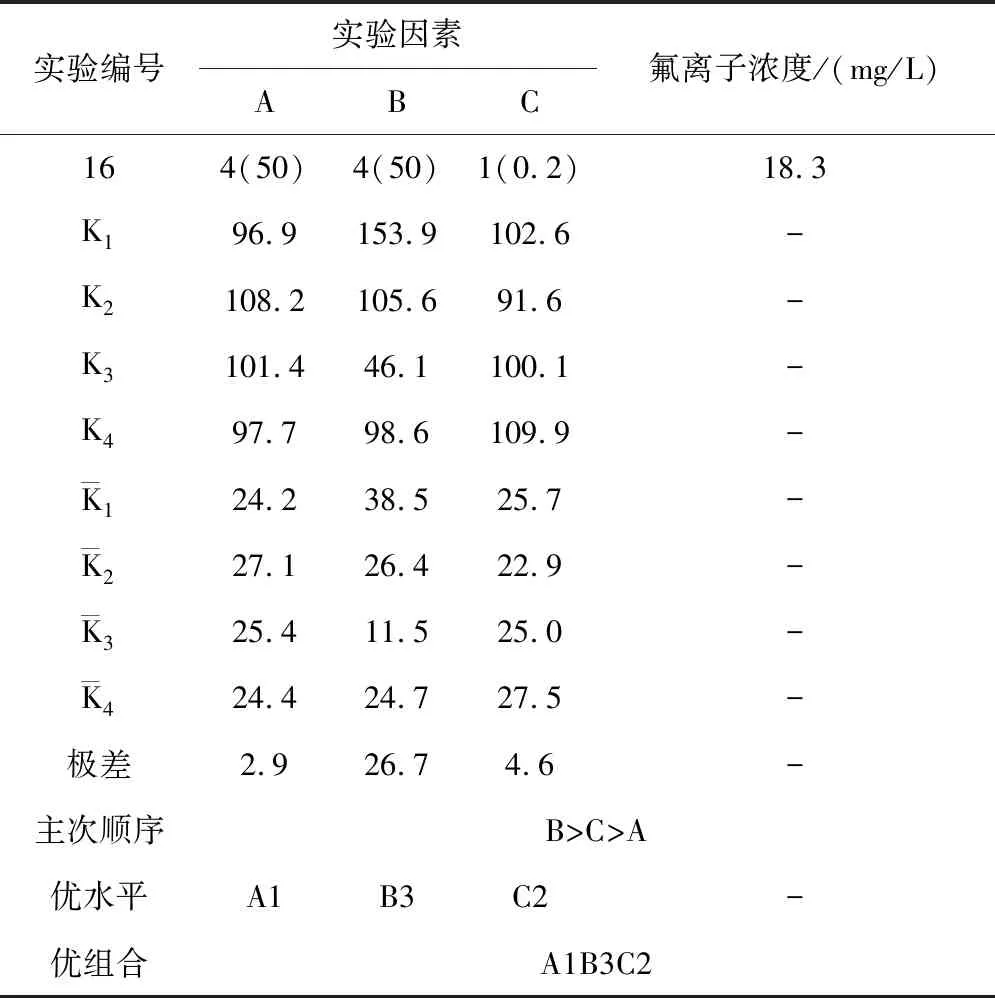
表4(续)
2.2.2 絮凝剂脱氟实验数据分析
由絮凝剂脱氟正交实验结果可以分析得出:
(1)在反应温度、絮凝剂Ⅰ用量、絮凝剂Ⅱ用量三种实验因素中,絮凝剂Ⅰ用量对脱氟效果影响最大,絮凝剂Ⅱ用量影响次之,反应温度影响最小。
(2)絮凝剂脱氟最优的反应条件是:反应温度20℃、絮凝剂Ⅰ用量40g/0.5L盐酸溶液、絮凝剂Ⅱ用量0.3g/0.5L盐酸溶液。
(3)在经过絮凝剂脱氟后,盐酸溶液中的氟离子浓度可以达到10mg/L以下。
3 结论
通过实验确定了沉淀法盐酸脱氟的最佳工艺条件为:
(1)第一步化学沉淀,无水氯化钙作以固体形式加入,加入量为理论值过量5%左右为宜,反应温度20℃,反应时间30~60min。
(2)第二步絮凝沉淀,絮凝剂以固体的形式加入,絮凝剂Ⅰ用量40g/0.5L盐酸溶液、絮凝剂Ⅱ用量0.3g/0.5L盐酸溶液,反应温度20℃,反应时间1h。
(3)经两步脱氟后,盐酸中氟离子浓度可由1000mg/L降为10mg/L以下。
