聚中性红修饰电极对微生物燃料电池(MFC)脱氮产电性能的影响
2019-10-16章静赵丝蒙周昱宏史惠祥
章静,赵丝蒙,周昱宏,史惠祥
(浙江大学环境与资源学院,浙江杭州310058)
0 引 言
在水污染领域,氮素污染是比较突出的问题[1]。硝酸盐主要来自工业废水[2]、农业污水[3]和生活污水,是造成水体富营养化、影响饮用水质的重要水体污染指标之一,与生态和人类的健康密切相关[4-7],目前受关注较多的是地下水的硝酸盐污染[8]。
新兴的MFC技术为废水脱氮提供了新的思路,其兼具脱氮及产电的能力,使MFC脱氮成为研究的热点。但MFC因输出功率低,抑制了其工业化应用,反硝化MFC中微生物与电极表面之间的电子传递效率是影响系统整体性能的主要因素之一。而MFC中微生物与电极间的电子传递效率较低,针对性的解决思路是降低MFC的电荷转移内阻,因此构建微生物与电极之间良好的接触和作用关系对推动反硝化MFC发展有十分重要的意义,通过改良电极来提高电子传递效率,是一种提高MFC性能的有效途径。
本文选用导电性和生物相容性良好的中性红(neutral red,NR)作为电极修饰材料,通过电化学聚合法制备得到聚中性红膜修饰的碳毡,构建聚中性红修饰阳极APNR-MFC、聚中性红修饰阴极CPNR-MFC,并设置对照组C-MFC。通过反应器去除硝酸盐污染物,研究聚中性红修饰电极作为阳极或阴极时对MFC废水处理效果及产电性能的影响;运用电化学分析方法以及微生物分析手段探讨聚中性红修饰电极对MFCs性能的影响机理,为MFCs电极材料改性以提升反应器性能的研究和实践化应用提供一定的理论基础和技术支持。
1 材料与方法
1.1 电极的制备
将碳毡裁剪成7 cm×1.8 cm规格,浸没于硝酸-水溶液(v:v=1:1.5)中,80℃加热3 h,冷却后取出用水冲洗,再将碳毡浸入乙醇-水溶液(v:v=1:1)中5 min,于去离子水中超声,置于80℃烘箱中烘干备用。
采用循环伏安法实现聚中性红膜在碳毡基体上的修饰。首先配制0.025 mol·L-1磷酸盐缓冲液(pH=6)、0.1 mol·L-1KNO3、1 mmol·L-1中性红作为电解液。设置电化学工作站,扫描电压设置为-1.4 ~ 1.4 V(vs Ag/AgCl),扫 描 速 率 为50 mV·s-1,扫描段数为20,进行电化学引发。再将扫描电压降至-1.0~ 0.6 V(vs Ag/AgCl),扫描速率50 mV·s-1不变,扫描段数为60,进行中性红的聚合沉积。
1.2 实验装置
MFC由有机玻璃制成,双室结构,由阴极和阳极2个半反应器组成,单室容积均为128 mL,中间用质子交换膜(Nafion 117,DuPont,USA)分隔,有效面积64 cm2。
共设置3组反应器,见表1。3组反应器的两极分别用导线引出,外接750 Ω电阻,形成闭合电路,电阻两端用导线与数据采集仪并联,每隔1 min采集一次反应器端电压,如图1所示。反应器启动前,将准备好的电极浸没于厌氧污泥和缺氧污泥中,浸泡30 d后取出投入反应器。

表1 MFC反应器参数Table 1 The parameters of MFC reactors
1.3 反应器的启动及运行
试验依据的电池反应如下:
阳极反应:

阴极反应:

总反应:
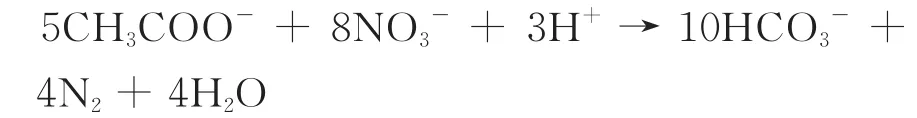
反应器置于恒温培养箱中(30℃),序批式启动,以48 h为周期更换经氮气除氧后的阳极液、阴极液。运行阶段,设置3轮实验,在初始模拟废水组分(pH=7±0.2)的基础上,改变阴极液NO3-的浓度,使阴极进水中NO3--N的浓度分别为50,100,150 mg·L-1,考察修饰电极以及不同浓度的NO3--N对电池反应及产电的影响。

图1 MFC装置图Fig.1 MFCs constructions
1.4 分析测试
1.4.1 电极材料表征
采用SEM观察电极材料表面形貌;采用EDS对材料微观区域的元素分布分别进行定性和定量分析;采用FTIR进行电极材料的官能团分析。
1.4.2 电化学测试
采用美国Agilent公司34970A型数据采集仪在线监测MFC反应器输出电压。测量电池的电极电势、功率密度、库伦效率,用极化曲线和电化学交流阻抗图谱(electrochemical impedance spectroscopy,EIS)来表征MFC的电化学性能。
1.4.3 微生物学测试
在MFCs运行6个月后,进行微生物学测试。采用蛋白质含量法表征生物膜的生物量[9],探究电极材料对生物膜的影响;为研究电极上的菌群分布信息,提取电极上的微生物DNA信息,构建克隆文库,在Illumina MiSeq平台上进行测序分析。
2 结果与分析
2.1 聚中性红修饰电极表征
2.1.1 电极表面形貌
利用扫描电镜观察碳毡电极修饰前后的形貌差异,见图2。中性红修饰碳毡的碳纤维表面附有明显的均匀薄膜,局部放大发现,碳纤维表面的膜为多孔结构。聚中性红修饰材料增加了电极材料的粗糙度,同时电极表面不规则的凸起也增强了电极与细菌细胞膜表面承担电子运输体功能的蛋白的接触。

图2 修饰前后碳毡电极型貌Fig.2 Profile of carbon felt electrode before and after modification
2.1.2 电极表面元素分析
采用能谱仪对电极表面元素进行分析,结果如图3所示。由图3可知,以碳毡为基底的修饰电极上检测出N元素的质量分数为5.28%,推测N元素源自中性红分子中的N。
2.1.3 电极表面官能团分析
采用傅里叶变换红外光谱仪对电极表面中性红聚合物的结构进行了测定,结果如图4所示。
图 4(a)中,3 165 cm-1与 3 331 cm-1处的 2个峰由NR中伯胺的N-H伸缩振动引起,表明中性红单体以-NH2的形式存在;在2 933 cm-1左右为νC-H吸收峰;1 443 cm-1属于-CH3的变形振动;1 380 ~1 250 cm-1的峰为 σC-N(Ar-N)。(b)中,3 408 cm-1为共轭度较大的聚合物大分子的νN-H[10];2 924 cm-1处的小吸收峰为νC-H;1 395 cm-1处的峰由-CH3或Ar-N的变形振动引起。对比显示,在3 000 和 3 500 cm-1之间的3 408 cm-1出现单峰,表明中性红聚合物是以-NH-的形式存在。GABRIELA等[11]也用核磁共振氢谱检测到聚合物链中的-NH-。结果表明,碳毡在中性红溶液中进行电聚合处理时,中性红单体转变为以仲胺相连的聚合物,并被成功修饰到碳毡电极表面。

图3 PNR修饰电极表面能谱图Fig.3 EDS spectra of PNR modified carbon felt

图4 中性红和聚中性红修饰电极的红外光谱图Fig.4 FTIR spectra of NR and PNR modified electrode
2.2 废水处理效果评价
2.2.1 阴极硝氮去除评价
对3组MFC在单个周期内阴极室NO3--N的浓度进行检测,得到不同进水NO3--N浓度下阴极室内NO3--N浓度随时间变化的曲线,见图5。
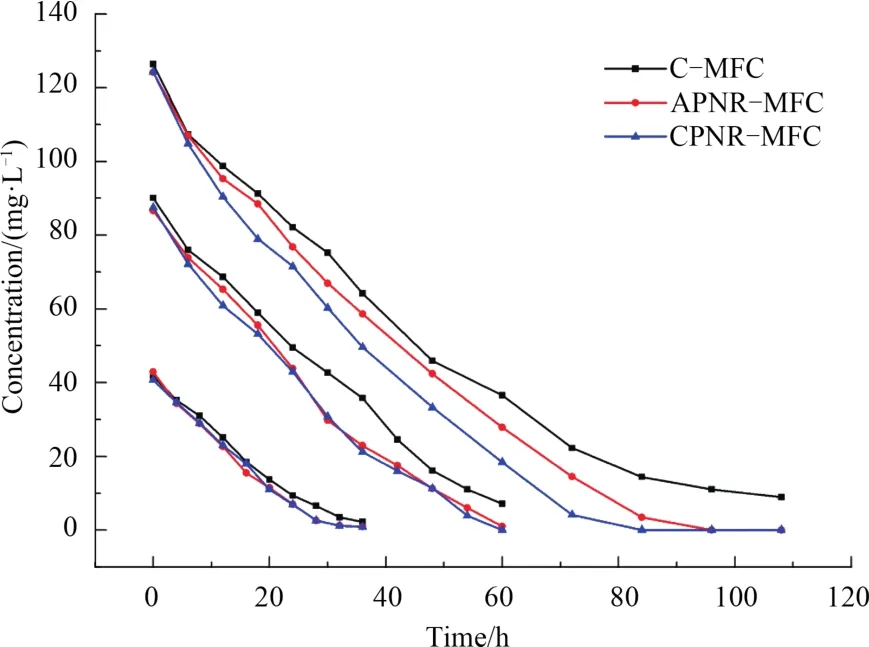
图5 不同基质浓度下C-MFC、APNR-MFC和CPNRMFC硝氮去除情况Fig.5 Removal of NO3--N at different initial substrate concentrations in C-MFC,APNR-MFC and CPNRMFC
随着进水NO3--N浓度的上升,反应器的周期变长。在不同进水NO3--N浓度下,3组MFC在反应周期结束后NO3--N去除率均能达到90%以上。在进水NO3--N 浓度为 150 mg·L-1时,当 CPNR-MFC中NO3--N被完全去除时,C-MFC中的NO3--N浓度仍有14.43 mg·L-1。
计算阴极室NO3--N去除速率。随着进水NO3--N浓度的增高 ,C-MFC、APNR-MFC、CPNR-MFC的去除速率分别提高了34.62%,32.14%和42.86%,CPNR-MFC最高达到0.040 kg·m-3·d-1,可见阴极室底物浓度对半电池反应的影响较大。此时,当进水NO3--N浓度升高时,CPNR-MFC的去除效果提升最明显,表明聚中性红修饰阴极,较大地提升了反应器性能,显示了CPNR-MFC在处理更高浓度硝氮废水方面具有更大的潜力。
2.2.2 阳极COD降解评价
为了更好地评价MFC去除NO3--N的性能,考察了不同进水NO3--N浓度下的MFC阳极室COD的降解情况,结果如图6所示。

图6 不同基质浓度下C-MFC、APNR-MFC和CPNR-MFC的COD降解情况Fig.6 Degradation of COD at different initial substrate concentrations in C-MFC,APNRMFC and CPNR-MFC
由图6知,在检测的周期范围内,相同进水浓度不同反应器COD的降解情况为:APNR-MFC的降解量最低,CPNR-MFC次之,即当阴极还原等量的硝氮时,APNR-MFC阳极消耗的COD最少,单位COD消耗得到的电子利用率最高,即表观有效产出最高,CPNR-MFC次之。
MFCs之间COD降解量的明显差异,本质上由修饰电极影响电极表面电活性微生物附着情况和电子传递效率造成,证实了聚中性红修饰电极的强化作用。阳极产电微生物比例增大能使有效产电的COD比例增高,促进电子转移,从而使接收阴极电子进行还原的硝氮所需的COD量降低。阴极电活性微生物比例增高,则能加速阴极自养反硝化速率,促使阴极电子和H+被快速消耗,两边反应室质子浓度差异的增大一定程度上能促进质子的跨膜传递,阳极室质子的消耗及电极上电子的及时转移,对阳极的电化学反应有促进作用,也能提升阳极的电子输出效率。
2.3 电化学性能评价
2.3.1 电极电势
为比较3组MFC的电极性能,不同硝氮浓度下的电极电势如图7所示。在低电流密度时,不同MFC之间的阳极电势较为接近,但在高电流密度下,APNR-MFC和CPNR-MFC的阳极电势较对照组更稳定。APNR-MFC的阳极被聚中性红修饰而能更加稳定地输出。不同阴极的开路电势及稳定性差异明显,相同电流密度、不同硝氮浓度下,CPNRMFC的阴极电势总是略高于其他2组MFC,并且随着电流密度的增大,不同MFC阴极的稳定性呈现出CPNR-MFC>APNR-MFC>C-MFC的明显变化,说明聚中性红的修饰使阴极性能显著增强。由此证明,采用聚中性红修饰MFC单边电极有助于电池整体性能的提高,且本试验中阴极性能的差异是影响电池整体性能的主要因素。
2.3.2 输出功率
MFC的功率密度是反映做功快慢的物理量,与反应体系的动力学特性有关[12]。图8给出了不同反应器在不同硝氮浓度下的功率密度。在3种NO3--N浓度下,APNR-MFC的最大功率分别为10.70,10.73和11.05 W·m-3,较C-MFC分别提高了43.70%,35.05%和31.93%,CPNR-MFC的最大功率分别为12.22,13.46和15.29 W·m-3,较C-MFC分别提高了64.06%,69.27%和82.51%。分析原因,CPNR-MFC阴极室反硝化反应速率最快,对外电路传递过来的电子及电极液中质子的消耗速度也较快,从而加快了阳极反应速率,加大了阳极产电输出,进而提高了MFC的产电性能。
提高进水NO3--N浓度,3组MFC的输出功率均有不同程度的提升,其中,CPNR-MFC在对照组的最大功率密度对底物浓度有正响应的基础上,增幅更为显著,说明该反应器采用聚中性红修饰碳毡作为阴极,阴极反硝化性能明显强化,在更高硝氮浓度下的产电性能更佳。
2.3.3 库伦效率
在不同进水硝氮浓度下反应器的库仑效率如表2所示,发现APNR-MFC和CPNR-MFC的阳极库仑效率与对照组相比均有显著提高,分别上升了(12.12±0.14)%和(11.36±0.26)%,其中,APNRMFC的库伦效率最高。数据表明,3组MFC中,APNR-MFC的阳极性能最佳,单位COD消耗的产能最高,CPNR-MFC次之,证实了聚中性红修饰电极对电池性能的强化作用。

图7 C-MFC(0#)、APNR-MFC(1#)和CPNR-MFC(2#)在不同初始硝氮浓度下的电极电势图Fig.7 Electrode potentials of C-MFC(0#),APNR-MFC(1#)and CPNR-MFC(2#)at different initial substrate concentrations

图8 C-MFC、APNR-MFC和CPNR-MFC在不同初始硝氮浓度下的功率密度Fig.8 Power density of C-MFC,APNR-MFC and CPNR-MFC at different initial substrate concentrations
表2 MFCs在不同初始硝氮浓度下的阳极库仑效率Table 2 Anodic coulombic efficiency of MFCs at different initial N-N concentration
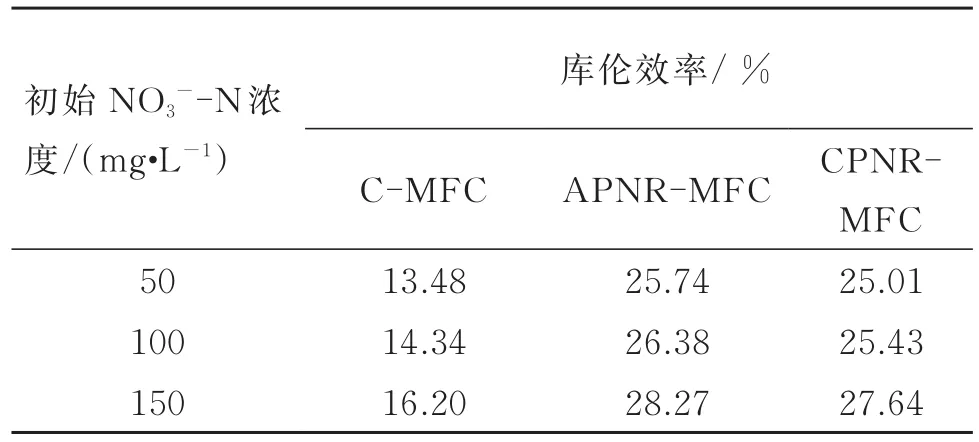
表2 MFCs在不同初始硝氮浓度下的阳极库仑效率Table 2 Anodic coulombic efficiency of MFCs at different initial N-N concentration
--N浓度/(mg·L-1)初始NO3images/BZ_77_1874_1878_2117_2119.png50 100 150 C-MFC 13.48 14.34 16.20 25.74 26.38 28.27 CPNRMFC 25.01 25.43 27.64
2.3.4 极化曲线
为了研究使用聚中性红修饰电极后MFC性能的提升与反应器内阻的变化是否关联,对不同进水硝氮浓度下的3组MFC作极化曲线,如图9所示。对极化曲线线性部分进行拟合,所得斜率即为表观总内阻。APNR-MFC和CPNR-MFC的内阻小于对照组C-MFC,表明经聚中性红修饰电极,MFC的内阻得到有效降低,此亦是MFC性能提升的宏观原因之一。
2.3.5 交流阻抗图谱
为考量聚中性红修饰电极对其性能及对微生物与电极间电荷转移过程的影响,对高频区的欧姆内阻和电荷转移内阻进行拟合,拟合交流阻抗曲线如图10所示,等效电路如图11所示,内阻数据见表3。

图9 不同硝氮浓度下C-MFC、APNR-MFC和CPNR-MFC的极化曲线Fig.9 Polarization curves of C-MFC APNR-MFC and CPNR-MFCat different initial substrate concentrations

图10 不同MFC的EIS测试Nyquist图及拟合结果Fig.10 Nyquist plots for cell,anode,cathode and fitting results of MFCs in this study
相比电荷转移内阻,C-MFC的阳极和阴极欧姆内阻很小,只有3.67和5.84 Ω,表明该阳极和阴极碳毡的导电性能良好[13]。尽管C-MFC的欧姆内阻已相对较低,但实验组的欧姆内阻更低,说明中性红的修饰进一步提升了电极的导电性。
实验组电池性能提升的主要原因是电荷转移内阻的下降。阳极电荷转移内阻,Rct(APNR-MFC)<Rct(CPNR-MFC)<Rct(C-MFC),且 APNRMFC和CPNR-MFC的阳极电荷转移内阻分别降至C-MFC的51.79%和65.56%。阴极电荷转移内阻,Rct(CPNR-MFC)<Rct(APNR-MFC)<Rct(CMFC),且APNR-MFC和CPNR-MFC的阴极电荷转移内阻分别降至C-MFC的68.48%和44.35%。电荷转移内阻在全电池的规律为:Rct(CPNRMFC)<Rct(APNR-MFC)<Rct(C-MFC),说明电池阴极的修饰对电池性能的影响更大。在MFC中,电荷转移内阻来自微生物细胞和电极之间的电子传递能量损失,而这与电活性微生物膜的活性、微生物与电极间的相互作用、电极材料的氧化还原性有关。

图11 等效电路图Fig.11 Equivalent electrical circuit
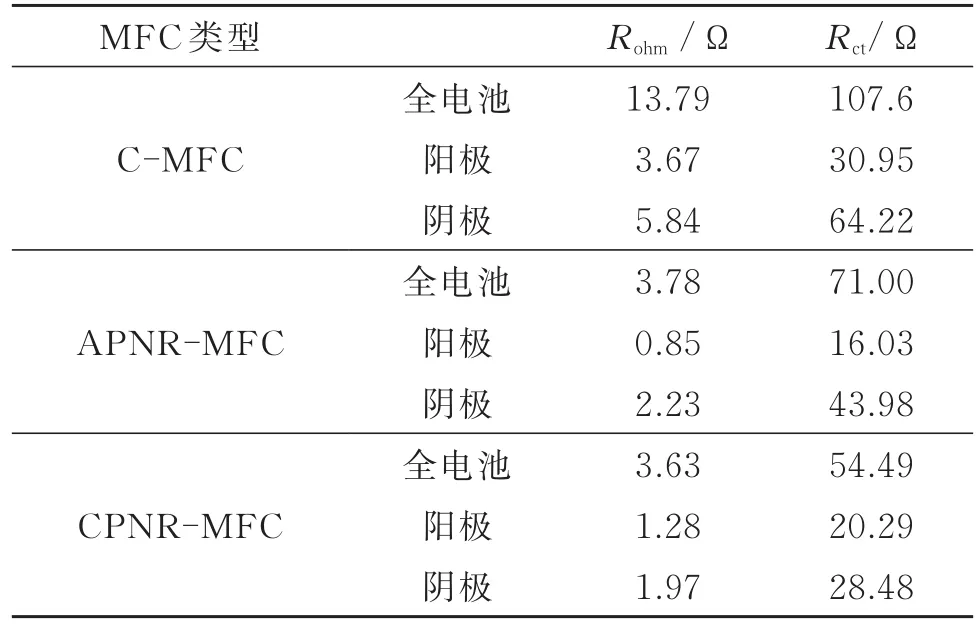
表3 MFCs等效电路拟合结果Table 3 Simulated values of equivalent circuit of MFCs
2.4 电极微生物特性分析
2.4.1 生物量分析
为探究修饰材料中性红对生物膜的影响,MFCs阳极和阴极生物量的测定结果如表4所示。根据数据分析,阳极生物量:APNR-MFC>CPNRMFC>C-MFC,APNR-MFC阳极显示了更好的生物相容性;阴极生物量:CPNR-MFC>APNRMFC>C-MFC,同理,CPNR-MFC阴极显示了更好的生物相容性。修饰电极上生物量较普通电极生物量分别有84.62%和90.00%的增长,证明中性红的修饰极大地促进了微生物的富集。同时,APNRMFC、CPNR-MFC中未修饰电极端的生物量也有明显的增加,说明通过半电池反应的加强,也能促进另一半电池的反应性能。

表4 MFCs电极生物量Table 4 The biomass test results of electrodes
2.4.2 电极微生物群落分析
为了探明体系中的功能菌组成,通过Illumina Misep高通量测序平台对3组MFC结束运行后的阳极以及阴极微生物进行群落结构分析,结果如图12和13所示。

图12 不同反应器阳极微生物群落结构分析Fig.12 Microbial community analysis of anodes in MFCs
对比不同反应器的阳极菌属组成,在可识别的菌属中,δ-变形菌纲的地杆菌属(Geobacter)[9,14-15]是被广泛研究的具有代谢乙酸盐和产电能力的菌属,在C-MFC、APNR-MFC和CPNR-MFC中的占比分别为6.87%,31.83%和24.88%,实验组阳极上有明显的地杆菌属富集,其占比分别为对照组的4.63倍和3.62倍。δ-变形菌纲的脱硫弧菌属(Desulfovibrio)[16]也具有产电能力,能够通过细胞色素C进行电子传递,在对照组反应器中占12.93%。此外,δ-变形菌纲的norank_f__Desulfarculaceae菌属以及β-变形菌纲的Azonexus菌属在实验组中的富集度也很高,占比在10%左右,该数值远高于对照组。因此,实验组阳极生物膜上富集到更多能参与电极电子传递的电活性微生物。

图13 不同反应器阴极微生物群落结构分析Fig.13 Microbial community analysis of cathodes in MFCs
观察不同反应器的阴极菌属组成,在对照组电极上,Lentimicrobium成为优势菌属,占比达32.21%。α-变形菌纲的Aquamicrobium[17]菌属是一种耐氧反硝化菌,无碳源下能将NO3-还原为NO2-,存在碳源时能完全还原成N2,在MFCs中占比分别为4.83%,5.24%和5.56%。β-变形菌纲的硫杆菌属Thiobacillus[18]是具有电活性的自养反硝化菌属,在MFCs中的占比分别为3.16%,1.79%和7.35%,证明CPNR-MFC阴极电极环境有利于其生长。α-变形菌纲的Afipia[19]菌属具有利用电极电子自养反硝化还原亚硝酸盐能力,在CPNR-MFC上生长较多,占8.90%,而在另外2组电极上不足0.5%。β-变形菌纲的unclassified_f_Comamonadaceae和Denitratisoma是常见的异养反硝化菌属,在对照组和实验组中均有一定的生长。结果表明,MFCs阴极成功富集了反硝化功能菌,并且这些菌属主要来自α-变形菌纲和β-变形菌纲。其中,CPNR-MFC阴极对于电化学活性的Thiobacillus和Afipia具有较高的富集度,自养反硝化反应过程占优势,与该反应器除氮性能最佳的结果相一致。
2.5 聚中性红修饰电极影响机理探究
根据反应器运行结果,APNR-MFC和CPNRMFC因使用修饰电极,脱氮产电性能显著增强,其中强化效果更明显的是CPNR-MFC。
中性红单体具有良好的导电性和生物相容性。经循环伏安法电聚合在碳毡表面形成聚合物薄膜,材料导电性得以保留。聚中性红修饰电极表面粗糙度提高,同时表面存在含N官能团,生物相容性好,促进了微生物附着,富集了电活性微生物。
对APNR-MFC微生物的分析表明,粗糙的聚中性红膜对阳极产电微生物Geobacter、Azonexus及norank_f_Desulfarculaceae具有良好的选择富集作用,产电微生物在电极微生物群落中的占比增大,电活性增强,因此,阳极室消耗单位COD产生的能够输出胞外的电子数量增加。修饰电极上细菌生物多样性降低,产电功能菌在生物膜中占据主导优势,竞争性代谢活动相对减少,有助于提高电子的输出率。
CPNR-MFC表现出的最佳性能及对高硝氮废水的处理潜力,与反应器性能受阴极性能控制有关。在阴极,聚中性红修饰电极对具有反硝化功能的电化学活性微生物Thiobacillus、Afipia和Aquamicrobium有较好的富集作用,与CPNR-MFC表现出的阴极反硝化性能相符。硝氮的还原反应是电池的限速步骤,阴极的修饰使得阴极微生物活性增强,半电池反硝化速率明显提高,对电子和质子的代谢速率加快,因此促进了阳极的电子输出和质子的跨膜传输,减少了电荷和质子积累,间接提高了阳极的产电性能。
3 结论
3.1 选择中性红为修饰材料,通过电聚合法对普通碳毡电极表面进行修饰,采用SEM、EDS、FTIR等表征手段,证实了碳毡电极表面被聚中性红膜成功修饰。
3.2 构建不同微生物燃料电池,对比反应器之间的性能差异。稳定运行阶段,MFCs均能实现90%以上的硝氮去除率。其中,CPNR-MFC的性能突出,硝氮去除速率达到 0.040 kg·m-3·d-1,最大功率密度15.29 W·m-3,证实了聚中性红修饰阴极电池性能提升作用更显著,这为硝酸盐废水处理提供了新思路。
3.3 对MFCs进行电化学和微生物特性分析,探究了聚中性红修饰电极对MFC性能影响的机理。研究表明,聚中性红的修饰使得MFC电极生物量附着大,功能菌占比高,从而为增加电子产量、电子利用率和电子传递效率提供了有利条件,使MFC电荷转移内阻降低,进而提升了反应器性能,可为其实践应用提供理论与技术支持。
