脾多肽联合FOLFIRI方案对直肠癌患者免疫功能的影响及疗效
2019-10-12姜慧员刘海义白文启王文渊梁艳杰王艳江波
姜慧员 刘海义 白文启 王文渊 梁艳杰 王艳 江波
山西省肿瘤医院(太原030013)
直肠癌是临床上最为常见的恶性肿瘤之一,我国直肠癌的发病率和病死率呈逐年上升趋势[1],不仅严重影响患者的身心健康,同时给家庭和社会造成了沉重的经济负担[2-3],临床研究证实化疗是治疗直肠癌的重要方法之一[4]。有研究[5]显示,化疗药物治疗疾病的过程中,增加药物的不良反应,降低患者的免疫功能,进而影响患者的治疗效果[5]。以往研究显示脾多肽对骨髓抑制有保护作用,但对直肠癌患者提高机体免疫力的研究鲜有报道。本研究回顾性分析我院2017年6月至2018年6月Ⅱ、Ⅲ期直肠癌单纯新辅助化疗患者临床资料,探讨脾多肽联合FOLFIRI化疗方案的疗效、免疫功能和对整体治疗的不良反应,以寻找更为安全、有效的直肠癌新辅助化疗方案,提高患者免疫功能,从而提高其生存质量。
1 对象与方法
1.1研究对象选取2017年6月至2018年6月山西省肿瘤医院住院病理证实为Ⅱ期、Ⅲ期的直肠癌患者为研究对象。根据患者自己及家属是否愿意行脾多肽联合FOLFIRI化疗方案分为两组,对照组74例,男48例,女26例,年龄平均(52.46±10.468)岁。治疗组74例,男47例,女27例,年龄平均(52.15±10.045)岁。两组患者在性别、年龄、病理类型(腺癌、黏液腺癌、其他)、分化程度(低分化、中分化、高分化)、临床分期(Ⅱ期、Ⅲ期)差异无统计学意义(均P>0.05)。
纳入标准:(1)符合直肠癌诊断标准,经肠镜取活检和(或)病理,明确诊断为结直肠癌;(2)病理证实为Ⅱ期、Ⅲ期的直肠癌患者;(3)ECOG评分0 ~ 2分;(4)未经抗肿瘤治疗的患者;(5)化疗期间不使用或不同时使用其他免疫制剂;(6)免疫功能检查提示指标低下;(7)年龄≥18周岁;(8)知情同意本研究。
排除标准:(1)有其他恶性肿瘤史;(2)对本方案药物过敏;(3)不能耐受化疗药物者;(4)免疫功能缺陷或免疫系统疾病;(5)未能完成整个周期化疗者。
1.2方法由调查员对患者进行问卷调查。包括(1)一般资料问卷:病理类型、分化程度、临床分期。(2)体力状况ECOG评分:是美国东部肿瘤协作组(ECOG)制定的评价癌症患者体力状况的量表。分为0~5六个级别。0分表示活动能力完全正常;1分能自由走动及从事轻体力活动;2分表示能自由走动及生活自理,工作能力丧失;3分表示生活部分自理,日间超出一半时间卧床或坐轮椅;4分表示卧床不起,无自理能力;5分为死亡。
1.2.1治疗方案对照组:采用FOLFIRI方案:第1天:将180 mg/m2盐酸伊立替康加至0.9%氯化钠注射液250 mL中,静脉滴注2 h;第1~2天:200 mg/m2亚叶酸钙加至5%葡萄糖注射液250 mL中,静脉滴注;5-氟尿嘧啶(5-Fu)400 mg/m2静脉推注。5-Fu 600 mg/m2持续微量化疗泵滴注22 h;2周为1个新辅助化疗周期,共3个化疗周期。
治疗组:在对照组基础上给予脾多肽注射液(吉林丰生制药有限公司,规格:2 mL)治疗:10 mL溶于0.9%氯化钠注射液500 mL,静脉滴注,每日1次,第1~10日,完成3个化疗周期。
两组患者均进行结直肠癌根治术治疗,均完成3个化疗周期。
1.2.2观察指标疗效观察:根据实体瘤疗效评价标准RECIS(1.1版)进行评估,分为完全缓解、部分缓解、疾病稳定、疾病进展。以完全缓解+部分缓解为有效率,以完全缓解+部分缓解+疾病稳定计算疾病控制率。
不良反应观察:美国国立癌症研究所(NCI)2009年不良事件通用毒性评价标准(CTC)4.0版进行分级,分为0~Ⅳ级。不良反应:血细胞减少:包括血小板减少、白细胞减少、血红蛋白减少;消化道反应:恶心、呕吐、腹泻;肝功能异常:胆红素升高、肝酶普升高;肾功能异常:肌酐增高、蛋白尿、血尿;心功能异常:心率异常、心肌缺血或梗死、高血压、心包炎、低血压;电解质紊乱:高血糖、低血糖、高钙血症、低钙血症、低钠血症、高钠血症、高钾血症、低钾血症;皮肤黏膜反应:口腔黏膜炎、脱发、皮肤过敏;神经毒性反应。
1.3统计学方法采用SPSS 22.0进行统计处理,计数资料以百分比表示,采用χ2检验;两组不良事件通用毒性评价标准的资料采用Z检验;正态分布计量资料采用独立样本t检验。以α=0.05为检验水准双侧检验。当P<0.05,认为差异有统计学意义。
2 结果
2.1疗效评估治疗组74例中完全缓解4例,部分缓解53例,疾病稳定13例,疾病进展4例,有效率77.03%(57/74),疾病控制率94.59%(70/74);对照组74例化疗后完全缓解1例,部分缓解38例,疾病稳定22例,疾病进展13例,有效率52.70%(39/74),疾病控制率82.43%(61/74),两组治疗疗效差异有统计学意义(P<0.05)。见表1。
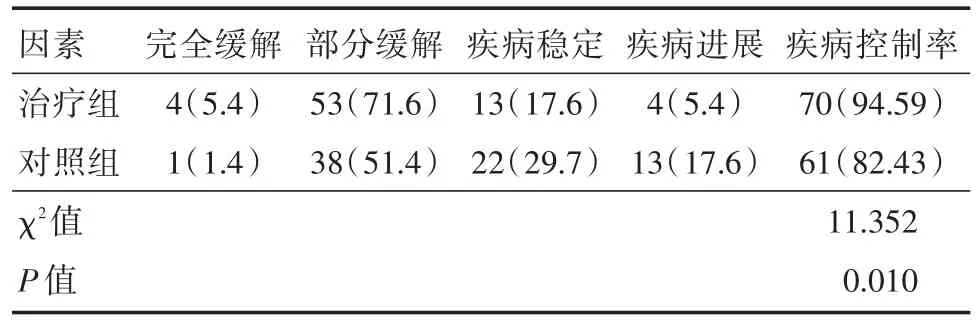
表1 两组患者疗效比较Tab.1 Comparison of curative effect between two groups例(%)
2.2两组患者化疗后不良反应比较结果显示,两组患者在白细胞减少、血红蛋白减少、血小板减少、恶心、呕吐、腹泻、肝功能损伤、肾功能损伤、食欲减退等不良反应比较差异无统计学意义(P>0.05)。见表2。
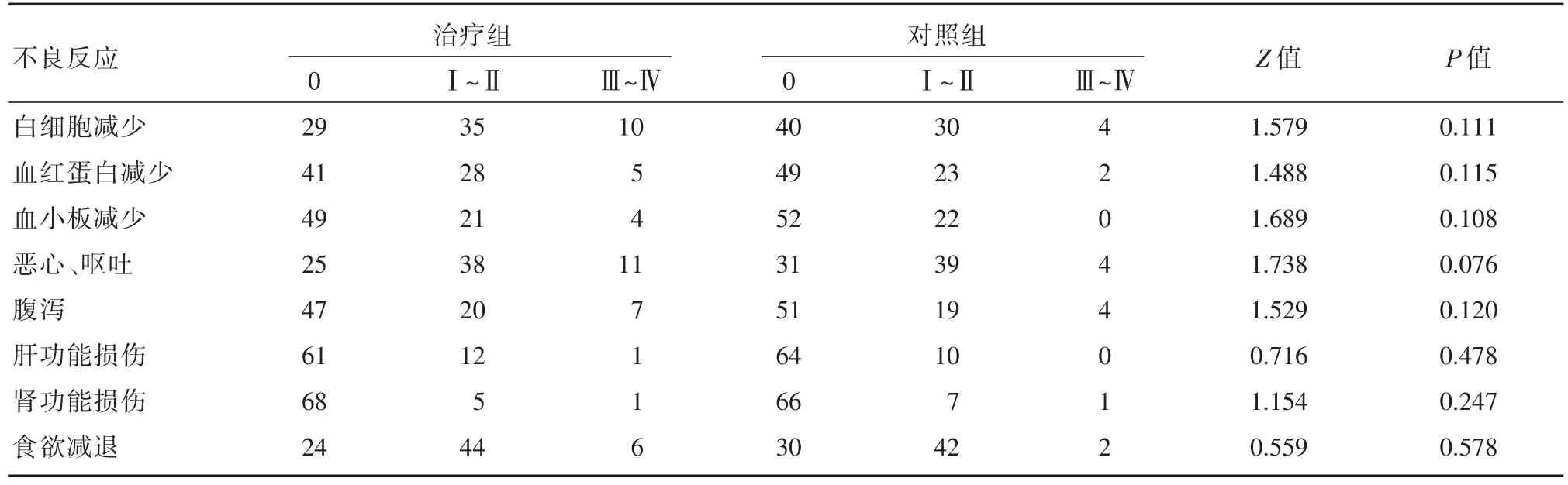
表2 两组患者不良反应比较Tab.2 Comparison of adverse reactions between two groups 例
2.3两组患者治疗前免疫功能比较结果显示,化疗前两组患者CD3+、CD4+、CD8+、NK差异无统计学意义(均P>0.05),两组均衡可比。见表3。
表3 两组患者治疗前免疫功能比较Tab.3 Comparison of immune function between two groups before treatment ± s
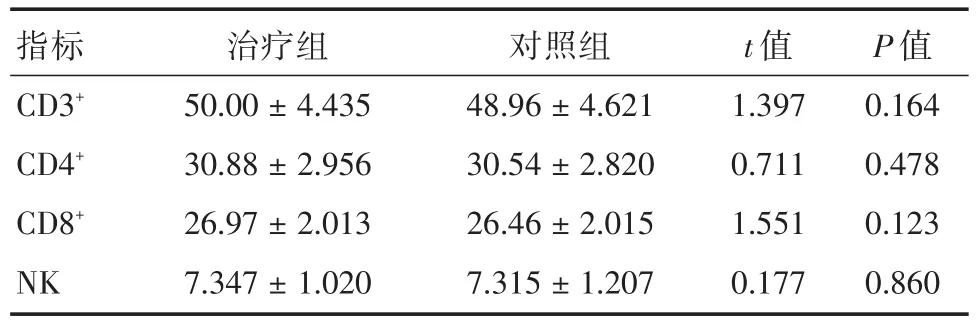
表3 两组患者治疗前免疫功能比较Tab.3 Comparison of immune function between two groups before treatment ± s
指标CD3+CD4+CD8+NK治疗组50.00±4.435 30.88±2.956 26.97±2.013 7.347±1.020对照组48.96±4.621 30.54±2.820 26.46±2.015 7.315±1.207 t值1.397 0.711 1.551 0.177 P值0.164 0.478 0.123 0.860
2.4两组患者治疗后免疫功能比较结果显示,两组患者治疗后CD3+、CD4+、CD8+、NK差异有统计学意义(均P<0.05),且两组患者治疗后CD3+、CD4+、CD8+、NK差值差异有统计学意义(均P<0.05),见表4。
表4 两组患者化疗后免疫功能比较Tab.4 Comparison of immune function between two groups after chemotherapy ± s
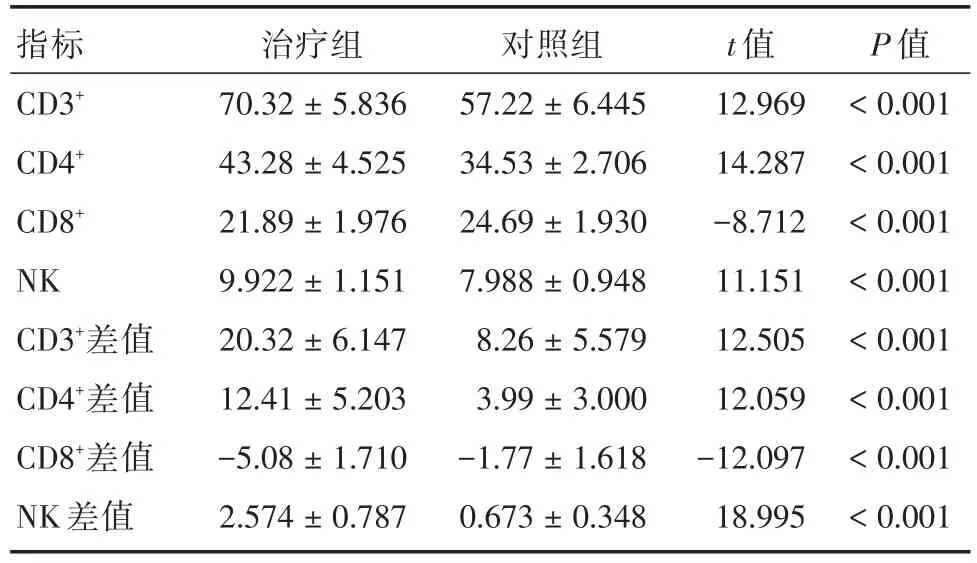
表4 两组患者化疗后免疫功能比较Tab.4 Comparison of immune function between two groups after chemotherapy ± s
指标CD3+CD4+CD8+NK CD3+差值CD4+差值CD8+差值NK差值治疗组70.32±5.836 43.28±4.525 21.89±1.976 9.922±1.151 20.32±6.147 12.41±5.203-5.08±1.710 2.574±0.787对照组57.22±6.445 34.53±2.706 24.69±1.930 7.988±0.948 8.26±5.579 3.99±3.000-1.77±1.618 0.673±0.348 t值12.969 14.287-8.712 11.151 12.505 12.059-12.097 18.995 P值<0.001<0.001<0.001<0.001<0.001<0.001<0.001<0.001
3 讨论
近年来,随着对直肠癌的深入研究,新辅助化疗逐渐被应用于临床。近年来关于术前新辅助化疗治疗进展期直肠癌的研究较多,但新辅助化疗后直肠癌患者大多数免疫功能低下,术后并发症发生率较高。脾多肽注射液是一种免疫调节剂,能提高患者免疫能力,有效调节患者免疫系统,以往多报道脾多肽注射液对晚期卵巢癌患者骨髓抑制的保护作用[6]、对肺癌患者化疗后骨髓抑制的保护[7]、提高HJ-PI01的抗肿瘤活性[8]中,且多报道不同基因在直肠癌患者中的表达[9-11],对于脾多肽联合FOLFIRI方案对直肠癌免疫功能影响和不良反应鲜有报道。本研究拟通过探讨脾多肽联合FOLFIRI方案对直肠癌治疗的疗效、免疫功能和不良反应,为临床治疗提供客观依据。
结果显示,两组患者治疗后 CD3+、CD4+、CD8+、NK差异有统计学意义,且两组患者治疗后CD3+、CD4+、CD8+、NK差值差异有统计学意义,与相关研究结果一致[12]。脾多肽注射液为提取于健康小牛脾脏的无菌水溶液,为分子量<6 kDa的多肽、游离氨基酸、核酸、总糖的无菌水溶液。脾多肽激活并增强非特异性免疫功能,加快T淋巴细胞成熟,激活未致敏的淋巴细胞,使其成为致敏的淋巴细胞,且通过激活单核细胞的蛋白激酶从而介导细胞分裂增生,增强机体细胞免疫功能,从而有效调节患者免疫系统,提高患者免疫能力。以往研究表明,胎盘多肽对骨髓抑制有保护作用,从而改善身体虚弱,降低患者的不良反应。
本研究还显示,两组患者在白细胞减少、血红蛋白减少、血小板减少、恶心、呕吐、腹泻、肝功能损伤、肾功能损伤、食欲减退等不良反应比较差异无统计学意义。其原因可能是本研究选择患者新辅助治疗期间,观察时间较短,因此不能完全观察不良反应的情况。
研究显示,两组患者治疗后,治疗组74例中完全缓解4例,部分缓解53例,疾病稳定13例,疾病进展4例,有效率77.03%(57/74),疾病控制率94.59%(70/74);对照组74例化疗后完全缓解1例,部分缓解38例,疾病稳定22例,疾病进展13例,有效率52.70%(39/74),疾病控制率82.43%(61/74),两组治疗疗效差异有统计学意义。与CAROLA等[13]的研究结果一致。该方案中亚叶酸钙属于作叶酸拮抗剂的解毒剂,是四氢叶酸的甲酰衍生物,主要用于高剂量甲氨蝶呤、乙胺嘧啶或甲氧苄啶等的解救叶酸拮抗剂解毒剂,与尿嘧啶联合应用,可提高氟尿嘧啶的疗效。氟尿嘧啶其代谢物能够通过伪代谢的形式进入RNA、DNA内干扰细胞功能。伊立替康水溶性好、毒性低,阻断癌细胞DNA复制,并抑制其修复DNA缺口,使癌细胞凋亡。伊立替康与其他抗肿瘤药物间具有较好的协同作用。
本研究仍存在不足,未做到随机对照,纳入的病例相对简单,需要进一步完善,且未对患者的远期生存期及生活质量进行随访,笔者将在后续的研究中进行更深一步的研究。
