显微镜和耳内镜下鼓膜修补术对麻醉管理和患者早期恢复的影响
2019-10-08朱跃新胡春波陈恺铮王武庆沈霞
朱跃新 胡春波 陈恺铮 王武庆 沈霞
(1.复旦大学附属眼耳鼻喉科医院麻醉科 2.耳鼻喉科 上海 200031)
鼓膜修补术的适用人群通常是慢性中耳炎但不伴发胆脂瘤的患者,其目的是修补穿孔的鼓膜和恢复听力。传统的耳显微手术路径为耳后切口[1]。显微镜的直视角度使得手术医师在耳道的视野受限,为获得满意的手术视野,有时需要在耳后切开皮肤并进行乳突切除等操作。该手术方式通常伴有较大的手术切口并在术后留有瘢痕,患者有明显的术后不适感。内镜辅助下行中耳手术始于1960年[1]。随着内镜及相关装置的发展和更新,内镜下中耳手术的优势变得日益突出和明显[2]。经耳道内镜手术可以提供一个开阔的视野,更清晰地放大和暴露中耳结构及一些在常规显微镜下难以暴露的结构如下鼓室、鼓窦和中鼓室下部[3]。随着耳内镜手术的开展,目前有少数研究比较了常规显微镜下鼓膜成形术和耳内镜鼓膜成形术的有效性[2],但关于这2种手术方式对麻醉管理和患者早期恢复的影响研究较少。
1 资料与方法
1.1 资料 回顾分析51例2018年1~7月行鼓膜修补术的患者,美国麻醉医师协会(American Standard of Anesthesiologist, ASA) Ⅰ~Ⅱ级,其中男性24例、女性27例;年龄16~60岁;体重51~75 kg。患者分为显微镜下鼓膜修补组(M组,n=25)和耳内镜下鼓膜修补组(E组,n=26)。2组患者均由同一位术者完成手术。排除标准:术前或术中诊断为中耳胆脂瘤,术中需要切除乳突。
1.2 方法 术前6 h禁食,2 h禁饮。入手术室后前臂留置20G留置针开放静脉,持续输注乳酸钠8~10 mL/kg。监测无创血压(每间隔5 min)、心电图、脉搏和血氧饱和度。麻醉诱导:利多卡因40 mg, 瑞芬太尼0.03 μg/kg, 丙泊酚2.0 mg/kg, 罗库溴铵0.6 mg/kg;2 min后置入可弯曲加强型喉罩。男性患者选用5号喉罩,女性患者选用4号喉罩。
麻醉维持:喉罩置入完成后行机械通气,潮气量为6~8 mL/kg,呼吸频率为13~15 次/min,吸呼比为1∶2,新鲜气流为2 L/min,吸入氧浓度为50%,维持呼气末CO2(end tidal CO2, ETCO2)为35~40 mmHg(1 mmHg=0.133 kPa),吸入七氟醚使呼气末浓度维持在0.7~1个最低肺泡气有效浓度 (minimum alveolar concentration, MAC)。手术结束前予以帕瑞昔布钠1 mg/kg、氢吗啡酮0.01 mg/kg用于术后镇痛;给予地塞米松0.01 mg/kg和阿扎司琼0.2 mg/kg预防术后恶心、呕吐。患者转入术后恢复室待苏醒。拔管指征:呼之睁眼,自主呼吸恢复,呼吸频率10~20 次/min, ETCO2≤45 mmHg,呼吸空气氧分压≥95%,潮气量>8 mL/kg。使用视觉模拟评分(visual analogue scale, VAS)评估术后疼痛情况,如>4分予以0.01 mg/kg 氢吗啡酮行疼痛补救治疗。
1.3 分析指标 ①2组患者的一般情况,如年龄、体重、手术和麻醉时间、术中瑞芬太尼用量等;②不同时间点的血压和心率变化:麻醉诱导前(T0)、喉罩置入后即刻(T1)、手术开始时(T2)、手术结束(T3)、患者转入术后恢复室即刻(T4);③ 患者苏醒情况包括自主呼吸恢复时间、拔管时间和定向力恢复时间等;④术后疼痛补救治疗情况;⑤术后第1天疼痛评分(0分为不痛,10分为难以忍受的疼痛)和患者满意程度(0分为最不满意,10分最满意)。
1.4 统计学处理 采用GraphPad Prism 5 软件进行统计分析,计量资料以均数±标准差表示,比较采用t检验,计数资料比较采用χ2检验,P<0.05为差异有统计学意义。
2 结果
2.1 患者一般情况 2组患者性别、年龄、体重差异均无统计学意义(P值均>0.05)。2组鼓膜修补时间、麻醉时间差异均有统计学意义(P值均<0.05,表1),术中瑞芬太尼用量差异也具有统计学意义(P<0.001,表1)。
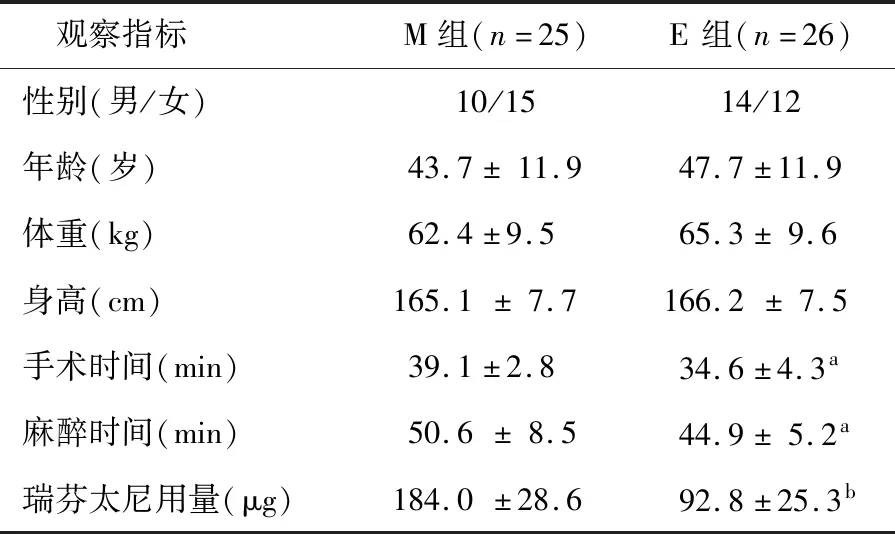
表1 2组患者一般情况
注:a示P<0.05,b示P<0.000 1
2.2 患者血流动力学变化 ①组内比较:2组患者在T1、T2和T3 时间点,平均动脉压及心率均低于T0, 维持在较麻醉诱导前下降20%~30%间;②组间比较:各时间点2组患者平均动脉压和心率差异均无统计学意义(P>0.05;表2)。
2.3 术后恢复情况 在术后恢复室,2组患者自主呼吸恢复时间、拔管时间差异均无统计学意义(P值均>0.05;表3)。定向力恢复时间、出恢复室时间、术后需要治疗疼痛比例差异均有统计学意义(P值均<0.05;表3)。术后第1天随访,2组患者总体满意度及疼痛评分差异也均有统计学意义(P值均<0.001;表3)。

表2 2组患者血流动力学变化()
注: MAP为平均动脉压;M组为显微镜组,E组为耳内镜组

表3 2组患者术后恢复情况()
注:a示P<0.05,b示P<0.000 1
2.4 其他 2组患者术后各有1例出现恶心、呕吐。
3 讨论
鼓膜修补术的目的是消除感染,修补穿孔的鼓膜和提高听力[4]。长久以来,显微镜下手术是进行鼓膜修补的常规方式。该方式可以双手操作,有较好的立体视野。然而,经耳道内操作不容易暴露鼓膜前部等,手术视野严重受限,为此术者选择耳后入路以获取良好的手术视野。耳后路径实施鼓膜修补的不利之处在于手术创伤较大,同时需要花费较多的时间处理周围组织和缝合伤口。而耳内镜经耳内途径,只需要很小的切口以获取筋膜,因此节约了手术时间。另外,在显微镜下操作时,为获取较好的手术视野可能需要切开扩大耳道,而耳内镜可以绕过狭窄的耳道获得良好的手术视野,并减少手术时间。我们的研究发现,显微镜下鼓膜修补的手术时间和麻醉时间长于耳内镜组,而且瑞芬太尼的使用量也比较大。
本研究发现,耳内镜患者术后定向力恢复和离开恢复室时间短于显微镜组。术后患者的快速恢复可显著提高手术室周转速度和利用率。其他研究也支持耳内镜下中耳手术患者占用医疗资源明显少于显微镜下中耳手术患者[5-6]。因此,耳内镜下鼓膜修补可以达到减少医疗成本的效果。耳内镜的缺点在于需要术者单手操作,一旦出血术野将受到严重损害,以及光源产热相关的中耳或内耳热损伤[2]。麻醉医师需要控制术中血压和心率以提供良好的手术视野。我们的研究发现,2组患者围手术期血流动力学变化差异无统计学意义,故瑞芬太尼使用剂量的差异可能源于手术创伤和手术时间的差异。
耳内镜除可以提供良好的手术视野外,只需要很小的手术切口,并保留了外耳和内耳的完整性。有研究[7]发现,在耳内镜下行胆脂瘤清理手术时可以避免不必要的乳突切除和外耳道扩大以及软组织损伤,避免了术后并发症如组织肿胀、伤口疼痛和耳道狭窄等。Choi等[8]发现,耳内镜手术的患者术后第1天的疼痛程度较轻。我们的研究发现,和显微镜组相比,耳内镜组患者在术后恢复室内需要镇痛治疗的人数较少,术后第1天的镇痛评分明显降低。
关于2种手术方式对于手术结局影响的研究显示,鼓膜愈合率和术后并发症在显微镜组和耳内镜组基本相当[5,8]。但耳内镜手术创伤小,对患者在心理和生理上的损伤和负担较小。这可以解释为什么手术医师和患者更愿意选择在内镜下进行中耳手术。我们的研究发现,2组患者的总体满意度存在显著差异,耳内镜组患者满意程度显著高于显微镜组。可能原因如下:首先,耳内镜组患者疼痛程度降低,因术后疼痛使用阿片类镇痛药可能产生的眩晕、便秘和恶心、呕吐等减少,从而提高了患者的满意度;其次,显微镜下修补鼓膜的材料往往采用颞肌筋膜,取筋膜以后,在手术以后的几天里会影响咀嚼;再次,显微镜手术患者需要术侧备皮,患者往往因为手术明显影响自己的形象而影响工作。
总之,耳内镜下鼓膜修补手术较显微镜下手术可以减少医疗资源的占用,包括减少麻醉药物用量和加快术后恢复,减少麻醉和手术时间,减少术后疼痛和提高术后满意度。
