聚乙二醇化重组人粒细胞集落刺激因子在乳腺癌辅助化疗后的应用
2019-09-29王松祥徐潮阳
王松祥 徐潮阳


[摘要] 目的 探讨聚乙二醇化重组人粒细胞集落刺激因子(PEG-rhG-CSF)在乳腺癌辅助化疗后的应用。 方法 选取2015年12月~2017年6月乳腺癌行辅助化疗患者共162例,采用抛银币法分为观察组和对照组。观察组患者予以PEG-rhG-CSF 100 μg/kg每周期单次注射,对照组患者予以重组人粒细胞集落刺激因子(rhG-CSF)5 μg/kg每日注射1次,连续7 d。观察并比较两组患者的临床疗效及安全性。 结果 观察组患者治疗后Ⅳ度中性粒细胞缺乏及延迟化疗发生率均明显少于对照组(P<0.05);观察组患者治疗后骨骼肌疼痛、发热、乏力等不良反应发生率均明显低于对照组(P<0.05)。 结论 PEG-rhG-CSF能够明显降低乳腺癌辅助化疗患者中性粒细胞减少及延迟化疗的发生,且用药更为方便易行,副反应小,患者的依从性更好。
[关键词] 乳腺癌辅助化疗后;聚乙二醇化重组人粒细胞集落刺激因子;重组人粒细胞集落刺激因子;中性粒细胞减少
[中图分类号] R737.9 [文献标识码] A [文章编号] 1673-9701(2019)20-0008-03
Application of pegylated recombinant human granulocyte colony-stimulating factor in adjuvant chemotherapy for breast cancer
WANG Songxiang XU Chaoyang
Department of Breast and Thyroid, Shaoxing People's Hospital in Zhejiang Province, Shaoxing 312000, China
[Abstract] Objective To investigate the application of pegylated recombinant human granulocyte colony-stimulating factor(PEG-rhG-CSF) in adjuvant chemotherapy for breast cancer. Methods A total of 162 patients receiving adjuvant chemotherapy for breast cancer from December 2015 to June 2017 were selected and divided into observation group and control group by silver coin method. Patients in the observation group were given a single injection of PEG-rhG-CSF 100 μg/kg per cycle, and the control group was given a daily injection of recombinant human granulocyte colony-stimulating factor(rhG-CSF) at 5 μg/kg for 7 consecutive days. The clinical efficacy and safety of the two groups were observed and compared. Results The incidence of Ⅳ degree of neutropenia and delayed chemotherapy in the observation group was significantly lower than that in the control group(P<0.05). The incidence of adverse reactions such as skeletal muscle pain, fever and fatigue in the observation group was significantly lower than that in the control group(P<0.05). Conclusion PEG-rhG-CSF can significantly reduce the incidence of neutropenia and delayed chemotherapy in patients receiving adjuvant chemotherapy for breast cancer, and it is more convenient with fewer side effects and better patient compliance.
[Key words] Post-adjuvant-chemotherapy for breast cancer; Pegylated recombinant human granulocyte colony-stimulating factor; Recombinant human granulocyte colony-stimulating factor; Neutropenia
乳腺癌是全世界女性最常見的恶性肿瘤,在我国乳腺癌发病率亦高居女性恶性肿瘤之首,且仍在快速增长[1,2]。手术是治疗乳腺癌的首选治疗方案,术后辅助化疗可以明显改善患者的无病生存与总生存率[3,4]。但辅助化疗极易引起中性粒细胞减少,轻者使患者无法按期、足量完成疗程,以致影响辅助化疗效果,重者可诱发粒细胞缺乏性发热,甚至出现难以控制的致死性感染[5]。预防性使用重组人粒细胞集落刺激因子(Recombinant human granulocyte colony stimulating factor,rhG-CSF)能避免中性粒细胞减少,但骨骼肌肉疼痛明显,且需每日去医院注射,患者依从性差[6]。聚乙二醇化重组人粒细胞集落刺激因子(Pegylated recombinant human granulocyte colony-stimulating factor,PEG-rhG-CSF)是将重组人粒细胞集落刺激因子经聚乙二醇化学修饰后制成的制剂,具有体内半衰期长、耐受性好、一个化疗周期只需用药一次的优点[7,8]。本研究分析乳腺癌辅助化疗中使用PEG-rhG-CSF预防中性粒细胞减少的疗效,同时观察其安全性,现报道如下。
1 资料与方法
1.1一般资料
选取2015年12月~2017年6月期间在我院就诊的乳腺癌术后行辅助化疗的患者共162例。纳入标准[9]:(1)符合2017年中国抗癌协会乳腺癌专业委员会制定的乳腺癌诊治指南与规范中的诊断标准,且通过手术病理活检确诊;(2)均为女性患者,年龄18~75岁。排除标准[10]:(1)患者术后无需接受化疗或不愿接受化疗;(2)近期3个月因其他疾病接受过化疗或6个月内接受过放疗;(3)伴有其他原因或服用药物可能导致骨髓抑制;(4)有器官移植或骨髓移植病史。采用抛银币法分为观察组和对照组。两组患者的年龄、病程等一般资料比较无明显统计学差异(P>0.05)。见表1。
1.2 治疗方法
所有患者均采用EC×4序贯T×4方案进行化疗:盐酸表阿霉素(浙江海正药业股份有限公司,国药准字:H19990280,规格:10 mg)100 mg/m2+环磷酰胺(江苏恒瑞医药股份有限公司,国药准字:H32020856,规格:0.1 g)600 mg/m2×4疗程序贯多西他赛(浙江海正药业股份有限公司,国药准字:H20093092,规格:0.5 mL:20 mg/s)100 mg/m2×4疗程,21 d重复1个疗程,共4个疗程。观察组患者在化疗后24~48 h内应用PEG-rhG-CSF(商品名:新瑞白,齐鲁制药有限公司,国药准字:S20150013,规格:3.0 mg:1.0 mL)100 μg/kg每周期单次注射,对照组患者在化疗24 h后应用rhG-CSF(商品名:瑞白,齐鲁制药有限公司,国药准字:S20063065,规格:100 μg:0.6 mL)每日注射1次,每次5 μg/kg,连续7 d。如果出现难以耐受的骨骼肌肉疼痛,以对乙酰氨基酚片(国药集团广东环球制药有限公司,国药准字:H44023356,规格:0.5 g×10 s)口服对症处理。观察并比较两组患者的临床疗效及安全性。
1.3 观察指标
1.3.1 Ⅳ度中性粒细胞缺乏及延迟化疗评估标准 分别在化疗第5天、第8天、第11天采空腹静脉血查血常规,观察中性粒细胞的变化,当中性粒细胞绝对计数<0.5×109/L时确定为Ⅳ度中性粒细胞缺乏,下次化疗前中性粒细胞绝对计数<3.0×109/L需延迟化疗。
1.3.2 不良反应发生情况 化疗后观察不良反应发生情况,包括乏力、发热及骨骼肌肉疼痛等。
1.4统计学方法
使用SPSS20.0 for windows统计学软件,计数资料比较采用χ2检验,计量资料使用均数±标准差(x±s)表示,比较采用t检验。以P<0.05为差异有统计学意义。
2 结果
2.1 两组患者治疗后Ⅳ度中性粒细胞缺乏及延迟化疗发生率比较
观察组患者治疗后Ⅳ度中性粒细胞缺乏及延迟化疗的发生率均少于对照组患者,差异有统计学意义(P<0.05)。见表2。
2.2 两组患者治疗后不良反应发生情况比较
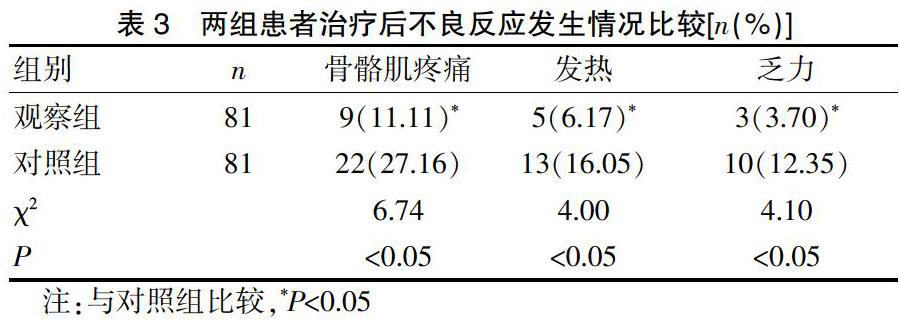
观察组患者治疗后骨骼肌疼痛、发热、乏力等不良反应的发生率低于对照组,两组不良反应数据比较差异有统计学意义(P<0.05)。见表3。
3讨论
随着乳腺癌诊治水平的提高,其死亡率有所下降,这主要归功于乳腺癌综合治疗的发展[11,12]。尤其是上世纪70年代Bonadonna对乳腺癌术后环磷酸胺、氨甲蝶吟、5-氟尿嘧啶(CMF)等辅助化疗进行临床研究,对患者进行近30年的随访,结果显示可以明显改善患者无病生存和总生存,由此临床研究确立乳腺癌术后辅助化疗在乳腺癌治疗中的地位。在乳腺癌的治疗过程中,无论患者处于疾病的早期,还是处于晚期复发转移阶段,化疗均占据着重要地位。对处于乳腺癌早期的患者使用化疗可以明显减少复发转移的风险,对处于乳腺癌晚期的患者使用化疗可以缓解病情进展,延长生存时间,提高生活质量,所以其在乳腺癌治疗中的基石地位不可动摇。而乳腺癌术后采用辅助化疗的目的是杀灭亚临床微转移灶,降低术后复发及远处转移的风险,随着蒽环类、紫杉类药物的相继出现,又大大提高了术后辅助化疗的效果[13,14]。但是,蒽环类、紫杉类药物联合应用的化疗方案属于高强度方案,极易引起Ⅳ度中性粒细胞减少,轻者使患者无法按期、足量完成疗程,影响辅助化疗效果,重者可诱发粒细胞缺乏性发热,甚至出现难以控制的致死性感染,有研究显示采用标准剂量的蒽环类、紫杉类化疗后中性粒细胞减少性发热的发生率达33%[15]。因此,乳腺癌患者在术后辅助化疗期间,大部分需要粒细胞集落刺激因子进行一级预防或二级预防,才能在保障化疗强度的前提下,按期完成预定的化疗疗程[16]。
rhG-CSF是防治肿瘤放化疗所致中性粒细胞减少症的有效药物,是化疗规范实施的重要保障之一[17],但是常规rhG-CSF半衰期短,仅为3~4 h,需要每日给药[18]。中国医学科学院北京协和医学院数据显示,对于强度并不很高的化疗方案,预防性使用rhG-CSF 的平均时间为9.57 d,应用更高强度的化疗方案时,使用rhG-CSF的中位时间为10~11 d,不仅患者的依从率较低,医护人员的工作量增加,并且药物费用也较高[19]。有研究表明,长效制剂PEG-rhG-CSF的药物耐受性更好,单次给药后缓解中性粒细胞抑制的效果比多次给予常规rhG-CSF的效果更強,疗效维持的时间也更长。据此认为,预防性应用PEG-rhG-CSF比预防性和延迟性应用rhG-CSF效能更优[20]。本研究结果也提示,在乳腺癌术后高强度的辅助化疗领域,每化疗周期1剂PEG-rhG-CSF预防性应用比连续7 d预防性应用rhG-CSF效能更优。这是由于长效制剂相对于常规rhG-CSF半衰期更长,不易被酶水解和肾脏清除,因此能动员出更多的造血干细胞和分化细胞。本组资料还显示,乳腺癌患者术后辅助化疗期间,单次注射长效制剂PEG-rhG-CSF预防化疗所致中性粒细胞减少症的副反应比连续7 d注射rhG-CSF的副反应要少,与对照组患者相比,观察组出现骨骼肌肉疼痛、发热及乏力的几率明显较少。这是由于注射长效制剂1个周期仅需1次,因此骨骼肌疼痛更少,而持续的骨骼肌肉疼痛是乳腺癌患者辅助化疗期间不愿意接受连续多日注射rhG-CSF的主要原因,长效制剂PEG-rhG-CSF的出现,为乳癌患者提供了一个新的选择,使其有可能在更少的痛楚下按期、足量地完成辅助化疗疗程。同时由于长效制剂的平稳释放,患者发热、乏力等情况出现的也较少。
总之,PEG-rhG-CSF能够明显降低乳腺癌辅助化疗患者中性粒细胞减少及延迟化疗的发生,且用药更为方便易行,副反应小,患者的依从性更好。
[参考文献]
[1] 姚娜,黄华兴,夏添松,等. TMEM158在乳腺癌的表达及其对乳腺癌细胞迁移侵袭能力的影响[J]. 中国肿瘤外科杂志,2018,10(2):81-86.
[2] Fan L,Strasser-Weippl K,Li JJ,et al. Breast cancer in China[J]. Lancet Oncol,2014,15(7):e279-289.
[3] 李永峰,陈杰,谢尚闹,等. 两种新辅助化疗方案对乳腺癌患者近期疗效及生存率的影响[J]. 中国现代医生,2015,53(32):84-86.
[4] Patel T,Gupta A,Shah M. Pathological predictive factors-for tumor response in locally advanced breast carcinomastreated with anthracycline-based neoadjuvant chemo-therapy[J]. J Cancer Res Ther,2013,9(2):245-249.
[5] Shi YK,Chen Q,Zhu YZ,et al. Pegylatedfilgrastim is comparable with filgrastim as support for commonly used chemotherapy regimens:a multicenter,randomized,cros-sover phase 3 study[J].Anticancer Drugs,2013,24(6):641-647.
[6] Pawloski PA,Larsen M,Thoresen A,et al. Pegfilgrastim use and bone pain: a cohort study of community-based cancer patients[J].J Oncol Pharm Pract,2016,22(3):423-429.
[7] 石远凯,许建萍,吴昌平,等. 聚乙二醇化重组人粒细胞刺激因子预防化疗后中性粒细胞减少症的多中心上市后临床研究[J]. 中国肿瘤临床,2017,44(14):679-683.
[8] Shin KH,Lim KS,Lee H,et al. An assessment of the pharmacokinetics,pharmacodynamics,and tolerability of GCPGC,a novel pegylated granulocyte colony-stimulating factor(G-CSF),in healthy subjects[J]. Invet New Drugs,2014,32(4):636-643.
[9] 中国抗癌协会乳腺癌专业委员会. 中国抗癌协会乳腺癌诊治指南与规范(2017年版)[J].中国癌症杂志,2017, 27(9):695-756.
[10] 黄倩,钟亚春,徐曼. BRCA1和BRCA2阴性家族性与散发性乳腺癌患者临床特征及影响新辅助化疗疗效的因素分析[J]. 临床和实验医学杂志,2018,17(8):861-864.
[11] 王涛武. 乳腺癌手术治疗以及综合治疗的效果分析[J]. 中國医药指南,2016,14(18):153-154.
[12] Beaver K,Williamson S,Briggs J. Exploring patient experiences of neo-adjuvant chemotherapy for breast cancer[J]. European Journal of Oncology Nursing,2016,20(2):77-86.
[13] Therasse P,Mauriac L,Welnicka-Jaskiewicz M,et al. Final results of a randomized phase III trial comparing cyclophosphamide,epirubicin,and fluorouracil with a dose-intensified eporubicin and cyclophamicle+filgrastimas neoadjuvant treatment in locally advanced breast cancer:An EORTC-NCIC-SAKK multicenter study[J]. Journal of Clinical Oncology,2013,21(5):843-850.
[14] Raphael MJ,Biagi JJ,Kong W,et al. The relationship between time to initiation of adjuvant chemotherapy and survival in breast cancer:A systematic review and meta-analysis[J]. Breast Cancer Res Treat,2016,160(1):17-28.
[15] 俞铭洁,吴雯婷,倪婷婷,等. 聚乙二醇化重组人粒细胞集落刺激因子用于卵巢癌及宫颈癌化疗的价值[J]. 浙江医学,2017,39(4):307-314.
[16] Madry R,Poplawska L,Haslbauer F,et al. Results of a prospective dose intensity and neutropenia prophylaxis evaluation programme(DIEPP) in cancer patients at risk of febrile neutropenia due to myelosuppressive chemotherapy[J]. Wiener Klinische Wochenschrift,2016,128(7-8):238-247.
[17] Renwick W,Pettengell R,Green M. Use of filgrastim and pegfilgrastim to support delivery of chemotherapy:Twenty years of clinical experience[J]. Bio Drugs,2009,23(3):175-186.
[18] Yanai H,Endo K,Matsumoto M,et al. The clinical utility of pegfilgrastim in combination with adjuvant FEC(100)and TC chemotherapy for breast cancer[J]. Gan To Kagaku Ryoho,2016,43(9):1087-1090.
[19] 杨晟,何小慧,刘鹏,等. 化疗后预防性使用重组人粒细胞集落刺激因子的持续时间及其影响因素[J]. 中华肿瘤杂志,2016,38(1):69-72.
[20] 刘芳,俞伟,梁岚清,等. 聚乙二醇重组人粒细胞集落刺激因子预防头颈部肿瘤同步放化疗后中性粒细胞减少症的研究[J]. 中国临床保健杂志,2015,18(4):386-389.
