0.03%他克莫司软膏长期间歇维持治疗儿童特应性皮炎的多中心随机对照临床研究
2019-09-24梁源刘玲玲王珊赵作涛马琳向欣顾恒陈崑王华易红陈瑾萍张金桃姚志荣郭一峰陈戟程颖朱学骏
梁源 刘玲玲 王珊 赵作涛 马琳 向欣 顾恒 陈崑 王华 易红 陈瑾萍 张金桃 姚志荣 郭一峰 陈戟 程颖 朱学骏
1首都医科大学附属北京儿童医院皮肤科国家儿童医学中心100045;2北京大学第一医院皮肤科皮肤病分子诊断北京市重点实验室100034;3中国医学科学院北京协和医学院皮肤病医院,南京210042;4重庆医科大学附属儿童医院皮肤科400014;5广州市儿童医院皮肤科510120;6上海交通大学医学院附属新华医院皮肤科200092;7上海儿童医学中心皮肤科200127
特应性皮炎(AD)是儿童最常见的瘙痒性炎症性皮肤病,其病程慢性持续,皮损反复发作伴剧烈瘙痒,因此长期管理和防止复发是治疗的重点。他克莫司软膏是经过大量循证医学研究充分证实对AD有效的第一个非激素类、可长期使用的外用抗炎药,主要用于中重度AD的治疗[1]。与糖皮质激素(简称激素)相比,外用他克莫司软膏与皮肤亲和力强,透皮吸收率低,且不影响成纤维细胞和血管内皮细胞功能,不良反应较少[2-6]。一项对267例2~15岁AD患儿进行的临床观察证实,欧洲白色人种AD患儿每周2次外用0.03%他克莫司软膏长期间歇维持治疗对于减少AD复发、延长复发间隔时间安全有效[7]。我们在国内首次采用随机对照试验观察0.03%他克莫司软膏每周2次长期间歇维持治疗对减少中国儿童中重度AD复发次数、延长复发间隔时间的有效性和安全性。
对象与方法
一、试验设计
2012年9月至2013年11月在北京大学第一医院、首都医科大学附属北京儿童医院、中国医学科学院皮肤病医院、重庆医科大学附属儿童医院、广州儿童医院、上海交通大学医学院附属新华医院、上海儿童医学中心共7个中心开展随机、开放、对照临床试验。试验设计参考文献[7],分为两个阶段。第一阶段,全部患儿均每日2次外用0.03%他克莫司软膏治疗,最长6周;第一阶段结束时,研究者总体评估(investigator′s global assessment,IGA)评分≤2分的患儿进入第二阶段,按照1∶1的比例随机分配至试验组(每周周一和周四2次外用0.03%他克莫司软膏间歇维持治疗)和对照组(不进行维持治疗)。AD急性复发(IGA评分>2)时,两组患儿均接受0.03%他克莫司软膏每日2次的常规治疗直至IGA评分≤2,整体观察期为6个月。患儿分别在第一阶段基线、2、4、6周和第二阶段第2周及2、4、6个月时接受随访,由研究者进行临床疗效和安全性评估,本研究经北京大学第一医院医学伦理委员会批准(SFDA批件号为2012B00260)。
二、病例选择
1.入选标准:2012年9月至2013年11月在全国7个中心皮肤科门诊收集就诊的2~15岁AD患儿。第一阶段入选标准:符合AD的Williams诊断标准[8-10],并以Rajka和Langeland标准[11]判断为中重度,试验期间能遵守用药要求;复发时,患儿可在3 d内返院。全部患儿家长或监护人均签署知情同意书,如果患儿能够理解研究目的和风险,也需签署知情同意书。第二阶段入选标准:完成第一阶段治疗,且第一阶段治疗结束后IGA≤2分。
2.排除标准:已知对他克莫司软膏中任何成分或大环内酯类药物过敏;AD皮损区域有严重的皮肤感染;患有严重肝肾疾病、血液系统疾病、自身免疫性疾病、慢性严重感染、糖尿病或精神疾病,有吸毒或酗酒行为等;患有恶性肿瘤或其他可能影响正确评估疗效的严重疾病;曾外用激素或其他免疫抑制剂药物且停药时间<1周,系统用激素或其他免疫抑制剂(环孢素、甲氨蝶呤、雷公藤等)停药时间<4周,光疗停止治疗时间<6周;1个月内参加过其他临床研究;研究者认为不能入选的其他原因(如依从性差、不能按期随诊)。
3.退出标准:患儿撤回知情同意;失访者;严重违反方案;第一阶段结束时IGA评分≤2分,但结束后7 d内IGA评分>2分;第二阶段复发时,经他克莫司软膏治疗6周IGA评分仍>2分;研究者认为终止治疗对受试者最有益。
三、用药方法
试验药物为0.03%他克莫司软膏[安斯泰来制药(中国)有限公司免费提供],规格为10 g/支。第一阶段全部患儿每日2次外用0.03%他克莫司软膏,疗程2~6周,IGA评分≤2者进入第二阶段[7]。第二阶段试验组患儿每周(周一和周四)2次外用0.03%他克莫司软膏,对照组在第二阶段开始后不进行维持治疗。两组患儿在两个阶段均常规使用润肤剂,如疾病复发,接受为期2~6周的他克莫司软膏每天2次的常规治疗及随访。观察期为6个月。治疗期间禁止的合并治疗包括紫外线光疗(长波或中波紫外线)、系统性激素、系统用非甾体类免疫抑制剂、其他外用药(如煤焦油、激素、同类免疫调节剂等)和其他临床研究药物。
四、疗效评估
1.主要疗效指标:首次复发时间,定义为第一阶段治疗结束至第一次复发(IGA>2)的天数。
2.次要疗效指标:包括第二阶段AD复发率、复发次数、复发时AD严重程度[用湿疹面积和严重程度指数(eczema and severity index,EASI)评估]、复发持续时间、复发时瘙痒评分[用视觉模拟尺(visual analog scale,VAS)评估,部分患儿由家长代为评分],以及他克莫司使用总量和第二阶段的总有效率。总体改善率=治疗前后EASI评分之差/基线EASI评分×100%,其中≥90%为痊愈,60%~89%为显效,20%~59%为进步,<20%为无效,痊愈率和显效率合计为总有效率。
3.安全性评估:研究期间主要采用研究者或患儿/监护人报告的不良事件发生率、异常的生命体征、体检等进行评估。
五、统计方法
应用SAS 9.1.3(TS1M3)软件进行统计学分析。计量资料符合正态分布时用两组独立样本t检验进行分析,如果不符合正态分布则用非参数秩和检验;计数资料采用卡方检验;采用Kaplan-Meier法对首次复发时间进行生存分析,计算中位生存时间(无复发时间)。采用双侧假设检验,P<0.05为差异有统计学意义。
结 果
一、临床疗效评估
1.试验完成情况:共171例中重度AD患儿进入第一阶段,其中125例(73%)在第一阶段结束时达到IGA评分≤2,进入第二阶段,包括试验组62例、对照组63例,两组间性别、年龄、身高、体重和体重指数以及进入第二阶段研究时EASI评分、IGA评分和瘙痒视觉模拟尺(VAS)评分差异均无统计学意义(P>0.05),见表1。11例在第二阶段因失访和违背方案等原因退出或中止治疗,脱落率为12%;因无有效随访资料剔除4例,剔除率为3.2%。共121例纳入全分析集(FAS)和安全性分析集(SS),包括试验组60例、对照组61例;110例纳入符合方案分析集(per-protocol set,PPS),每组55例。
2.首次复发时间:第二阶段FAS集试验组与对照组的首次复发时间分别为(46.9±37.7)d和(28.8±32.3)d(Z=1 093.50,P=0.020),Kaplan-Meier曲线显示进入第二阶段后在6个月的随访期内保持不复发的患儿比例在试验组显著高于对照组,差异有统计学意义(Z=1 093.50,P=0.020),见图1。
3.第二阶段复发的患儿例数及次数:第二阶段期间,FAS集试验组60例中25例(41.7%)复发,对照组61例中46例(75.4%)复发,试验组复发率显著低于对照组(χ2=14.20,P<0.001)。试验组总复发次数为31次,每例复发(0.52±0.68)次,对照组总复发86次,每例复发(1.41±1.23)次,试验组每例复发次数显著低于对照组(t=4.96,P<0.001)。
4.其他疗效评估指标:第二阶段FAS集两组患儿在复发期间AD严重程度评分(EASI)、复发持续时间和瘙痒评分(VAS)差异均无统计学意义(P>0.05),见表2。第二阶段结束时,试验组总有效率为83.3%(50/60),对照组为75.4%(46/61),差异无统计学意义(χ2=1.16,P=0.280)。试验组他克莫司总用量为(8.0±7.0)支,高于对照组(4.2±6.9)支(成组T′检验,T′=3.01,P=0.003)。但是,他克莫司软膏日用量在试验组为(0.06±0.06)支,对照组(0.09±0.09)支,对照组较试验组显著增加(成组T′检验,T′=-2.23,P=0.028)。

表1 第二阶段两组特应性皮炎患儿人口统计学资料及病情评分比较
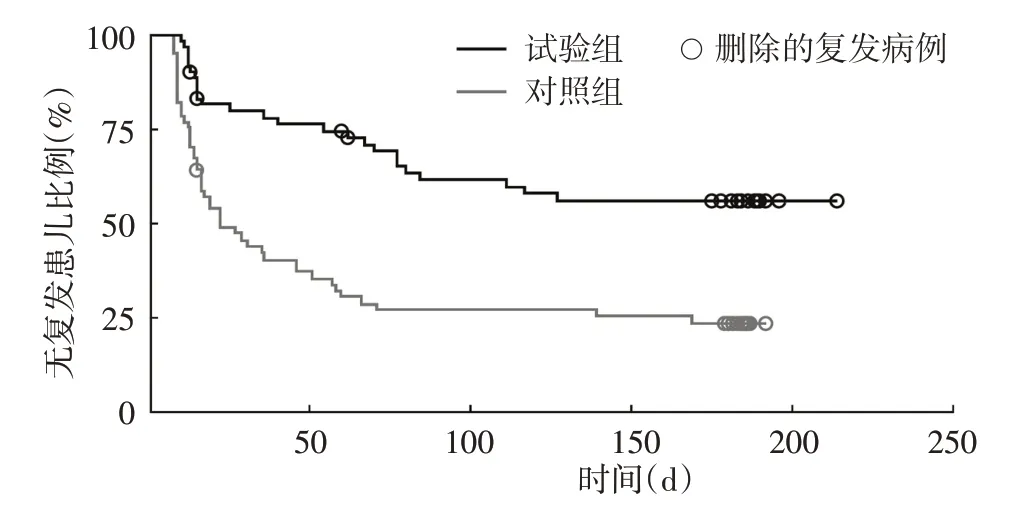
图1 Kaplan-Meier曲线显示随时间推移在全分析集中无复发的特应性皮炎患儿的比例

表2 两组特应性皮炎患儿全分析集在试验第二阶段复发时次要疗效指标比较[M(P0,P100)]
二、安全性评估
在第一阶段,23例患儿(13.5%)报告34件不良事件,均为轻中度。在第二阶段,试验组16例(26.7%)报告19次不良事件,对照组16例(26.2%)报告27次不良事件,见表3。所有不良事件的严重程度均为轻中度。试验组中6例(10.0%)和对照组中4例(6.6%)发生与他克莫司相关的不良反应,其中试验组最常见的不良反应为脓疱疹(4例),另有2例发生传染性软疣;对照组中最常见的不良反应为脓疱疹(2例)和毛囊炎(2例)。两组间第二阶段不良反应发生率和构成比差异均无统计学意义(连续校正卡方检验,χ2值分别为0.13、0.99,P值分别为0.72、0.32)。

表3 两组特应性皮炎患儿不良事件发生情况[安全分析集,例(%)]
讨 论
以往AD长期治疗的理念为每日应用润肤剂,在发作期外用抗炎药物如激素或钙调磷酸酶抑制剂等对症治疗,这种发作期给药、以按需为基础的常规治疗方案被称为反应性或被动治疗(reactive therapy)[12-13]。大量研究显示,AD患者外观正常的未受累皮肤也呈现出皮肤结构、屏障功能以及免疫功能的异常改变,活动期皮损消退后,貌似正常的皮肤也存在亚临床炎症反应[14-16],Wollenberg和Bieber[17]因此提出“主动治疗(proactive therapy)”的新概念,即发作早期使用集中强化的抗炎治疗至皮损全部或大部分消退后,在原来的受损部位继之以长期、小剂量、间歇外用抗炎治疗,联合外用润肤剂,目的是通过皮损部位使用最少量药物和具有修复皮肤屏障功能作用的保湿剂来控制残留的亚临床炎症,从而阻止、推迟和减少AD发作,保持长期临床缓解状态。早期研究显示,缓解期间断外用激素的治疗方案可以降低复发风险并延长缓解时间[18-19],然而,儿童患者长期外用中强效激素可伴发皮肤萎缩、萎缩纹、色素减退和继发感染等不良反应[20-22]。
本研究为国内首次比较0.03%他克莫司软膏每周2次长期间歇维持治疗与常规治疗方案对中重度AD患儿的有效性和安全性的大规模多中心随机对照临床研究,结果显示,与采用传统的反应性治疗的对照组AD患儿相比,使用主动治疗的试验组AD患儿首次复发时间比对照组延长,复发率(41.7%)低于对照组(75.4%),6个月随访期内保持不复发的患儿比例也显著高于对照组。生存分析评估显示,0.03%他克莫司软膏每周2次间歇维持主动治疗可以有效减少AD的复发次数,延长复发间期,维持AD的长期稳定,与欧洲和美国的类似研究结果一致[23-25]。此外,在第二阶段结束后两组患儿总有效率相似,第二阶段中每次复发时疾病严重程度、复发持续时间和瘙痒评分等指标在两组间差异均无统计学意义,但对照组他克莫司软膏的日均用药量为试验组的1.5倍,尽管试验组总用药量增加,但复发次数和复发持续时间明显减少,日均用药量减少,疾病控制满意,从而可提高家长依从性,最终实现对AD患儿的长期有效管理[23-29]。
在本研究第一阶段为期6周和第二阶段为期6个月的随访期内,所有患儿对0.03%他克莫司软膏耐受性良好,无严重不良事件发生。与他克莫司软膏相关的最常见不良反应主要为局部烧灼感,但可自行缓解,另一常见不良反应为皮肤感染如脓疱疹、毛囊炎和传染性软疣,与此前每周2次间歇治疗或每日2次0.03%他克莫司软膏常规治疗的临床研究结果一致[2,22,26-29]。
本研究第一阶段入组171例中重度AD患儿,经过为期2~6周每日2次外用0.03%他克莫司软膏的常规治疗后,125例患儿皮损全部或大部分消退,顺利进入第二阶段的治疗,但是仍有46例患儿在6周时IGA>2分,因此被排除在第二阶段外。对于部分严重AD,0.03%他克莫司软膏治疗6周可能时间尚短或是患儿对他克莫司治疗的敏感性较低,因此本研究结果可能会向对他克莫司治疗敏感的AD患儿偏倚。
总之,本研究证实,在充分抗炎基础上,0.03%他克莫司软膏长期间歇外用的主动治疗方案可以有效延长中国儿童中重度AD的首次复发时间,预防和减少复发并延长复发间期。同时,与传统的被动治疗方案相比,主动治疗方案使患儿日平均用药量减少一半且耐受性良好,并未增加药物相关的不良反应。
利益冲突安斯泰来制药(中国)有限公司作为本次临床试验的申办方,免费提供试验药物0.03%他克莫司软膏,并参与试验方案设计和试验结果的统计分析。所有作者均声明不存在利益冲突
志谢参加本试验的研究者、医学统计专家、受试患儿及家长
