rGO/TNTs复合光催化剂的制备及其降解苯酚的性能研究
2019-09-19李红艳程济慈李尚明
李红艳,程济慈,张 峰,王 芳,李 超,李尚明
(1.太原理工大学 环境科学与工程学院,山西 晋中 030600;2.山西省市政工程研究生教育创新中心,山西 晋中 030600;3.山西省生物研究院有限公司 食用菌研究中心,太原 030006;4.首安工业消防有限公司 第一设计部,北京 101304;5.太原理工大学 材料科学与工程学院,太原 030024)
二氧化钛(TiO2)晶体因具有粒径小、比表面积大、界面原子占比较大等特点,是目前被广泛深入研究的光催化剂之一[1]。但TiO2禁带宽度较宽,只能吸收利用占太阳光总能量约4 %的紫外光部分,由P25为前驱体合成的二氧化钛纳米管(TNTs)比TiO2具有更高的比表面积和改进的光催化性能,但TNTs仍存在光生电子和空穴易复合的问题。二维碳原子晶体石墨烯具有优异的机械性能[2-3]、良好的导电导热性[4-5]和巨大的比表面积[6-7]。GO与TNTs结合增加TNTs的比表面积、拓宽TNTs的光响应范围和降低光生电子和空穴对的复合率。QI et al[8]将氧化石墨烯(GO)与TiO2结合制得GO/TiO2纳米管,对亚甲基蓝的降解率比TNTs提高了20%.
苯酚是一种高致癌物[9],我国“水中优先控制污染物”中,苯酚被列为有毒性和致癌的危险品之一。美国环保局《饮水规程和健康建议》中列出200种有机物的毒性、对人体的危害和标准规定的浓度值,其中苯酚2.56 mg/L对淡水水生生物产生慢性毒性,3.5 mg/L是对人体产生危害的极限质量浓度,0.3 mg/L是保证河水不产生味道的限定质量浓度[10]。
本文采用浓碱水热法,将P25煅烧后制备TNTs,方法简单且价廉易得。用Hummers法将石墨超声后制备GO,水热法将GO与TNTs复合制备还原氧化石墨烯/二氧化钛钠米管(rGO/TNTs).通过研究rGO/TNTs对苯酚降解的动力学特征来研究其光催化效能,并为rGO/TNTs降解苯酚废水的实际应用奠定理论基础。
1 仪器、试剂与方法
1.1 仪器与试剂
仪器:100 mL反应釜(上海一凯仪器设备有限公司)、FE20精密pH计(梅特勒托利多仪器(上海)有限公司)、STP型电子分析天平(上海上平仪器有限公司)、HJ-1型磁力搅拌器(天津红杉实验设备厂)、CMD-20X型烘箱(上海琅环实验仪器有限公司)、LD-4型离心机(常州天瑞仪器有限公司)、KQ-100M型超声波清洗机(科桥超声波设备有限公司)、GZZ10型10 W高压汞灯(上海季光特种照明电器厂)、GXZ500型500 W氙灯(上海季光特种照明电器厂)、XL-1型马弗炉(北京科伟永兴仪器有限公司)、752型紫外可见分光光度计(上海菁华科技仪器有限公司)等。
试剂:P25、苯酚、重铬酸钾、氢氧化钠、石墨粉、硝酸钠、高锰酸钾、浓硫酸、浓盐酸、过氧化氢溶液、乙二胺四乙酸二钠(EDTA-Na2)、异丙醇(IPA)、三氯甲烷等,均为分析纯。
1.2 实验方法
1.2.1浓碱水热法制备TNTs
将2.5 g P25分散在70 mL 10 mol/L NaOH溶液中搅拌2 h,所得悬浮液移至不锈钢高压釜中加热到130 ℃,水热反应72 h后离心收集,并用蒸馏水洗涤至中性;所得材料用1 mol/L HCl洗涤至pH值为1并浸泡1 h,用蒸馏水离心洗涤三次,然后于80 ℃烘箱烘干后研磨过200目筛;最后将粉末于400 ℃马弗炉中煅烧2.0 h,得到锐态矿相的TNTs.
1.2.2水热法制备rGO/TNTs
采用改进Hummers法制备氧化石墨烯(GO),将0.2 g TNTs和0.01 g GO加入到70 mL蒸馏水中,超声30 min后所得混合液移至不锈钢高压釜中加热,于180 ℃下水热反应3 h完成复合过程。离心收集悬浮液,用蒸馏水洗涤3次,在60 ℃真空烘箱中烘干即得rGO/TNTs.
1.2.3材料表征
样品形貌采用扫描电子显微镜(SEM,Japan;JEOL JSM-7800F)表征;样品表面官能团及化学成分采用傅里叶红外吸收光谱(FTIR,Germany,TENSOR27)进行分析;样品元素种类和含量用X射线能谱(EDS,Japan,JEOL JSM-7800F)定量分析。
1.2.4光催化性能测试
室温下称取一定量rGO/TNTs光催化剂,加入到200 mL不同质量浓度的苯酚溶液中,暗反应30 min以达到rGO/TNTs-底物吸附平衡;然后在10 W紫外光和500 W可见光下进行光催化反应,每30 min取样5 mL离心分离10 min,用0.22 μm滤纸过滤后测定剩余苯酚质量浓度。分光光度法于270 nm波长下测试苯酚吸光度,由苯酚标线y=0.012 1x+0.0207,R2=0.999换算苯酚质量浓度,其中x为苯酚吸光度,y为其质量浓度。
1.2.5光催化反应动力学方程
本文采用一级反应动力学方程揭示rGO/TNTs对苯酚的光催化性能,进一步评估rGO/TNTs的降解反应速率和降解能力。一级反应动力学方程如下:
ln(ρt/ρ0)=-k·t.
(1)
式中:c0和ct分别为溶液中苯酚的初始质量浓度和t时刻质量浓度,mg/L;k为一级反应速率常数[11],1/min;t为反应时间,min.
不同条件实验数据拟合的一级反应动力学直线方程为:
y=k·x+b.
(2)
式中:y为-ln(ct/c0);x为反应时间,min;b为一级反应动力学拟合的直线方程常数。
2 光催化剂的表征分析
2.1 SEM表征分析
图1为样品的SEM表征图。GO呈透明的层状形态,厚度较薄,有褶皱。TNTs中观察到大量纳米管结构,表明通过浓碱水热法成功制备TNTs.纯TNTs的内径和外径分别约为3.5 nm和10 nm.rGO/TNTs中观察到TNTs附着在rGO纳米片的表面上,因rGO的屏蔽作用,rGO/TNTs的纳米管略微模糊。TNTs的微小尺寸、GO转化为rGO及TNTs与rGO表面之间的强相互作用均可提高rGO/TNTs的光催化活性。

图1 GO,TNTs和rGO/TNTs的SEM表征Fig.1 SEM of GO, TNTs and rGO/TNTs
2.2 FTIR表征分析

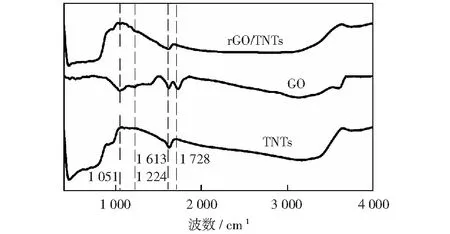
图2 样品的FTIR表征Fig.2 FTIR analysis of sample
2.3 EDS表征分析
图3和表1分别是rGO/TNTs的EDS图及样品的元素分析表。rGO/TNTs复合光催化剂主要含有C,O,Ti三种元素,表明GO和TNTs经超声水热反应后复合到一起。由表1可知GO中C,O含量较高。TNTs中Ti,O含量较高,还有一定量的N,可能是因P25易受潮烘干时空气中的N2所导致。rGO/TNTs中C含量比TNTs中C含量略微增加而O含量变化不大,这是因复合少量GO所致。rGO/TNTs的降解效果明显比TNTs好,推测起主要降解苯酚作用的元素可能是Ti,O和C.这与FTIR表征结果一致,即rGO/TNTs中产生Ti—O—C键,使其光催化效果提高。
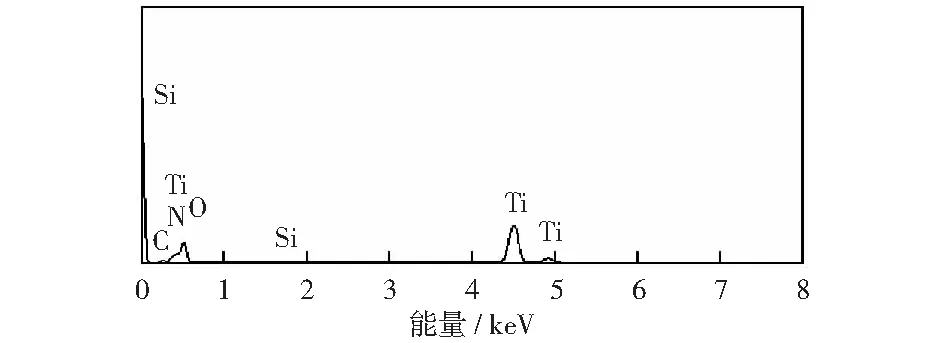
图3 rGO/TNTs的EDS图Fig.3 EDS of rGO/TNTs

Table 1 Ultimate analysis of samples %
3 结果与讨论
3.1 TNTs降解苯酚的光催化性能
0.5 g/L TNTs不同煅烧下温度对10 mg/L苯酚进行光催化降解,结果如图4(a),4(b)和表2所示。在不同煅烧温度下,TNTs对苯酚的降解满足一级反应动力学方程(R2≥0.95).400 ℃时TNTs对苯酚降解的反应速率常数最高,降解效果最好,450 ℃次之,300 ℃最差。这表明400 ℃煅烧温度使TNTs具有良好的晶型和较好的纳米管结构,450 ℃及以上煅烧温度下TNTs因高温使管状结构崩塌并且团聚较严重[12],300 ℃煅烧温度下TNTs虽有较好的管状结构但无较好的晶型。
3.2 rGO/TNTs降解苯酚的光催化性能
3.2.1苯酚初始质量浓度对降解率的影响
取0.5 g/L rGO/TNTs分别对1,5,10,20,30和50 mg/L的苯酚溶液进行光催化降解,结果如图5(a),5(b)和表3所示。由图5(a)可知,在苯酚质量浓度1~10 mg/L范围内,随苯酚质量浓度的增加光催化效果提高,苯酚降解率由78 %提高到95%,并在10 mg/L时光催化效果最好。但苯酚质量浓度继续增加,苯酚降解率将降低,rGO/TNTs光催化效果变差。由图5(b)和表3可知,在不同苯酚质量浓度下,rGO/TNTs复合光催化剂对苯酚的降解满足一级反应动力学方程(R2≥0.95).在1~10 mg/L范围内,随苯酚质量浓度的增加反应速率常数随之升高,当苯酚质量浓度为10 mg/L时,反应速率常数达最高,但当苯酚质量浓度超过10 mg/L之后,继续增加,反应速率常数逐渐降低。
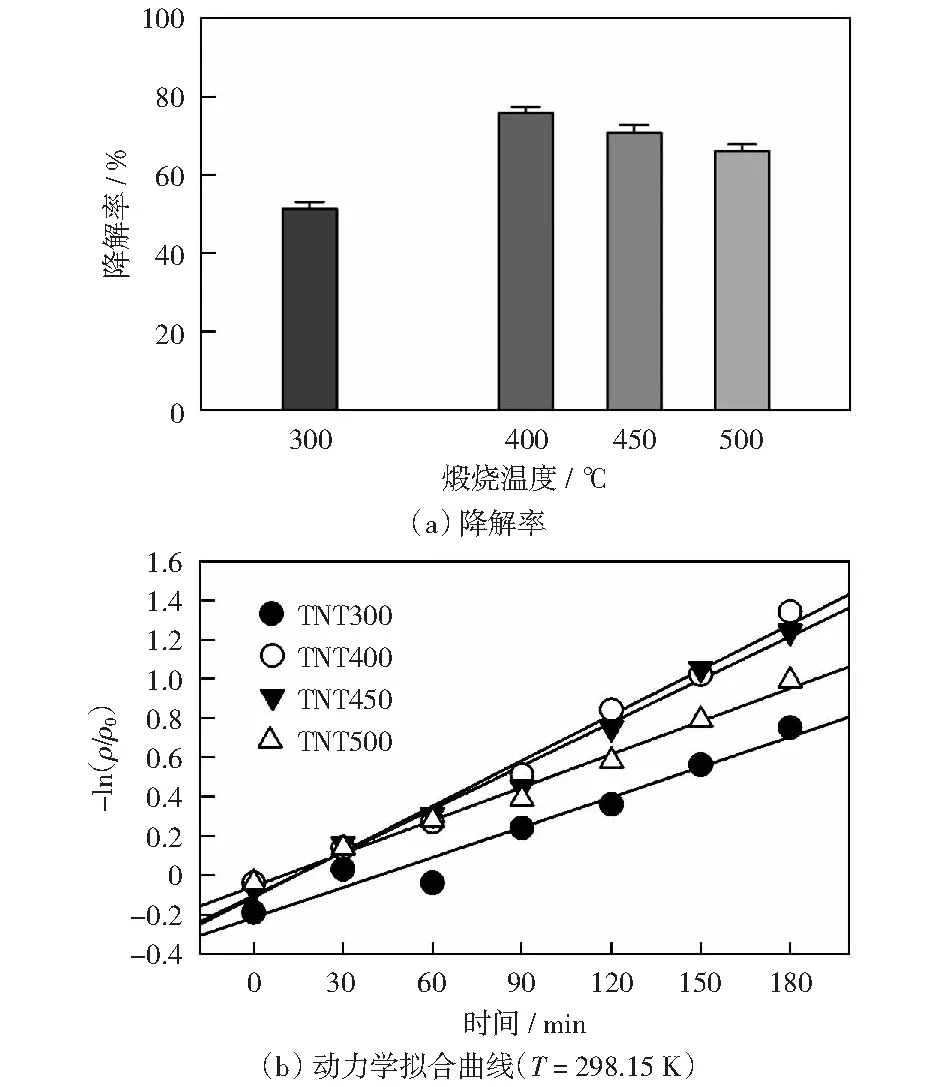
图4 不同煅烧温度下TNTs对苯酚的降解率的影响及动力学拟合曲线Fig.4 Degradation rate of phenol and kinetic fit of phenol degradation by TNTs at different calcination temperatures
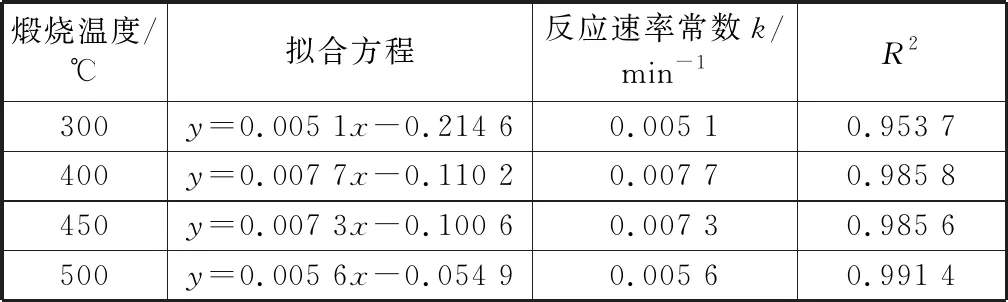
煅烧温度/℃拟合方程反应速率常数k/min-1R2300y=0.005 1x-0.214 60.005 10.953 7400y=0.007 7x-0.110 20.007 70.985 8450y=0.007 3x-0.100 60.007 30.985 6500y=0.005 6x-0.054 90.005 60.991 4
在光强和催化剂不变时,在相同时间内产生的光生电子和空穴数目是相同的。在污染物浓度较低时,过量的光催化剂会提供更多的反应活性位点。浓度越高需要被吸附的苯酚分子大量增加,然而反应活性位点数是一定的。因此,苯酚质量浓度越小,被降解去除的相对值也就越大;浓度质量越高,被降解去除的相对值也就越小。
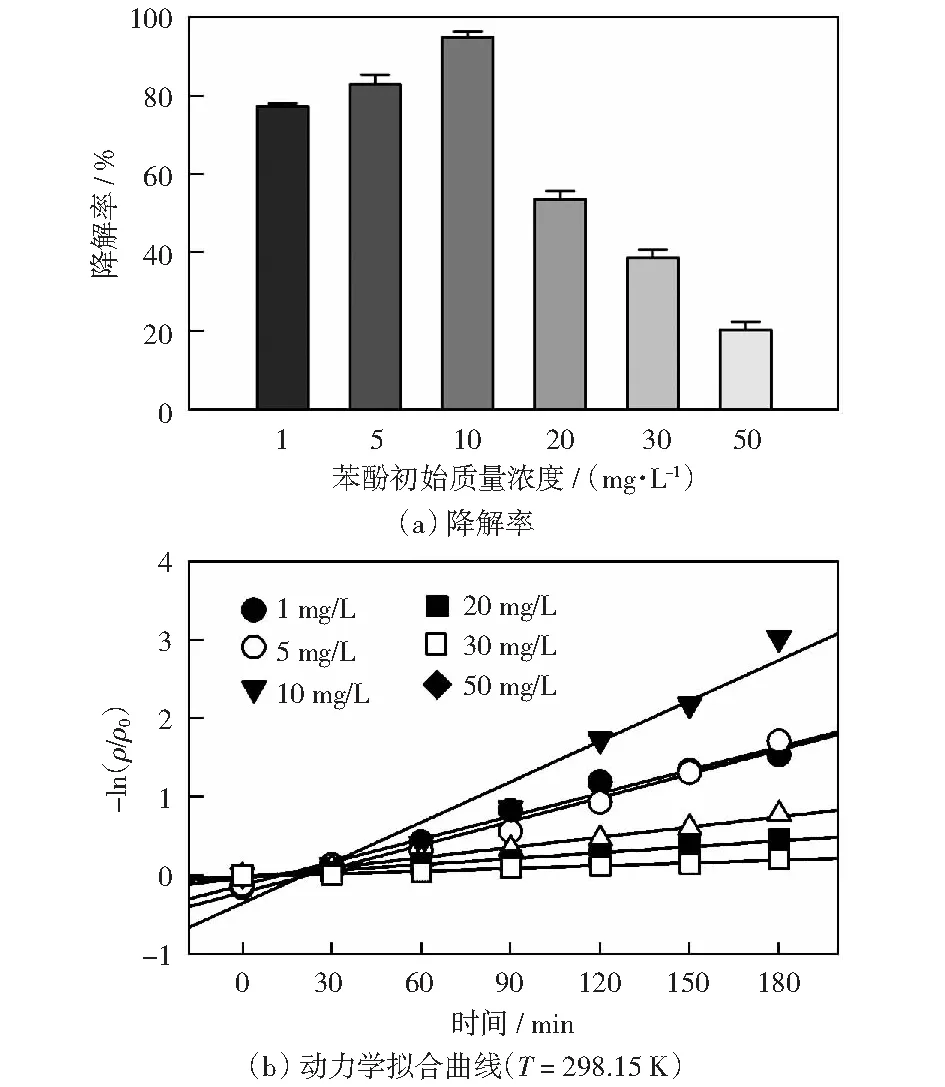
图5 不同苯酚初始质量浓度下rGO/TNTs对苯酚的降解率影响及动力学拟合Fig.5 Degradation rate of phenol and kinetic fit of phenol degradation by rGO/TNTs at different phenol initial mass concentrations
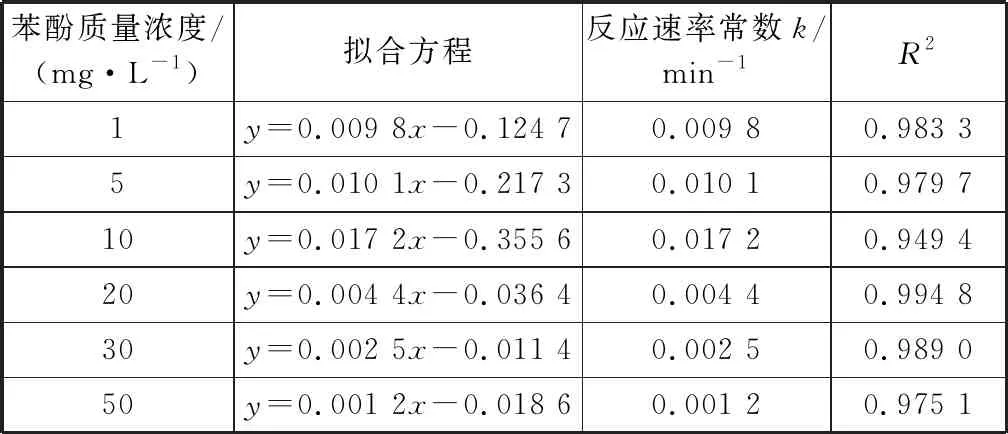
苯酚质量浓度/(mg·L-1)拟合方程反应速率常数k/min-1R21y=0.009 8x-0.124 70.009 80.983 35y=0.010 1x-0.217 30.010 10.979 710y=0.017 2x-0.355 60.017 20.949 420y=0.004 4x-0.036 40.004 40.994 830y=0.002 5x-0.011 40.002 50.989 050y=0.001 2x-0.018 60.001 20.975 1
3.2.2rGO/TNTs投加量对降解率的影响
取不同量的rGO/TNTs对10 mg/L的苯酚溶液进行光催化降解,结果如图6(a),6(b)和表4所示。由图6(a)可知,rGO/TNTs在0~0.5 g/L投加量范围内,随投加量的增加光催化效果提高,在0.5 g/L时,苯酚降解率最高达96.1%,光催化效果最佳。当超过0.5 g/L时,光催化剂投加量继续增加,苯酚降解率降低,光催化效果变差。由图6(b)和表4可知,不同rGO/TNTs投加量,rGO/TNTs对苯酚的降解满足一级反应动力学方程(R2≥0.95).投加量在0.1~0.5 g/L范围内,随投加量增加反应速率常数逐渐增加,在0.5 g/L时达到最大值。但随投加量继续增加,k值逐渐减小。

图6 不同rGO/TNTs投加量下苯酚的降解率及动力学拟合Fig.6 Degradation rate of phenol and kinetic fit of phenol degradation by rGO/TNTs at different rGO/TNTs dosages

rGO/TNTs投加量/(g·L-1)拟合方程反应速率常数k/min-1R20.10y=0.004 9x-0.239 30.004 90.958 70.25y=0.005 0x-0.140 00.005 00.955 70.50y=0.017 2x-0.355 60.017 20.949 40.75y=0.007 6x+0.017 80.007 60.996 31.00y=0.006 7x+0.019 20.006 70.995 2
在rGO/TNTs一定投加量范围内,随投加量增加苯酚的降解率逐渐增加。一方面是因为rGO/TNTs具有较好的表面吸附面积,即活性中心数量越多,苯酚被氧化降解的量就越多。另一方面是因rGO作为TNTs光生电子的载体,可将TNTs光生电子快速转移,使其在可见光范围的吸收增加,加速对苯酚的氧化降解,提高光催化效果。当投加量超过0.5 g/L后,苯酚的降解率随rGO/TNTs投加量的增加而减少,这是因rGO/TNTs的颗粒浓度过大,对紫外光产生反射和散射的作用,使得一部分紫外光不能被利用[13],降低了活性组分的利用率,使rGO/TNTs降解率随之降低。
3.2.3溶液pH值对rGO/TNTs降解率的影响
取0.5 g/L rGO/TNTs分别对pH值为4.0,5.0,6.5,8.0和9.0的苯酚溶液进行光催化降解,结果如图7(a),7(b)和表5所示。由图7(a)可知,酸性溶液中随pH值增加苯酚降解率升高,碱性溶液中随pH值增加苯酚降解率减小,且酸性溶液苯酚的降解率明显高于碱性时的降解率。当pH值为6.5时苯酚的降解率最高,即光催化效果最好。由图7(b)和表5可知,对不同pH值的苯酚溶液,rGO/TNTs对苯酚的降解满足一级反应动力学方程(R2≥0.91).酸性溶液苯酚降解的反应速率常数比碱性的反应速率常数高,当pH值为6.5时,苯酚降解反应速率常数最高,这是因为pH=6.5为rGO/TNTs的等电点,此时rGO/TNTs表面呈中性,光催化效果最好。

图7 不同溶液pH值下rGO/TNTs对苯酚的降解率影响及动力学拟合曲线Fig.7 Degradation rate of phenol and kinetic fit of phenol degradation by rGO/TNTs at different solution pH values
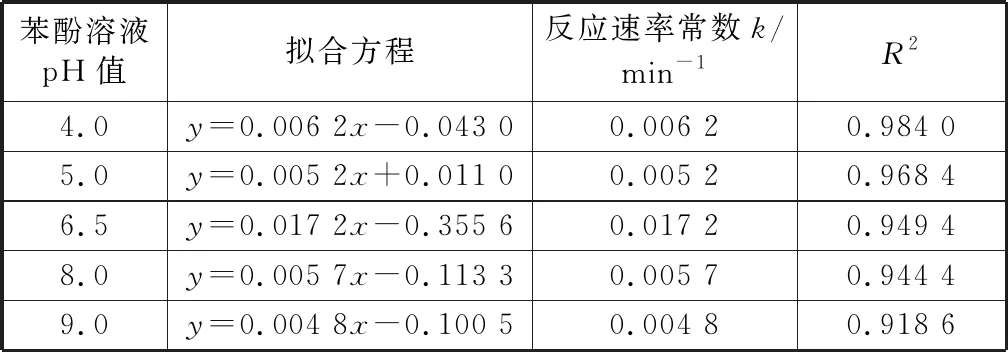
苯酚溶液pH值拟合方程反应速率常数k/min-1R24.0y=0.006 2x-0.043 00.006 20.984 05.0y=0.005 2x+0.011 00.005 20.968 46.5y=0.017 2x-0.355 60.017 20.949 48.0y=0.005 7x-0.113 30.005 70.944 49.0y=0.004 8x-0.100 50.004 80.918 6
在苯酚降解的光催化体系中,苯酚降解中间产物呈负电性,而rGO/TNTs具有表面双亲性。在酸性时,rGO/TNTs表面呈正电性,其有限的活性中心与苯酚中间产物结合,使苯酚降解率升高;而在碱性时,rGO/TNTs表面呈负电性,rGO/TNTs的活性中心与苯酚中间产物出现排斥现象,抑制rGO/TNTs的活性中心与苯酚相结合,使苯酚降解率降低。
3.2.4H2O2添加量对rGO/TNTs降解率的影响
H2O2协同rGO/TNTs(0.5 g/L)降解10 mg/L的苯酚溶液进行光催化降解,结果如图8(a),8(b)和表6所示。由图8(a)可知,添加微量H2O2即可大幅提高rGO/TNTs的光催化效果。H2O2在0~0.2 mL范围内,光催化效果随H2O2添加量的增加而升高,在0.2 mL时苯酚降解率最高达99%,光催化效果最佳。当超过0.2 mL时,H2O2添加量继续增加,苯酚降解率降低,光催化效果变差。由图8(b)和表6可知,在不同H2O2添加量下,rGO/TNTs对苯酚的降解满足一级反应动力学方程(R2≥0.91)。在添加H2O2(0~0.2 mL)范围内,随H2O2添加量的增加反应速率常数明显上升。在添加量为0.2 mL时,反应速率常数最大,反应2 h降解率最高达97%;当H2O2添加量超过0.2 mL时,随H2O2添加量的增加k值有所降低。表明H2O2和rGO/TNTs具有协同作用,但过量H2O2降低光催化反应性能。
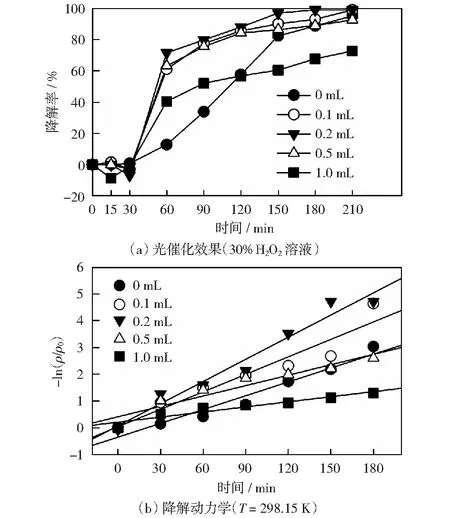
图8 不同H2O2量下rGO/TNTs对苯酚的光催化效果及降解动力学Fig.8 Photocatalytic effect and degradation kinetics of phenol by rGO/TNTs at different H2O2 contents
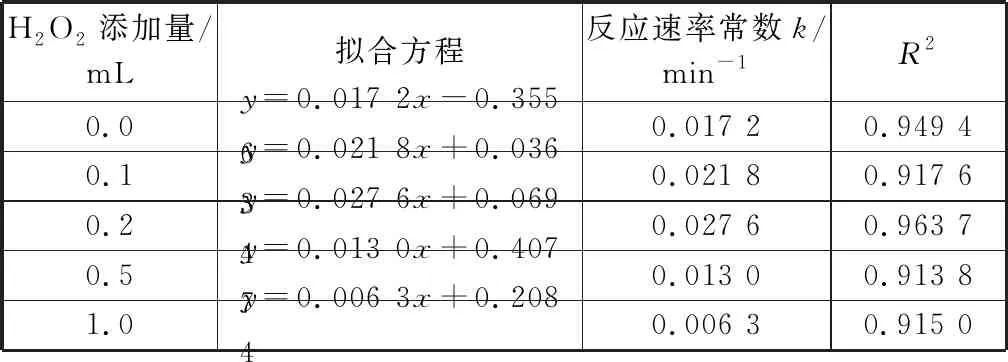
H2O2添加量/mL拟合方程反应速率常数k/min-1R20.0y=0.017 2x-0.355 60.017 20.949 40.1y=0.021 8x+0.036 30.021 80.917 60.2y=0.027 6x+0.069 40.027 60.963 70.5y=0.013 0x+0.407 70.013 00.913 81.0y=0.006 3x+0.208 40.006 30.915 0
H2O2强化了rGO/TNTs对苯酚的光催化降解[14]。尤其是在光反应开始60 min内,苯酚降解率几乎提高了3~5倍。其强化机理根据AUGUGKIARO et al[15]提出的机理解释:在rGO/TNTs光催化体系中,H2O2不仅被光子分解产生·OH,提高光子的利用率和有机物的降解率,同时还是光生电子-空穴对的受体,有效减少光生电子-空穴对的复合。但并非H2O2添加量越多其光催化效果越好,过量H2O2和·OH发生反应,导致体系中·OH自由基减少,使rGO/TNTs对苯酚的降解率下降。
3.3 rGO/TNTs和TNTs在可见光下对苯酚的降解性能
分别取0.5 g/L TNTs和rGO/TNTs,加入0.2 mL H2O2,在500 W氙灯下对10 mg/L的苯酚进行降解。暗反应30 min,光反应150 min,每30 min取样测试一次,结果如图9所示。由图9可知,在暗反应阶段,TNTs和rGO/TNTs对苯酚的降解率先降低后提高,并且rGO/TNTs对苯酚的降解效果明显高于TNTs,光反应150 min苯酚降解率可达98%,而未复合的TNTs在光反应150 min时苯酚的降解率仅达36%。因此,rGO/TNTs复合光催化剂拓宽了TiO2在可见光的吸收范围,提高了光催化效果,这与表征分析结果一致。
3.4 循环实验
取0.5 g/L rGO/TNTs对10 mg/L的苯酚溶液进行降解,暗反应30 min光反应3 h后测其吸光度,循环反应5次。每次将其离心并用蒸馏水离心洗涤数次后,放入50 ℃烘箱中烘干,烘干后取出进行下一次反应测试,结果如图10所示。未循环使用的rGO/TNTs降解率为95%,循环使用5次后,其降解率仍可达84%,表明rGO/TNTs具有较高的光催化性能和回收率。循环使用后降解率降低可能是因每次取出测其吸光度,离心洗涤以及烘干等步骤产生质量损失,也可能是因rGO/TNTs表面吸收的污染物再次浸入到溶液中,导致其光催化效果降低。总之,rGO/TNTs的光催化性能比较稳定。
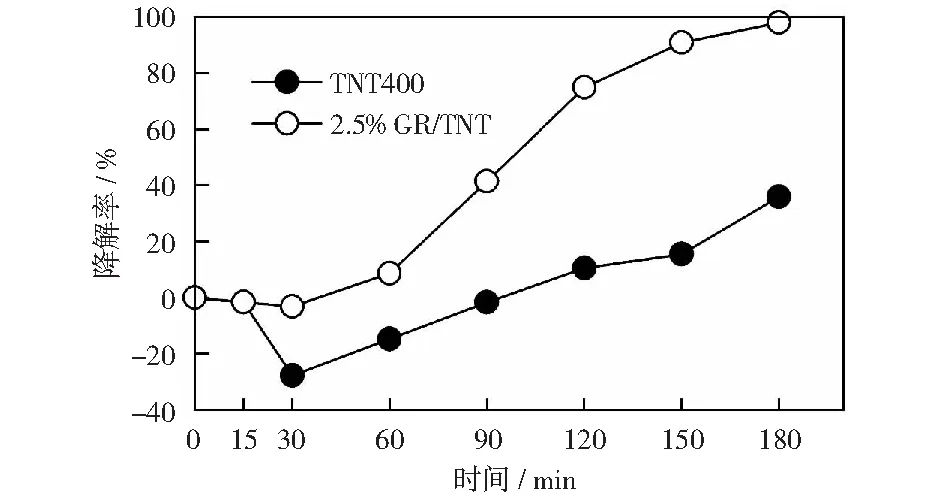
图9 可见光下不同催化剂对苯酚的光催化效果Fig.9 Photocatalytic effect on phenol under visible light
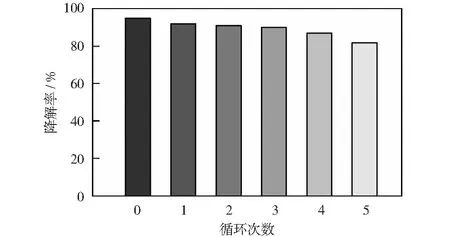
图10 循环次数对苯酚降解的影响Fig.10 Number of cycles of degradation of phenol by rGO/TNTs
4 结论
1) 采用浓碱水热法用P25制备TNTs,水热法将GO和TNTs结合生成rGO/TNTs复合光催化剂。通过对10 mg/L苯酚溶液进行降解,确定rGO/TNTs的最佳煅烧温度为400 ℃,降解反应满足一级反应动力学方程(R2≥0.98).
2) 表征结果表明,rGO与TNTs的复合并非简单的物理复合,而是以Ti—O—C化学键紧密结合到一起。加入rGO可抑制TNTs空穴和电子间的复合,从而提高TNTs的光催化效率,且rGO的引入拓宽了TNTs的光响应范围,将rGO/TNTs光催化活性延伸到可见光范围。
3) 光催化反应结果表明,苯酚初始质量浓度为10 mg/L、rGO/TNTs投加量为0.5 g/L、溶液pH值为6.5及H2O2添加量为0.2 mL时,rGO/TNTs对苯酚的光催化效果最佳,苯酚降解率达95%以上且降解反应满足一级反应动力学方程(R2≥0.95).
4) 在最佳光催化反应条件下,10 W紫外光照下反应2 h 和500 W可见光照下反应2.5 h,rGO/TNTs对苯酚的降解率可分别达97%和98%.rGO/TNTs具有较高的稳定性及回收利用率,可为其在苯酚废水处理的实际应用提供理论基础。
