水提醇沉法提取薏米多糖及其对羟自由基的清除作用
2019-09-18闫旭宇李玲
闫旭宇,李玲
(延安大学生命科学学院,陕西延安716000)
薏米,又叫薏苡仁,为禾本科植物薏苡(Coix lacryma-jobi L.)的种仁。薏苡是一种营养丰富的粮药兼用的一年生或多年生植物,其种仁薏米具有较全面的营养成分和特殊的药用保健功效。薏米多糖的单糖组分较复杂,包括葡萄糖、甘露糖、阿拉伯糖、鼠李糖、半乳糖[1],是药理活性较高的物质,具有降血脂、降血糖、调节免疫和防治肿瘤[2]等功效。同时,薏米多糖具有良好的耐热性能,在100 ℃左右具有较好的稳定性[3];并具有一定的抗氧化性,对超氧阴离子自由基(O2-·)、羟基自由基(·OH)以及DPPH 自由基具有清除能力[1]。对薏米多糖提取工艺的已有研究有水提法、超声或微波辅助提取法[4]、以及亚临界水萃取法[5]等。超声波作为一种辅助提取方法,通过增大溶剂分子的运动速度和穿透力,加快细胞破碎的速度,使溶剂快速的渗透到细胞中,提高有效成分的提取率和纯度[6]。基于此,本研究利用超声辅助水提醇沉法从薏米中提取多糖,通过对羟自由基的清除能力明确其抗氧化功效,为薏米多糖的进一步开发和利用提供理论依据。
1 材料与方法
1.1 材料与仪器
1.1.1 材料
薏米:市售。
1.1.2 试剂
石油醚、95 %乙醇、无水乙醇、无水乙醚、5 %苯酚、浓硫酸、硫酸亚铁、30%双氧水、水杨酸(分析纯):天津市福晨化学试剂厂。
1.1.3 仪器
AUV120 电子分析天平:上海玉博生物科技有限公司;WG-71 鼓风干燥机粉碎机:天津市泰斯特仪器有限公司;HH-W600 数显三用恒温水箱:金坛市亿通电子有限公司;KQ3200E 超声波清洗器:昆山舒美超声仪器有限公司;R-201 真空旋转蒸发器:郑州长城科工贸有限公司;UV2800 紫外可见分光光度计:上海舜宇恒平科学仪器有限公司;TG16G 高速离心机:湖南省凯达科学仪器有限公司;GDYQ-701S 样品提取仪:长春小天鹅仪器有限公司。
1.2 试验方法
1.2.1 薏米多糖提取工艺流程
筛选薏米→粉碎→脱脂→超声水浴浸提→过滤→旋转蒸发→滤液醇沉→离心→洗涤→干燥→粗多糖→溶解→待测液→测吸光度
关键步骤如下:
1)薏米脱脂:准确称取20 g 薏米粉,置于索氏提取器,加石油醚回流(60 ℃)脱脂 2 次,每次 2 h 得到脱脂产物,于3 ℃贮藏备用。
2)超声水浴浸提:取一定量的脱脂薏米粉,加入蒸馏水,搅拌均匀,超声提取50 min 后,在电热恒温水浴锅中加热提取多糖。
3)滤液醇沉:将上清液浓缩至原来的三分之一,再加入3 倍体积的95%乙醇溶液,静置30 min 后离心(转速为6 500 r/min,时间为20 min),去上清液,得沉淀物,此沉淀物就是粗多糖。
4)洗涤:依次用无水乙醇、乙醚洗涤2 次,以便破坏水解残留的脂溶性杂质。
1.2.2 测定多糖含量
采用苯酚-硫酸法测定多糖含量。
1)标准曲线绘制:精密称取干燥葡萄糖0.151 g,加蒸馏水溶解,定容至100 mL 容量瓶中,充分摇匀,得到质量浓度为100 mg/mL 的葡萄糖标准溶液。吸取1.0、2.0、3.0、4.0、5.0 mL 的葡萄糖标准溶液分别置于100 mL 容量瓶中,定容、摇匀。分别吸取各溶液2 mL于试管中,分别加入5%苯酚1.0 mL、浓硫酸5.0 mL,用2.0 mL 蒸馏水做空白对照和调零,静置10 min,于60 ℃恒温水浴10 min 取出,迅速冷却至室温20 ℃。在波长为490nm 下测定吸光度,绘制标准曲线并进行回归处理,得到回归方程为Y=0.011 9x+0.010 3,R2=0.993 2。在0~80 μg/mL 范围内,吸光度和葡萄糖标准液的浓度呈良好的线性关系。
2)待测液中多糖的测定:精确吸取待测液2 mL 于10 mL 的容量瓶中,加蒸馏水稀释至刻度,摇匀、静置。从中吸取2.0 mL 液体至试管中,加入5%苯酚1.0 mL、浓硫酸5.0mL,摇匀。室温20 ℃静置10min 后放置60℃恒温水浴10min 取出,迅速冷却至室温20 ℃。在波长为490nm 下测得吸光度值,根据标准曲线回归方程计算出多糖浓度,求出多糖得率。多糖得率的计算公式如下:

式中:C 为薏米多糖浓度,mg/mL;V 为稀释总体积,mL;M 为薏米粉的质量,g。
1.2.3 单因素试验
1)料液比的选择:固定水提取液pH 值为5.0,水浴加热温度为70℃,提取3 h,料液比分别设置为1∶10、1∶15、1∶20、1∶25、1∶30(g/mL),平行试验 3 次,研究料液比对薏米多糖得率的影响。
2)提取温度的选择:固定水提取液pH 值为5.0,体积60 mL,水浴加热温度分别设置为65、70、75、80、85 ℃,提取3 h,平行试验3 次,研究提取温度对薏米多糖得率的影响。
3)pH 值的选择:固定水提取液体积60 mL,水浴加热温度为 70 ℃,pH 值分别设置为 3.5、4、4.5、5、5.5,提取3 h,平行试验3 次,研究pH 值对薏米多糖得率的影响。
4)提取时间的选择:固定水提取液pH 值为5.0,体积60 mL,水浴加热温度为70 ℃,提取时间分别设置为 0.5、1.0、1.5、2.0、2.5 h,平行试验 3 次,研究提取时间对薏米多糖得率的影响。
1.2.4 正交优化试验
在单因素试验的基础上,以提取温度、提取时间、料液比及pH 值为试验因素,根据单因素试验结果,进行四因素三水平试验确定水提醇沉法提取薏米多糖的最佳工艺参数。
1.2.5 羟基自由基清除试验
薏米多糖及维生素C 对羟基自由基的清除率,采用水杨酸法进行测定。对羟基自由基的清除率按下式计算:
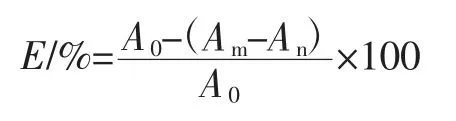
式中:E 为羟基自由基的清除率;A0为空白对照液的吸光值;Am为加入多糖后的吸光值;An为不加H2O2时多糖的吸光值。
2 结果与分析
2.1 单因素试验结果
2.1.1 料液比的确定
在其他因素条件不变情况下,不同水平的料液比对薏米多糖得率的影响如图1 所示。

图1 料液比对薏米多糖得率的影响Fig.1 Effect of the solid-liquid ratio on polysaccharide extraction rate in adlay
由图1 可知,随着液体量的增加,薏米多糖得率逐渐提高,当料液比为1∶25(g/mL)时,薏米多糖得率达到最高,之后下降。这可能是由于一定比例的料液比已经使溶出的多糖量达到平衡,继续增大料液比,可能使其他物质溶出,多糖的相对得率就降低了。另外,料液比过大会增加溶剂的用量,本着节约成本的原则,料液比为 1∶25(g/mL)左右为宜。
2.1.2 提取温度的确定
在其他因素条件不变情况下,不同水平的提取温度对薏米多糖得率的影响如图2 所示。

图2 温度对薏米多糖得率的影响Fig.2 Effect of the extraction temperature on polysaccharide extraction rate in adlay
由图2 可知,随着提取温度升高,薏米多糖得率不断增加,在75 ℃时,薏米多糖得率最高,之后缓慢下降。这可能是由于温度升高,分子运动速度加快,多糖更容易浸出,但是过高的温度易导致多糖结构被破坏,进而造成多糖含量降低。因此,提取温度应控制在75 ℃左右为宜。
2.1.3 pH 值的确定
在其他因素条件不变情况下,不同水平的pH 值对薏米多糖得率的影响如图3 所示。
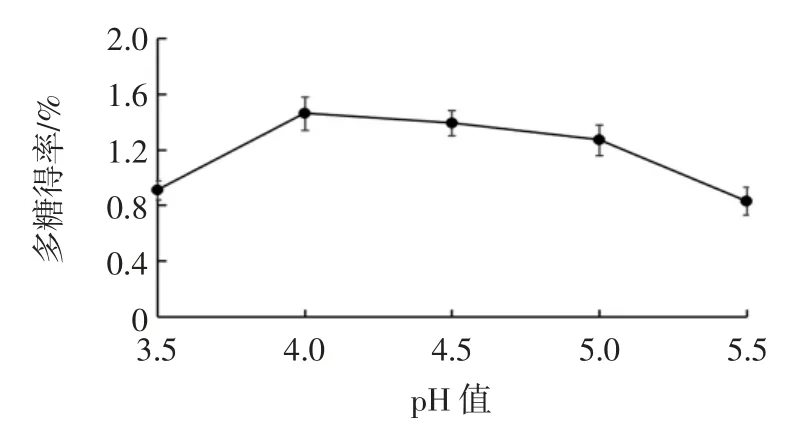
图3 pH 值对薏米多糖得率的影响Fig.3 Effect of the pH value on polysaccharide extraction rate in adlay
由图3 可知,薏米的多糖得率随着pH 值的升高而增大,pH 值为4 时多糖得率达到最大,继续升高pH值多糖得率开始降低,但在pH 值为4.5 和5 时降低幅度不明显。这可能是由于pH 值为4~5 时,有利于多糖最大程度的溶出,继续升高pH 值会影响多糖的结构稳定性。因此,pH 值应控制在4~5 之间。
2.1.4 提取时间的确定
在其他因素条件不变情况下,不同水平的提取时间对薏米多糖得率的影响如图4 所示。
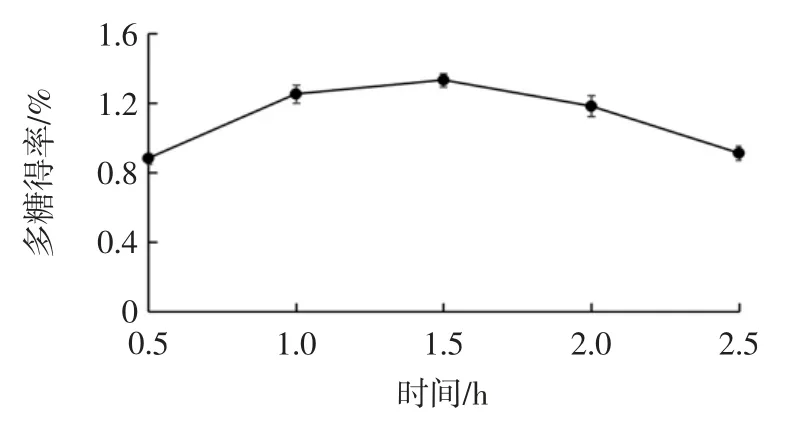
图4 时间对薏米多糖得率的影响Fig.4 Effect of the extraction time on polysaccharide extraction rate in adlay
如图4 所示,随着提取时间增加,薏米多糖得率不断增加,在提取时间为1.5 h 时,薏米多糖得率最高,之后逐渐下降。这可能是由于提取时间过短,多糖还没有充分溶出,时间过长又使其他物质的溶出,影响多糖的浸出影响,或多糖提取物中的结构分被破坏。因此,提取时间选择1.5 h 左右为宜。
2.2 正交试验结果
根据单因素试验结果,以料液比、提取温度、pH值、提取时间为考察因素,以多糖得率为考察指标,进行L9(34)正交试验,因素水平见表1,正交试验结果见表2。
由表2 的极差值大小可知,影响薏米多糖得率的主次因素依次为料液比(A)>pH 值(C)>提取时间(D)>提取温度(B),料液比对多糖得率的影响相对较大。超声辅助水提醇沉法提取薏米多糖的最佳组合为A2B2C3D3,即料液比为 1∶20(g/mL),提取温度 75 ℃,pH值为5.0,提取时间为2 h。在此条件下进行验证试验,最终得到薏米多糖得率为1.56%。

表1 因素水平表Table 1 Factors and levels of the orthogonal test

表2 正交试验结果Table 2 The results of the orthogonal test for optimal conditions
2.3 薏米多糖对羟基自由基的清除作用
植物多糖对羟基自由基有一定清除作用。薏米多糖羟基自由基的清除作用对如图5 所示。
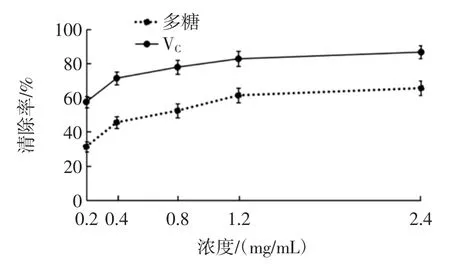
图5 薏米多糖对羟基自由基的清除率Fig.5 The hydroxy radical scavenging rate of the polysaccharide extracted from adlay
由图5 可知,在一定范围内,薏米多糖提取物和维生素C 对羟基自由基清除率均逐渐增强,说明多糖提取物和维生素C 对羟基自由基的清除能力存在着一定的量效关系。在相同质量浓度下,薏米多糖提取物对羟基自由基具有一定的清除作用,但效果弱于维生素C。
3 讨论与结论
多糖广泛存在于植物体内,具有较高的药理活性。水提醇沉法目前在植物活性多糖提取中应用最多,利用该法提取黄精多糖肽得率为0.34%[7],提取山苦茶[8]、苦瓜[9]、芦竹[10]及向日葵茎芯[11]等多糖得率分别为1.012%、3.12%、4.80%和6.56%。可见,不同的植物利用水提醇沉法提取多糖得率差别较大。利用超声波辅助提取,多糖的浸提过程和活性不发生改变,浸提时间缩短,可以提高提取效率。本试验在超声辅助水提醇沉法的最优条件下,即提取时间为2 h,提取温度为 75 ℃,pH 值为 5,料液比为 1∶20(g/mL)时,薏米多糖得率为1.56%,高于刑真等[12]利用热水浸提法提取薏米多糖的提取率1.25%以及利用超声波辅助提取薏米多糖的提取率1.41%。综合考虑时间和能耗因素,超声波辅助水提醇沉法适宜于在省时节能的情况下提取薏米多糖。
羟基自由基能破坏细胞膜、杀死机体红细胞、诱导基因突变、诱发多种疾病,进而引起生命发生系统性的紊乱。研制价格低廉经济有效的抗氧化剂是对抗羟基自由基的有效途径。研究表明,羊肚菌[13]、别克参[14]、玫瑰茄[15]等的多糖均具有一定的抗氧化能力。本试验中,在相同质量浓度下,薏米多糖提取物对羟基自由基具有一定的清除作用,但效果弱于维生素C。因此,加强薏米活性成分研究,扩大薏米资源的开发利用,有助于进一步推动薏米产业化发展。
