(Mg1-xSrx)2SiO4∶(Eu3+,F-)荧光粉的物相及光谱
2019-09-16徐诗林孙传耀
汪 雨, 罗 岚,2*, 郭 锐, 徐诗林, 孙传耀
(1. 南昌大学 材料科学与工程学院, 江西 南昌 330001;2. 南昌大学 江西省轻质高强结构材料重点实验室, 江西 南昌 330001)
1 引 言
在稀土掺杂荧光粉产业,碱土硅酸盐[1-2]由于具有良好的热稳定性、化学稳定性、物理稳定性和原料广泛、价格低廉、高发光效率、结构和成分易调整等优点使其成为稀土发光材料理想的基质材料[3-4]。随着碱土离子种类、碱土离子配比的不同,碱土正硅酸盐结构改变极大,可为正交(Ba2SiO4)、单斜(β-Sr2SiO4)或三斜(α-Ca2SiO4)等结构,稀土掺杂后在可见光范围内表现出丰富的发射谱带,不仅可用于各类照明(三基色荧光灯、LED[5]等)、闪烁计数器、显示(FDP、CRT、PDP等),还可用作路标指示(长余辉荧光材料)等[3],其光谱特性及发光机理备受关注。Poort、Blasse[6-7]等发现碱土正硅酸盐(如Ba2SiO4[8])非常适合Eu2+掺杂;Li等[9-10]认为其可作为新一代LED荧光粉;Wen[11]、Lv[12]等深入研究了稀土离子掺杂后二元、三元碱土硅酸盐(如M3MgSi2O8(M:Ba, Sr,Ca)[13-14])的发光特性,开发出Ba3MgSi2O8∶Eu2+[15]、Ca3MgSi2O8∶Eu2+[16-17]、Sr3MgSi2O8∶Eu2+[18]等高效白光LED荧光粉材料。Eu3+掺杂正硅酸盐与Eu2+相比,是非等价态取代,研究报道较少[19]。本文采用高温固相法制备了(Mg1-xSrx)2SiO4(x=0~1),分析Sr离子含量的变化对基体物相组成、光谱性能的影响,并进行基体筛选和制备优化,在此基础上进行Eu3+掺杂浓度及Eu3+能量传递传递机理研究。
2 实 验
2.1 (Mg1-xSrx)2-ySiO4∶y(Eu3+,F-)粉体的制备
(Mg1-xSrx)2-ySiO4∶y(Eu3+,F-)粉体以SrCO3(上海科易精细化学品公司,分析纯)、Mg2CO3(上海统亚华工科技发展有限公司,分析纯)、SiO2(天津市致远化学试剂有限公司,分析纯)、EuF3(瓦里西化工,99.99%)为原料,按照化学计量比称量并在研钵中研磨混合均匀,空气气氛下以20 ℃/min的速度升温至1 150 ℃并保温3 h,随后随炉冷却得到粉末。制备(Mg0.8Sr0.2)2-ySiO4∶y(Eu3+,F-)粉体时,按照化学计量比称量原料,制备时除煅烧温度为1 250 ℃外,其他条件不变。
2.2 测试与表征
样品物相表征采用PANalytical X射线衍射仪进行X射线衍射测得,测试范围为20°~80°。样品在254 nm和365 nm激发下的发光状态采用WFH-203B型三用紫外分析仪进行观察,并用数码相机进行拍照、记录。粉体的荧光性质(Photoluminescence spectrum,PL)采用PE公司的FS F-4500荧光光谱仪测得。量子效率(Absolute PL quantum yields)和荧光寿命(lifetime)采用Hamamatsu公司的C9920-02G量子效率测量仪测得。样品的XPS(X-ray photoelectron spectroscopy)采用ThermoFisher公司的K-Alpha(Al Kα源,1 486.6 eV)测得(C1s~284.6 eV为内标)。
3 结果与讨论
3.1 结构分析
图1(a)、(b)显示了按照2.1制备得到的(Mg1-xSrx)2SiO4粉体的物相组成。当x=1时,粉体为α-Sr2SiO4(15.385%)和β-Sr2SiO4(84.615%)混合物,主晶相为β-Sr2SiO4;x=0.8时,粉体中除α-Sr2SiO4(50.000%)和β-Sr2SiO4(33.333%)外,新增β-Mg2SiO4(8.333%)、Sr3MgSi2O8(8.333%)相,主晶相为α-Sr2SiO4;x=0.6,0.4,0.2时,其所包含物相与x=0.8一致,但随着x值减小,α-Sr2SiO4和β-Sr2SiO4减少、Sr3MgSi2O8先增后减、γ-Mg2SiO4和β-Mg2SiO4增加且β-Mg2SiO4增加速度最快;当x=0.2时,α-Sr2SiO4(21.053%)、β-Sr2SiO4(5.263%)、Sr3MgSi2O8(15.789%)、γ-Mg2SiO4(11.111%)、β-Mg2SiO4(47.368%)即β-Mg2SiO4为主晶相;x=0时,粉末为γ-Mg2SiO4(55.6%)、β-Mg2SiO4(44.4%),γ-Mg2SiO4相为主晶相。
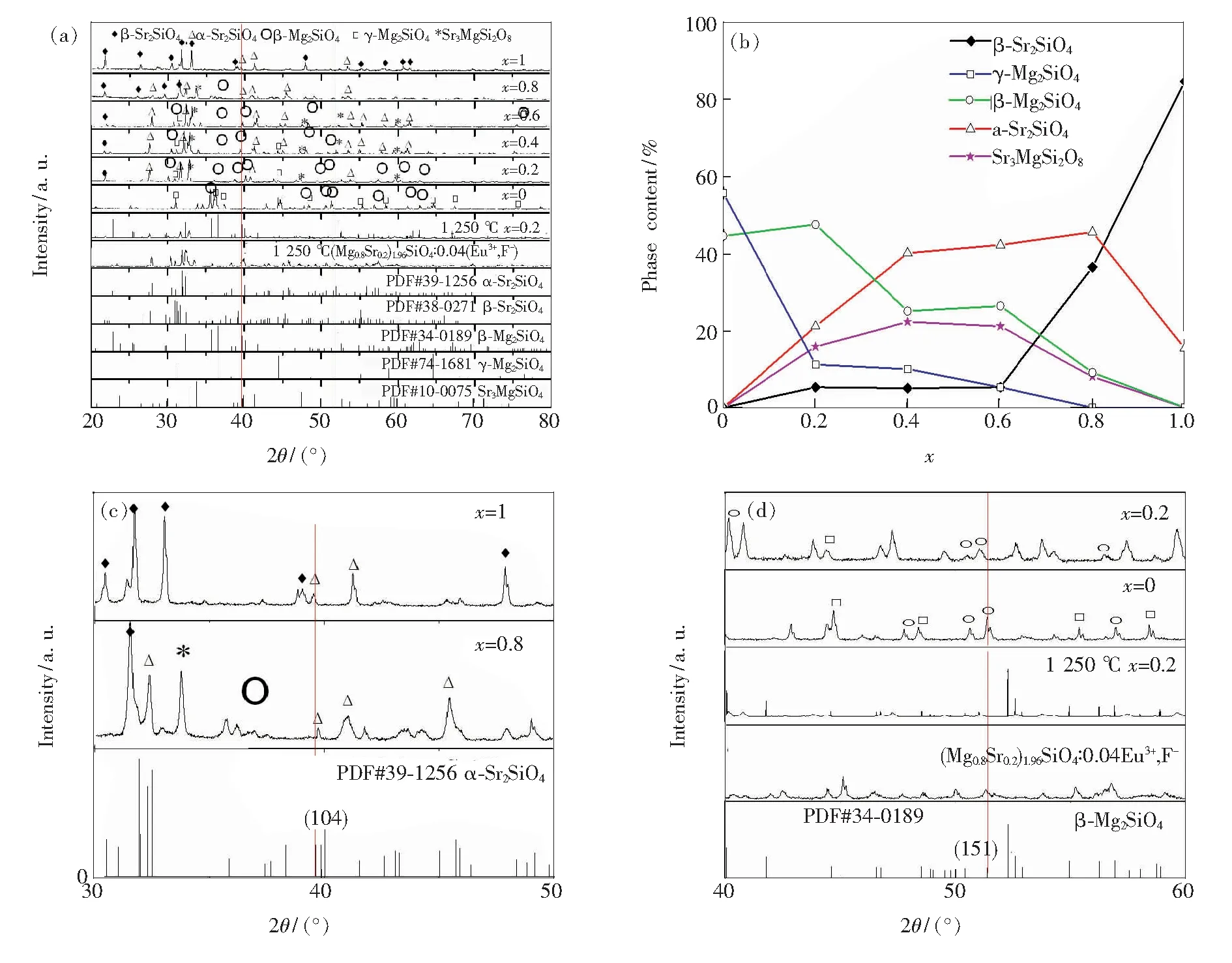
图1 (Mg1-xSrx)2SiO4和(Mg0.8Sr0.2)1.96SiO4∶0.04(Eu3+,F-)粉体:(a)XRD 图谱,(b)物相质量百分比。(c)x=1, 0.8和(d)x=0.2, 0时(Mg0.8Sr0.2)1.96SiO4∶0.04(Eu3+,F-)的XRD放大图谱。
Fig.1 Phase constitution of (Mg1-xSrx)2SiO4and (Mg0.8Sr0.2)1.96SiO4∶y(Eu3+,F-) powders: (a) XRD patterns, (b) weight percent of the phases; and amplified XRD patterns at (c)x=1, 0.8 and (d)x=0.2, 0.

表1 (Mg1-xSrx)2SiO4粉体涉及物相晶体结构参数
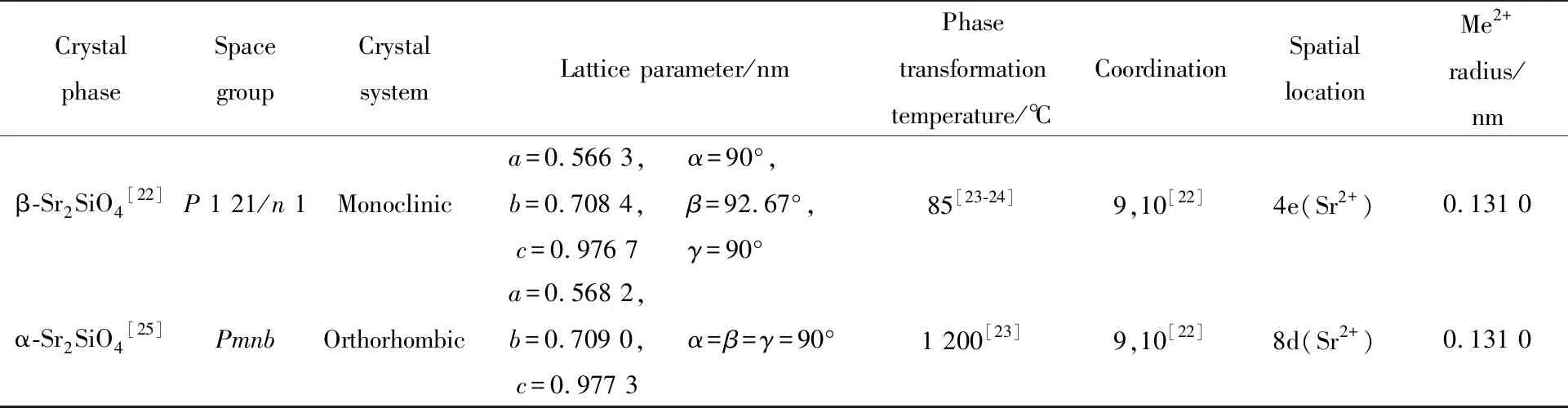
表1(续)
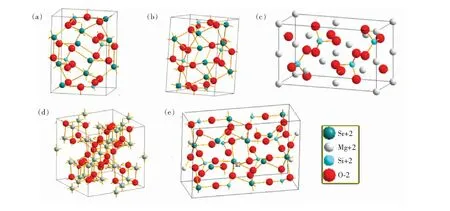
图2 α-Sr2SiO4(a)、β-Sr2SiO4(b)、β-Mg2SiO4(c)、γ-Mg2SiO4(d)、Sr3MgSi2O8(e)的晶体结构图。
结合晶体结构(图2)及晶格信息(表1),我们进一步分析了1 150 ℃煅烧温度条件下(Mg1-x-Srx)2SiO4粉末随Sr离子含量物相组成的演变原因。x=1时,β-Sr2SiO4相比α-Sr2SiO4相更稳定(Tβ→α≥1 200 ℃),此时β-Sr2SiO4为主晶相;而x=0时,γ-Mg2SiO4比β-Mg2SiO4稳定(Tγ→β≥1 500 ℃),此时γ-Mg2SiO4为主晶相。正交α-Sr2SiO4和正交β-Mg2SiO4两个Sr(Ⅰ)、Sr(Ⅱ)占据4c位置,Mg(Ⅰ)占据4a、Mg(Ⅱ)占据4c位置,碱土离子配位体空隙大小相似,因此在富Sr2SiO4或富Mg2SiO4区间容易形成有限固溶体[26]。由图1(c)可见,x=0.8和x=1时,粉末中α-Sr2SiO4相(104)衍射面(约39.077°附近),前者比后者略微向高角区移动了1.983°,这意味Mg取代Sr离子进入α-Sr2SiO4,其晶格参数将略微减小。由图1(d)可见,x=0.2和x=0时,粉末中β-Mg2SiO4相衍射面(151)(约51.019°附近),前者比后者略微向低角区移动了0.504°,这意味Sr取代Mg离子进入β-Mg2SiO4,其晶格参数将略微增大。固溶体能促进对应物相的稳定性,即在x=0.8时α-Sr2SiO4为主晶相,而x=0.2时β-Mg2SiO4为主晶相。单斜β-Sr2SiO4相Sr(Ⅰ)、Sr(Ⅱ)占据4e位置,Sr离子处于5个硅氧四面体围成的空隙,10配位Sr(Ⅰ)离子形成(Si—O—Sr(Ⅰ)—O—Sr(Ⅱ))锯齿链,9配位Sr(Ⅱ)离子形成(Sr(Ⅰ)—O—Sr(Ⅱ)—O—Sr(Ⅰ))线型[27]。当半径较小Mg离子进入时,会使得b、c轴压缩,同时b、c轴夹角减小,直接转变为单斜Sr3MgSi2O8相(具有KNaSO4型层状结构,层状结构由位于角落的共用MgO6八面体和SiO4四面体构成,Sr2+占据不同的层间结晶位点,Sr(Ⅰ)位于层间空间的中心(A位),Sr(Ⅱ)嵌入层框架(B位)),因此随着Sr减少,β-Sr2SiO4相快速减少,Sr3MgSi2O8物相含量先增后减;γ-Mg2SiO4晶格中Mg(Ⅰ)和Mg(Ⅱ)分别占据8a、16d位置,其空间过小无法固溶大半径的Sr离子,因此随着Sr离子减少,γ-Mg2SiO4缓慢增加。
由上述分析可知1 150 ℃制备的Sr2SiO4-Mg2SiO4粉体物相组成演变规律为:组分配比为Sr2SiO4时,粉体中β-Sr2SiO4比α-Sr2SiO4更稳定,故β-Sr2SiO4相为主晶相;随着Mg离子增加,不仅会出现γ-Mg2SiO4、β-Mg2SiO4、Sr3MgSi2O8相,且α-Sr2SiO4、β-Sr2SiO4相含量减少;其中α-Sr2SiO4相中发生Mg离子取代形成固溶体稳定增强,其含量减少速度比β-Sr2SiO4相慢;且由于Sr离子进入β-Mg2SiO4也可形成固溶体,β-Mg2SiO4相增长速度比γ-Mg2SiO4更快;组分配比为Mg2SiO4时,γ-Mg2SiO4比β-Mg2SiO4稳定,故γ-Mg2SiO4相为主晶相。
3.2 光谱分析
图3为(Mg1-xSrx)1.96SiO4∶0.04(Eu3+,F-)(从左到右x=0,0.2,0.4,0.6,0.8,1)紫外发光照相记录。紫外光激发下(254 nm、365 nm),随着x值的增加,(Mg1-xSrx)1.96SiO4∶0.04(Eu3+,F-)发射出红光的亮度逐渐降低,同一样品在365 nm激发下比254 nm激发亮度更亮,且两种激发条件下x=0.2时红光最亮。

图3 (Mg1-xSrx)1.96SiO4∶0.04(Eu3+,F-)紫外激发发光照相记录。(a)白光;(b) 254 nm;(c) 365 nm。
Fig.3 Photos of (Mg1-xSrx)1.96SiO4∶0.04(Eu3+,F-) phosphor under UV light excitation. (a) White light. (b) 254 nm. (c) 365 nm.
(Mg1-xSrx)1.96SiO4∶0.04(Eu3+,F-)光谱分析如图4所示。254 nm、365 nm激发下(图4(a)、(b))荧光粉有595,615,655,705 nm红光锐峰发射(对应5D0→7Fn,n=1,2,3,4)且615 nm发射强度最大。且当x≥0.2时随着x值增加,615 nm红光发射有所减弱且x=0.2时红光强度大于x=0(即x=0.2
时红光最亮)。以620 nm为监测波长得到(Mg1-x-Srx)1.96SiO4∶0.04(Eu3+,F-)激发谱(图4(c)),在250~450 nm有宽带激发峰(对应电荷转移吸收(Charge transfer band,CTB),主峰在365 nm附近)及415 nm锐峰激发峰(对应Eu3+的7F0→5L6跃迁),且随着Sr的增加(x值增加),CTB的主峰值略有红移。
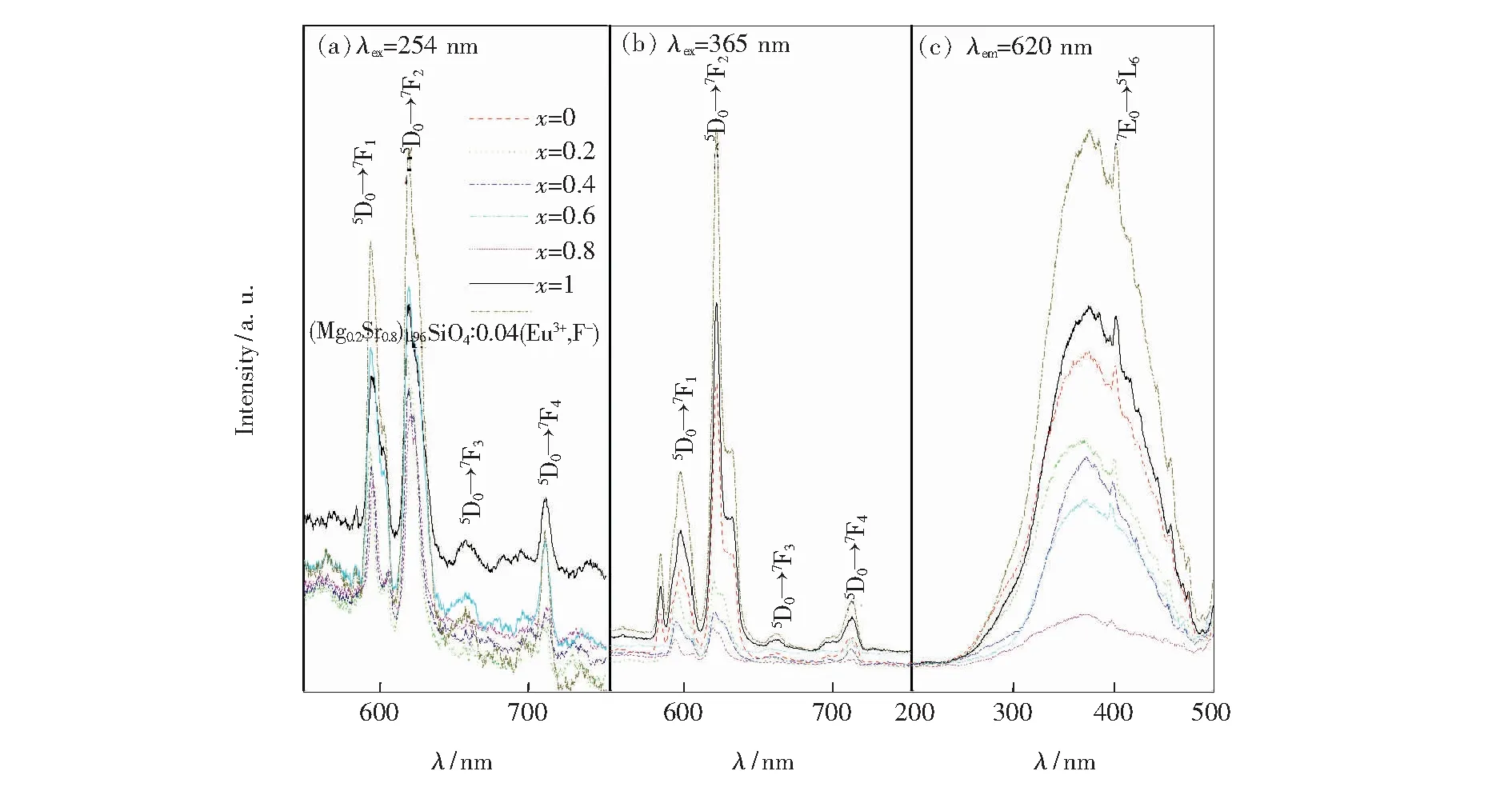
图4 (Mg1-xSrx)1.96SiO4∶0.04(Eu3+,F-)的荧光光谱
3.3 (Mg0.8Sr0.2)2-ySiO4∶y(Eu3+,F-)荧光粉
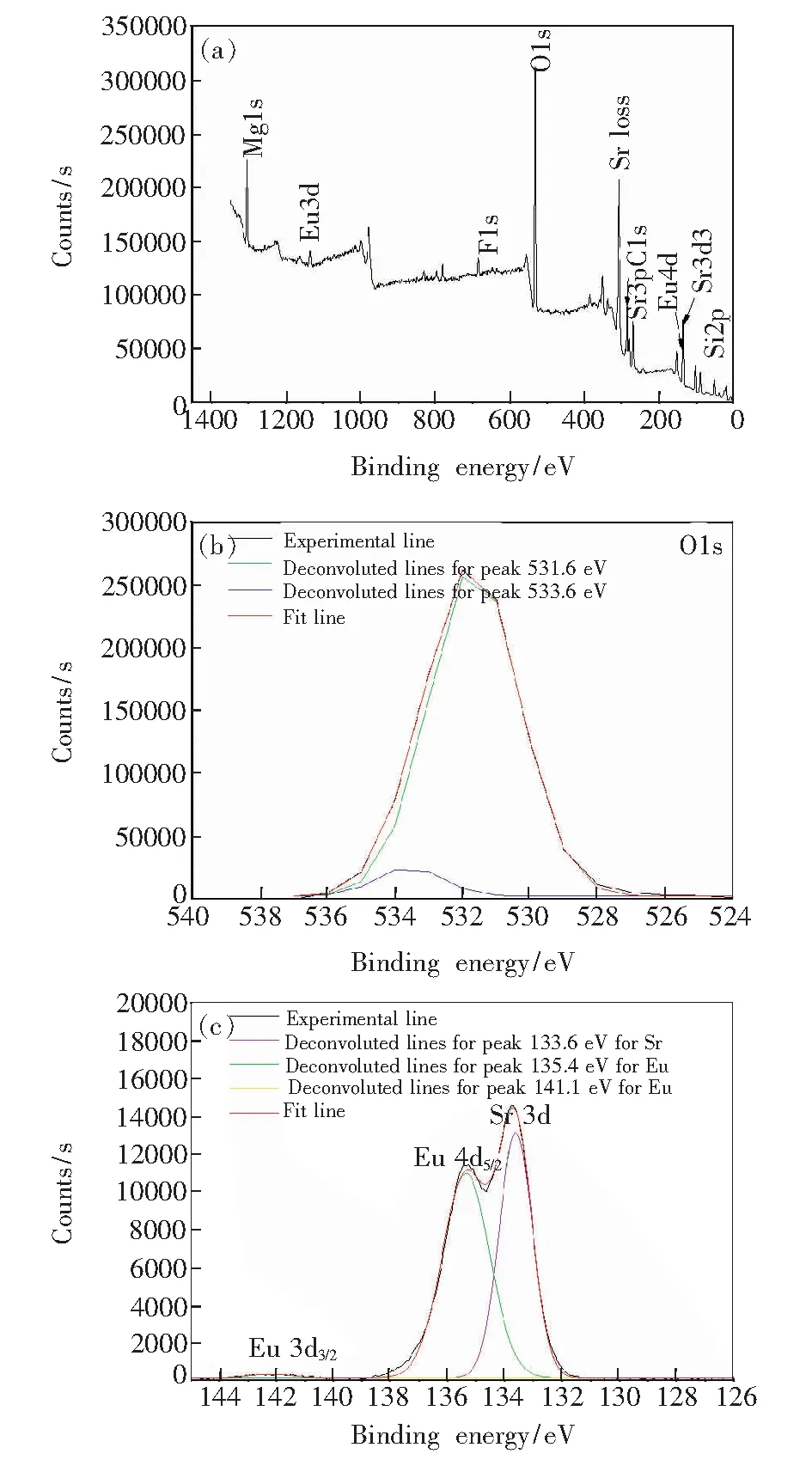
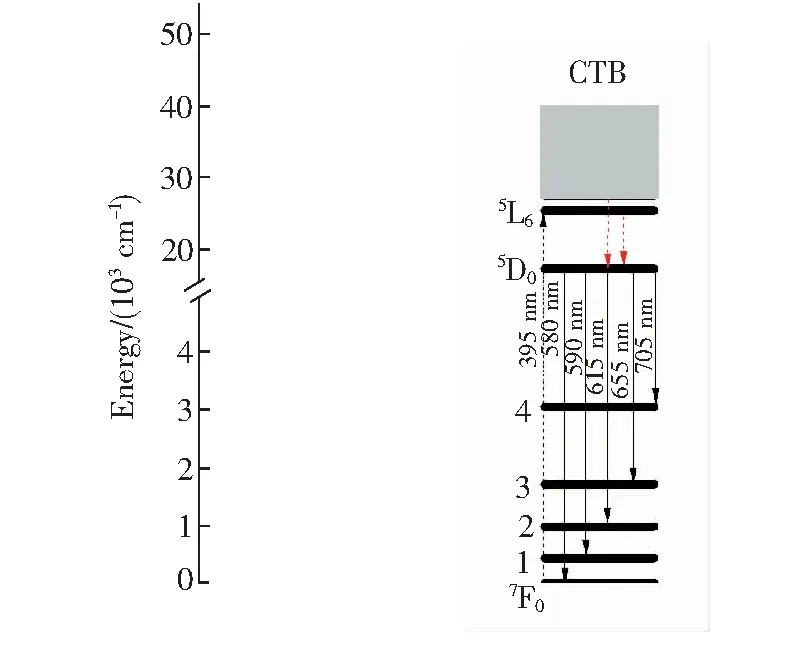
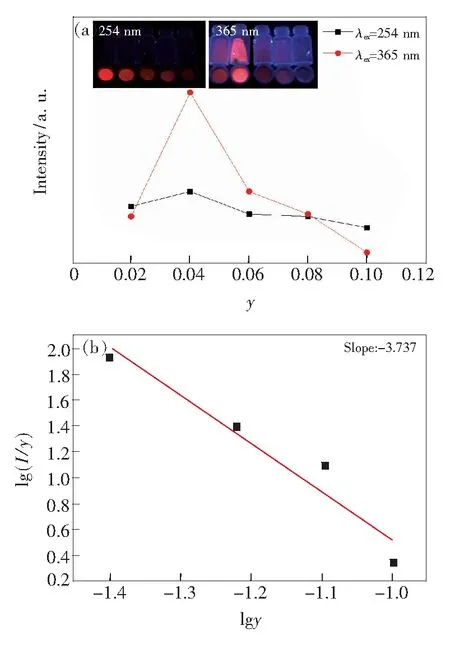
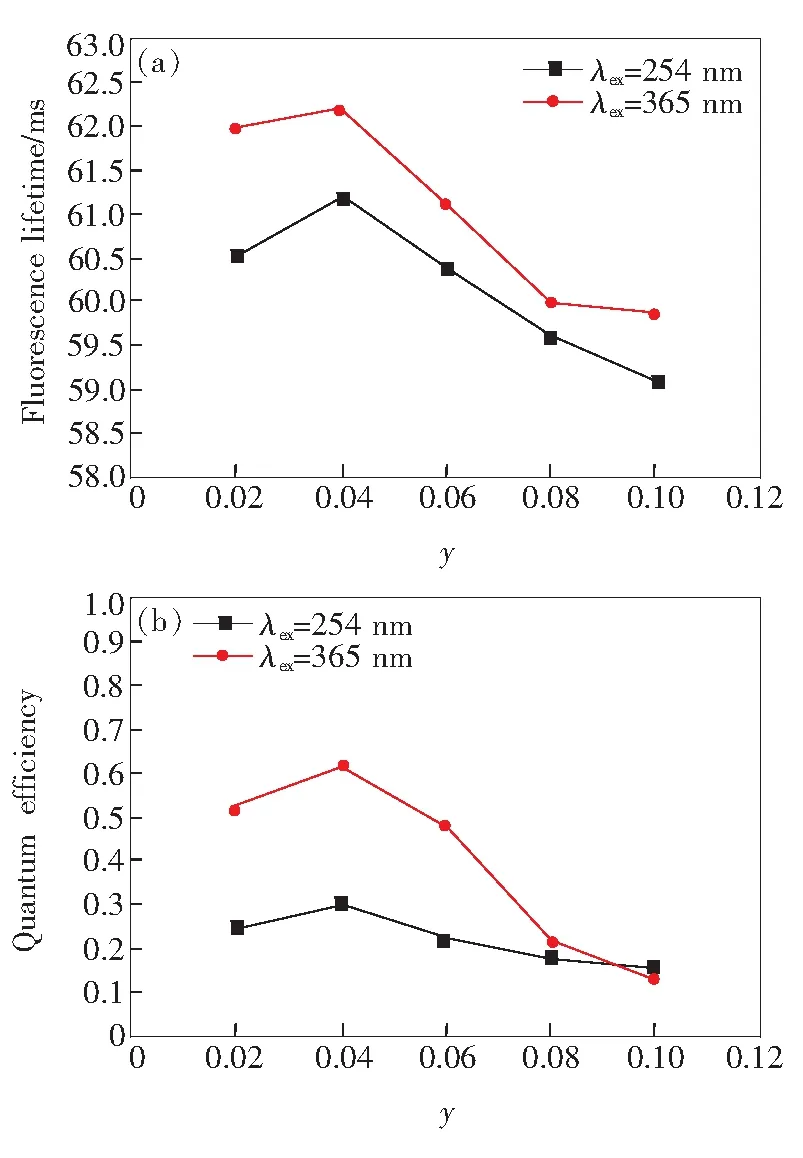
由3.2光谱分析可知(Mg0.8Sr0.2)1.96SiO4∶0.04(Eu3+,F-)为(Mg1-xSrx)1.96SiO4∶0.04(Eu3+,F-)中最亮荧光粉,结合3.1结构分析可知,此时粉末中以β-Mg2SiO4相为主(存在Sr的固溶),并含有α-Sr2SiO4、β-Sr2SiO4、γ-Mg2SiO4、Sr3MgSi2O8杂质相。随着温度的升高固溶度增加[28],按(Mg0.8Sr0.2)2SiO4化学计量比配置原料并在1 250 ℃煅烧可得到β-Mg2SiO4单相粉末,如图1(a)所示。由图1(a)、(d)可知,在(Mg0.8-Sr0.2)2SiO4中由于Sr离子的存在会使β-Mg2SiO4的晶格参数略微增大(Mg2+0.089 nm 图5 (Mg0.8Sr0.2)1.96SiO4∶0.04(Eu3+,F-)粉末粒径分布 Fig.5 Size distribution of (Mg0.8Sr0.2)1.96SiO4∶0.04(Eu3+, F-) powder (Mg0.8Sr0.2)1.96SiO4∶0.04(Eu3+,F-)的XPS全谱及O1s、Eu4d/Sr3d核心电子结合能精细谱(经Shirley去除背底和高斯线性拟合[29])如图6所示。XPS全谱可见Sr3d3、O1s、Eu4d、Si2p、F1s峰(分别对应133.6,532,135,92,685 eV结合能,图6(a)),由此可见粉末中所含组分均为设计成分,并未出现其他杂质。图6(b)为O1s能级精细谱,其结合能峰由2个光电子峰组成,低结合能峰(约531.6 eV)来源于晶格氧,高结合能(约533.6 eV)的光电子峰来源于氧缺陷有关(三价Eu离子取代二价碱土离子,为了保持电中性而产生间隙氧缺陷,这种电价不平衡还可以用F离子来补偿,在XPS全谱中检测到F1s的结合能峰),间隙氧光电子峰的积分强度与晶格氧光电子峰积分强度之比为0.042 6。文献[30]报道Eu3+离子的4d5/2和4d3/2的光电子峰分别位于约135.0 eV和约140.5 eV处,自旋轨道劈裂约为5.5 eV;而Eu2+离子的4d5/2的结合能要比相应的Eu3+低约7 eV。由图6(c)144~126 eV结合能范围的精细谱可见Eu3+离子的4d3/2和4d5/2分别对应141.1 eV和135.4 eV(结合能的能差为5.7 eV),Sr3d则对应133.6 eV, 而无Eu2+离子对应结合能峰。由XPS分析结果可知(Mg0.8Sr0.2)1.96SiO4∶0.04(Eu3+,F-)原料在固相法反应中基本按化学计量比反应(XPS结果中未检测出杂质成分且如3.1节描述XRD分析显示为单相),Eu离子以三价进入晶格,且有2个峰位(Eu4d核心电子结合能精细谱未出现二价Eu4d5/2离子结合能峰)。 图6 (Mg0.8Sr0.2)1.96SiO4∶0.04(Eu3+,F-)的XPS能谱(a)和O1s高分辨率XPS谱(b);(c)Eu4d/Sr3d。 Fig.6 XPS survey spectrum of the (Mg0.8Sr0.2)1.96SiO4∶0.04(Eu3+,F-)(a) and high-resolution XPS spectra of O1s(b). (c) Eu4d/Sr3d. 由图4还可看出,在254 nm和365 nm激发下,1 250 ℃制备的(Mg0.2Sr0.8)1.96SiO4∶0.04(Eu3+,F-)荧光粉与1 150 ℃的激发和发射光谱相似,强度明显提高。由激发和发射谱可知Eu3+在β-Mg2SiO4相((Mg0.8Sr0.2)2SiO4)晶格中的能级结构(如图7所示),其对应的红光发射过程为基体(Mg0.8Sr0.2)2SiO4吸收能量通过电荷转移传递给Eu3+发光中心,Eu3+的电子吸收能量跃迁到高能级随后驰豫到5D0能级进而产生5D0→7Fn(n=1,2,3,4)的红光发射;可见光发射的过程还可是Eu3+的电子吸收能量跃迁到5L6,随后无辐射驰豫到5D0能级进而产生5D0→7Fn(n=1,2,3,4)的红光发射。 图7 Eu3+在 (Mg0.8Sr0.2)2SiO4晶体场中的能级结构 Fig.7 Energy levels of Eu3+in (Mg0.8Sr0.2)2SiO4structure 图8 (Mg0.8Sr0.2)2-ySiO4∶y(Eu3+,F-)荧光粉:(a)Eu离子掺杂量不同的发光强度曲线,插图为对应照相记录(y=0.01~0.1,监视波长为615 nm),(b)365 nm激发下615 nm发射的 lgy-lg(I/y)对数函数。 Fig.8 (Mg0.8Sr0.2)2-ySiO4∶y(Eu3+,F-) phosphor: (a) phosphor 615 nm luminescence intensities with different Eu content, the inserts are the photograph of the phosphors under ultraviolet excitation, (b) lgy-lg(I/y) plot for 615 nm emission of phosphor under 365 nm excitation. (Mg0.8Sr0.2)2-ySiO4∶y(Eu3+,F-)(y=0.01~0.1)荧光粉以615 nm监测,其365 nm和254 nm激发下发射强度随Eu离子含量的变化如图8(a)所示(插图为254 nm和365 nm光激发下的照相记录),由图可见当y=0.04时亮度最大,即(Mg0.8Sr0.2)1.96SiO4∶0.04(Eu3+,F-)最亮。 最佳掺杂浓度大小受激活离子能量传递方式的影响,而能量传递分为辐射能量传递(激活离子之间因为共振作用)和非辐射能量传递(激活离子之间产生交叉弛豫)两种方式。利用临界距离可以判断掺杂离子能量传递方式,临界距离可由基于Blasse理论的公式计算: (1) 其中晶胞的体积用V表示,每个晶胞中的分子数用N表示,最佳掺杂浓度用XC表示。其中,对于(Mg0.8Sr0.2)1.96SiO4∶0.04(Eu3+,F-),V= 0.311 937 nm3,XC=0.04,N=4,计算得出RC=1.549 9 nm。基于Blasse 理论,当临界距离在0.5~0.8 nm之间时[31],能量传递的方式以非辐射跃迁为主,因此可以得出结论:β-Mg2SiO4中Eu3+发生浓度猝灭的原因不是非辐射跃迁,而是辐射跃迁,即基于共振能量传递(电偶极子和磁偶极子的作用)。由掺杂浓度和亮度关系可以推测其具体作用方式。如下述公式所示: I/y(1+A)/γ[α1-s/3Γ(1+s/3)], (2) 其中,掺杂离子浓度(不低于最佳掺杂浓度)用y表示,发光强度用I表示,激活剂的跃迁概率用γ表示,电多极效应用s表示,在已有基质和相同的激发条件下A和Γ是常量[31]。利用转化公式,以lgy为横坐标、lg(I/y)为纵坐标做图,并拟合s/3直线斜率,由s值可推测出能量传递方式:s=3时,表示掺杂离子的交换作用;s=6时,表示电偶极-电偶极作用(d-d);s=8时,表示电偶极-电四级作用(d-q);s=10时,表示电四极-电四极作用(q-q)。y与I/y的对数函数如图8(b)所示,拟合得到直线斜率数值为3.738,则s的值为11.214,接近于10,因此可以推断出β-Mg2SiO4相(Mg0.8-Sr0.2)2-ySiO4∶y(Eu3+,F-)中Eu离子的能量交换方式为电四极-电四极作用。 以615 nm为监测波长,测定(Mg0.8Sr0.2)2-ySiO4∶y(Eu3+,F-)(y=0.02,0.04,0.06,0.08,0.1)的红光荧光寿命及量子效率,如图9所示。254 nm激发下样品的荧光寿命依次为60.5,61.2,60.4,59.6,59.1 ms(图9(a)),且对应的量子效率分别为0.25,0.3,0.22,0.18,0.16(图9(b))。365 nm激发下样品的荧光寿命依次为62,62.2,61.1,60,59.9 ms(图9(a)),且对应的量子效率分别为0.52,0.62,0.48,0.22,0.14(图9(b))。由图9可见,同一样品365 nm激发与254 nm激发相比,其红光荧光寿命更长,量子效率更大。在y=0.04时,两种激发条件下(254 nm和365 nm)样品的红光荧光寿命(61.2 ms(62.2 ms))和量子效率(0.3(0.62))均达到最大值。 图9 (Mg0.8Sr0.2)2-ySiO4∶y(Eu3+,F-)以615 nm为监测波长的荧光寿命(a)与量子效率(b) Fig.9 Fluorescence lifetime(a) and quantum efficiency(b) of (Mg0.8Sr0.2)2-ySiO4∶y(Eu3+,F-) monitoring at wavelength 615 nm 采用高温固相法在1 150 ℃制备了(Mg1-x-Srx)2-ySiO4∶y(Eu3+,F-)(x=0~1)粉末。物相分析表明,组分为Sr2SiO4时(x=1),β-Sr2SiO4比α-Sr2SiO4更稳定,故β-Sr2SiO4相含量较高;随着Mg离子增加(0.8≥x≥0.2),不仅会出现γ-Mg2SiO4、β-Mg2SiO4、Sr3MgSi2O8相,且α-Sr2SiO4、β-Sr2SiO4相含量逐渐减少,但α-Sr2SiO4相中发生Mg离子取代形成固溶体而变得更为稳定,其含量减少速度比β-Sr2SiO4相慢;进一步进行晶体结构分析表明,由于Sr离子进入β-Mg2SiO4也可形成固溶体,β-Mg2SiO4变得更稳定且其含量增长速度比γ-Mg2SiO4更快,故x=0.8时α-Sr2SiO4为主晶相,而x=0.2时β-Mg2SiO4为主晶相;组分为Mg2SiO4时(x=0),γ-Mg2SiO4比β-Mg2SiO4稳定,故γ-Mg2SiO4相更多。紫外发光照相和光谱表明,(Mg1-xSrx)1.96SiO4∶0.04(Eu3+,F-)中当x=0.2时红光发射亮度最大。化学配比为(Mg0.8-Sr0.2)2SiO4粉末在1 250 ℃煅烧可以得到体积平均粒径为21.68 μm的单相β-Mg2SiO4粉末。XRD分析表明Eu离子掺杂不会影响(Mg0.8-Sr0.2)2SiO4物相结构,且XPS表明Eu离子以三价进入晶格。单相(Mg0.8Sr0.2)2-ySiO4∶y(Eu3+,F-)系列荧光粉在365 nm(或254 nm)激发下有595,615 (主峰),655,705 nm红光锐峰发射(对应5D0→7Fn,n=1,2,3,4),且y=0.04为最佳掺杂量,其荧光寿命为62.2 ms(或61.2 ms),量子效率为0.62(或0.30)。结合能级结构图可知其对应的红光发射过程为基体(Mg0.8Sr0.2)2SiO4吸收能量通过电荷转移传递给Eu3+发光中心,Eu3+的电子吸收能量跃迁到高能级随后驰豫到5D0能级进而产生5D0→7Fn(n=1,2,3,4)的红光发射;或Eu3+的电子吸收能量跃迁到5L6,随后无辐射驰豫到5D0能级进而产生5D0→7Fn(n=1,2,3,4)的红光发射。临界距离RC和lgy-lg(I/y)分析还表明,发光中心Eu3+之间的能量传递方式是基于辐射跃迁的电四极-电四极耦合。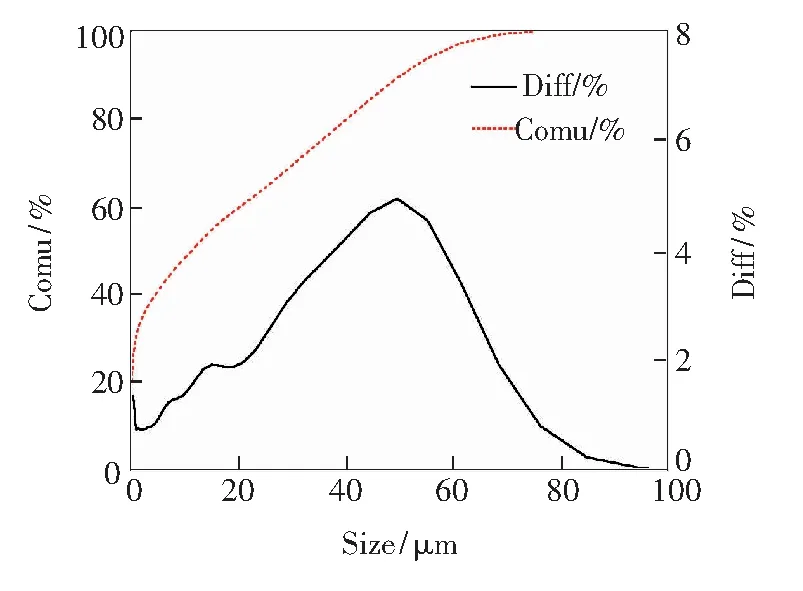
4 结 论
