多西他赛联合希罗达治疗复发转移性乳腺癌的疗效观察
2019-09-16吴家宝邓江波林元沛巫国海张名文朱美婷
吴家宝 邓江波 林元沛 巫国海 张名文 朱美婷
(广东省英德市人民医院颈胸外科 英德513000)
乳腺癌是临床常见的恶性肿瘤,指乳房腺体或导管上皮细胞发生癌变。虽然原位乳腺癌并不致死,但是乳腺癌细胞具有局部侵犯和远处转移的能力,通常会向肺、骨、肝脏等器官转移,所形成的肿瘤成为转移瘤或转移癌[1]。近年,我国乳腺癌的发病率呈现逐年上升的趋势,已经成为威胁我国女性生命安全的重大疾病。当前临床常使用蒽环类、紫杉醇等药物联合化疗治疗乳腺癌,但随着药物的多次使用,易让患者产生耐药性,导致乳腺癌复发和转移[2]。本研究旨在探讨多西他赛联合希罗达治疗复发转移性乳腺癌的有效性和安全性。现报道如下:
1 资料与方法
1.1 一般资料 选取2014 年1 月~2018 年12 月我院收治的60 例复发转移性乳腺癌患者,采用随机数字表法分为对照组和观察组各30 例。观察组年龄31~73 岁,平均年龄(44.62±2.37)岁;内脏转移16 例,骨转移12 例,软组织转移2 例。对照组年龄33~75 岁,平均年龄(45.74±2.86)岁;内脏转移18例,骨转移11 例,软组织转移1 例。两组一般资料比较,差异无统计学意义,P>0.05,具有可比性。本研究经我院医学伦理委员会审核批准。
1.2 纳入与排除标准 (1)纳入标准:经术后病理检查以及影像学检查确诊为转移性乳腺癌;均为女性;KPS 评分>90 分;病理分期Ⅳ期;签署知情同意书。(2)排除标准:对本研究使用药物过敏者;肝、肾等重要器官功能障碍者;妊娠或哺乳期女性。
1.3 治疗方法 对照组给予多西他赛(国药准字H20183209)75 mg/m2静脉滴注,持续滴注1 h,在给予多西他赛前30 min,给予地塞米松(国药准字H20056794)10 mg 静脉注射,苯海拉明(国药准字H32021435)40 mg 肌内注射,雷尼替丁(国药准字H32021588)50 mg 静脉滴注,化疗前10 min 加用10 mg 地塞米松,连续用药3 周为1 个疗程。观察组在对照组的基础上联合希罗达(国药准字H20073023)治疗,计划剂量2 500 mg/(m2·d),分早晚2 次于餐后30 min 服用,持续用药2 周后停药1周,3 周为1 个疗程。两组患者均治疗2 个疗程。
1.4 观察指标 (1)依据实体瘤疗效评价标准(RECIST1.1)判定两组临床疗效。完全缓解(CR):病灶完全消失,维持时间>4 周;部分缓解(PR):肿瘤最大直径及最大垂直直径的乘积缩小≥50%,维持时间>4 周;疾病稳定(SD):肿瘤最大直径及最大垂直直径的乘积缩小<50%,增大≤25%,维持时间>4 周;疾病进展(PD):肿瘤最大直径及最大垂直直径的乘积增大>25%[3]。临床控制总有效率=(CR+PR)/总例数×100%。(2)采集两组患者治疗前后空腹肘静脉血液5 ml,使用电化学发光法检测血清中的癌胚抗原(CEA)及糖类抗原CA19-9 水平。(3)统计两组患者治疗期间不良反应发生情况。
1.5 统计学方法 采用SPSS20.0 统计学软件处理数据,计量资料以表示,采用t 检验,计数资料用%表示,采用χ2检验,P<0.05 为差异具有统计学意义。
2 结果
2.1 两组临床疗效比较 观察组控制总有效率高于对照组,P<0.05,差异具有统计学意义。见表1。
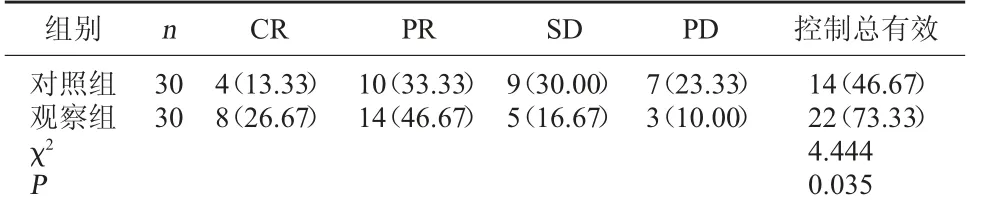
表1 两组临床疗效比较[例(%)]
2.2 两组治疗前后CEA、CA19-9 水平比较 治疗前,两组CEA、CA19-9 水平比较,差异无统计学意义,P>0.05;治疗后,两组CEA、CA19-9 水平均较治疗前明显降低,且观察组显著低于对照组,P<0.05,差异具有统计学意义。见表2。
表2 两组治疗前后CEA、CA19-9 水平比较
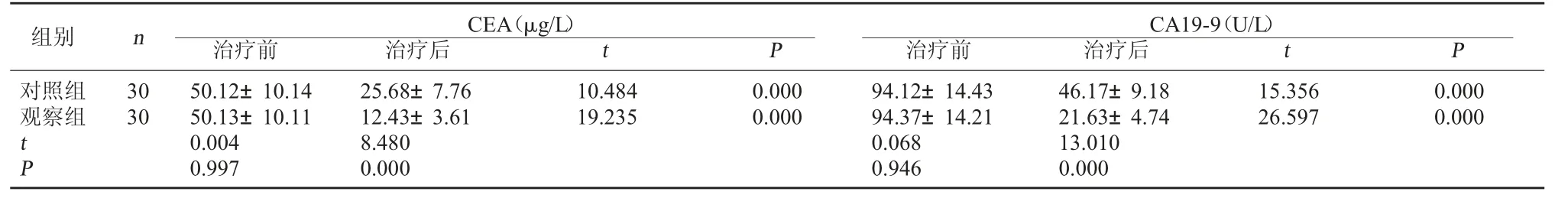
表2 两组治疗前后CEA、CA19-9 水平比较
组别 n治疗前 治疗后C EA(μg/L)t P治疗前 治疗后C A 19-9(U/L)t P对照组3050.12±10.1425.68±7.7610.4840.00094.12±14.4346.17±9.1815.3560.000观察组3050.13±10.1112.43±3.6119.2350.00094.37±14.2121.63±4.7426.5970.000 t 0.0048.4800.06813.010 P 0.9970.0000.9460.000
2.3 两组不良反应发生情况比较 两组中性粒细胞减少、手足综合征及乏力发生率比较,差异均无统计学意义,P>0.05。见表3。
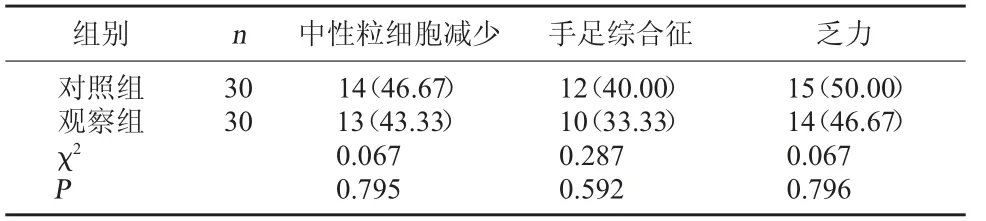
表3 两组不良反应发生情况比较[例(%)]
3 讨论
据相关数据统计[4],20%~40%的乳腺癌患者在手术治疗后会出现复发和转移,由于癌细胞扩散,增加了治疗难度。虽然复发转移性乳腺癌无法治愈,但近年来随着医疗水平发达,复发转移性乳腺癌在治疗后生存期均得到延长,生活质量得到提高[5]。
CEA 是一种蛋白多糖复合物,广泛存在于癌症患者的血清中,是一种较好的肿瘤标志物;CA19-9是细胞膜上的糖脂质,作为乳腺癌的肿瘤标志物,特异性和敏感性可达90%以上[6]。因此,CEA 和CA19-9水平变化可评估癌细胞扩散程度。本研究结果显示,观察组控制总有效率高于对照组(P<0.05);治疗后,两组CEA、CA19-9 水平均较治疗前明显降低,且观察组显著低于对照组(P<0.05);两组中性粒细胞减少、手足综合征及乏力发生率比较,差异均无统计学意义(P>0.05)。说明多西他赛联合希罗达治疗复发转移性乳腺癌可以抑制癌细胞扩散,提高疗效,且安全性较高。多西他赛是人工合成的紫杉类抗肿瘤药物,可特异性地作用于肿瘤细胞周期,发挥加强微管蛋白聚合和抑制微管解聚作用,从而达到破坏肿瘤细胞有丝分裂的效果,抑制癌细胞扩散[7]。研究表明[8],多西他赛虽属紫杉类药物,但是使用相同剂量的紫杉醇,多西他赛在细胞内的药物浓度是紫杉醇的三倍,且与紫杉醇不会发生交叉耐药。但多西他赛副作用较大,在使用前必须给予地塞米松,减少体液潴留的发生率。希罗达是肿瘤内优先活化的氟尿嘧啶类抗肿瘤药,可单独用于治疗复发转移性乳腺癌[9]。在被肠道吸收后,可水解为5'-脱氧-5-氟胞苷(5'-DFCR),在肿瘤组织中5'-DFCR 可转化为5'-脱氧-5 氟尿苷(5'-DFUR),与胸腺嘧啶磷酸化酶(TP)结合后催化5-Fu,对癌细胞表现出细胞毒性,对于正常组织而言,不会转化为5-Fu,故不会损害正常组织细胞,不良反应较少[10]。因此,多西他赛联合希罗达能够通过不同机制杀灭癌细胞,阻止乳腺癌细胞向周围器官扩散,并且因副作用多由多西他赛引起,两药联合使用安全性变化较小。综上所述,复发转移性乳腺癌患者采用多西他赛联合希罗达治疗,可抑制癌细胞扩散,且安全性高,值得临床推广。
