佛手标准汤剂中两种成分的测定方法研究
2019-09-10孙福仁高晗李雪利张肖建李军山李振江
孙福仁 高晗 李雪利 张肖建 李军山 李振江


摘要:为提高佛手配方颗粒的质量评价标准,利用佛手标准汤剂控制佛手配方颗粒的内在质量。以15批不同产地的佛手饮片为原料,制备佛手标准汤剂,建立含量测定方法,以柚皮苷、橙皮苷为指标成分,测定了15批佛手标准汤剂的相关含量。结果表明:柚皮苷、橙皮苷分别在0.0251~0.1255,0.1605~0.8023μg范围内线性关系良好(r=0.9999),平均加样回收率分别为102.27%和101.48%,重复性考察RSD值分别为0.78%和0.89%,12h稳定性考察RSD值分别为0.59%和1.46%。所提出的方法能同时测定柚皮苷和橙波苷两种成分,节约了分析时间,提高了佛手产品的质量标准。
关键词:中药化学;佛手标准汤剂;橙皮苷;柚皮苷;含量测定
中图分类号:R284.1文献标志码:A
doi:10.7535/hbgykj.2019yx03012
文章编号:1008-1534(2019)03-0221-06
佛手系芸香科植物佛手的干燥果实,具有梳理肝气、止痛、和胃的功效[1],为常用理气中药。成熟佛手果实中含有柠檬油素、5-异戊烯氧基-7-甲氧基香豆素、6,7-二甲氧基香豆素、7-羟基-6-甲氧基香豆素、4-甲氧基联卞、柠檬内酯、Δ5,22-豆甾烯醇、棕榈酸等成分[2-3]。现代药理学研究表明:佛手具有降低脂质代谢、降低总胆固醇、促进糖脂代谢等生物活性[4-6];佛手醇提液具有显著镇咳、平喘、祛痰作用,可提高机体的抗应激能力[7]。
关于佛手中相关含量的测定研究,文献[8]和文献[9]介绍了采用RP-HPLC法测定佛手中的橙皮苷含量;金晓玲等[10]测定出佛手饮片中的粗蛋白质量分数为9.37%,氨基酸质量分数为8.334%;曹斯琼等[11]应用UPLC指纹图谱方法,对广佛手饮片、水煎液、配方颗粒进行了相似度评价研究。HPLC指纹图谱方法的建立,可用于评价佛手质量[12-13]。然而,迄今尚未见有佛手标准汤剂含量测定方法的报道。佛手标准汤剂是以传统煎煮法为理论依据,经提取制备而成的膏粉或浓缩液,用于衡量佛手配方颗粒的内在质量。笔者收集了不同产地的佛手饮片制备佛手标准汤剂,采用建立的能够同时测定柚皮苷、橙皮苷含量的测定方法,对15批佛手标准汤剂含量进行了测定。
1主要仪器与材料
CPA225D电子分析天平,德国赛多利斯股份公司提供;KH-7200E超声波清洗器,江苏昆山禾创超声波仪器有限公司提供;WATERSCLASSHUPLC液相色谱仪,AgilentZorbaxEcilpesC18色谱柱(2.1mm×100mm,1.7μm)。
15批不同产地、不同批次的佛手饮片,分别采购于四川、广东、缅甸、越南、泰国等地,且于不同时间采收加工,经原河北省药品检验所孙宝惠老师鉴定,确定为芸香科植物佛手的干燥果实经炮制加工后的饮片,饮片来源及批号见表1。
橙皮苷对照品,中国药品生物制品检定所提供,纯度为94.5%;柚皮苷对照品,中国药品生物制品检定所提供,纯度为96.5%;甲醇,色谱纯,天津科密欧有限公司提供;乙腈,色谱纯,天津科密欧有限公司提供;其余试剂均为分析纯,水为纯化水。
2方法与结果
2.1色谱条件和系统适用性
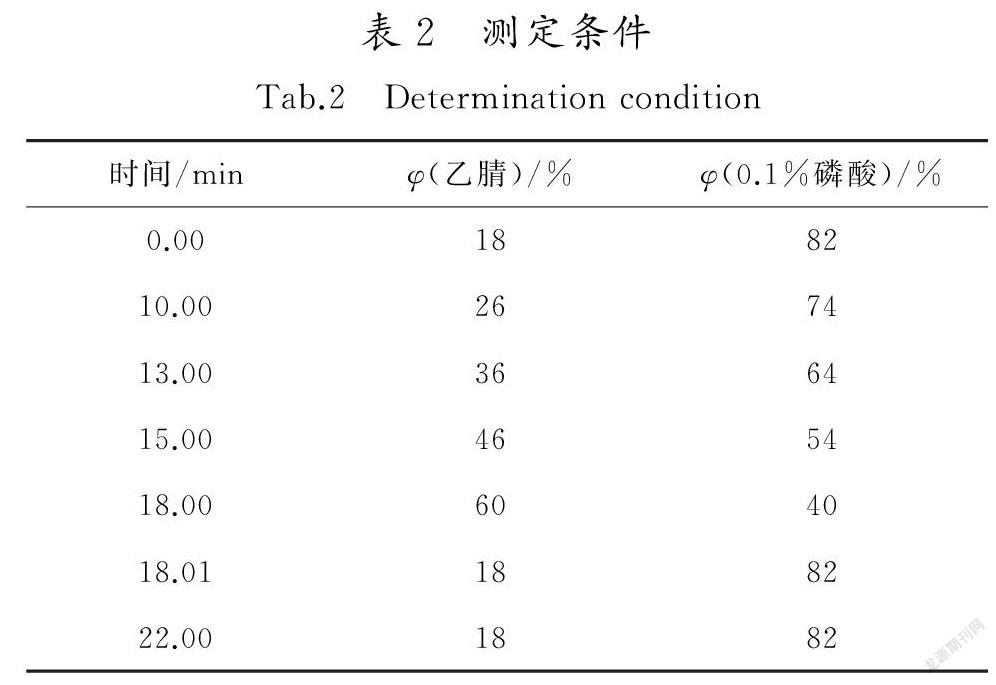
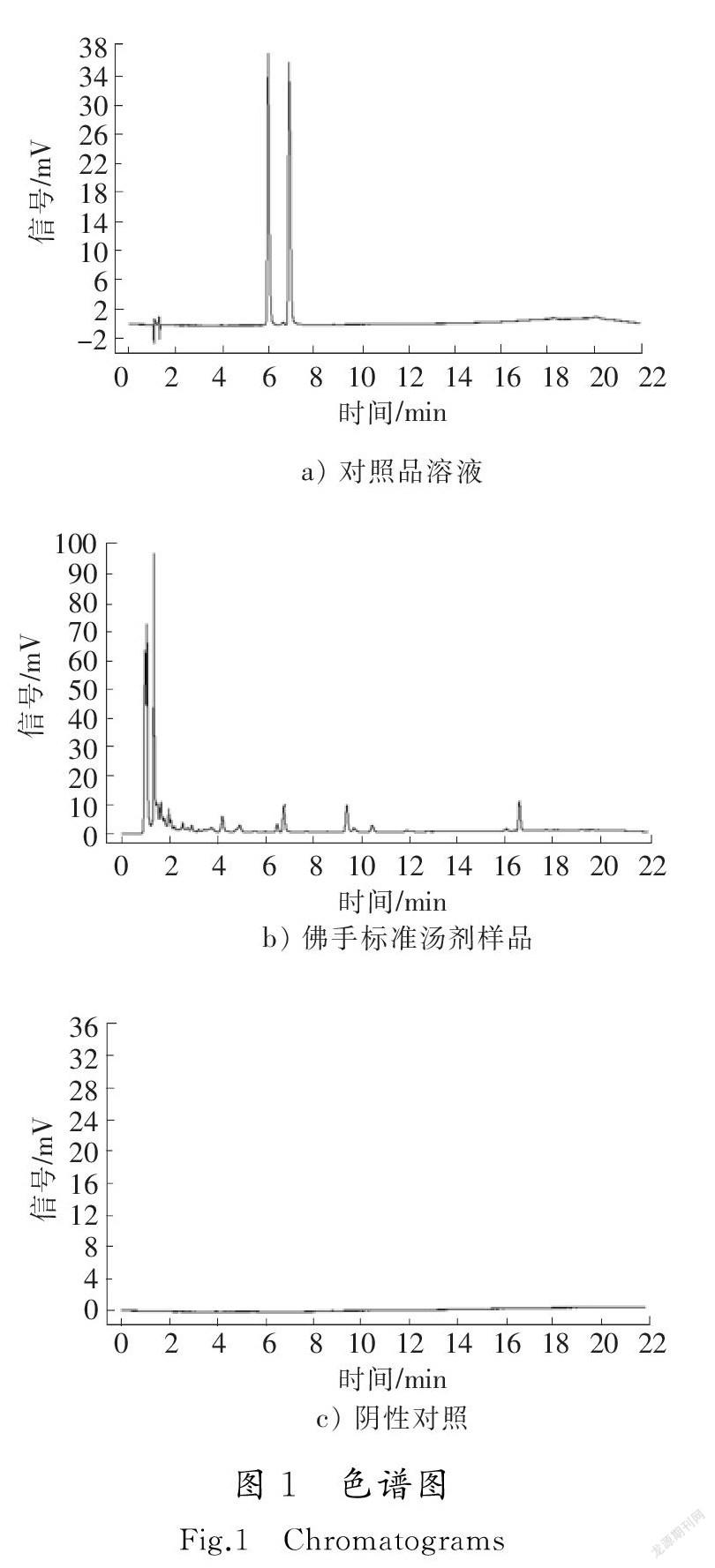
采用AgilentZorbaxEcilpesC18色谱柱(2.1mm×100mm,1.7μm),以乙腈-0.1%(体积分数,下同)磷酸为流动相,检测波长为283nm,柱温为30℃,流速为0.2mL/min,理论板数按橙皮苷、柚皮苷峰计算应不低于5000[14-15],测定条件见表2,色谱图见图1。
2.2对照品溶液的制备
精密称定用干燥剂减压干燥24h的柚皮苷5.51mg、橙皮苷9.73mg,置于50mL容量瓶中,用甲醇溶解并定容至刻度,摇匀。精密吸取2mL,放入10mL容量瓶中,加入甲醇定容至刻度,摇匀,即得每1mL含柚皮苷22.0μg、橙皮苷38.9μg的混合对照品溶液。
2.3佛手标准汤剂的制备
取各批次佛手饮片,除去杂质。称取100g,放入圆底烧瓶中,加入饮片量12倍的水,浸泡30min,加热煎煮30min。第2次加入饮片量10倍的水,加热煎煮20min。合并2次煎液,用0.074mm(200目)筛网过滤煎煮液,合并滤液。在高于60℃的温度下,将佛手提取液用旋转蒸发仪浓缩,浓缩至生药量与浓缩液体积比约为1∶3,再经浓缩液冷冻干燥机干燥,得到干膏粉,即佛手标准汤剂。
2.4供试品溶液的制备
取各批次佛手标准汤剂,粉碎过2号筛。精密称定0.3g,转移至具塞锥形瓶中,精密加入90%甲醇25mL,超声(功率为250W,频率为40kHz)处理10min,再称定质量。用90%甲醇补足减失的质量,摇匀,过滤,即得。
2.5方法学考察
2.5.1標准曲线
分别精密吸取对照品溶液0.4,0.8,1.2,1.6,2.0μL,按上述色谱条件进行测定,记录峰面积。分别以柚皮苷、橙皮苷的进样量(X)为横坐标,测定的峰面积(Y)为纵坐标,线性关系结果见表3。结果表明,2种成分在适当范围内线性关系良好。
2.5.2精密度
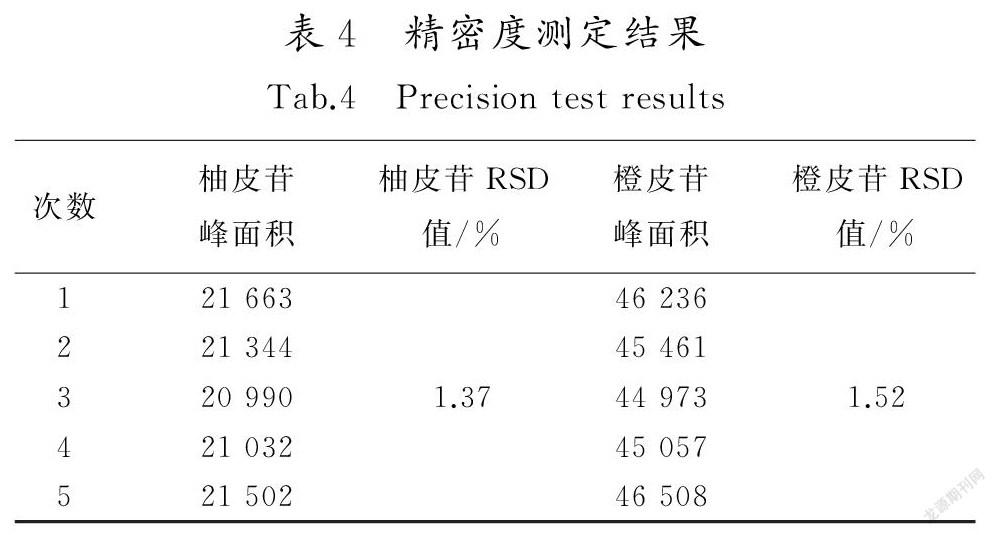
取佛手标准汤剂S13样品,参考供试品制备方法进行处理,依照上述色谱条件连续进样5次,计算峰面积的RSD值,测定结果见表4。结果表明,柚皮苷与橙皮苷峰面积基本不变,RSD值分别为1.37%和1.52%,说明仪器的精密度良好。
2.5.3稳定性
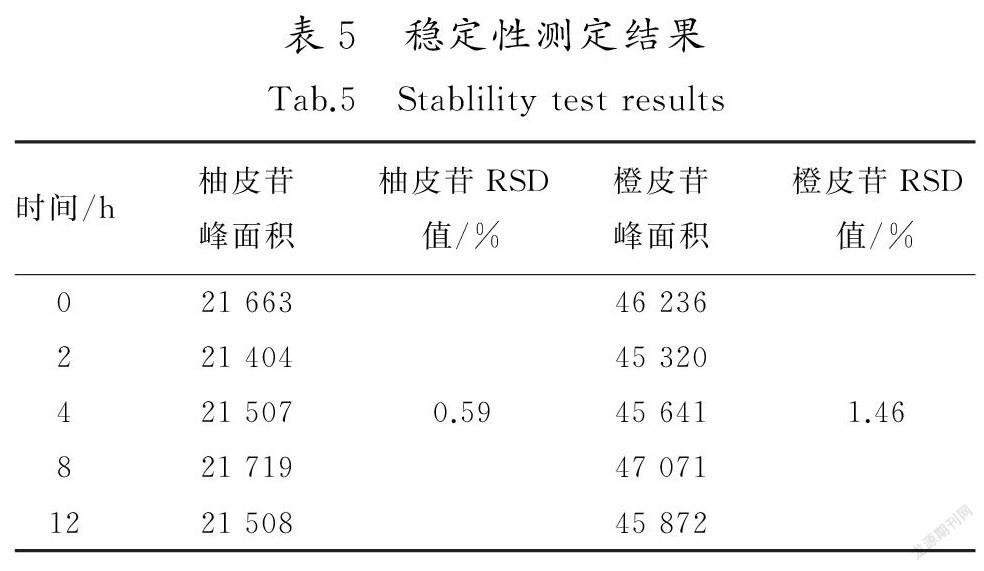
取佛手标准汤剂S13干膏粉适量,按供试品溶液制备方法制备供试品溶液,依照上述色谱条件分别于0,2,4,8,12h进样测定,计算柚皮苷的峰面积,结果见表5。由表5可知,柚皮苷和橙皮苷RSD值分别为0.59%和1.46%(n=5),表明样品中柚皮苷、橙皮苷在溶液状态下12h内稳定。
2.5.4重复性
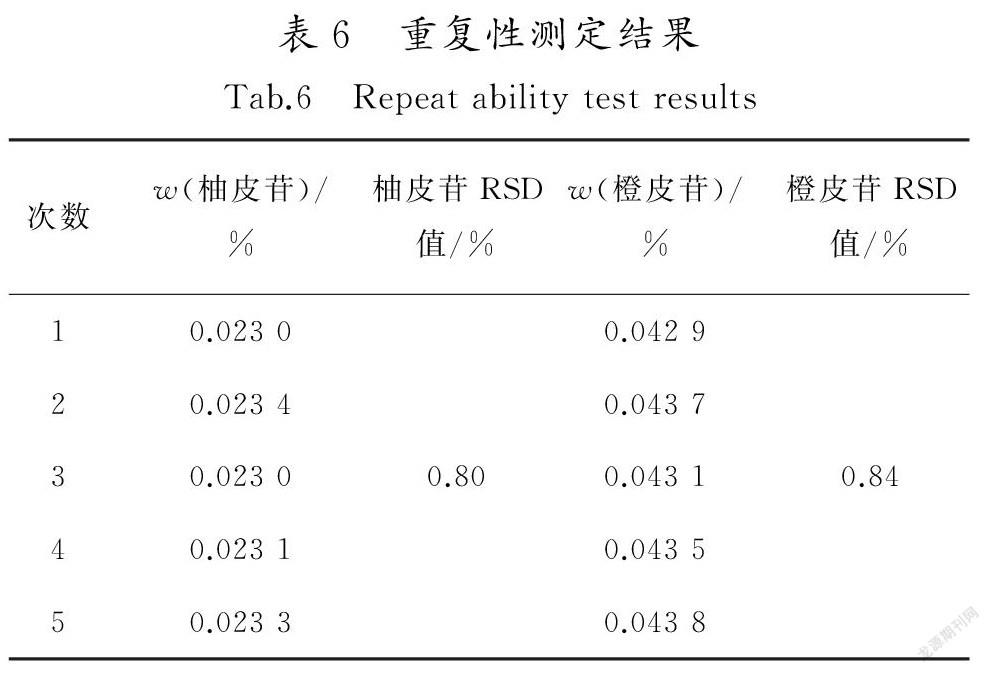
取佛手标准汤剂S13干膏粉适量,分别称取5份,按供试品溶液制备方法制备。精密吸取供试品溶液1μL,依照上述色谱条件进行测定,结果见表6。结果表明,供试品溶液中柚皮苷、橙皮苷含量的RSD值分别为0.80%和0.84%(n=5),说明方法的重复性良好。
2.5.5加样回收率
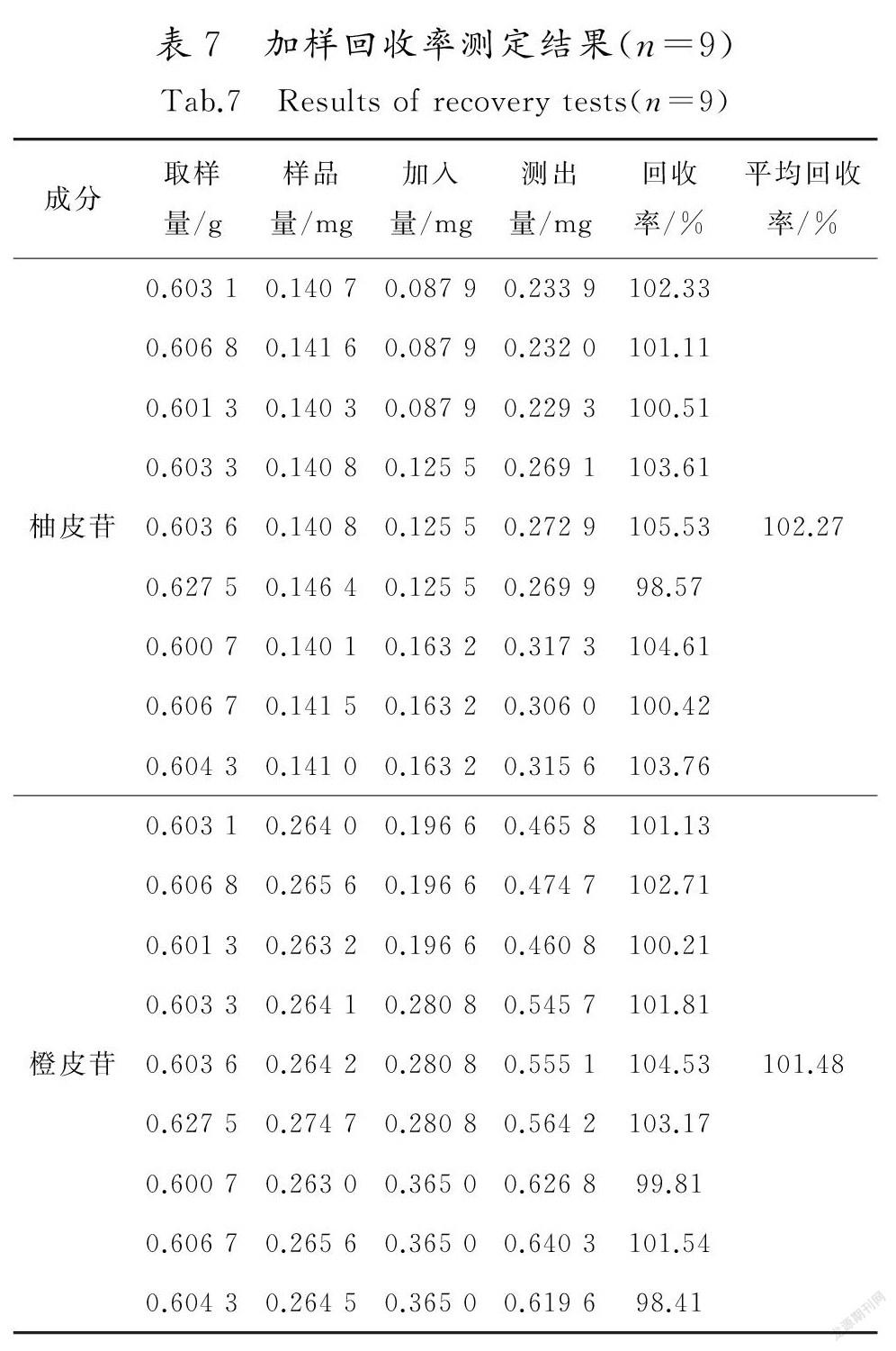
取同一批干膏粉(S13)9份,精密称定。分别精密加入一定量的柚皮苷、橙皮苷储备液,依照供试品溶液制备方法制备,按上述色谱条件测定,每份平行测定2次,结果见表7。由表7可知,柚皮苷的平均回收率为102.27%(n=9),橙皮苷的平均回收率为101.48%(n=9)。说明方法的回收率较好,符合要求。
2.6样品测定
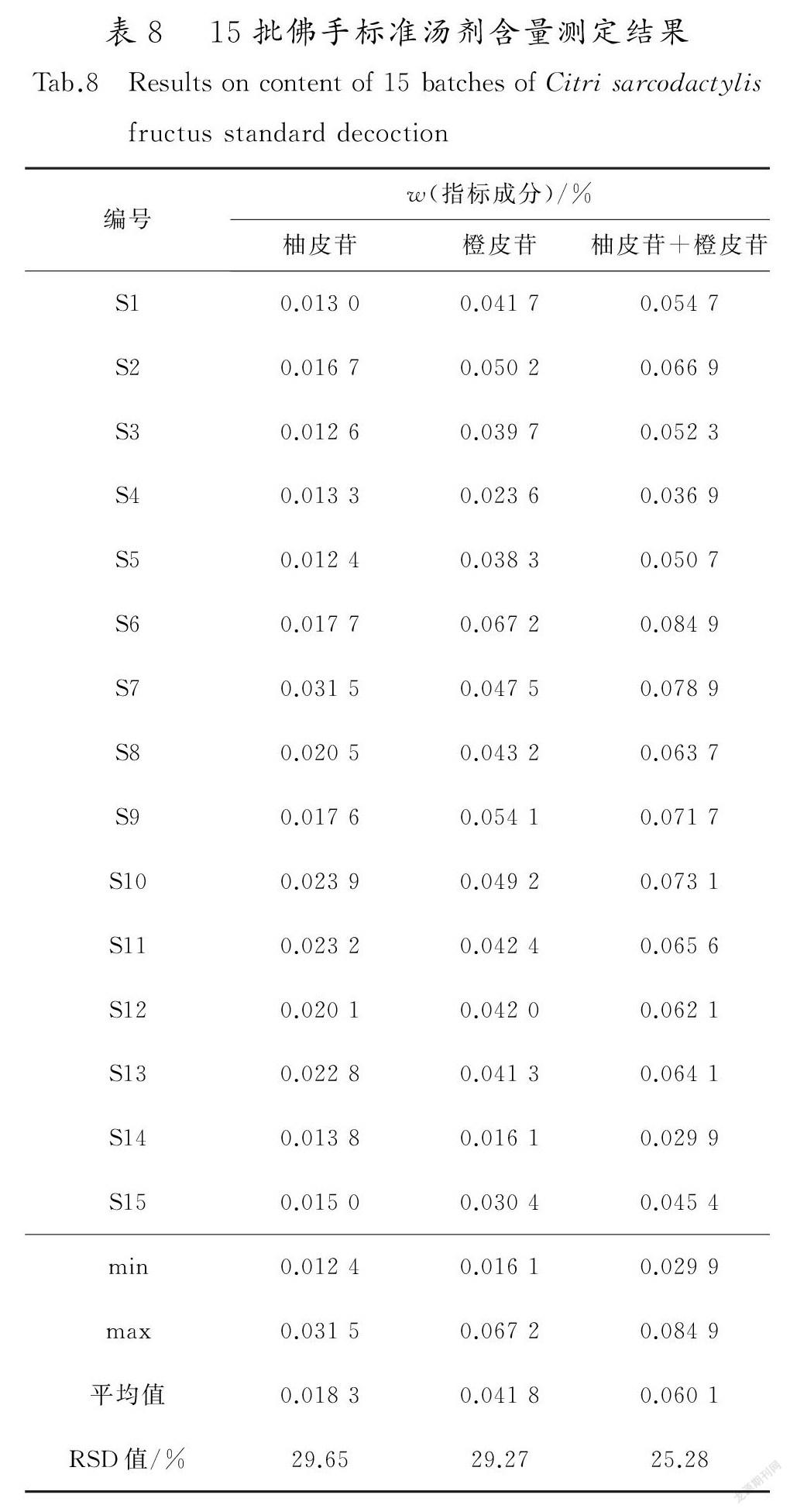
取佛手标准汤剂适量,按照2.4项所述方法制备样品溶液。另取柚皮苷、橙皮苷对照品适量,按照2.2项所述方法制备对照品溶液。按上述色谱条件进样,记录柚皮苷、橙皮苷峰面积,计算含量,结果见表8。
由表8可知,标准汤剂中柚皮苷与橙皮苷的含量测定和转移率数据平行性良好。15批佛手标准汤剂中指标成分柚皮苷与橙皮苷含量之和为0.0299%~0.0849%,平均含量为0.0601%,SD值为0.0152%,RSD值为25.28%。柚皮苷与橙皮苷含量之和平均值的70%~130%的范围为0.0420%~0.0781%,平均值加减3倍SD值的范围为0.0145%~0.1056%。
3讨论
3.1检测波长的选择
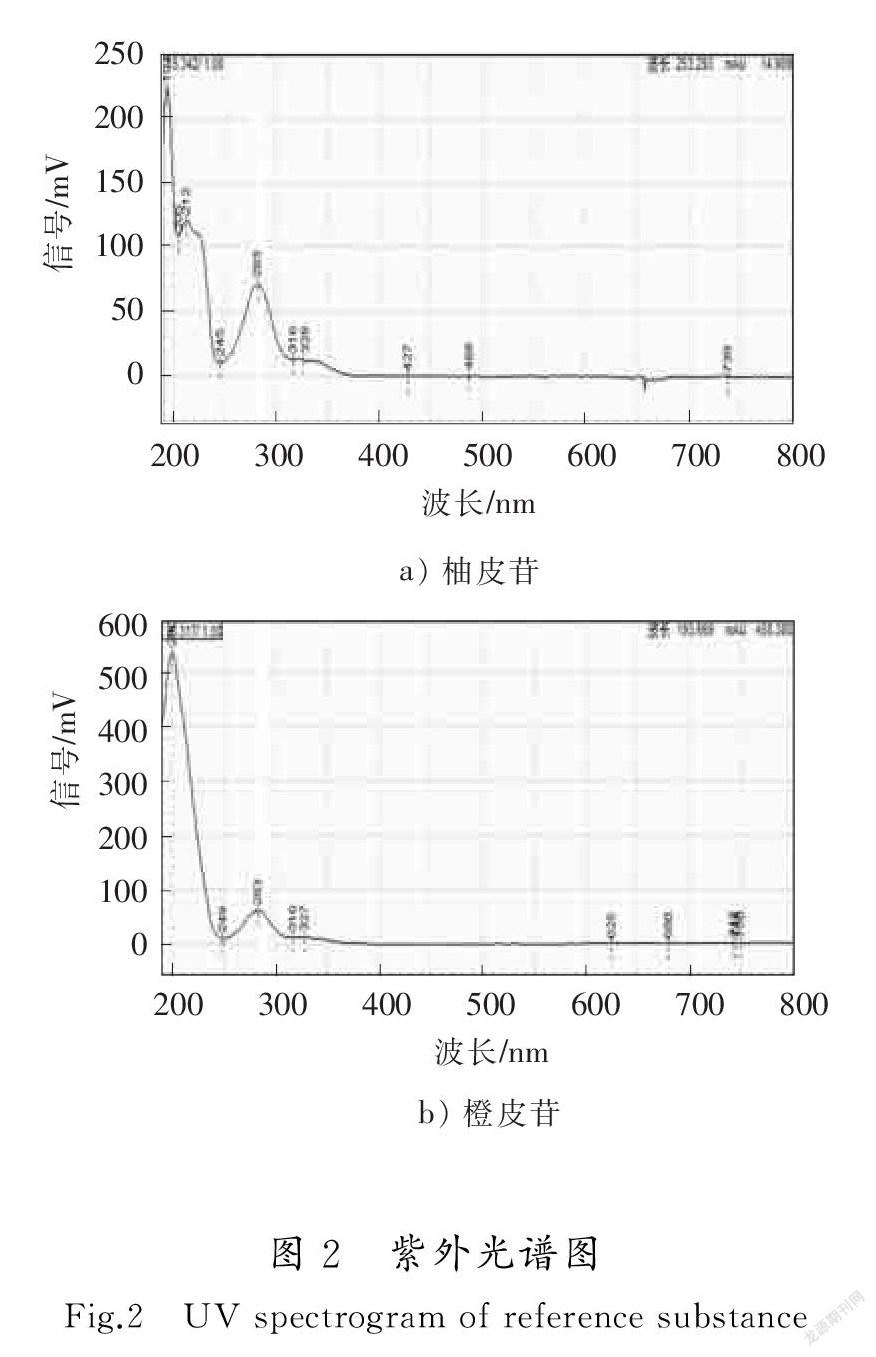
柚皮苷、橙皮苷紫外光谱图如图2所示。由图2可从看出,柚皮苷、橙皮苷均为黄酮类成分,在紫外多个波段有吸收,283nm波长处有最大紫外吸收,故确定283nm为检测波长。
3.2提取溶剂的选择
柚皮苷、橙皮苷2种成分水溶性极差,适宜用有机溶剂提取。考虑到佛手标准汤剂使用水作为提取溶媒、使用100%甲醇作提取溶剂时,膏粉容易结块,不能完全分散开,经实验考察,分别使用甲醇、90%甲醇、70%甲醇、50%甲醇为提取溶剂进行含量比较,发现采用90%甲醇为提取溶剂时的含量最高,故选择90%甲醇作为提取溶剂。
3.3流动相选择
分别比较了乙腈-水、乙腈-0.1%磷酸、甲醇-0.1%磷酸3种流动相,结果发现,采用乙腈-0.1%磷酸为流动相的分离效果较好,故确定其作为流动相。此外,橙皮苷、柚皮苷化学结构类似,极性接近,使用梯度洗脱的方法分析时间较长,故采用梯度洗脱方式分离,可使佛手标准汤剂中的其他成分与目标成分之间实现较好地分离。
4结语
1)《中华人民共和国药典》2015版中仅介绍了佛手含量测定以橙皮苷单一成分为指标。通过方法摸索,在UPLC设备上建立了能夠同时测定柚皮苷、橙皮苷2种成分的方法,节约了分析时间,提高了质量标准。
2)受佛手产地地理位置的影响,15批佛手饮片中橙皮苷的含量相差较大。标准汤剂以水作为溶媒时橙皮苷的水溶性较差,而15批佛手标准汤剂中柚皮苷与橙皮苷含量之和转移率范围为28.01%~43.64%,因此,佛手标准汤剂应以柚皮苷、橙皮苷含量之和作为指标成分。
3)本次研究利用UPLC法,采取梯度洗脱,建立了能够同时测定柚皮苷和橙皮苷2种成分的分析方法,对文献报道中的5,7-二甲氧基香豆素的成分也进行了相关分析。然而,由于此成分在佛手标准汤剂中的含量较低,含量转移率低于5%,故在含量测定指标筛选时,舍去了该成分。黄酮类成分在佛手标准汤剂中所占的量较大,今后需对其作进一步的研究。
参考文献/References:
[1]国家药典委员会.中华人民共和国药典(一部)[M].北京:中国医药科技出版社,2015.
[2]张颖,孔令义.佛手化学成分的研究[J].中国现代中药,2008,8(6):16-17.
ZHANGYing,KONGLingyi.StudiesontheconstituentsofCitrusmedicaL.var.sarcodactylisSwingle[J].ModernChineseMedicine,2008,8(6):16-17.
[3]高幼衡,黄海波,徐鸿华,等.佛手化学成分研究[J].中药材,2002,25(9):639-640.
GAOYouheng,HUANGHaibo,XUHonghua,etal.StudiesonthechemicalconsitutentsofCitrusmedicaL.var.sarcodactylis[J].JournalofChineseMedicinalMaterials,2002,25(9):639-640.
[4]史晶晶,时博.橙皮苷对高脂血症模型大鼠代谢紊乱的影响[J].中医学报,2016,31(4):554-557.
SHIJingjing,SHIBo.Effectofhesperidinonlipidmetabolismdisorderinhyperlipemiamodelrats[J].ActaChineseMedicine,2016,31(4):554-557.
[5]PARAFATIM,LUSCIAA,MORITTAVM,etal.Bergamedpolyphenolfractionpreventsnonalcoholicfartyliverdiseaseviastimulationoflipophagyincafeteriadietinducedratmodelofmetabolicsyndrome[J].JournalofNutritionalBiochemistry,2015,26(9):938-948.
[6]吴昊,橘波,何俏军,等.新橙皮苷在制备预防糖尿病药物中的应用[P].中国专利:CN102772424A,2012-06-13.
[7]金曉玲,徐丽珊,何新霞.佛手醇提取液的药理作用研究[J].中国中药杂志,2002,27(8):604-606.
[8]宋剑锋,富同义.RP-HPLC法测定佛手饮片中橙皮苷含量[J].中华中医药学刊,2007,25(5):1036-1037.
SONGJianfeng,FUTongyi.ContentdeterminationofhesperidininfructusCitrissarcodactylisbyRP-HPLC[J].ChineseArchivesofTraditionalChineseMedicine,2007,25(5):1036-1037.
[9]曾建伟,吴锦忠,林忠宁,等.HPLC测定不同产地佛手中橙皮苷的含量[J].中国实验方剂学杂志,2012,18(19):97-99.
ZENGJianwei,WUJinzhong,LINZhongning,etal.DeterminationofhesperidininfructusCitrissarcodactylisfromdifferentprovenancesbyHPLC[J].ChineseJournalofExperimentalTraditionalMedicalFormalae,2012,18(19):97-99.
[10]金晓玲,曹诣斌,徐丽珊,等.佛手氨基酸及多糖含量的测定[J].浙江师范大学学报(自然科学版),2002,25(1):66-68.
JINXiaoling,CAOYibin,XULishan,etal.ContentsofaminoacidsandpolysaccharidesfromBergamot[J].JournalofZhejiangNormalUniversity(NaturalSciences),2002,25(1):66-68.
[11]曹斯琼,陈向东,黄丹丹,等.佛手配方颗粒UPLC指纹图谱研究[J].海峡药学,2018,30(6):48-52.
CAOSiqiong,CHENXiangdong,HUANGDandan,etal.UPLCfingerprintanalysisofCitrusmedicaL.var.sarcodactylisSwingleformulagranules[J].StraitPharmaceuticalJournal,2018,30(6):48-52.
[12]李金玉,贺文婷,王喜英.不同采收期广佛手指纹图谱研究[J].安徽农业科学,2015,43(14):99-101.
LIJinyu,HEWenting,WANGXiying.HPLCfingerprintoffructusCitrisarcodactylisindifferentpickingtimes[J].JournalofAnhuiAgriculturalSciences,2015,43(14):99-101.
[13]林乐维,蒋林,郝大庆,等.不同产地广佛手药材HPLC指纹图谱的研究[J].中成药,2009,31(12):1805-1808.
LINLewei,JIANGLin,HAODaqing,etal.HPLCfingerprintoffructusCitrisarcodactylisfromGuangdongprovince[J].ChinsesTraditionalPatentMedicine,2009,31(12):1805-1808.
[14]孙福仁,李军山,马浩,等.基于UPLC特征图谱与主成分分析评价白芷配方颗粒质量研究[J].河北工业科技,2018,35(6):454-458.
SUNFuren,LIJunshan,MAHao,etal.StudyonevaluationofthequalityofformulagranuleofAngelicaedahuricaebasedonUPLCandPCA[J].HebeiJournalofIndustrialScienceandTechnology,2018,35(6):454-458.
[15]田方,李军山,常云凤,等.一测多评法同时测定车前子配方颗粒中3种成分含量[J].河北工业科技,2018,35(6):459-464.
TIANFang,LIJunshan,CHANGYunfeng,etal.SimultaneousdeterminationofthreeconstituentsinPlantagoseedformulagranulesbyQAMS[J].HebeiJournalofIndustrialScienceandTechnology,2018,35(6):459-464.
