应用限制性片段长度多态性检测幽门螺杆菌对克拉霉素的耐药性
2019-09-05吴文冰方超英吴绍莲
吴文冰,方超英,陈 雯,吴绍莲
(1福建医科大学省立临床医学院,福建省立医院检验科,福州 350001;2福建医科大学省立临床医学院,福建省立医院内镜中心)
幽门螺杆菌(Helicobacterpylori,HP)是一种在人类胃黏膜中发现的革兰阴性微需氧菌,研究发现其与各种消化性疾病,例如消化性溃疡、胃炎及黏膜相关淋巴组织淋巴瘤等关系密切,同时也是胃癌的高危因素之一[1]。以克拉霉素为基础的三联疗法是目前根治HP感染最重要的方法之一,近年来随着克拉霉素的泛应用,其耐药性呈上升趋势,而HP对克拉霉素耐药是导致治疗失败的主要原因[2,3]。本研究通过建立应用限制性片段长度多态性(restriction fragment length polymorphism,RFLP)分析来检测HP的23S rRNA V区DNA序列突变的方法,探讨23S rRNA V区基因与耐克拉霉素的相关性及其耐药的分子机制,同时为临床提供更为简便、经济、快速的检测方法。
1 材料与方法
1.1 研究对象
收集2017-06~2017-12本院胃镜室尿素酶快速检测法(福建三强公司)阳性的胃窦部或胃体部黏膜活检标本100例,其中确诊为消化性溃疡31例,胃炎69例,男性66例,女性34例,年龄24-69岁,平均年龄(32.1±12.7)岁,所有研究对象均签署知情同意书。所有活检标本经充分研磨混匀后分成两份,一份用于抽提组织DNA,另一份用于培养及药敏鉴定。
1.2 研究方法
1.2.1 HP的培养及药敏鉴定 培养采用含HP选择添加剂(OXOID公司)的哥伦比亚琼脂(OXOID公司)培养基,微需氧环境(5%O2,10%CO2及85%N2)培养5 d,所得单个菌落经显微镜检形态吻合,且尿素酶、过氧化氢酶及氧化酶均阳性的判定为HP。药敏鉴定参照文献[4]采用纸片琼脂扩散法,即取纯培养72 h的菌落,用生理盐水调成1.0×108CFU/ml,接种于含5%羊血的水解酪蛋白(Mueller-Hinton,M-H)培养基平板,在培养基平板中央贴15 μg的克拉霉素药敏纸片(OXOID公司),微需氧环境(5%O2,10%CO2及85%N2)培养5 d,根据临床和实验室标准协会(2012)标准,用游标卡尺读取抑菌环直径,当抑菌环直径≥17 mm时为克拉霉素敏感菌株,当抑菌环直径≤13 mm时为克拉霉素耐药菌株。
1.2.2 HP的DNA抽提及PCR扩增 耐药菌菌株DNA及其对应的胃黏膜组织DNA抽提分别采用QIAamp DNA Mini Kit和DNeasy Tissue kit(Qiagen公司),严格按操作说明书进行,所得产物作为模板,按照文献[5]合成HP 23S rRNA V区PCR扩增引物,上游引物为:5′-CCACAGCGATGTGGTCTCAG-3′,下游引物为:5′-CTCCATAAGAGCCTGACT-3′(上海铂尚公司合成)。50 μl PCR反应体系含:5 μl DNA、1.5 mmol MgCl2、0.5 μmol引物,200 μmol dNTP,1 U Taq polymerase(Takara公司)。PCR条件:95 ℃变性60 s,95 ℃ 30 s、58 ℃ 30 s及72 ℃ 30 s,共35个循环,72 ℃延伸2 min,取5 μl产物进行琼脂糖电泳,紫外灯下观察结果,其余PCR产物采用DNeasy Tissue kit(Qiagen公司)进行纯化,所得产物保存于-20 ℃冰箱。
1.2.3 PCR产物RFLP分析 将上述PCR纯化产物采用BbsⅠ和BsaⅠ(New England Biolabs)进行RFLP分析,20 μl反应体系含:5 μl PCR纯化产物、5UBbsⅠ或BsaⅠ。反应条件:BbsⅠ在37 ℃酶切12 h,BsaⅠ在50 ℃酶切12 h,各取5 μl酶切产物进行琼脂糖凝胶电泳,紫外灯下观察结果。
1.2.4 DNA测序 将耐药菌菌株DNA及其对应的胃黏膜组织DNA送上海铂尚公司进行测序。
2 结果
2.1 克拉霉素耐药率
从100例活检样本中鉴定出37例耐克拉霉素的HP,耐药率为37%。
2.2 PCR扩增产物电泳结果
37例耐药菌菌株及其相对应的胃黏膜组织抽提所得DNA均扩增出特异性条带,扩增片段大小为425 bp,与设计的片段大小相一致(见图1)。
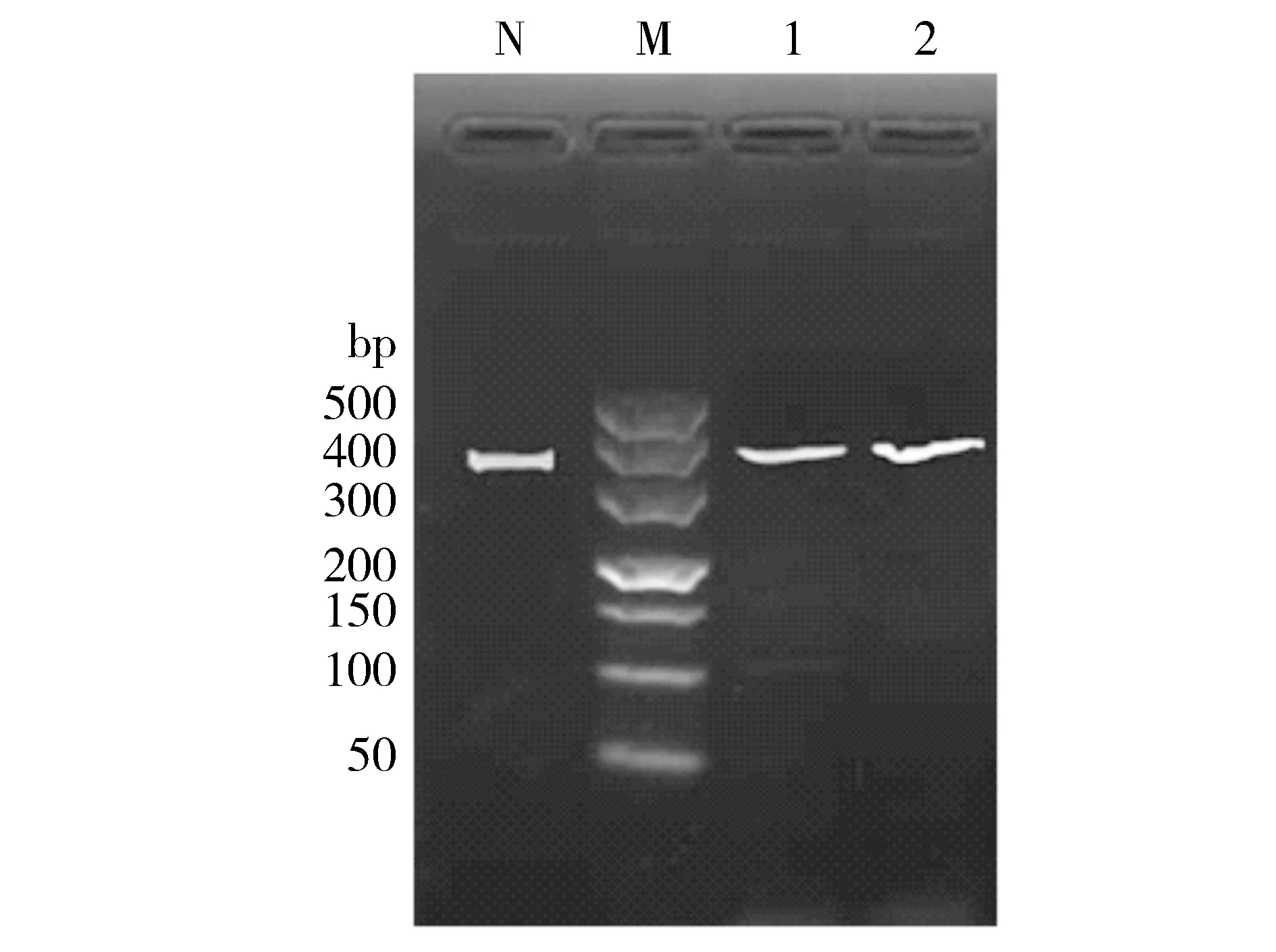
N.NCTC11637野生株;1.耐药菌菌株DNA;2.胃黏膜组织DNA;M.DL500 DNA Marker(Takara公司)图1 耐药菌菌株和胃黏膜组织PCR扩增产物电泳图Figure 1 The PCR product of clinical Helicobacter pylori isolates resistant to clarithromycin and gastric biopsies
2.3 RFLP分析结果
37例耐药菌菌株DNA及其相对应的胃黏膜组织DNA的PCR产物经RFLP分析,各菌株对应的胃黏膜组织RFLP分析结果完全一致,其中21例能被BbsⅠ内切酶切开,13例能被BsaⅠ内切酶切开,3例不能被BbsⅠ和BsaⅠ内切酶切开(见图2)。

N.为NCTC11637野生株;M.为DL500 DNA Marker(Takara公司);1.耐药菌菌株PCR产物经BbsⅠ酶切;2.耐药菌菌株PCR产物经BsaⅠ酶切;3.胃黏膜组织PCR产物经BbsⅠ酶切;4.胃黏膜组织PCR产物经BsaⅠ酶切图2 耐药菌菌株和胃黏膜组织PCR产物RFLP分析结果Figure 2 RFLP analysis of PCR products from clinical Helicobacter pylori isolates resistant to clarithromycin and gastric biopsies
2.4 PCR产物测序结果
37例耐药菌的菌株DNA和胃黏膜组织DNA的PCR产物测序结果完全一致,21例能被BbsⅠ内切酶切开的DNA序列存在A2142G突变,13例能被BsaⅠ内切酶切开的DNA序列存在A2143G,3例不能被BbsⅠ和BsaⅠ内切酶切开的DNA序列不存在点突变(见图3)。

图3 耐药菌菌株和胃黏膜组织PPCR产物测序结果图Figure 3 Sequencing of the PCR products from clinical Helicobacter pylori isolates resistant to clarithromycin and gastric biopsies
3 讨论
克拉霉素的化学名称是6-甲基红霉素,是目前应用最广泛的大环内酯类抗生素之一,其抗菌作用机制是进入细菌细胞内并结合在HP23S rRNA功能区中V区的50S大亚基上,抑制肽酰基转移酶,影响核糖体的移位过程,阻止肽链的延长,从而抑制细菌蛋白合成,达到清除HP的目的[6],而且克拉霉素还具有对酸稳定和在胃黏膜中浓度高、口服后生物利用率高和不良反应少等优点,因此克拉霉素很快成为根除HP治疗方案的主要抗菌药物,临床上含克拉霉素的三联疗法较之不含克拉霉素的三联疗法相比,HP根除率可以提高10%-20%。同其他抗生素一样,随着克拉霉素的广泛使用,临床上逐渐开始出现耐克拉霉素的HP,耐药率从10%到30%不等(如法国国为10%,意大利为24.2%)[7],更为严重的是在儿童中也出现了高耐药的HP[8],因此建立HP对克拉霉素耐药性的快速检测,为临床用药提供指导具有重要的意义。
目前有关克拉霉素耐药机制的研究主要集中在HP 23S rRNA V区的肽基转移酶基因编码区域出现的基因点突变[9,10],V区基因的突变导致克拉霉素不能和50S大亚基结合,也就无法对HP进行清除,从而出现耐克拉霉素的HP。这些点突变包括A2142G,A2143G,A2144G,T2182C,T2190C,A2223G,和C2195T[11],不同地区、不同种族、不同人群的主要突变类型虽不完全相同,但仍以A2142G和A2143G最常见[12],因此对这两个位点的检测显得的尤为重要。
限制性片段长度多态性(polymerase chain reaction based restriction fragment length polymorphism, RFLP)分析是利用限制性内切酶能识别DNA分子的特异序列,并在特定序列处切开DNA分子,产生不同长度大小、不同数量限制性片段,经电泳、转膜等进行检测的实验技术。1997年Versalovic等[13]首次通过PCR-RFLP证实了HP 23S rRNA的V区的A2058G(即A2142G[14])和A2059G(即A2143G[14])点突变与HP耐药有关,该研究表明,高达91.4%的耐克拉霉素的HP中存在A2142G或A2143G点突变,其中A2142G点突变占52.5%,A2143G点突变占39%,而且这种突变还与克拉霉素的耐药性存在相关性,在克拉霉素高耐药菌(MIC>64 mg/L)中,A2142G点突变占了65%。RFLP被认为是检测HP 23S rRNA V区点突变的唯一参考方法[15],而且还具有价格低廉、操作简便等特点。
我们利用BbsⅠ内切酶能够识别并切开5′GAAGAC(N)2↓3′序列来检测A2142G点突变,利用BsaⅠ内切酶能够识别并切开5′↓(N)5GAGACC 3′序列来检测A2143G点突变。实验结果表明:在37例耐药菌中,有34例(91.9%)耐药菌存在A2142G或A2143G点突变,3例(8.1%)未检测出点突变,其中A2142G点突变占61.8%(21/34),A2143G点突变占38.2%(13/34),结果与Versalovic等[13]的研究结果相近,但由于Etest试剂比较昂贵,加之经费有限,我们无法采用Etest来验证A2142G或A2143G点突变与克拉霉素耐药性之间的关系,而是采用经典的纸片琼脂扩散法来检测克拉霉素的耐药性。
值得一提的是我们也将这37例耐药菌株对应的胃黏膜组织DNA进行RFLP分析,得到了相同的实验结果,提示RFLP不但可以用于菌株DNA,也可以用于组织DNA的检测,这为临床提供了一个更为快速的检测方法,从而避免了耗时的培养过程,更为临床尽早采取正确的治疗方案提供依据。
综上所述,RFLP完全可以用来检测对克拉霉素耐药的HP 23S rRNA的V区的A2142G或A2143G点突变,而且可以直接检测胃黏膜组织DNA,减少了耗时的培养过程,为临床提供了一种简便、快速、有效的检测方法,对临床治疗具有重要的指导意义。
