EBUS-GS技术结合现场快速评价对肺外周结节的诊断价值
2019-09-02沈青严杰蒋春燕宋嘉房宇坤陈清勇
沈青 严杰 蒋春燕 宋嘉 房宇坤 陈清勇*
随着人们健康体检意识的提高,胸部多排螺旋CT普查的日益推广,肺外周结节(直径≤3cm)的检出率逐渐提高,但由于结节病因复杂,常缺乏特异性影像学特征,临床上不易明确其良恶性。近年来,新辅助技术被不断应用,包括虚拟支气管镜、磁导航、径向超声、超细支气管镜等[1],对肺结节的诊断率逐渐提高。此外,在病灶活检后,如何判断是否得到靶标本,标本是否足够或合适等问题对于诊断也是至关重要的。快速现场评价(ROSE)是一项实时伴随于取材过程的快速细胞学判读技术,其优点在于能快速的反映标本的特点及对标本的质量做出评估[2]。近年来在诊断性介入肺脏病学操作中得到充分的应用和发展。本研究旨在探讨EBUS-GS技术结合ROSE对提高肺外周结节诊断率的临床价值。现报道如下。
1 资料与方法
1.1 一般资料 2017年2月至2018年9月本医院收治的肺外周结节患者87例,所有患者均行EBUSGS引导下支气管肺活检术(TBLB)。随机分为2组,EBUS-GS+ROSE组46例,EBUS-GS组41例,纳入标准:胸部CT示中外2/3肺野病变,影像学特点肺结节直径0.8~3cm,被肺实质包绕的病变,支气管镜检查前常规评估心肺功能、出凝血时间及过敏史;排除标准:(1)严重心肺功能障碍;(2)凝血功能障碍;(3)身体极度虚弱不能耐受手术者;(4)不同意或中途退出的试验者。本项目经本院伦理委员会批注,所有患者知情并签署知情同意书。
1.2 方法 (1)检查设备:支气管镜(Olympus BF-260 型;Olympus BFP260F 型);微型超声主机(EndoEcho EU-ME1,Olympus);腔内超声环扫探头(UM-S20-17S Olympus);超细支气管镜(BF-P260F,外径4.0 mm,工作孔径2.0 mm)引导鞘套装及活检套装,以上均为(OLYMPUS)。Probe Driving Unit 超声探头驱动装置(MAJ-935,Olympus);Olympus K201 活检套装。GE 64排螺旋CT;试剂迪夫A(Diff-quikA)溶液、迪夫B(Diff-quikB)溶液、磷酸盐缓冲液;玻片。(2)VBN、超细支气管镜联合EBUS-GS技术检查:①术前检查:完善血常规、血凝全项、输血三项、乙肝三项、心电图、肺功能和胸部CT(层厚0.5~1.25mm)。导入CT扫描的DICOM数据至计算机,经VBN软件创建目标支气管的虚拟支气管镜图像。检查前禁食至少8h,术前2%利多卡因15ml雾化吸入,患者仰卧位,连接心电监护仪,建立静脉通路(术中镇静药物为丙泊酚及芬太尼),建立人工气道,连接机械通气。②支气管镜检查:常规支气管镜按顺序先后观察气管、隆突、健侧各级支气管及病侧各级支气管,清理气道分泌物,未发现病变退镜,换用Olympus BF-P260F型超细支气管镜,根据虚拟引导路线确认到达病变区域并进行超声图像确认。助手将径向超声探头插入引导鞘内,沿活检孔道送入目标部位,有明显阻力感时开始超声探查,发现病变超声图像时估算从开始探查到出现病变图像中间的距离,在临近支气管分别探查尽可能找到病变最佳的图像,明确探头与病变的位置关系后固定引导鞘管,抽出探头,于超声病灶定位处活检钳、细胞刷依次送入引导鞘管,到达靶标后进行活检、刷片。ROSE组所获得的活检材料立即行ROSE检查,评估是否需要再活检。另一组使用4%的福尔马林溶液实施固定。(3)标本处理:①ROSE评估:ROSE组所制玻片行迪夫快速染色(Diff-quikstain),采用印片法(适用于穿刺取到的组织条)、喷片及喷片推片法(适用于穿刺刷片到的细胞),准备试剂迪夫A(Diff-quikA)溶液、迪夫B(Diff-quikB)溶液、磷酸盐缓冲液,标本固定后在迪夫A 液中染色20s,然后在磷酸盐缓慢浸泡冲洗掉迪夫A 液,轻轻甩干玻片后放在迪夫B 液中染色10s,水洗、干燥、由2名经验丰富的细胞学医师显微镜观察细胞成分及形态变化,并结合基础病理知识与临床资料特点,判断穿刺是否有效,评估是否需继续穿刺,最终做出初步的细胞学诊断。②组织病理学评估:操作结束后所有玻片及组织送病理科脱色后行HE染色及后续处理,由2名高年资病理科医师阅片并确定最终诊断,如结果不一致则交由第3位病理科医师共同讨论决定,最终病理结果作为“金标准”。③评价指标:ROSE对良恶性病变的初步判断,ROSE和组织病理结果的符合率。
1.3 随访及干预 如活检后ROSE未能获得细胞病理结果、病理学未能明确诊断,根据病情二次活检、行CT或B超引导下经皮肺穿刺、PET-CT或者外科手术,若患者不考虑进一步检查,随访半年。
1.4 统计学方法 采用SPSS 17.0统计软件。符合正态分布计量资料用(±s)描述,两组间比较采用t检验,多组间均数比较采用单因素方差分析(One-Way ANOVA),各组间诊断率比较用χ2检验,ROSE 和气管镜下组织病理学结果一致性采用Kappa检验,P<0.05为差异有统计学意义。
2 结果
2.1 一般资料 共纳入87例患者,其中男48例,女39例。随机分成2组,现场细胞组患者46 例,男26例,女20例;平均年龄(53±8.04)岁,吸烟20例。非现场细胞学组患者41 例,男22例,女19 例;平均年龄(56±8.45)岁,吸烟19例,两组年龄、性别、吸烟史比较差异无统计学意义(P>0.05),具有可比性。2.2 病理结果 见表1。

表1 72例病理结果及构成比较(%)
2.3 EBUS-GS技术诊断率影响因素分析 见表2。
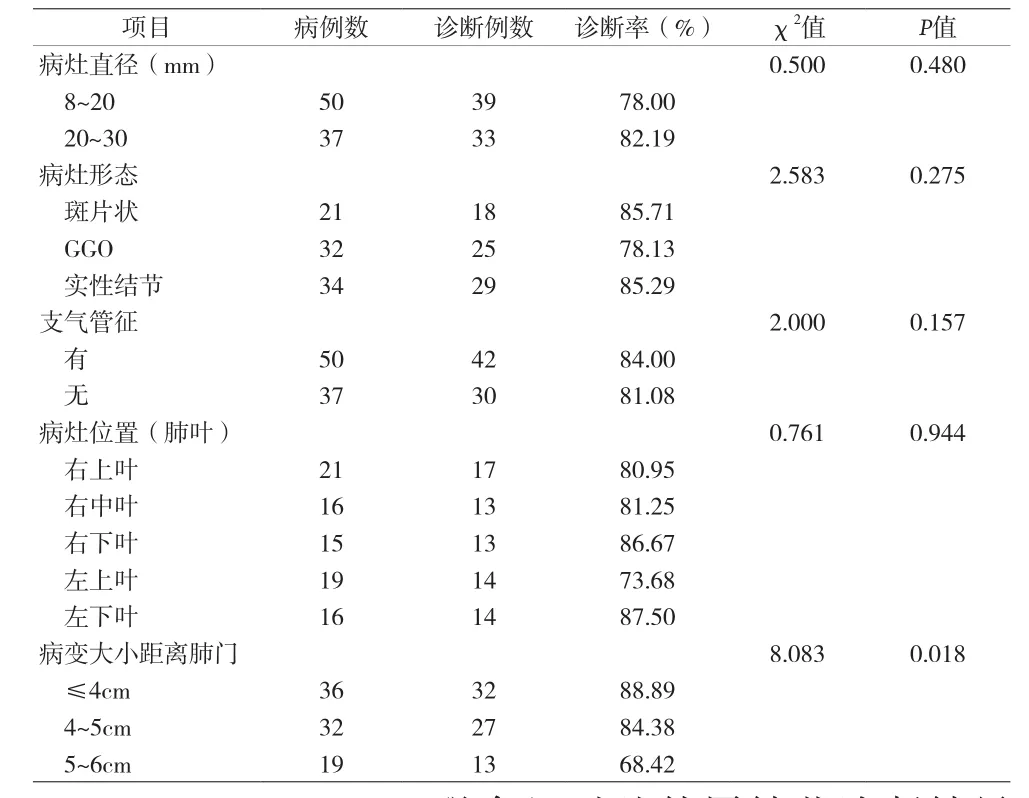
表2 EBUS-GS技术诊断率的影响因素分析
2.4 EBUS-GS+ROSE联合组对肺外周结节诊断结果与病理结果的诊断率比较 共46例患者入组EBUSGS+ROSE组,38例与最终病理学结果一致,总体诊断率为82.61%。其中,恶性病变患者31例,良性病变患者7例。以确诊的恶性病变患者作为阳性(+)病例,良性病变患者作为阴性(-)病例(见表3)。ROSE组诊断恶性病变的灵敏度为93.54%、特异度为85.71%,阳性预测值96.99%,阴性预测值75%,约登指数:0.79。一致性kappa=0.751,P=0.000,与金标准高度一致。

表3 ROSE和组织病理学诊断的符合情况
2.5 单用EBUS-GS与EBUS-GS联合ROSE技术对肺外周结节诊断价值的比较 EBUS-GS联合ROSE对肺外周结节的诊断率82.61%,单用EBUS-GS对肺外周结节的诊断率为82.92%,差异无统计学意义。
2.6 两组穿刺相关指标比较 见表4。

表4 两组活检相关指标的比较
3 讨论
以往肺外周结节的活检方法主要包括常规支气管镜检查、CT/超声引导经皮穿刺肺活检和外科手术,但诊断率较低,且存在放射接触、气胸、咯血、空气栓塞、肿瘤种植转移、过度手术等缺点。近年来,研究表明[3],应用EBUS-GS技术对肺外周结节有较高的诊断价值,诊断率在58.3%~84.4%,甚至在直径<1cm的肺结节,其诊断阳性率达到76%,且极少发生出血和气胸等常见并发症。Ikezawa等[4]报道肺外周毛玻璃样病变(GGO),EBUS-GS的诊断阳性率仍可达到57%。Asano等[5]发现超细支气管镜、EBUSGS及VBN导航系统联合对孤立性肺结节的诊断率为84.4%。本资料总体诊断率是71.26%,与文献报道基本一致,且在恶性病变的诊断率高于良性病变。
影响肺外周结节诊断率的因素很多,如超声探头位置、结节大小、结节位置、支气管充气征、结节形态、SUV值等,但目前尚未有统一的结果。本资料显示结节距肺门不同距离,诊断率差异有统计学意义(χ2=8.083,P=0.018),而病灶大小、形态、位置、有无支气管充气征均无统计学意义。虽然借助EBUSGS技术可以到达肺周围的部位,但无法快速评估标本合格率,而ROSE技术可协助快速评估支气管镜检查是否取到靶部位的标本以及取材的满意度,从而形成初步诊断,实时指导介入操作。ROSE 技术最早应用于妇科疾病的诊疗中,随后逐步发展应用于其他疾病的诊断。目前ROSE技术已用于协助诊断肺门和纵隔病变、肺外周病变和胸膜病变等。本资料结果显示,ROSE对恶性病变有较高的诊断价值,同时能进行初步病理类型判读。Sara Ravaioli等[6]将ROSE应用于评估273例肺癌患者通过TBNA或EBUS-TBNA获得细胞学标本,与组织病理结果比较,准确率达到90%~97%。
在并发症方面,国内外文献报道[7],ROSE技术联合EBUS-TBNA、VBN、EBUS-GS等诊断性介入技术,可以减少活检次数,缩短操作时间,降低并发症的发生率,提高诊断阳性率。本资料显示ROSE虽可快速的评估活检标本性质,但EBUS-GS+ROSE组的活检次数较单用EBUS-GS组少,可能是由于ROSE技术为取材提供指导,避免重复操作;而活检时间较长,可能是由于染色、制片、阅片花费时间。同时ROSE组少量出血,无气胸,由此可见以上技术是安全有效的。
综上所述,EBUS-GS技术对肺外周结节的诊断率较高,且对恶性病变的诊断率更高,进一步分析影响因素,发现病变距离肺门越近,诊断率越高。ROSE和组织病理诊断结果一致性好,有助于早期认识病变并帮助术者了解组织病理取材是否得当,且患者并发症发生率明显减低,安全有效。
