3,4-二(氟二硝甲基)氧化呋咱: 一种高密度氧化剂
2019-09-02罗义芬张家荣翟连杰
李 婧,罗义芬,张家荣,翟连杰
3,4-二(氟二硝甲基)氧化呋咱: 一种高密度氧化剂
李 婧1,罗义芬2,张家荣2,翟连杰2
(1. 中国兵器科学研究院,北京,100089;2. 西安近代化学研究所,陕西 西安,710065)
以3,4-二(偕氯肟基)氧化呋咱为原料,经过重氮化、硝化、成盐及氟化合成了一种含氟二硝基甲基的高密度氧化剂3,4-二(氟二硝甲基)氧化呋咱,利用红外光谱、核磁共振(13C NMR和19F NMR)、元素分析对3,4-二(氟二硝甲基)氧化呋咱进行了结构表征。采用差示扫描量热技术(DSC)研究了3,4-二(氟二硝甲基)氧化呋咱的热分解过程。采用密度泛函理论方法,在B3LYP/6-31+G(,)水平上优化了3,4-二(氟二硝甲基)氧化呋咱分子构型,预估了理论密度()、标准生成焓(ΔH())、爆速()和爆压()。结果表明,3,4-二(氟二硝甲基)氧化呋咱的热稳定性良好,在高温下具有挥发特性;3,4-二(氟二硝甲基)氧化呋咱的、ΔH()、和值分别为2.01 g/cm3、-78.6 kJ/mol、9 025 m/s和38.5GPa,是一种能量水平较高的氧化剂。
含能氧化剂;氟二硝甲基;合成;爆轰性能
高能量密度材料(HEDM)是武器系统的毁伤威力来源和动力能源,是构成推进剂、炸药和发射药的主要材料,在各类武器系统中发挥着至关重要的作用[1-2]。近年来,设计并合成基于咪唑、吡唑、三唑、四唑、噁二唑和四嗪等富氮杂环的新型含能材料已成为重要研究方向[3-5]。其中氧化呋咱类含能化合物因能量密度高、标准生成焓大、氢含量少(或者无氢)、氧含量高等特点,受到世界各国含能材料研究者的广泛关注。相比于呋咱或异呋咱,氧化呋咱结构单元氮氧含量达69.7%,导致其生成焓(ΔH=197.8 kJ/mol)和氧平衡(CO=-18.6%)较高。氧化呋咱环配位氧一侧含有1个“潜”硝基结构,是1个有效的爆炸性基团结构单元。含能分子中氧化呋咱环取代呋咱环,可使化合物密度提高0.06~0.1g/cm3,爆速提高300 m/s[6-8]。通过对比化合物3,4-双(4-硝基呋咱)呋咱(LLM-137)和3,4-双(4-硝基呋咱基)氧化呋咱(BNTF)性能,可以看出用氧化呋咱环取代呋咱环,可使化合物的密度和爆速分别提高约0.1g/cm和700m/s[9-10]。
氟二硝基甲基是一种能量水平高且热稳定良好的含能基团,与三硝甲基相比,热稳定性和感度更低,综合性能优异。本课题组近几年设计并合成了多种含氟二硝基甲基的高能呋咱化合物,如3,3’-双(氟二硝基甲基)二呋咱醚和3,4-双(3-氟二硝基甲基呋咱-4-氧基)呋咱[11-12],均显示出优越的爆轰性能和良好的热稳定性。若将氟二硝基甲基和氧化呋咱相连,即4,5-双(氟二硝基甲基)氧化呋咱,分子的氧含量和能量水平将进一步提高。Adolph等人于1967年首次报道了一种基于氟二硝基乙酰肟合成4,5-双(氟二硝基甲基)呋咱的方法[13],但其核磁谱图、热性能以及爆轰性能尚未报道。本研究以3,4-二(偕氯肟基)氧化呋咱为原料,经重氮化、硝化、成盐及氟化4步合成了3,4-二(氟二硝基甲基)氧化呋咱,采用红外、碳谱、氮谱对其结构进行了表征,采用Kamlet-Jacbos方程预估了爆速和爆压。
1 实验部分
1.1 实验仪器与试剂
仪器:NEXUS870型傅里叶变换红外光谱仪,美国热电尼高力公司;AV500型(500 MHz)超导核磁共振仪,瑞士BRUKER公司;Vario EL-Ⅲ型元素分析仪,德国EXEMENTAR公司;LC-2010A 液相色谱仪,日本岛津公司; Q-200型差示扫描量热仪,美国TA公司。
试剂:碘化钾,二氟化氙,乙腈,三氯甲烷,均为分析纯,百灵威试剂有限公司;五氧化二氮,自制。
1.2 实验原理
合成路线见图1。
1.3 实验步骤
3,4-二(偕氯肟基)氧化呋咱和3,4-二(二硝甲基)氧化呋咱二钾盐依据文献[14-15]合成。

图1 化合物的合成路线
室温下,将0.74 g(2 mmol)3,4-二(二硝甲基)氧化呋咱二钾盐加入到15mL无水乙腈中,搅拌均匀后分批加入2.03g(12mmol)二氟化氙,保温反应96h。反应结束后减压蒸馏除去乙腈,剩余物溶于二氯甲烷中,水洗至中性,硫酸镁干燥后减压除去二氯甲烷液得无色液体0.39g,收率59%,纯度96.4%。13C NMR (DMSO-d6, 125MHz) :141.70, 114.62, 113.91, 103.84; 19F NMR (DMSO-d6, 470.5 MHz) :: -93.87, -100.16; IR (cm-1, KBr) 1 662, 1 611, 1 484, 1 360, 1 342, 1 300, 1 260, 1 212, 1 158, 989, 926, 835, 793, 705, 632;Anal. calcd for C4N6O10F2(%):C 14.56, N 25.46, found C 14.48, N 25.33。
2 结果与讨论
2.1 红外光谱及核磁谱
采用NEXUS870型傅里叶变换红外光谱仪,获得了3,4-二(氟二硝甲基)氧化呋咱的红外吸收谱图,如图2所示,并对其特征吸收峰进行了归属。
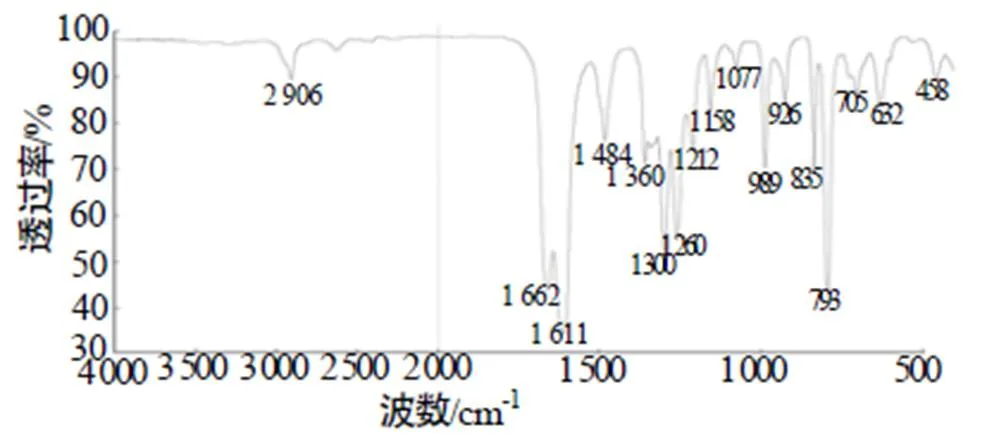
图2 3,4-二(氟二硝甲基)氧化呋咱红外吸收谱图
由图2可以看出,氧化呋咱环上氮氧键伸缩振动吸收峰出现在1 360~1 342 cm-1,碳氮双键在1 662cm-1处显示强吸收峰。硝基的不对称伸缩振动吸收峰出现在1 611cm-1,对称伸缩振动吸收在1 300~1 260cm-1范围内。另外,C–F键在1 212 cm-1处显现中等强度吸收峰[16]。图3为3,4-二(氟二硝甲基)氧化呋咱的碳谱和氟谱。3,4-二(氟二硝甲基)氧化呋咱碳谱有4组峰,化学位移在103.84 ppm处为氧化呋咱中配位氧一侧碳原子共振峰,氧化呋咱环上另外1个碳在141.70ppm出峰。2个氟二硝甲基化学位移分别为114.62ppm和113.91ppm,由于氟对碳的裂分作用,氟二硝甲基上的碳均显示出两重峰,耦合常数113C-19F为286Hz。3,4-二(氟二硝甲基)氧化呋咱上氟的化学位移分别为-93.87ppm和-100.16ppm。
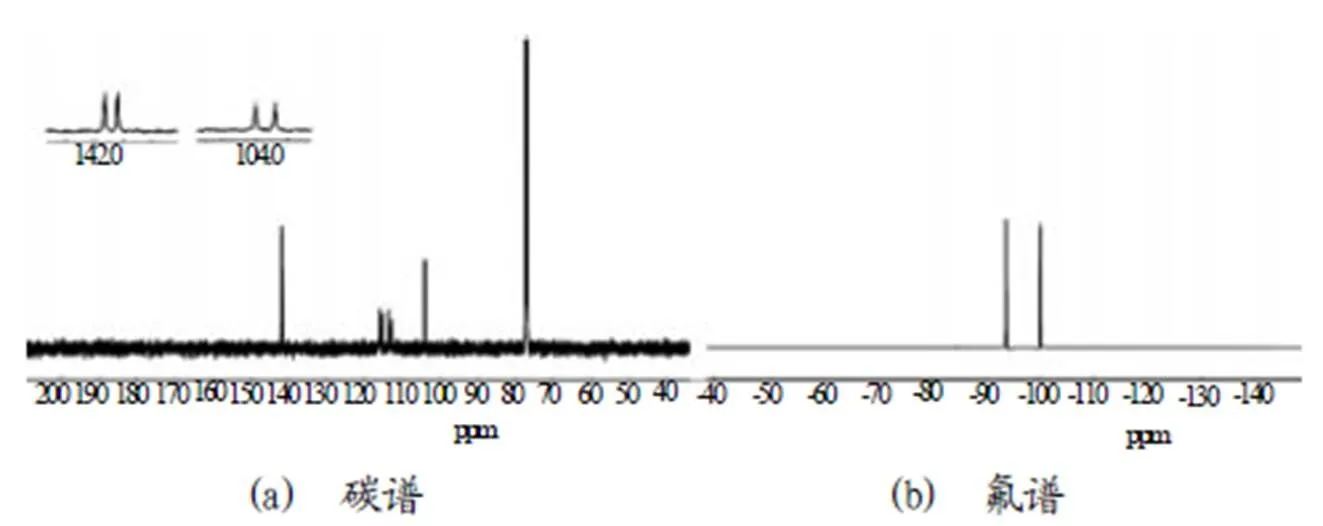
图 3 3,4-二(氟二硝甲基)氧化呋咱碳谱和氟谱
2.2 物化和爆轰性能
在升温速率10℃/min的条件下,获得了3,4-二(氟二硝甲基)氧化呋咱的热性能数据,如图4所示。图4表明3,4-二(氟二硝甲基)氧化呋咱在115.5 ℃时开始缓慢挥发,表现出缓慢吸热的特性,随着温度的不断升高,在153.0℃左右,吸热峰消失,表明3,4-二(氟二硝甲基)氧化呋咱已挥发完,整个过程中并无放热峰,表明3,4-二(氟二硝甲基)氧化呋咱分解温度不低于153.0℃,说明其热稳定性较好。
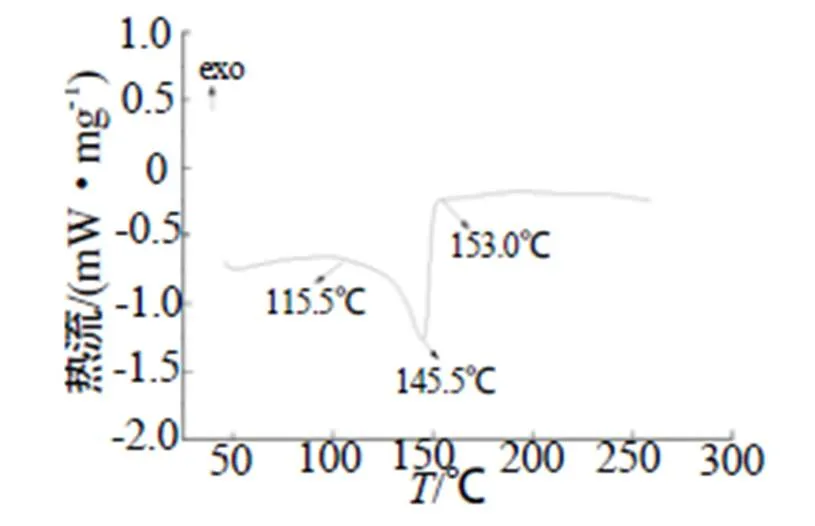
图4 3,4-二(氟二硝甲基)氧化呋咱DSC图
在B3LYP/6-31+G(,)水平优化了3,4-二(氟二硝甲基)氧化呋咱的构型,用Monte-Carlo法[17]计算3,4-二(氟二硝甲基)氧化呋咱分子体积,为了减小误差,取100次计算值的平均值为3,4-二(氟二硝甲基)氧化呋咱的摩尔体积,得其理论密度为2.01 g/cm3。使用原子化方案[18],利用完全基组方法(CBS- 4M)[19]计算了298K时3,4-二(氟二硝甲基)氧化呋咱的焓° (298 K),进而求得生成焓为-78.6 kJ/mol。
采用Kamlet-Jacbos[20]公式预估了3,4-二(氟二硝甲基)氧化呋咱的爆速与爆压,并与黑索今(RDX)和奥克托今(HMX)[21]进行了对比,结果见表1。
由表1可知,3,4-二(氟二硝甲基)氧化呋咱的爆速为9 025 m/s,爆压为38.5GPa,优于 RDX (34.9 GPa, 8 748 m/s),但比HMX(39.5 GPa, 9 320 m/s)的爆压和爆速略低。3,4-二(氟二硝甲基)氧化呋咱的氧平衡(CO2)为14.5%,远高于RDX (-21.6%) 和HMX (-21.6%)。
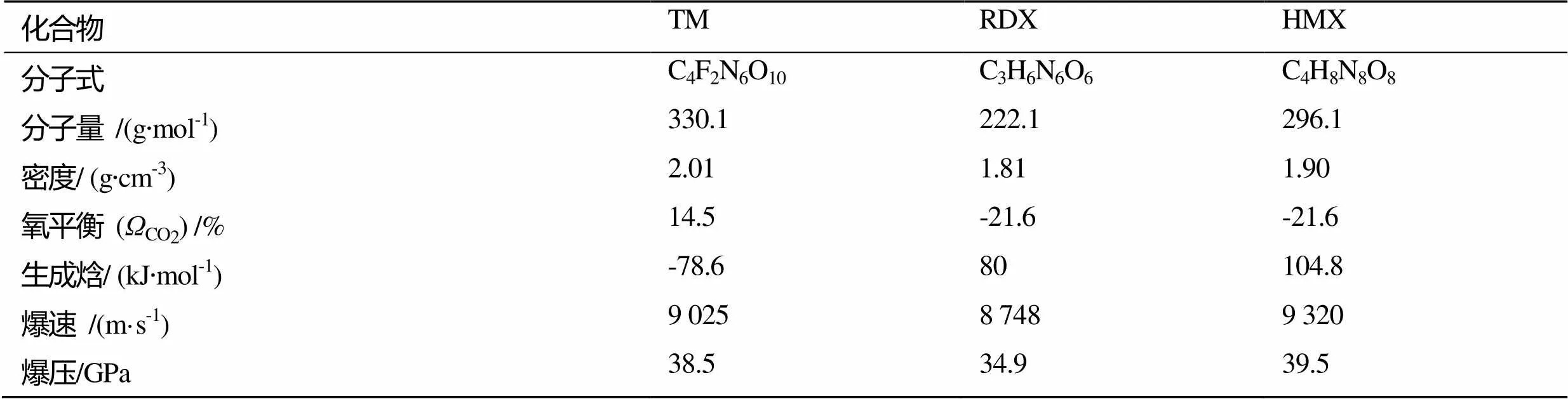
表1 3,4-二(氟二硝甲基)氧化呋咱与RDX、HMX的物化和爆轰性能对比
3 结论
本文开发了一种新的3,4-二(氟二硝甲基)氧化呋咱的合成方法,并通过红外、核磁、元素等分析方法进行了表征。探讨了3,4-二(氟二硝甲基)氧化呋咱红外光谱和核磁共振谱,完成了信号归属。利用DSC及量子化学手段研究了3,4-二(氟二硝甲基)氧化呋咱的热性能和爆轰性能,结果表明,3,4-二(氟二硝甲基)氧化呋咱热稳定性好,理论密度高(2.01 g/cm3),氧平衡高(14.5%),爆轰性能优异(爆压38.5GPa,爆速9 025m/s),表明3,4-二(氟二硝甲基)氧化呋咱有望成为一种新型高能氧化剂。
[1] Badgujar D M, Talawar M B, Asthana S N, et al. Advances in science and technology of modern energetic materials: an overview [J]. Journal of Hazardous Materials, 2008, 151(2): 289-305.
[2] 董海山. 高能量密度材料的发展及对策[J]. 含能材料, 2004, 12(z1): 1-12。
[3] Paraskos A J, Cooke E D, Caflin K C. Bishydrazinium and diammonium salts of 4,4,5,5-tetranitro-2,2-biimidazolate (TNBI): synthesis and properties [J]. Propellants Explosives Pyrotechnics, 2015, 40(1): 46-49.
[4] Dippold A A and Klapötke T M. A study of dinitro-bis-1,2,4-triazole-1,1′-diol and derivatives: design of high-performance insensitive energetic materials by the introduction of N‑oxides [J]. Journal of the American Chemical Society, 2013, 135(26): 9 931-9 938.
[5] Gao Hai-xiang and Shreeve J M. Azole-based energetic salts [J]. Chemical Reviews, 2011, 111(11): 7 377-7 436.
[6] Huang Hai-feng, Zhou Zhi-ming, Liang Li-xue et al. Nitrogen-rich energetic monoanionic salts of 3, 4-bis(1H-5 -tetrazolyl)furoxan [J]. Chemistry-An Asian Journal, 2012, 7(4): 707-714.
[7] Pivina T S , Sukhachev D V, Evtushenko A V. Comparative characteristic of energy content calculating methods for the furazan series as an example of energetic materials [J] .Propellants, Explosives, Pyrotechnics,1995(20):5-10.
[8] Liang Li-xuan, Wang Kai, Bian Cheng-ming, et al. 4-nitro -3-(5-tetrazole)furoxan and its salts: synthesis, characterization, and energetic properties[J].Chemistry-A European Journal, 2013, 19(44):14 902 - 14 910.
[9] Fischer D, Klapötke T M and Stierstorfer J. Synthesis and characterization of diaminobisfuroxane[J]. European Journal of Inorganic Chemistry, 2014(34):5 808-5 811.
[10] ZHANG Yu, ZHOU Chen, WANG Bo-zhou, et al. Synthesis and characteristics of bis(nitrofurazano)furazan (BNFF), an insensitive material with high energy-density [J]. Propellants, Explosives, Pyrotechnics, 2014, 39(6): 809-814.
[11] Kim T K, Choe J H, Lee B W, et al. Synthesis and characterization of BNFF analogues [J]. Bulletin of the Korean Chemical Society, 2012, 33(8): 2 765-2 768.
[12] ZHAI Lian-jie, WANG Bo-zhou, XU Kang-zhen, et al. A new synthetic route for 3,3’-bis(fluorodinitromethyl) difurazanyl ether (FOF-13) and its energetic properties [J]. Journal of Energetic Materials, 2016, 34(1):92-102.
[13] ZHAI Lian-jie, FAN Xue-zhong, WANG Bo-zhou, et al. 3,4-bis(3-fluorodinitromethylfurazan-4-oxy)furazan: a new thermally stable energetic plasticizer with high energy density [J]. Chinese Journal of Energetic Materials(Hanneng Cailiao), 2016, 24(9):922-924.
[14] Adolph H G. Oxidation reactions of 2,2,2-fluorodinitroe thylamine and some N-alkyl-2,2,2-fluorodinitro- ethylamines [J]. Journal of Organic Chemistry, 1975, 40(18): 2 625-2 630.
[15] Fischer D, Klapötke T M, Reymann M, et al. Energetic alliance of tetrazole-1-oxides and 1,2,5-oxadiazoles [J]. New Journal of Chemistry, 2014, 39(3): 1 619-1 627.
[16] Patai S. The chemistry of functional group: the chemistry of the carbon-halogen bond: part 1[M]. London:J. Wiley & Sons Ltd., 1973.
[17] Rice B M, Hare J J, Byrd E F E. Accurate predictions of crystal densities using quantum mechanical molecular volumes [J]. Journal of Chemical Physics A, 2007, 111(42): 10 874-10 879.
[18] Curtiss L A, Raghavachari K, Redfern P C, et al. Assessment of Gaussian-2 and density functional theories for the computation of enthalpies of formation[J]. Journal of Chemical Physics, 1997, 106(3): 1 063-1 079.
[19] Ochterski J W, Petersson G A, Montgomery J A. A complete basis set model chemistry V. extension to six or more heavy atoms[J]. Journal of Chemical Physics, 1996, 104(7): 2 598-2 619.
[20] Politzer P, Murray J S, Grice M E, et al. Calculation of heats of sublimation and solid phase heats of formation[J]. Molecular Physics, 1997, 91(5): 923-928.
[21] YIN Ping, Parrish D A, Shreeve J M. Energetic multi-functionalized nitraminopyrazoles and their ionic derivatives: ternary hydrogen-bond induced high energy density[J]. Journal of the American Chemical Society, 2015, 137(14): 4 778-4 786.
3,4-Bis(fluorodinitromethyl)furoxan: A High Density Oxidizer
LI Jing1,LUO Yi-fen2,ZHANG Jia-rong2,ZHAI Lian-jie2
(1.China Ordnance Science Research Institute, Beijing, 100089;2.Xi’an Modern Chemistry Research Institute, Xi’an,710065)
A fluorodinitromethyl-containing high density oxidizer 3,4-bis(fluorodinitromethyl)furoxan was synthesized by fluorination. The compound was characterized by FT-IR, multinuclear NMR spectroscopy (13C NMR,19F NMR), elemental analysis, and differential scanning calorimetry measurements (DSC). 3,4-Bis(fluorodinitromethyl)furoxan shows good thermal stability and exhibits a volatile process at high temperature. Its density is calculated to be 2.01 g·cm-3. Based on the calculated standard enthalpy of formation and density, the detonation pressure, velocity and standard enthalpy were computed by using the empirical Kamlet-Jacobs computer programand found to be 38.5 GPa, 9 025 m·s-1and -78.6kJ/mol, respectively, which make it promising high density energetic oxidizer.
Oxidizer;Fluorodinitromethyl;Synthesis;Detonation properties
TQ560.4
A
10.3969/j.issn.1003-1480.2019.03.009
1003-1480(2019)03-0035-04
2019-04-13
李婧(1985 - ),女,高级工程师,主要从事含能材料制备与应用研究。
国家自然科学基金(21805224)。
