应用达芬奇机器人切除原发性腹膜后巨大肿瘤的临床研究
2019-08-29汪金荣何乐业刘斌
汪金荣,何乐业,刘斌
(中南大学湘雅三医院 泌尿外科,湖南 长沙 410013)
达芬奇机器人手术系统(Da Vinci surgical system,DVSS)已广泛运用于外科、妇产科和耳鼻喉科等临床科室,尤其是复杂肿瘤手术,达芬奇机器人优势明显。腹膜后肿瘤位置深,周围毗邻大血管和脏器较多,肿块较大时,开放手术和腹腔镜手术暴露和分离肿瘤难度大。达芬奇机器人拥有4个机械臂和7个自由度的内腕,灵活而精准,且有10倍以上放大效果,处理腹膜后巨大肿瘤优势较大。本院2015年10月-2018年1月实施达芬奇机器人原发腹膜后巨大肿瘤切除术5例,手术均完成顺利,术后恢复好。现报道如下:
1 资料与方法
1.1 一般资料
本组患者共5例。其中,男3例,女2例,年龄45~59岁,平均50.6岁,体质指数(body mass index,BMI)<24 kg/m2的 2例,24~ 28 kg/m2的 3例。合并高血压3例,合并糖尿病1例,1例患者术前有间歇发热2个月的症状。肿瘤位于盆腔以上腹膜后3例,其中2例位于肾蒂旁,1例位于左肾上方;盆腔腹膜后肿瘤2例,分别位于膀胱后方和盆腔右侧。肿瘤长径为6.0~13.0 cm,长径平均9.0 cm,切除最大肿瘤约13.0 cm×10.0 cm(图1)。术前检查均无肿瘤远处转移。
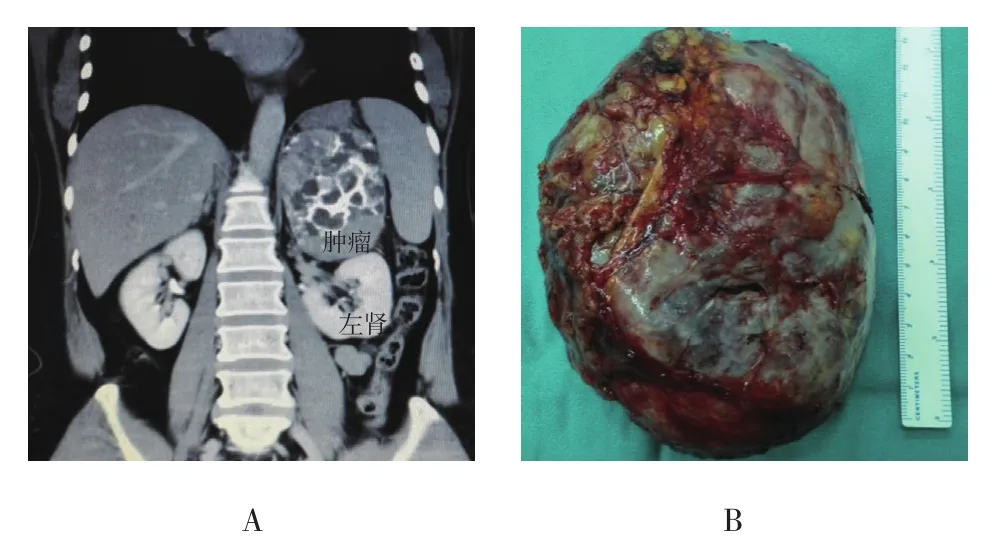
图1 腹膜后巨大肿瘤CT影像与手术切除标本Fig.1 Imaging of CT and surgical specimen of huge retroperitoneal tumor
1.2 手术方法
1.2.1 经腹途径盆腔以上腹膜后肿瘤经腹途径体位。气管插管全身麻醉,健侧侧卧位或60~70°斜侧卧位,抬高腰桥。以Veress针穿刺建立气腹,保持气腹压12~14 mmHg。镜头孔Trocar位于脐部或脐部附近,1、2号器械孔Trocar位于锁骨中线附近,分别距镜头孔8.0~10.0 cm,辅助孔位于镜头孔与1号器械孔连线中点内下方,置入12 mm Trocar(图2A)。机器臂从患者背侧进入,连接机器臂与各Trocar,器械安装好后,沿结肠旁沟打开后腹膜,离断肝(脾)结肠韧带,将结肠翻向内侧,显露肿瘤,沿肿瘤表面游离,供应肿瘤较粗血管以钛夹或Hemo-lock夹闭后离断,完全游离肿瘤,扩大穿刺通道后,将肿瘤完整取出送病理检查。

图2 机器人辅助腹膜后肿瘤切除术经腹途径Trocar定位Fig.2 The Trocar location of robot-assisted laparoscopic retroperitoneal tumor resection through transperitoneal approach
盆腔肿瘤经腹途径。全身麻醉,下肢剪刀位,头低脚高15~30°,以Veress针穿刺建立气腹。镜头孔Trocar位于脐部上方1.0~2.0 cm,左右器械孔位于左右锁骨中线上,距镜头孔8.0~10.0 cm,留置10 mm Trocar,辅助孔位于右器械孔外下方,留置12 mm Trocar(图2B)。安装好器械后,于膀胱直肠凹或膀胱左(右)侧打开盆腔腹膜,显露肿瘤后游离,术中注意保护膀胱、直肠及闭孔神经。
1.2.2 经腹膜后途径全身麻醉,健侧侧卧位,抬高腰桥。于腋中线内侧2.0 cm髂嵴上方2.0 cm处作一小切口,置入12 mm Trocar作镜头孔,以镜体直接分离腹膜后间隙,将腹膜推向内下方,直视下于腋后线12肋下、腋前线内侧2.0 cm处留置10 mm Trocar,作1、2号器械孔,辅助孔位于镜头孔与腋前线内侧器械孔连线中点内下方约8.0 cm,留置12 mm Trocar。见图3。清除腹膜外脂肪后,打开Gerota筋膜,游离肾周脂肪,找到腹膜后肿瘤,沿肿瘤表面游离,夹闭后离断肿瘤较粗供应血管,完整取出肿瘤。
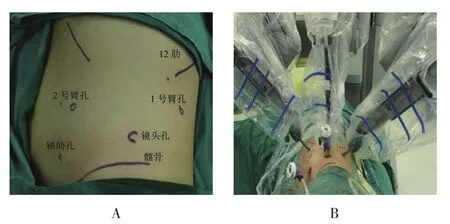
图3 机器人辅助腹膜后肿瘤切除术经腹膜后途径Trocar定位Fig.3 The Trocar location of robot-assisted laparoscopic retroperitoneal tumor resection through retroperitoneal approach
2 结果
5例患者均顺利完成手术,无中转开放。经腹手术入路3例,经腹膜后手术入路2例。手术时间100~160 min,平均122 min;术中出血20~800 ml,平均404 ml,2例术中输浓缩红细胞300 ml,3例未输血,术后5例患者均未再输血。术中术后无ClavienⅡ级以上并发症。住院时间12~18 d,平均15 d。术后病理检查结果显示淋巴瘤、神经鞘瘤、血管周上皮样细胞肿瘤(perivascular epithelioid cell tumor,PEComa)、副神经节瘤和间叶源性肿瘤各1例。
随访6~33个月,术后1个月复查CT与生化检查,然后每3个月复查1次。随访至2018年7月,1例腹膜后淋巴瘤患者,残留少许肿瘤附着于腔静脉壁,出院1个月后转肿瘤科行化疗,经4个疗程化疗后,残留肿瘤明显缩小,达部分缓解。其他4例患者腹膜后肿瘤完整切除,无复发。
3 讨论
腹膜后肿瘤是指发生于腹膜后间隙的原发肿瘤,来源于脂肪组织、血管、神经、淋巴管、肌肉和胚胎残留组织等,不包括腹膜后脏器(肾、肾上腺等)来源的肿瘤和转移肿瘤[1],60%~80%的腹膜后肿瘤为恶性肿瘤。腹膜后间隙空间小、位置深,腹膜后肿瘤手术显露相对困难。传统的腹膜后肿瘤手术方式主要有开放手术和腹腔镜手术。为充分暴露肿瘤,开放手术切口长、创伤大,且恢复慢。当腹膜后肿瘤较小时,腹腔镜手术基本能顺利切除肿瘤,但肿瘤较大时,由于普通腹腔镜器械为直杆式、仅有4个自由度,分离肿瘤背侧时,往往需用力挤压肿瘤与周围脏器,会导致肿瘤破裂、出血或相邻脏器损伤,如果手术时间长,术者较易疲劳。大于6.0 cm的腹膜后肾上腺肿瘤腹腔镜切除术,手术难度显著增加,术中失血、中转开放手术率、包膜破裂和种植转移风险明显增加[2]。近年来,随着我国引进手术机器人越来越多,在一些大型医院中,机器人辅助腹膜后肿瘤手术开展逐渐增多,由于其发病率低,机器人辅助腹膜后原发肿瘤切除报道较少,多数为个案报道[3-5]。相对普通腹腔镜,DVSS具有以下优势:①采用双摄像头,形成高清晰度的三维立体影像,且为裸眼3D,放大倍数可达10~15倍,手术视野更加清晰、结构层次更加清楚,可减少肿瘤周围血管、组织损伤;②有4个机械臂,每个机械臂有6个关节7个方向自由度,每个关节活动范围超过90°,操作更加灵活,可深入狭小空间进行精细操作;③通过操控机械臂进行手术,可避免人的生理震颤,增加了手术的稳定性和安全性;④动作缩减系统能按比例(5∶1和3∶1)缩小术者的动作幅度[4],术者移动操作杆5 mm或3 mm,器械末端仅移动1 mm,使操作更加精细;⑤术者可操控各机械臂和镜头,使术者的意图得到充分贯彻,减少了术者和助手之间的不协调;⑥人机分离,操作杆的设计符合人体工程学,术者可舒适地坐着手术,极大地减轻术者的疲劳度;⑦学习曲线比腹腔镜短[6-8]。由于以上优点,使DVSS在复杂肿瘤手术运用中优势明显。DVSS仍存在一些缺点,如:无触觉反馈,机器占地面积大,设备昂贵,手术费用高。因此,尚无法在基层医院普及。本组5例原发性腹膜后肿瘤患者,肿瘤直径均≥6.0 cm,平均直径达9.0 cm,5例患者均成功实施DVSS辅助腹膜后肿瘤切除术,无中转开放手术。其中4例完整切除肿瘤,1例腹膜后淋巴瘤患者,肿瘤与腔静脉粘连,质地较脆,无法完整切除,残留少许肿瘤附着于腔静脉壁。本组患者术后均恢复良好,除2例患者术中输血外,所有患者无Clavien Ⅱ级以上并发症。术后随访6~33个月,淋巴瘤患者术后行化疗,残余肿瘤明显缩小,达部分缓解,余患者均无复发,由于随访时间短,长期疗效还需进一步观察。
DVSS腹膜后肿瘤手术可采用经腹与腹膜后入路,经腹入路空间大,建立穿刺通道比较方便,国外术者多采用此途径,但术中肠道及肝脾等脏器会影响肿瘤暴露,术后有发生粘连性肠梗阻的风险。经腹膜后入路空间较经腹入路小,但腹膜外器官少,有时可直接抵达肿瘤位置,术后肠道功能恢复快。本科早期均采用经腹途径,在对DVSS操作熟练后,经腹膜后途径手术逐渐增多,由于机械臂关节较粗,如果穿刺通道Trocar之间距离较近,手术时可造成机械臂之间碰撞和干扰。因此,两穿刺通道距离最好>8.0 cm。笔者采用直视下镜体直接扩张腹膜后空间的方法,而非用球囊扩张法。首先建立镜头孔Trocar,在直视下以镜体直接钝性分离腹膜后间隙,然后置入腋后线12肋下Trocar,通过此Trocar以吸引器或剥离棒将腹膜尽量向内侧推开,以便建立腋前线内侧Trocar和下腹部辅助孔Trocar,1个辅助孔即可。腹膜后机器人手术建立穿刺通道比较关键,当腹膜被充分推开后,穿刺通道间距合适,即可获得满意的手术空间。腹膜后空间建立后,手术步骤与传统腹腔镜类似,机器人专用钳和剪的末端关节较灵活,可弯曲、旋转,活动度>90°,使其可深入狭小的空间和肿瘤的背侧进行精细游离。腹膜后巨大肿瘤供应血管较多,且肿瘤常与腹主动脉、腔静脉、髂血管和肾动静脉等大血管关系密切,在分离肿瘤与周围血管时,机器人镜头可将术野放大10倍以上,且无手臂震颤的干扰,可清晰地进行精细游离,明显减少周围重要血管的损伤,术中出血少。3D打印可提供肿瘤与周围血管和器官三维图像和模型,术者可据此制定手术方案,选择最佳手术入路,还可在模型上进行模拟手术,提高手术熟练度,在术中分离时,可预知何处有重要血管、器官,以避免损伤。苏昭杰等[9]进行了3D打印在腹膜后肿瘤手术中运用的研究,取得了满意效果。如有条件,术前可行腹膜后肿瘤3D打印,对手术帮助较大。
腹膜后肿瘤病理来源广泛,本组5例腹膜后巨大肿瘤病例,其病理来源各不相同,包括:淋巴瘤、神经鞘瘤、PEComa、副神经节瘤和间叶源性肿瘤各1例。腹膜后淋巴瘤罕见,无特异性症状,肿瘤可累及多个淋巴结,融合成团,形态不规则,常包绕血管但不侵犯,手术切除往往比较困难,对化疗敏感[10-11],术前可在B超或CT引导下穿刺活检或手术取材定性。本组1例淋巴瘤患者体检发现腹膜后肿块,无明显症状,术前血常规与骨穿检查均无明显异常,CT扫描示肝肾隐窝处肿块,由于肿瘤被血管和周围脏器遮挡,术前无法行穿刺活检。术中见肿瘤包膜菲薄,且与腔静脉和肾蒂血管紧密粘连,分离困难,采取紧贴腔静脉和肾动静脉切除肿瘤,有少许肿瘤残留。术后患者体温恢复正常,确诊淋巴瘤后继续行化疗。血管周上皮样细胞分布于毛细血管周围,是一种多潜能细胞,其发生的肿瘤称为PEComa,PEComa家族包括:血管平滑肌脂肪瘤(angiomyolipoma,AML)、肺透明细胞“糖”瘤(clear cell “sugar” tumor of the lung,CCST)、淋巴管平滑肌瘤(lymphangioleiomyoma,LAM)、镰状韧带透明细胞肌黑色素瘤(clear cell myomelanocytic tumor,CCMMT)和少见的发生于胰腺、直肠、腹膜、子宫、阴道、大腿和心脏的透明细胞肿瘤,非AML、CCST和LAM的PEComa相当罕见[12]。本组1例腹膜后PEComa患者,肿瘤巨大,大小11.0 cm×10.0 cm×10.0 cm,位于膀胱与直肠之间,外观呈囊状,内含清亮液体。腹膜后间叶源性肿瘤、副神经节瘤和神经鞘瘤报道相对稍多,多数有包膜或假包膜。
DVSS具有高倍放大的3D视野、灵活的机械臂和除颤功能,使其能安全地完成复杂的腹膜后巨大肿瘤手术,术后并发症少、恢复快。在熟练掌握机器人操作后,经腹和腹膜后途径均能很好地完成手术。
