TiO2负载型Fe0.8Mg0.2Oz催化剂NH3-SCR脱硝特性
2019-08-26徐丽婷牛胜利胡利华路春美巩志强
徐丽婷,牛胜利,胡利华,路春美,张 亢,张 起,巩志强
(1.光大环保技术研究院(南京)有限公司,南京 210000;2.山东大学能源与动力工程学院,济南 250061)
伴随着社会经济的日益发展,能源需求的增长带来了严重的环境污染问题.作为大气首要污染物之一的氮氧化物 NOx(主要指 NO及 NO2)主要来源于化石燃料的燃烧.大量的 NOx排入大气中会造成一系列的环境问题,如硝酸型酸雨、与 O3发生化学反应导致的臭氧层空洞、与碳氢化合物发生光化学反应引起的光化学烟雾等,严重威胁着人类健康和生存环境[1-3].面对日益严苛的氮氧化物排放标准,减排形势刻不容缓.NH3-SCR(以 NH3为还原剂的选择性催化还原)作为一项成熟、高效、运行可靠的脱硝技术,广泛应用于燃煤电厂烟气中氮氧化物的脱除.催化剂作为 SCR技术的核心,决定了脱硝系统的效率和运行成本[4-5].目前商用 V2O5-WO3(MoO3)/TiO2[6-12]催化剂活性温度窗口多位于 300~400℃,但因钒钛催化剂具有成本高、V2O5可氧化SO2为 SO3、钒的生物毒性易迁移等缺点,在国家加强废烟气脱硝催化剂管理及危险废弃物监管的背景下,寻求可替代商用钒钛催化剂的环境友好型催化剂势在必行.
研究表明,铁基 SCR催化剂在中高温具备良好的催化活性、N2选择性,同时其来源广泛、价格低廉,广为学者研究[13-14].目前围绕铁基 SCR脱硝催化剂的研究主要有 Mn-Fe/TiO2[13]、Ce-Fe/WMH[15]、Fe/WO3-ZrO2[16]、Fe/TiO2[17]、Fe-Ti[18]、Fe/Ce-Ti[19]、Fe-Mn-Ce/γ-Al2O3[20]和FexEr1-xVO4/TiO2-WO3-SiO2[21]等.Casanova等[21]研究Fe对催化剂SCR活性影响,采用沉淀法制备 Fe-Er-V/TiO2-WO3-SiO2催化剂,实验结果表明 Fe含量直接影响中低温段 SCR活性,Fe-Er之间协同作用是催化剂具备高脱硝活性及良好稳定性的重要原因.Cao等[20]研究 Fe的掺杂对负载型锰铈催化剂活性的影响,采用溶胶凝胶法制备 Fe-Mn-Ce/γ-Al2O3催化剂,活性试验表明,Fe掺杂有利于提高催化剂反应活性;微观表征表明 Fe掺杂明显增强催化剂表面酸性,同时比表面积、比孔容显著增大.前期研究发现,新型铁镁复合氧化物催化剂Fe0.8Mg0.2Oz[22]具备良好的脱硝性能,最大脱硝效率可达99%,在250~350℃脱硝效率均可保持90%以上,但其在 350℃以上 NH3氧化为 NO的副反应导致脱硝效率大幅下降,且在 H2O及 SO2存在的情况下脱硝效率有明显的下降,需要对其进行进一步改性,使其能够适用于燃煤电厂实际运行工况.学者研究表明,TiO2在 200℃以上同 SO2及 SO3均不发生反应,作为载体其良好的抗 SO2中毒性能使其在SCR催化剂中得到广泛应用.基于 Fe0.8Mg0.2Oz催化剂及 TiO2载体的优势,采用浸渍-共沉淀微波热解法制备不同 TiO2载体量的 Fe0.8Mg0.2Oz/TiO2(m)催化剂,在活性测试反应台考察其脱硝性能以及 SO2、H2O对其脱硝活性的影响,在此基础上借助 X射线衍射、N2吸附-脱附、扫描电子显微镜、能谱分析等表征手段,对催化剂元素组成、晶相、孔隙结构、微观形貌等进行分析,旨在为TiO2负载型Fe0.8Mg0.2Oz催化剂的进一步研发与应用提供理论依据.
1 催化剂制备测试及表征方法
1.1 催化剂制备
分别选取硫酸亚铁(FeSO4·7H2O)、硝酸镁(Mg(NO3)2·6H2O)、TiO2、氨水(NH3·H2O,25%),采用浸渍-共沉淀微波热解法制备Fe0.8Mg0.2Oz/TiO2(m)催化剂.按照比例称取一定质量硫酸亚铁、硝酸镁溶解于去离子水中制成 250mL混合溶液,搅拌1h至充分溶解.将TiO2缓慢加入混合溶液并持续搅拌6h后,将沉淀剂氨水(2mol/L)缓慢滴定到混合溶液,直至其 pH 值升至 9~10;悬浊液过滤后去离子水反复冲洗滤饼,直至滤液呈中性;滤饼在 1mol/L Na2CO3溶液浸渍数次后进行微波热处理,得到的前驱体去离子水反复洗涤至中性;前驱体烘干温度为 105℃,烘干时间 10h;烘干后的前驱体400℃煅烧 5h得到样品.冷却后的样品经破碎、研磨、筛分,取 40~60目(粒径为0.28~0.45mm)作为实验用催化剂.催化剂记为 Fe0.8Mg0.2Oz/TiO2(m),其中m表示TiO2载体含量,250mL的0.02mol/L混合溶液的TiO2载体量分别为5g、10g、15g和20g.
1.2 催化剂活性测试
催化剂活性测试系统由气体预配、预热及反应区、烟气分析处理 3部分组成.实验装置系统如图1所示.实验用模拟烟气由各标准气瓶提供,分别为N2(≥99.2%)、O2(≥99.2%)、NO(10%,N2为平衡气)及 NH3(10%,N2为平衡气).气体经过质量流量计按照一定的流量在混气罐中均匀混合.均匀混合的气体通过预热段预热后,进入石英固定床反应器中进行脱硝反应,反应后的尾气经尾气处理装置除去未反应氨气,由烟气分析仪进行成分分析.
实验工况参数为 NO体积分数为 0.1%、NH3体积分数为0.1%、O2体积分数大于或等于3.5%,空速比 30 000 h-1、催化剂体积为 4 mL、气体总流量为2 000 mL/min.活性测试温度范围 100~400℃(每25℃作为 1个测试温度点),为消除催化剂吸附的影响,每次实验前稳定运行 50min后进行测试.反应前、后烟气由MGA 5型烟气分析仪取样分析其NO、NO2及 NOx总浓度.催化剂的脱硝活性由 NOx转化率η反映,即

图1 活性实验装置系统示意Fig.1 Schematic diagram of NH3-SCR test of flue gas with a quartz fixed-bed reactor

1.3 催化剂表征
X射线衍射(X-ray diffraction,XRD)使用日本理学公司 Rigaku D/max 2500PC转靶 X射线衍射仪.测试条件为:Cu靶为辐射线源,电压50kV,电流150mA,步长 0.1°,扫描速率 4°/min,扫描角度取10°~90°.采用 ASAP2020比表面积分析仪进行 N2吸附-脱附测试,利用 BET方程、BJH模型分别计算获得催化剂的比表面积、吸附平均孔径、比孔容及孔径分布.催化剂SEM微观表面形貌采用JSM-6700F冷场发射扫描电子显微镜进行观测.采用 Oxford INCA X sight 能谱分析仪(energy dispersive spectrometer,EDS)分析催化剂元素类别及含量.
2 实验结果与讨论
2.1 TiO2载体量对Fe0.8Mg0.2Oz催化剂SCR活性的影响
图2为 TiO2载体量对 Fe0.8Mg0.2Oz催化剂脱硝活性的影响.从图2中可以看出,Fe0.8Mg0.2Oz催化剂在325℃时NOx转化率最大,为99%;当反应温度为250~350℃时,NOx转化率可维持90%以上,在温度超过350℃时催化剂NOx转化率急剧下降,到400℃时仅为 40%,出现该现象的主要原因是 NH3在高温时发生氧化、分解等副反应.

图2 TiO2载体量对 Fe0.8Mg0.2Oz催化剂 SCR活性的影响Fig.2 NH3-SCR activities over Fe0.8Mg0.2Oz/TiO2 catalysts
在负载型催化剂中,Fe0.8Mg0.2Oz/TiO2(10g)催化剂活性温度窗口 300~400℃,NOx转化率最大可达100%,表现出最优的脱硝性能.Fe0.8Mg0.2Oz/TiO2(10g)催化剂 NOx转化率在 250~300℃温度范围相比 Fe0.8Mg0.2Oz催化剂转化率略有降低,但其活性温度窗口更贴近实际运行中的脱硝温度窗口,具有较强的工业适用性.分析不同 TiO2载体量与 Fe0.8Mg0.2Oz催化剂SCR活性的关系,认为当载体量较小时,活性成分在TiO2表面分散不均匀;当载体量过量时,载体用量的加大不可避免地导致铁镁含量减少,导致催化剂活性明显下降.综上分析,当TiO2载体量与铁镁含量适宜时,明显抑制了 Fe0.8Mg0.2Oz催化剂 350℃以上副反应的发生.
2.2 Fe0.8Mg0.2Oz/TiO2(10 g)催化剂抗水抗硫性能研究
图3为 SO2、H2O 氛围对 Fe0.8Mg0.2Oz催化剂及Fe0.8Mg0.2Oz/TiO2(10g)催化剂SCR活性的影响.实验中选取SO2体积分数为0.04%,H2O体积分数为10%(通常燃煤电厂尾部烟气SO2体积分数为 0.02%~0.1%,H2O体积分数为1%~10%).实验中每1h记录1次数据,催化剂在 350℃稳定运行 1.5h后通入0.04%SO2.

图3 SO2、H2O 对 Fe0.8Mg0.2Oz/TiO2(10 g)催化剂 SCR活性的影响Fig.3 Effect of SO2 and H2O on SCR performances over Fe0.8Mg0.2Oz/TiO2(10 g)catalysts
Fe0.8Mg0.2Oz催化剂在通入 SO2后脱硝活性急剧下降,NOx转化率由94%逐渐降至77%,在10h时,在 0.04%SO2基础上通入 10%H2O稳定运行 10h,NOx转化率进一步降至68%.在0.04%SO2存在的情况下,Fe0.8Mg0.2Oz/TiO2(10g)催化剂的 NOx转化率由 99%降至约 96%,继续通入 10%H2O后,NOx转化率稍有下降,可维持约93%稳定运行10h.通过以上分析可知,TiO2作为载体可以显著提高Fe0.8Mg0.2Oz催化剂抗水、抗硫性能.
2.3 TiO2负载型Fe0.8Mg0.2Oz催化剂XRD分析
图4为TiO2负载型Fe0.8Mg0.2Oz催化剂XRD谱图.Fe0.8Mg0.2Oz催化剂在 2θ为 30.21°、35.53°、43.22°、53.79°、57.38°和 62.85°处出现明显的晶格衍射峰,对比 JCPDS标准 PDF卡片#39-1346,该晶格衍射峰为γ-Fe2O3的晶格衍射峰,说明Fe0.8Mg0.2Oz催化剂中 γ-Fe2O3为主要活性物质,同时在 XRD 图谱中没有Mg及其氧化物的衍射峰出现,推断Mg在催化剂中以无定形态存在或高度分散.除上述 γ-Fe2O3衍射峰外,Fe0.8Mg0.2Oz/TiO2催化剂XRD谱图中还存在锐钛矿TiO2衍射峰(#21-1272)及金红石TiO2衍射峰(#21-1276).由此可见,载体 TiO2加入削弱了 γ-Fe2O3衍射峰强度,其在催化剂中的存在形式以锐钛矿TiO2为主.

图4 TiO2负载型Fe0.8Mg0.2Oz催化剂XRD谱图Fig.4 XRD spectrum of Fe0.8Mg0.2Oz/TiO2 catalysts
采用 Debye-Scherrer公式定量分析计算催化剂晶粒尺寸,即

式中:D为样品的晶粒尺寸,nm;k为Scherrer常数,为0.89;λ为入射X射线波长,为 0.154046nm;θ为布拉格衍射角,采用弧度制;β为对应衍射峰的半高峰宽.消除背景及 Kα2的影响,读取 3处最强峰处的衍射角θ及半高峰宽β,代入公式(2)求平均值,求得催化剂晶粒尺寸,如表1所示,可以看出TiO2作为负载降低了 γ-Fe2O3结晶程度,减小了晶粒直径,使得晶粒得到细化.

表1 Debye-Scherrer计算的催化剂晶粒尺寸Tab.1 Average crystallite size of the catalysts calculated by Debye-Scherrer formula
2.4 TiO2负载型Fe0.8Mg0.2Oz催化剂孔隙结构分析
催化剂的微观孔隙结构(如比表面积、比孔容、孔径等)与催化剂的 SCR宏观脱硝活性密切相关[23].表 2为 TiO2负载型 Fe0.8Mg0.2Oz催化剂的微观孔隙结构参数.

表2 催化剂比表面积、比孔容、平均孔径Tab.2 Surface properties of the catalysts
随着 TiO2载体量的增加,Fe0.8Mg0.2Oz/TiO2催化剂的比表面积先增大,当载体量过大时比表面积下降;比孔容、平均孔径随 TiO2载体量的增加依次递增.通常认为催化剂表面活性位数量影响其脱硝活性,活性位数量越多,脱硝活性越好;而催化剂比表面积和平均孔容直接影响并决定其活性位总数.TiO2载体的加入使 Fe0.8Mg0.2Oz催化剂的比表面积、比孔容及平均孔径均有所增加,但与 Fe0.8Mg0.2Oz催化剂相比,Fe0.8Mg0.2Oz/TiO2催化剂脱硝性能并非随 TiO2的加入均有所提高,由此可见比表面积等空隙结构参数并非是影响催化剂脱硝性能的唯一因素.结合活性测试结果,同样说明 Fe0.8Mg0.2Oz/TiO2催化剂的活性并非随着 TiO2载体用量的加大而依次增强,当负载量适宜时催化剂获得最佳活性.
表3为Fe0.8Mg0.2Oz/TiO2催化剂的t-Plot微孔分析,可知其微孔孔容很小,接近为0;其介孔孔面积远大于微孔孔面积,表明催化剂中仅含有少量微孔.
图5为Fe0.8Mg0.2Oz/TiO2催化剂孔径分布特性曲线,可以看出,催化剂中孔径在 2~10nm 区间内集中分布,说明催化剂中孔结构以介孔(2~50nm)为主;而在孔径小于 2nm 范围内几乎没有分布,说明催化剂内部几乎不含有微孔.相比 Fe0.8Mg0.2Oz催化剂,Fe0.8Mg0.2Oz/TiO2催化剂孔容分布曲线中 50~100nm内呈现明显的上升趋势,说明催化剂中还存在一定数量的大孔,大孔的存在可以减小反应气体的扩散阻力,有利于传质.
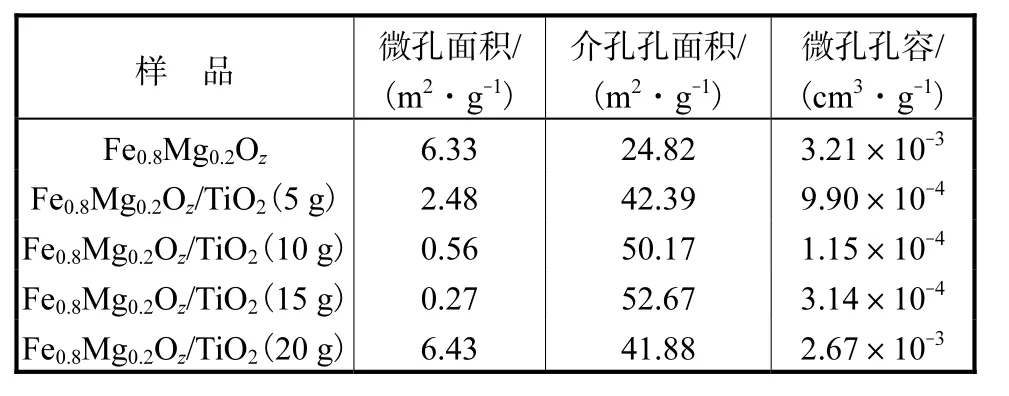
表3 催化剂t-Plot微孔分析Tab.3 t-Plot properties of the catalysts

图5 Fe0.8Mg0.2Oz/TiO2催化剂孔分布特性Fig.5 Pore distribution characterization of Fe0.8Mg0.2Oz/TiO2 catalysts
图6为Fe0.8Mg0.2Oz/TiO2催化剂N2等温吸附-脱附曲线.Fe0.8Mg0.2Oz/TiO2催化剂等温吸附脱附曲线根据IUPAC(international union of pure and applied chemistry)分类方法,隶属于V型曲线,伴随H3滞后环.由曲线及滞后环类型推测气-固反应在催化剂表面片状颗粒松散堆积形成的楔形孔(狭缝孔,属介孔)中发生.
2.5 TiO2负载型Fe0.8Mg0.2Oz催化剂SEM分析
图7为 Fe0.8Mg0.2Oz催化剂及 Fe0.8Mg0.2Oz/TiO2催化剂 SEM 形貌分析.由图可知,相较于Fe0.8Mg0.2Oz催化剂,Fe0.8Mg0.2Oz/TiO2催化剂颗粒细化程度明显得到改善.其中 Fe0.8Mg0.2Oz/TiO2(5g)出现严重的孔结构坍塌,很难观察到清晰的孔隙结构.Fe0.8Mg0.2Oz/TiO2(10g)催化剂表面颗粒分布均匀,能够形成丰富的孔间结构,且表面孔道清晰,具备明显的孔隙结构,为反应气体在催化剂表面的吸附提供丰富的吸附位点,从而有利于提高催化剂脱硝性能.Fe0.8Mg0.2Oz/TiO2(15g)催化剂孔结构坍塌堵塞严重,几乎难以观察到可见孔隙结构.Fe0.8Mg0.2Oz/TiO2(20g)催化剂表面颗粒堆积紧密,出现黏连团聚现象,从而增加了反应气体进入催化剂表面结构的阻力,导致部分反应气体未能参与反应,因而降低了催化剂的脱硝性能.
因此,催化剂表面颗粒呈现球状,且相互独立、分布均匀,可以保证良好的孔隙结构,减小反应气体在孔隙结构内的扩散阻力,利于传质的进行;同时可提供较大的比表面积,为反应提供更多的吸附位点.综上原因使得 Fe0.8Mg0.2Oz/TiO2(10g)催化剂表现出优越的脱硝性能.

图6 催化剂N2等温吸附-脱附曲线Fig.6 N2-adsorption-desorption isotherms of catalysts

图7 Fe0.8Mg0.2Oz/TiO2催化剂SEM形貌Fig.7 SEM images of Fe0.8Mg0.2Oz/TiO2 catalysts
2.6 TiO2负载型Fe0.8Mg0.2Oz催化剂EDS分析
为了解 Fe0.8Mg0.2Oz催化剂及 Fe0.8Mg0.2Oz/TiO2催化剂的元素成分及含量,对其表面元素成分定量分析,结果如表4所示.Fe0.8Mg0.2Oz催化剂中含有Fe、Mg和 O,Fe0.8Mg0.2Oz/TiO2催化剂主要元素组成为Fe、Mg、O和Ti.TiO2作为载体可促进晶格氧向催化剂表面富集;丰富的表面晶格氧可提高其表面氧化性,将NO氧化为NO2,诱发快速SCR反应的发生,从而保证了催化剂的脱硝性能[24].
图8为 Fe0.8Mg0.2Oz催化剂和 Fe0.8Mg0.2Oz/TiO2催化剂固定区域元素分布面扫.由图可见,在Fe0.8Mg0.2Oz催化剂和 Fe0.8Mg0.2Oz/TiO2催化剂中,元素均呈现均匀分布.相较于 Fe0.8Mg0.2Oz催化剂,Fe0.8Mg0.2Oz/TiO2催化剂中元素分布更加均匀.表面元素的均匀分布说明铁、镁、氧和钛之前存在强烈的相互作用,与XRD结果一致.

表4 催化剂表面元素成分分析Tab.4 EDS elementary composition of Fe0.8Mg0.2Oz/TiO2 catalysts

图8 催化剂EDS固定区域元素面扫Fig.8 EDS mapping of the catalysts
3 结 论
(1) Fe0.8Mg0.2Oz/TiO2(10g)催化剂在 NH3-SCR反应中表现出良好的脱硝活性及抗 SO2/H2O性能.其最大脱硝效率可达 100%,在 300~400℃温度窗口内可保持 90%以上的脱硝效率,在体积分数为0.04%的 SO2及10%的H2O存在的情况下仍能保持93%以上的脱硝效率.
(2) Fe0.8Mg0.2Oz/TiO2(10g)催化剂中,TiO2作为载体可以降低 γ-Fe2O3结晶程度,减小催化剂晶粒直径,提高晶粒的细化程度.
(3) Fe0.8Mg0.2Oz/TiO2(10g)催化剂中,较大的比表面积、比孔容能够为反应气体在催化剂表面吸附与活化提供丰富的表面活性位;合理的孔结构分布、良好的孔间连通性则利于传质的快速进行,表面丰富的晶格氧有效保证了催化剂的SCR脱硝性能.
