前臂贵要静脉不同转位方式建立动静脉内瘘
2019-08-24叶祖扬尹友生毕慧欣欧俊潘罅冷斌王函
叶祖扬 尹友生 毕慧欣 欧俊 潘罅 冷斌 王函
桂林医学院附属医院肾内科(广西桂林541001)
血液透析是终末期肾病的重要替代治疗方式,自体动静脉内瘘是血液透析首选的血管通路。中国血管通路专家共识在对自体内瘘的优先次序中建议,首选腕部自体内瘘,次选前臂转位内瘘,最后选择肘部自体内瘘[1]。随着透析质量的提高及医疗保险的普及,血液透析患者的透析龄逐渐延长,首选的腕部自体内瘘不可避免面临失功-重建-失功的局面,最终导致头静脉耗竭;另外,高龄、糖尿病、静脉反复留置针等因素可引起头静脉纤细、血栓、闭塞。前臂贵要静脉作为次选方案,可行直桥式转位与桡动脉吻合,或行U形转位与肱动脉末段或桡尺动脉起始段吻合。目前国内外尚未见贵要静脉直桥式和U形转位内瘘的对比性研究报道,本文将对两者的临床效果进行比较分析。
1 资料与方法
1.1 一般资料选择2015年3月至2018年6月在我院行前臂贵要静脉转位内瘘术患者38例为研究对象,男 22例,女 16例,年龄 32~73岁,平均(56.5±9.5)岁,透析龄1~125个月。纳入标准:(1)肾小球滤过率<15 mL/min,诊断慢性肾脏病5期;(2)前臂头静脉内径小于1 mm或先天闭锁,或内瘘术后头静脉耗竭;(3)贵要静脉内径>1 mm,血管通畅,无狭窄及血栓;(4)动脉内径>1.5 mm,峰值流速>40 cm/s。术者均为本文第一作者。前臂桡动脉内径>1.5 mm患者行贵要静脉直桥式转位手术共21例(A组),前臂桡动脉内径<1.5 mm患者行贵要静脉U形转位手术共17例(B组)。A组肾衰竭的病因:慢性肾小球肾炎8例(38.1%),梗阻性肾病7例(33.3%),高血压肾病4例(19%),糖尿病肾病1例(4.8%),多囊肾1例(4.8%)。B组肾衰竭的病因:慢性肾小球肾炎7例(41.2%),梗阻性肾病5例(29.4%),高血压肾病4例(23.5%),糖尿病肾病1例(5.9%)。A组动脉内径1.5~3.8 mm,B组动脉内径2.5~4.5 mm,A组平均动脉内径比B组小,两组差异有统计学意义(P<0.05)。A组静脉内径1.0~2.5 mm,其中17例<2 mm(81%),4例≥ 2 mm(19%);B组静脉内径1.3~2.6 mm,其中13例<2 mm(77%),4例≥ 2 mm(23%)。两组患者性别、年龄、透析龄、转位原因、平均静脉内径差异无统计学意义(P>0.05)。见表1。
表1 两组手术前情况比较Tab.1 Comparison of preoperative conditions between the two groups±s

表1 两组手术前情况比较Tab.1 Comparison of preoperative conditions between the two groups±s
观察指标男/女(例)年龄(岁)透析龄(月)转位原因(头静脉纤细/头静脉耗竭,例)动脉内径(mm)静脉内径(mm)A组12/9 56.2±9.1 36.1±31.9 6/15 2.3±0.6 1.7±0.3 B组10/7 56.7±10.2 33.6±28.2 5/12 3.8±0.5 1.8±0.4 t或χ2值0.011-0.168 0.258 0.003-8.252-0.847 P值0.917 0.868 0.798 0.955 0.000 0.403
1.2 术前准备血管评估及手术方案的设计:ALLEN试验评估行内瘘肢体的桡、尺动脉血供,全部病例均为阴性。肘上束缚压脉带,待贵要静脉充盈,用食指和中指指腹感受血管弹性、充盈度及走行情况,并用记号笔标记其走行及主要的分支。用彩超测量贵要静脉和动脉的内径、流速,了解有无血栓、狭窄、闭塞段。
全身状态的准备:控制患者的血压、血糖,充分透析减轻机体水负荷,充分进行医患沟通,告知手术方案的选择及手术风险等。
1.3 手术方法A组:沿贵要静脉走行处,用1%利多卡因局部浸润麻醉,沿术前标识的贵要静脉主干作间断的纵切口,每个切口长度3~4 cm,每个切口间隔2~3 cm,钝性分离皮下组织,4-0丝线结扎贵要静脉属支,分离出贵要静脉18~23 cm。结扎离断贵要静脉远心端,用肝素盐水缓慢冲洗分离出来的贵要静脉近心端,并行液性扩张。将分离出的贵要静脉摆放至原设计的转位路径,再次评估决定前臂远心端动脉的皮肤切口,作2~3 cm纵形切口,分离出约2 cm的桡动脉备用。在设计好的皮下隧道走行处用1%利多卡因局部浸润麻醉,根据原贵要静脉的属支方向捋顺静脉,避免扭转,用专用皮下隧道针末端与贵要静脉远心端固定,将隧道针穿过皮下,牵引贵要静脉转位至分离出的桡动脉处,再次予肝素盐水冲洗贵要静脉,可触及明显水流震颤,判断静脉无扭转。修剪静脉血管口,桡动脉侧切7~8 mm,用7-0血管缝线连续外翻做端侧吻合贵要静脉与桡动脉,缝合间距及边距均为1 mm左右。缝合后,开放血流,可见内瘘血管充盈,血管走行处触及明显血管震颤。
B组:除以下操作有区别外,余操作同直行转位组:当贵要静脉分离处理后,用隧道针建立U形皮下隧道,将贵要静脉转位至肘下肱动脉末段或桡动脉起始段,两者行端侧吻合。
1.4 手术注意事项(1)静脉分支结扎处离主干1 mm以上,避免术后血管扩张受限导致相对狭窄。(2)结扎的属支方向做好记录或者用记号笔标记,避免转位时血管扭转。(3)钝性分离贵要静脉时,注意保留贵要静脉周围结缔组织,避免破坏原血管外膜的血供,防止术后血管壁缺血导致的狭窄。(4)贵要静脉分离后要用肝素生理盐水冲洗,观察是否有管腔破损渗漏,如发现管腔破损渗漏,用7-0血管缝线修补,避免转位术后出现皮下血肿,严重时压迫可导致内瘘闭塞。(5)贵要静脉要用肝素生理盐水逐步做均匀的液性扩张后再通过皮下隧道,避免有局限性的狭窄,但应注意避免过度扩张。(6)贵要静脉穿过皮下隧道时,要注意深浅适中,避免张力过大,并使静脉尽可能多地转位至掌面,以方便成熟后穿刺使用。(7)注意松解靠近肱骨内上髁处的贵要静脉,避免其受压及转角过大。(8)U形转位时,在保证转弯处不打折的情况下,减小转弯的距离,以尽可能多地增加术后穿刺长度。
1.5 观察指标观察两组患者(1)手术成功率及术后1个月、6个月、1年、2年的通畅率。(2)手术时间、成熟时间、血透流量、可穿刺长度、平均使用时间、并发症。(3)COX风险比例回归模型对内瘘使用时间的影响因素进行分析,以明确哪些因素可能对内瘘远期预后产生影响。
1.6 评价标准(1)术后内瘘可触及震颤、闻及血管杂音评价为手术成功。(2)彩超提示内瘘自然血流量>500 mL/min,能成功穿刺行血液透析,血透泵控流量>200 mL/min为内瘘成熟。(3)两组患者转位内瘘成熟后每周透析3次,每次透析4 h。随访时间8~47个月,观察终点为2019年2月28日。
1.7 统计学方法实验数据采用SPSS 22.0统计软件进行统计学处理,连续变量数据均以表示,比较差异性用χ2检验或t检验。使用Kaplan-Meire法绘制内瘘使用时间的生存曲线来比较两种手术方式的通畅率。采用COX风险比例回归模型对患者内瘘使用时间的远期预后进行多因素分析。P<0.05为差异有统计学意义。
2 结果
2.1 手术成功率及通畅率两组全部取得手术成功,成功率达100%。两组内瘘均能成熟使用,术后1个月、6个月、1年通畅率两组比较差异无统计学意义(P>0.05),两组2年通畅率差异有统计学意义(P<0.05),见表2。
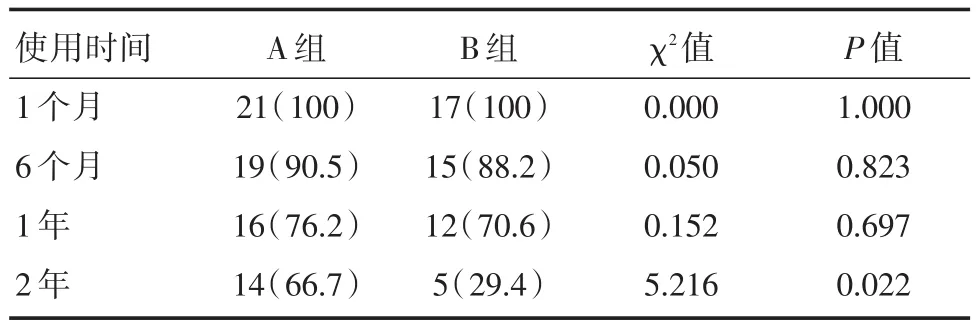
表2 两组术后不同时期通畅率比较Tab.2 Comparison of patency rates in different periods after operation between the two groups 例(%)
2.2 手术及内瘘使用情况A组手术时间明显短于B组(P<0.05),A组内瘘可穿刺长度大于B组(P<0.05),内瘘的成熟时间、血透流量差异无统计学意义。A组内瘘最长使用时间47个月(仍在随访中),B组内瘘最长使用时间26个月(仍在随访中),A组平均使用时间较B组长(P<0.05),见表3、图1。两组手术后均未发生皮下血肿、术口感染、肿胀手综合征、窃血综合征、肢端淤血、心功能不全等并发症。
表3 两组术后指标观察比较Tab.3 Comparison of postoperative indexes between the two groups±s

表3 两组术后指标观察比较Tab.3 Comparison of postoperative indexes between the two groups±s
观察指标手术时间(min)内瘘成熟时间(周)术后3个月血透流量(mL/min)术后3个月可穿刺长度(cm)平均使用时间(月)A组93.6±12.9 8.9±2.1 253.1±19.6 16.8±1.2 24.1±11.4 B组114.4±10.0 8.7±1.7 241.5±19.9 12.4±1.7 16.8±7.5 t值-5.449 0.413 1.806 9.433 2.269 P值0.000 0.682 0.079 0.000 0.029
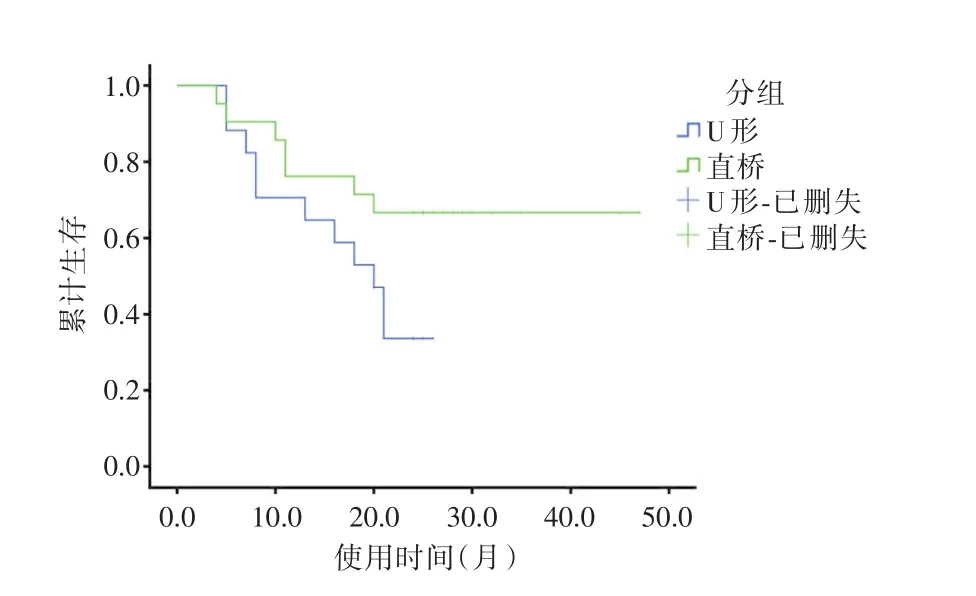
图1 直桥式与U形转位内瘘Kaplan-Meire生存曲线Fig.1 Kaplan-Meire survival curve of direct transposition andlooped transposition arteriovenous fistula
2.3 多因素COX风险回归分析结果以内瘘使用时间>2年为标准对前臂贵要静脉转位内瘘术后使用时间的影响进行多因素COX风险回归分析,以内瘘功能为因变量(赋值:通畅=0,失功=1),以性别(赋值:男=0,女=1)、年龄、动脉内径、静脉内径、内瘘可穿刺长度、不同手术方式(赋值:直桥式内瘘=0,U形转位内瘘=1)为自变量。结果显示,不同手术方式是影响患者内瘘远期使用的独立预后因素(P<0.05),见表4。
3 讨论
贵要静脉在前臂位于尺背侧,由于其特殊的解剖位置,很少用于静脉穿刺或静脉输注,静脉状况良好,对于头静脉先天纤细的患者,贵要静脉可与尺动脉建立动静脉内瘘,但使用起来很不方便。如果患者曾建立桡动脉-头静脉标准内瘘,为了避免手部缺血,不建议在这种情况下使用尺动脉与贵要静脉建立内瘘,所以贵要静脉的使用受到了限制。贵要静脉转位内瘘手术创伤大,手术耗时长,对手术医生的技术要求高,所以当腕部标准内瘘失功后,更多临床医生选择高位重建内瘘,但其高输出量心力衰竭及窃血综合征的问题成了争论的焦点[2]。近年来的研究发现贵要静脉转位内瘘作为血液透析的替代通路效果显著[3-4],有研究[5]表明,上臂贵要静脉转位内瘘比人造血管内瘘具有更好的通畅性、更少的并发症。前臂贵要静脉转位内瘘和上臂贵要静脉转位内瘘均能取得满意的通畅性[6]。本研究中术后两组患者即刻成功率均为100%,说明本中心手术者成熟掌握了复杂疑难内瘘手术的技术。手术后1个月两组保持100%通畅,内瘘术后早期均能成熟使用,术前存在动脉差异的情况并未影响内瘘的成熟。直桥式转位内瘘6个月、1年通畅率高于U形转位内瘘,但差异无统计学意义,两组均低于本中心腕部标准内瘘的通畅率[7],这可能与转位手术要分离的静脉较长有关。分离的静脉越长,其外膜的滋养血管破坏得越多,且皮下隧道愈合过程会出现疤痕粘连,导致静脉扩张受到一定程度的限制,最终导致狭窄闭塞。直桥式转位内瘘2年通畅率明显高于U形转位内瘘,两者差异有统计学意义,说明直桥式转位内瘘有更长远的通畅率。
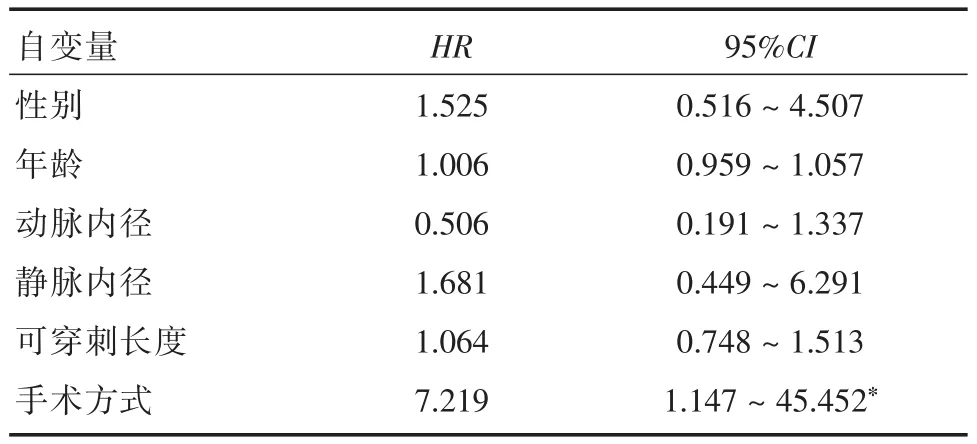
表4 内瘘远期使用影响因素的多因素COX风险回归分析Tab.4 Multifactor COX risk regression analysis of influencing factors of long-term use of arteriovenous fistula
回顾国内外的研究报道,前臂贵要静脉直桥式转位内瘘的1年通畅率79.1% ~ 90%[3,8-9],U形转位内瘘1年通畅率75% ~77%[10-11],从这些不同研究中心的数据看,直桥式转位内瘘的1年通畅率比U形转位高,这与本研究的结果相吻合。但是上述研究的1年通畅率均比本中心的高,分析其原因,考虑与静脉条件有关。国外的研究贵要静脉内径全部>2.5 mm,国内的研究贵要静脉内径至少>2 mm,本研究直桥式转位组贵要静脉内径>2 mm仅占19%,U形转位内瘘组占23%,而全部患者贵要静脉内径>2.5 mm的仅有1例(2.3%)。从上述数据可以看出,本中心患者静脉内径普遍偏小,考虑与所处的地理位置及人种特点有关,有研究提示,广西成年人身高和体重均排在全国后列[12],本中心所处的广西桂北地区比广西沿海地区人种更矮小,血管更细小。所以本研究中对静脉的选择只能放宽标准,在内径>1 mm的患者均尝试建立内瘘,术后通畅率受到一定的影响。虽然受静脉条件的限制,转位内瘘的术后通畅率会有所下降,但贵要静脉直桥式转位内瘘仍在随访中的患者最长使用时间47个月,平均使用时间24.1个月,表现出很好的临床应用价值,从充分利用血管的角度选择,其应优先于人工血管内瘘及高位内瘘。
本研究表明,直桥式转位内瘘比U形转位内瘘平均使用时间长。按正常解剖学关系,肱动脉末段或桡尺动脉起始段比腕部桡尺动脉有更大的内径、更高的流速[13]。本中心观察两组患者的动脉内径符合上述规律,U形转位内瘘所使用的动脉比直桥式转位内瘘的大,两者差异有统计学意义。术前观察对比两组患者性别、年龄、原发病、透析龄、选择贵要静脉转位的原因、贵要静脉内径,这些因素差异均无统计学意义。在上述条件下,贵要静脉U形转位与内径更大的肘部动脉吻合,理论上效果应该更好,内瘘使用时间和通畅率应该比直桥式转位高。但研究结果却相反,虽然肘部动脉内径更大,U形转位内瘘的平均使用时间和长远通畅率却更低,差异存在统计学意义。出现这种结果考虑与以下因素有关:(1)U形转位更复杂:虽然术中已做好血管走向标记,但自体血管质软,由于贵要静脉行U形转位皮下隧道操作的复杂性,其比直桥式转位更容易出现血管不同程度扭转或打折的可能,扭转或打折处会表现为相对狭窄,影响内瘘的使用寿命。(2)穿刺长度较短:本研究证实了U形转位内瘘的穿刺长度较短,相比直桥式内瘘差异有统计学意义,因为U形转位内瘘转弯处血管弯曲,不方便穿刺,导致穿刺长度缩短。穿刺长度缩短导致穿刺点减少,每个穿刺点达不到2~3周的间隔修复时间,频繁穿刺容易出现穿刺部位狭窄导致闭塞。(3)血流动力学影响:动脉血流入静脉后,U形转位内瘘在经过一段直行血流后突然转弯,弯型内瘘血管壁承受的剪切力比直行大,另外肘部动脉压力较大,相应的剪切力更大,所以内膜增生明显,更容易出现狭窄[14]。
U形转位内瘘因为要处理环形转位时的角度和评估检测避免血管扭转,需要耗费更多的时间。本研究表明,U形转位内瘘的手术时间明显长于直桥式转位内瘘,两者差异有统计学意义,说明U形转位内瘘的操作难度更大,对手术医生的要求更高,必须掌握熟练的显微外科技术,并有足够的耐心,更要细心地操作才能成功地完成手术。虽然两组手术时间存在差异,但两种方式转位内瘘在手术后的成熟时间在9周左右,不存在差异,血透时均能满足透析流量,血透流量>200 mL/min。并发症方面,有研究提示[15],上臂贵要静脉转位会出现假性动脉瘤、出血或血肿。本研究中前臂贵要静脉两种方式转位内瘘均未出现上述并发症,且未出现窃血综合征、肢端淤血、高输出量心力衰竭等并发症,与JAIRATH等[16]报道无明显差异。
多因素COX风险回归分析结果显示,虽然两组患者术前动脉内径、术后可穿刺长度存在差异,但并不是影响内瘘远期预后的独立因素,前臂贵要静脉转位动静脉内瘘术不同的手术方式才是内瘘远期通畅的独立预后因素。
综上所述,贵要静脉直桥式转位内瘘较U形转位内瘘手术时间更短,并有更长的使用时间及更长远的通畅率,在前臂动脉条件尚可的情况下,虽然肘部动脉更好,也建议优先选择直桥式转位内瘘。不能否认,贵要静脉U形转位内瘘平均使用时间也较高,并发症少,在前臂动脉条件不佳时,仍是一个很好的替代。前臂贵要静脉转位动静脉内瘘在血液透析中值得大力推广应用。
