硫酸头孢喹肟注射液在猪体内的生物等效性研究
2019-08-22李龙飞冯言言吴连勇
李龙飞,孔 梅,郑 莉,陈 玲,冯言言,常 雪,崔 进,吴连勇∗
(1.齐鲁动物保健品有限公司,济南250100;2.山东省兽药质量检验所,济南250022)
头孢喹肟(cefquinome,CEF)又名头孢喹诺、头孢喹咪,是德国赫斯特公司(Hoechst)于20世纪80年代开发的第一个第4代动物专用头孢类抗生素[1],临床应用中常用其硫酸盐。其抗菌谱广,抗菌活性强,对临床分离的大多数G+菌、G-菌均有较强的抗菌活性。金黄色葡萄球菌、链球菌、埃希氏大肠杆菌、溶血性巴氏杆菌、胸膜肺炎放线杆菌等菌对其敏感性较高。由于头孢母核的7位甲氧亚胺基-5-氨基噻唑取代基,其为抗菌活性的必须基团,和第三代头孢菌素不同的是其母核的3位有一个季铵盐基团,即头孢喹肟是一个两性离子,头孢核带负点荷,四价季铵离子基团带正电荷。这一结构有助于头孢喹肟快速穿透细胞膜,并决定了它对β-内酰胺酶的亲和力降低,且二者形成的复合物的稳定性也降低,所以头孢喹肟对β-内酰胺酶高度稳定,不易产生耐药性和交叉耐药性[2-3]。目前已被欧盟[4-6]批准用于猪和牛的呼吸系统疾病、牛急性乳腺炎、牛蹄病、牛败血症、母猪子宫炎-乳腺炎-无乳综合征、马败血症和呼吸系统疾病等。7.5%的硫酸头孢喹肟注射液,作为英国英特威(Intervet)公司于1994年研发的长效注射液,具有半衰期长、药效持久的特点。鉴于其药物作用范围广,毒性反应小,国内多为2.5%制剂,因此,市场应用价值大。本研究采用长效缓释技术成功仿制了该产品。按照生物等效性试验相关规范要求,以猪为研究对象,按照农业农村部颁发的《兽用化学药品生物等效性试验指导原则》的试验要求,对国产硫酸头孢喹肟注射液在猪体内的药代动力学特征研究,并与国外原研硫酸头孢喹肟注射液进行药动学参数比较及生物等效性分析,以期为国产硫酸头孢喹肟注射的研制和临床使用提供重要参考依据。
1 材 料
1.1 仪器 液相色谱-串联质谱仪:Waters Acquity UPLC,配电喷雾离子源,Waters公司;色谱柱:Waters BEH C18,100 ×2.1 mm,1.7 μm,Waters 公司;UPH-11-20T型优普超纯水制造系统:成都超纯科技有限公司;HQ-60-Ⅱ型漩涡混合器:北方同正生物技术有限公司;MIKRO 22R型高速冷冻离心机:德国Hettich科学仪器公司;ES 225SMDR型分析天平:感量0.00001 g,瑞士 Precisa公司;可调微量移液器:1~10、20~200、100~1000 μL,热电(上海)仪器有限公司;指形管(5 mL及1.5 mL),扬子化工玻璃仪器有限公司。
1.2 药品与试剂 硫酸头孢喹肟注射液受试品(惠可宁®):规格为 50 mL:3.75 g,生产批号:2310001,生产企业为齐鲁动物保健品有限公司有限公司。硫酸头孢喹肟注射液参比品(克百特®):规格为50 mL:3.75 g,生产批号:A173A01,有效期3年,生产商为默沙东制药有限公司。硫酸头孢喹肟标准品:纯度不小于99%,购自Dr.Ehrenstorfer.GmbH,Lot:40416。 甲醇、乙腈,均为色谱纯,美国TEDIA公司;甲酸,质谱纯,德国CNW公司;正己烷,色谱纯,德国CNW公司;超纯水,由MiLi-Q超纯水仪制取的超纯水,符合GB/T 6682二级用水规定。
乙腈饱和的正己烷:取100 mL正己烷和50 mL于250 mL分液漏斗中,振摇1 min,静置分层后,弃掉乙腈。
2 方 法
2.1 试验动物 根据硫酸头孢喹肟注射液生物等效性预试验结果,计算硫酸头孢喹肟正式试验所需动物的样本容量为18头,为了保证试验结果的可靠性,选择北京市海淀区苏家坨周春生养殖场内平均70日龄的20头体重27.62±1.84 kg健康三元杂交猪,公母各半。试验地点为北京市海淀区苏家坨周春生养殖场,实验动物符合国家实验动物标准普通级实验动物微生物学、寄生虫学等等级要求,且在试验前1 d经兽医检查确认是处于良好的健康状况下,试验前1个月内未用过相关药物治疗。试验猪于实验前在新环境经过至少1周的适应期。给药前禁食过夜12 h,自由饮水,给药4 h后恢复正常饮食。饲料为不添加任何药物的全价饲料,给药前1 d统一用磅秤称量体重。
2.2 实验设计与给药方案 20头体重较一致的试验猪随机分为2组,每组猪公母各半,采用双处理、双周期随机交叉试验设计。第一周期第一组1~10号猪单剂量(3 mg/kg b.w.)肌内注射克百特®(参比制剂),第二组11 ~20 号猪单剂量(3 mg/kg b.w.)肌内注射惠可宁®(受试制剂);第二周期第一组1~10 号猪单剂量(3 mg/kg b.w.)肌内注射惠可宁®(受试制剂),第二组 11~20号猪单剂量(3 mg/kg b.w.)肌内注射克百特®(参比制剂)。两阶段给药间隔期为2周。
2.3 血样采集 猪站立保定后经前腔静脉丛采血。给药前采空白血,记为0 h,肌内注射给药后分别于0.167、0.333、0.5、0.75、1、2、3、4、8、12、24、36、48 h采血。每次采血量约4 mL。血样采集后置于用肝素浸润并烘干的离心管内,3800 r/min离心10 min,吸取上层血浆放在聚丙烯管中,密封,避光,-20℃短时保存待用。
2.4 色谱条件[4]色谱柱:Waters BEH C 18(100×2.1 mm,1.7 μm);流动相:0.1% 甲酸水溶液:0.1%甲酸乙腈溶液,流速:0.3 mL/min;柱温:25 ℃;进样量:5 μL(表 1)。
2.5 质谱条件[4]质谱仪:Waters Wuattro Premier;离子源:电喷雾离子源;扫描方式:正离子扫描;检测方式:多反应监测;离子源温度:120℃;脱溶剂温度:380℃;毛细管电压:3.0 kV;脱溶剂气流速:700 L/h;Q1,Q3 均为单位分辨率(表2)。
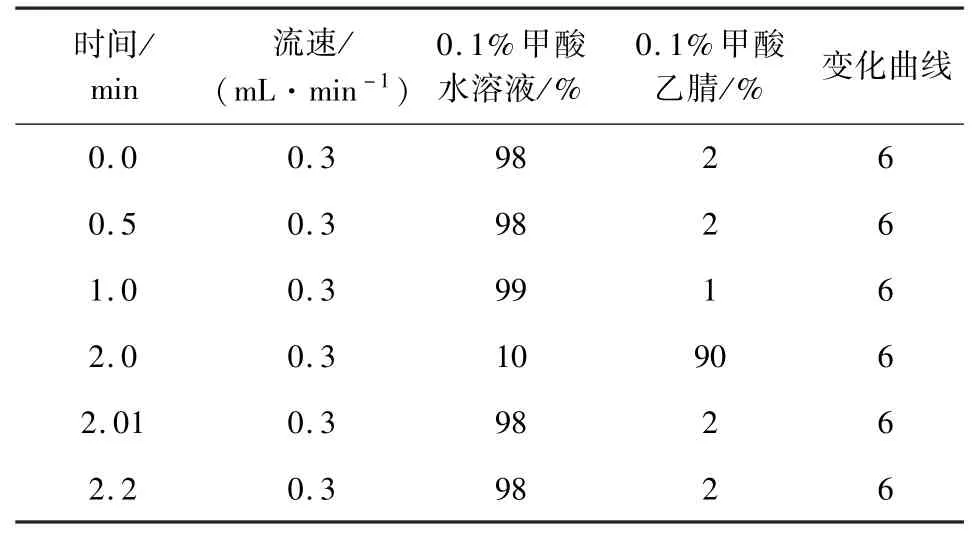
表1 超高效液相色谱梯度洗脱条件Tab 1 Ultrahigh performance liquid chromatography gradient elution conditions

表2 定性定量离子对、锥孔电压和碰撞能量Tab 2 Qualitative and quantitative ion pair,tapered hole voltage and collision energy
2.6 方法学实验 对硫酸头孢喹肟标准品进行准确度、精密度和稳定性试验(储备液稳定性、室温稳定性、冰冻和冻融稳定性),考察方法的合理性。
2.7 血浆样品处理[4]将冷冻保存的猪血浆室温下自然解冻,摇匀后精密移取200 μL血浆置于5 mL离心管中,混合涡旋10 s,加入800 μL乙腈去蛋白,混合涡旋2 min,4℃以下8 000 r/min离心10 min,把上层提取液转移至另一5 mL离心管,加入400 μL乙腈饱和的正己烷,振荡2 min,弃去正己烷,过0.2 μm 的滤膜,取 30 μL 进样供 UPLCMS/MS分析[4]。每批生物样品测定时建立新的标准曲线,并将每批生物样品测定结果(峰面积)采用新建立的标准曲线计算出硫酸头孢喹肟的含量。每批生物样品测定时随行测定低、中、高(50、500、1000 ng/mL)三个浓度的质控样品。质控样品测定结果的偏差小于20%。
2.8 数据分析 将实测血药浓度-时间数据采用WINNONLIN 6.3药动学分析软件进行非房室模型分析,计算药代动力学参数,药动学参数根据中国药科大学的杨劲老师编的《人体生物利用度数据处理通用程序,BAPP》软件进行生物等效性检验。对参数Cmax与AUC0-τ(已进行对数处理)进行多因素方差分析、90%置信区间及双单侧t检验,对受试品和参比品进行生物学等效性比较。
3 结果与分析
3.1 方法学实验结果
3.1.1 标准曲线 硫酸头孢喹肟注射液的血浆药物浓度在20.0 ~2000.0 ng/mL 范围内,血浆药物浓度与峰面积比值呈良好的线性关系(相关系数≥0.99)。以峰面积为横坐标,血药浓度为纵坐标,典型的标准曲线方程为:y=2.49136x-21.9872,r2=0.996563。
3.1.2 准确度和精密度 血浆中硫酸头孢喹肟UPLC-MS/MS测定方法的结果表明,空白血浆添加样品在50~1000 ng/mL范围内,批内和批间系数分别小于8.23%和5.95%,精密度良好;空白血浆中硫酸头孢喹肟添加浓度在50、500、1000 ng/mL时的平均回收率在99.42% ~100.31%,回收率稳定(表3)。
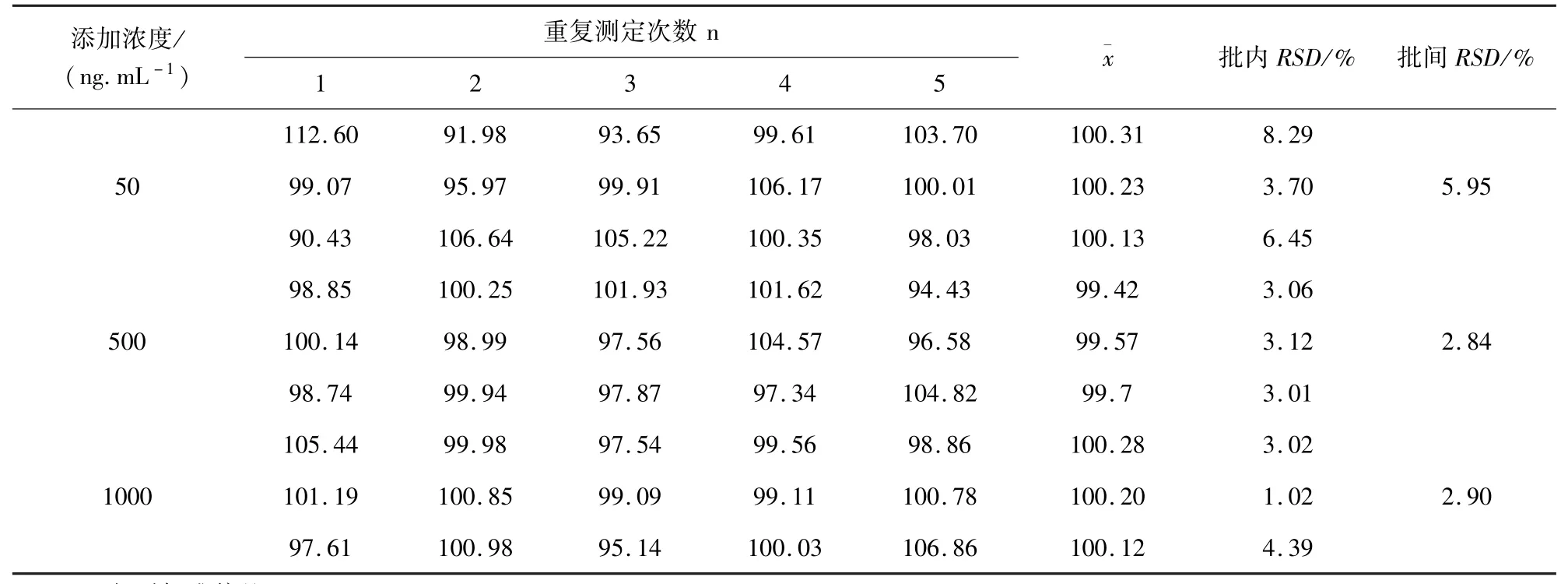
表3 准确度和精密度结果Tab 3 Accuracy and precision results
3.1.3 稳定性试验 对于猪血浆中的硫酸头孢喹肟而言,新鲜制备及制备后保存60 d的储备液中待测药物的响应值的变异系数低于20%,依然保持稳定,于-20℃条件下冻存时能够保持稳定21 d以上,在3个冻融循环之后仍可保持稳定,于室温条件(约22℃)下储存时可保持稳定达24 h。
3.2 猪单剂量肌内注射硫酸头孢喹肟受试品与参比品的实测血药浓度及动力学特征 猪单剂量(3 mg/kg b.w.)肌内注射硫酸头孢喹肟受试制剂和参比制剂后,不同时间测得的受试品和参比品对应的平均血药浓度-时间曲线见图1。血药浓度时间数据采用WINNONLIN 6.3版药代参数计算软件进行非房室模型分析计算药动学参数,结果见表4。
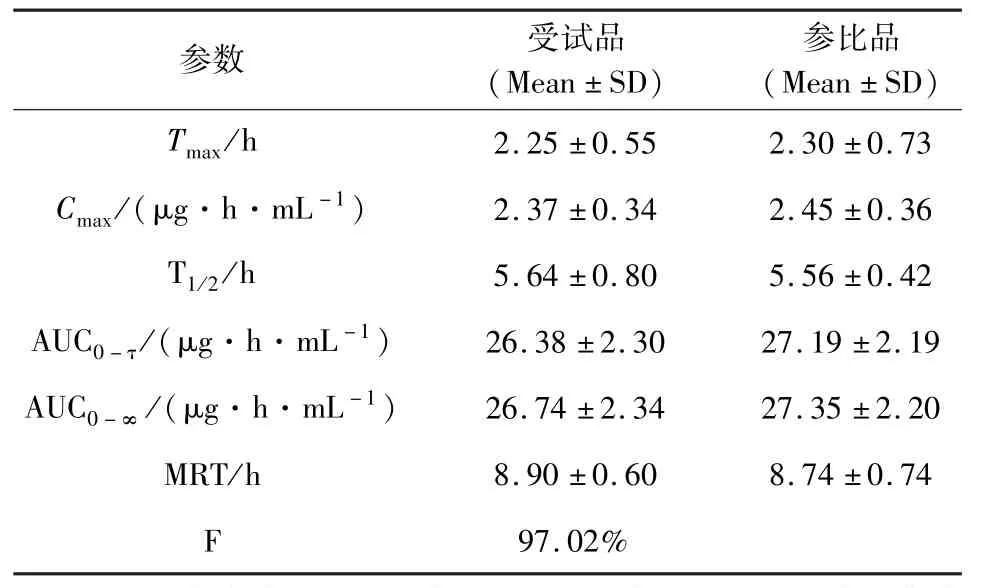
表4 两种制剂主要药动学参数Tab 4 Major pharmacokinetic parameters of two formulations
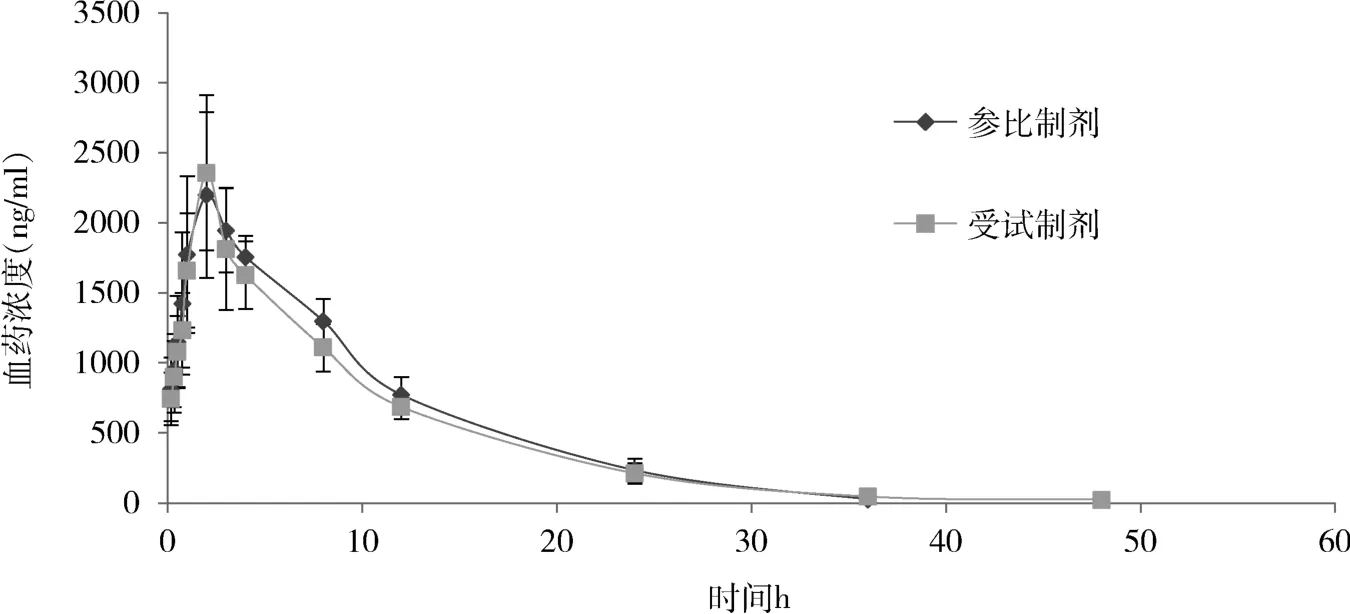
图1 两种制剂平均血药浓度-时间曲线Fig 1 Mean plasm concentration-time curves of two formulations
3.3 硫酸头孢喹肟注射液注射液受试品和参比品的生物等效性结果 采用中国药科大学的杨劲老师编的《人体生物利用度数据处理通用程序,BAPP》软件进行生物等效性检验。釆用WINNONLIN 6.3药动学分析软件对参数Cmax与AUC0-τ(已进行对数处理)进行多因素方差分析,每个参数在产品间、周期间以及个体间的差异均不显著(P>0.05),无统计学意义;对达峰时间(未进行对数处理)应用非参数检验后,结果显示两组数据差异不显著(P>0.05),说明两种产品在猪体内的达峰时间存在生物等效。受试产品参数AUC0-τ的对数平均值和参比产品参数AUC0-τ经生物等效性分析后,90%置信区间为97.26% ~105.21%,介于参比产品80%~125%之间;受试产品参数Cmax的对数平均值和参比产品参数Cmax的对数平均值经生物等效性分析后,90%置信区间为89.42% ~104.97%,介于参比产品70% ~143%之间[5]。综上结果表明,国产自研硫酸头孢喹肟注射液(惠可宁®)与默沙东制药公司生产的注射液(克百特®)在猪体内存在生物等效。
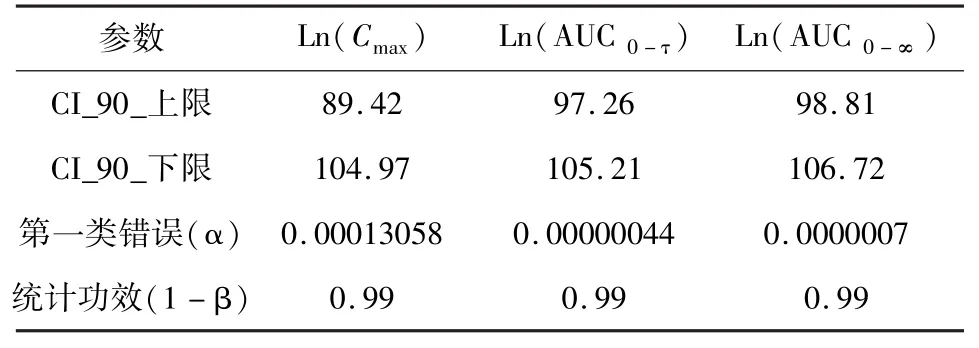
表5 生物等效性分析Tab 5 Bioequivalence analysis
4 讨论与结论
肌内注射受试产品和参比产品硫酸头孢喹肟注射液后,受试产品与参比产品的主要药物动力学参数:药 - 时曲线下面积 AUC0-τ、AUC0-∞、Cmax、Tmax数值接近,无显著性差异。符合生物等效要求。相对于参比品,受试产品的相对生物利用度F为97.02%。
釆用 WINNONLIN 6.3软件对参数 Cmax与AUC0-τ(已进行对数处理)进行多因素方差分析,每个参数在产品间、周期间以及个体间的差异均不显著(P >0.05),无统计学意义;(未进行对数处理)应用非参数检验后,结果显示两组数据差异不显著(P>0.05),说明两种产品在猪体内的达峰时间存在生物等效。依据制剂生物等效性评价标准[8]:供试制剂和参比制剂的 AUC对数比值的90%可信限在80%~125%置信区内;供试制剂和参比制剂的Cmax对数比值的90%可信限在70%~143%置信区内;供试制剂和参比制剂的AUC、Cmax的双向单侧t检验均得到P<0.05的结果,t1≥t1-α(υ)与 t2≥t1-α(υ)同时成立;Tmax经非参数法检验无差异,则供试品与参比制剂具有生物等效性。依据上述制剂生物等效性评价标准检验,表明受试品制剂和参比品制剂为生物等效制剂。
头孢喹肟(cefquinome,CEF)作为第4代动物专用头孢类抗生素,其抗菌谱广,抗菌活性强,对临床分离的大多数G+菌、G-菌均有较强的抗菌活性。金黄色葡萄球菌、链球菌、埃希氏大肠杆菌、溶血性巴氏杆菌、胸膜肺炎放线杆菌等菌对其敏感性较高。目前已被欧盟批准用于猪和牛的呼吸系统疾病、牛乳腺炎、牛败血病和马呼吸系统疾病等多种严重感染的疾病。齐鲁动物保健品有限公司研制的7.5%的硫酸头孢喹肟注射液,通过改变其剂型技术延长了在动物体内作用时间,临床药效时间更持久,减少了给药次数,为养殖户带来了更多选择。
欧洲药物委员会(EMEA)[6-9]报道,牛、猪、马、羊、狗等动物肌内注射、皮下注射1 mg/kg b.w.的头孢喹肟后,达峰时间Tmax介于0.5~2 h之间,达峰浓度在 2.5 ~3.8 μg/mL 之间,血浆蛋白结合率为5% ~15%。其半衰期较短,猪、牛、山羊分别为1~2、1~3、2 h。主要以原型经肾随尿液排出。刘利峰[10]等进行了硫酸头孢喹肟在猪体内的药代动力学研究。 结果显示,猪肌内注射(2 mg/kg b.w.)的主要药代动力学参数消除半衰期(t1/2)为2.28±0.49 h,达峰时间(Tmax)为 0.80 ± 0.05 h,峰浓度(Cmax)为 2.44 ± 0.24 μg/mL;杨大伟[11]等进行了头孢喹肟注射液在猪体内的药代动力学及生物利用度的研究,研究发现,猪颈部肌肉单剂量注射给药后,消除半衰期(t1/2)为 2.76 h,达峰时间(Tmax)为0.32 h,峰浓度(Cmax)为 1.80 μg/mL。 本试验中,单剂量肌内注射(3 mg/kg b.w.)硫酸头孢喹肟注射液(7.5%)参比品后,参比品的平均消除半衰期(t1/2) 为 5.56 ± 0.42 h, 药 时 曲 线 下 面 积(AUC0-τ)为 27.19 ± 2.19 μg·h/mL,达峰时间(Tmax)为(2.30 ±0.73) h,达峰浓度(Cmax)为(2.45±0.36) μg/mL。 单剂量肌内注射硫酸头孢喹肟受试品(7.5%)后,平均消除半衰期(t1/2)为(5.64±0.80) h,药时曲线下面积(AUC0-τ)为 26.38 ±2.30 μg·h/mL,达峰时间(Tmax)为 2.25 ±0.55 h,达峰浓度(Cmax)为 2.37 ± 0.34 μg/mL,相对于参比品的平均相对生物利用度为97.02%。通过对比以上药动学研究结果表明,硫酸头孢喹肟注射液(7.5%)与普通制剂相比,肌内注射给药后自注射部位吸收较迅速,半衰期时间明显增长,体内消除较缓慢,36 h能检测到血液中的药物浓度,达到了长效的目的,因此,本研究开发的长效硫酸头孢喹肟制剂,对延长该药物在体内的作用时间具有重要的临床意义。
本次实验严格遵守药动学试验要求规范展开[12],根据生物等效性分析标准,采用常用的双单侧t检验和90%置信区间统计分析方法来评价和判断药物间的生物等效性,结果表明符合国内仿制药生物等效要求。对国产自研硫酸头孢喹肟注射液(7.5%)肌内注射给药在猪的药动学特征研究,不仅对指导临床合理用药、新药评价、个体化给药及预测药物在猪体内的消除动态、蓄积特性和残留消除规律等具有重要的参考价值;同时药动学研究成果还可用于指导优选给药方案、新药设计、改进药物剂型,对提供高效、长效、低毒、低副作用的药物制剂具有重要指导意义,为国产自研硫酸头孢喹肟注射液(7.5%)的研制以及上市提供重要参考依据。
