芡种壳粉对水中亚甲基蓝和盐基品红的吸附特性
2019-08-20陈静陈志宏张汆张孟
陈静 陈志宏 张汆 张孟

摘要:采用静态和动态吸附法分析芡种壳粉对水相中亚甲基蓝和盐基品红2种染料的吸附特性。结果表明,芡种壳粉对2种染料的吸附过程符合准二级吸附动力学模型,其吸附行为符合Freundlich模型。芡种壳粉对亚甲基蓝和盐基品红显示出很强的吸附能力,在浓度为20 μg/mL时,芡种壳粉对亚甲基蓝和盐基品红的饱和吸附量分别为49.20和47.40 mg/g。动态吸附过程中,虽然芡种壳粉对上述2种染料的饱和吸附量较高且接近,但相同浓度下盐基品红的穿透体积很小,远低于亚甲基蓝的穿透体积。芡种壳粉对亚甲基蓝的吸附为优惠型吸附,而对盐基品红的吸附为非优惠型吸附。因此,若作为染料吸附剂,芡种壳粉更适合于吸附水中的亚甲基蓝,而非盐基品红。
关键词:芡种壳粉;亚甲基蓝;盐基品红;吸附特性;Freundlich模型;Langmiur模型
中图分类号: X703文献标志码: A
文章编号:1002-1302(2019)09-0288-05
目前,工业上常用的废水处理方法主要有絮凝沉淀(气浮)法、电解法、氧化法、生物降解法、导流电凝聚法和吸附法等,对于含染料的废水,吸附法是最便捷、最常用的方法之一,许多农作物副产物和生物质资源,如活性炭、纤维素、橘皮等,对染料均显示出较好的吸附作用[1-4]。芡实是睡莲科(Nymphaeaceae)芡属植物(Euryale)芡(Euryale ferox)的種仁,俗称“鸡头米”,是我国传统的中药原料和滋补食材,年产量4万t左右。芡种子外被一层厚约1~2 mm的木质种壳(芡种壳,Euryale ferox seed coat,简称EFSC),约占其种子质量的40%~50%,是芡米加工中的主要副产物,目前尚未被开发利用。前期研究发现,芡种壳中含有丰富的多酚物质,可作为提取植物多酚的材料[5-7]。自然状态下,芡种壳中的多酚物质与其中的纤维素类分子络合在一起,类似于将多酚物质固定在纤维素分子上,是一种天然功能性材料[8]。为了充分利用芡种壳资源,本研究以芡种壳粉作为吸附剂,对其吸附染料亚甲基蓝和盐基品红的性质进行研究,旨在为其在染料污水处理方面的应用提供依据。
1 材料与方法
1.1 材料与设备
于2016年秋季,在滁州学院生物与食品工程学院食品化学与分析实验室进行试验。
芡种壳粉(芡种壳40 ℃干燥后,粉碎,过60目筛网,装入聚乙烯自封袋内,于4 ℃冰箱内贮存备用)、亚甲基蓝(天津市光复精细化工研究所)、盐基品红(国药集团化学试剂有限公司)、盐酸和氢氧化钠(分析纯试剂)。
Varian Cary 100 Scan型紫外可见分光光度计(美国Varian公司)、DGX-9073 BC-1型鼓风干燥箱(上海福玛实验设备有限公司)、PH SJ-3F型实验室pH计(上海精科实业有限公司)、CL-2型恒温加热磁力搅拌器(郑州长城科工贸有限公司)、CP 224S型分析天平(德国Sartorius公司)、高速中药材粉碎机(天津市泰斯特仪器有限公司)。
1.2 试验方法
1.2.1 染料浓度计算 配制不同浓度的染料溶液,用分光光度法分别测定其在最大吸收波长处的吸光度,根据染料浓度与吸光度的回归方程计算染料浓度及吸附量。
1.2.2 吸附动力学测定[4,9] 静态吸附:用去离子水配制一定浓度的染料溶液(pH值为6.78),分装于20个150 mL三角瓶内,每个三角瓶中装50 mL,再分别加入芡种壳粉 0.50 g,室温(25 ℃)下磁力搅拌,每隔5 min依次吸取其中一个三角瓶内溶液5 mL,过滤,测其吸光度,以此计算其静态吸附量Q,绘制其静态吸附动力学曲线。动态吸附:在层析柱(直径 2.6 cm,长25 cm)中加入一定量的芡种壳粉,将不同染料溶液从上端加入,测定下端流出液的吸光度,计算吸附量,绘制动态吸附动力学曲线。吸附量按下述公式计算:
Q=[(C0-Ce)×V]/m。
式中:Q为吸附量(μg/g);C0为初始浓度(μg/mL);Ce为平衡浓度(μg/mL);V为吸附液的体积(mL);m为芡实壳粉质量(g)。
1.2.3 吸附等温线[10-11] 取1.00 g芡种壳粉加入100 mL不同浓度(4、8、10和20 μg/mL)的染料溶液中,在不同温度(15、25、35和45 ℃)下磁力搅拌2 h后吸取5 mL溶液,过滤,测其吸光度,计算2种染料在不同温度下的平衡吸附量(Qe),用Freundlich和Langmuir 2种模型进行拟合。
Freundlich吸附等温方程为
lnQe=1/n×lnCe+lnKf。
式中:Qe为平衡吸附量(μg/g);Ce为初始浓度(μg/mL);n为吸附分子与吸附剂表面作用强度有关的常数;Kf为Freundlich常数。
Langmuir吸附等温方程为
Ce/Qe=1/(αQmax)+Ce/Qmax
式中:Ce为平衡浓度(μg/mL);Qe为平衡吸附量(μg/g);Qmax为最大吸附量(μg/g);α为常数。
1.2.4 pH值对静态吸附量的影响 配制浓度为20 μg/mL不同pH值的染料溶液,分别加入10个250 mL锥形瓶中,在每个锥形瓶中再加入1.00 g芡种壳粉。常温下磁力搅拌 2 h,每隔5 min吸取5 mL溶液,过滤,测定吸光度,计算芡种壳粉对染料的吸附量。
1.3 数据处理方法
采用Excel和DPSv 7.55数据处理软件对数据进行分析,采用多重比较法进行显著性分析。所有试验重复测定3次,取平均值,表示为平均值±标准差。
2 结果与分析
2.1 吸附动力学性质
芡种壳粉对2种染料的平衡吸附量均随溶液中染料初始浓度的增加而显著增加(P<0.01),在染料浓度为20 μg/mL时,芡种壳粉对亚甲基蓝和盐基品红的静态饱和吸附量分别为1.862、1.942 mg/g。
由图1-a可见,在动态吸附过程中,芡种壳粉对亚甲基蓝染料的吸附效率很高,在染料浓度为10、20 μg/mL时,芡种壳粉对亚甲基蓝动态吸附的穿透体积分别为1 420、 620 mL,达到动态吸附平衡时的平衡体积分别为3 420、 1 880 mL,达到平衡时的饱和吸附量分别为49.60、 49.20 mg/g,远高于其静态平衡吸附量,接近海泡石对亚甲基蓝的动态吸附量(51.18 mg/g)[11]。
由图1-b可见,芡种壳粉对盐基品红染料的动态吸附效率较低,不同浓度染料溶液的穿透体积均为20 mL,但一直都有吸附,平衡时间较长。染料浓度为10、20 μg/mL时,达到平衡时的平衡体积分别为4 000、2 400 mL,达到平衡时的饱和吸附量分别为47.43、46.40 mg/g。
总体而言,虽然芡种壳粉对水溶液中盐基品红的吸附(脱色)效率不高,但其饱和吸附量与亚甲基蓝接近。相对而言,芡种壳粉对亚甲基蓝的吸附效率较高,在染料浓度为10、20 μg/mL时,达到穿透体积时(1 420、620 mL),芡种壳粉对亚甲基蓝的吸附量分别为30.22、23.86 mg/g。
2.2 pH值对吸附量的影响
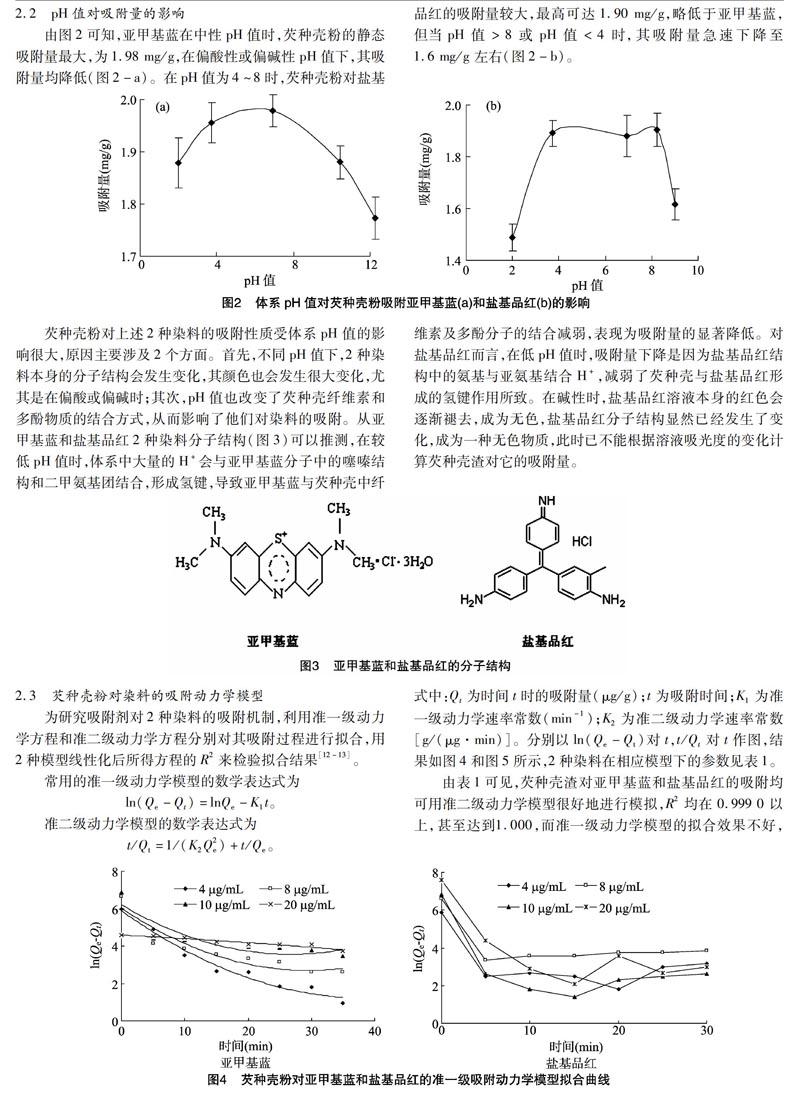
由图2可知,亚甲基蓝在中性pH值时,芡种壳粉的静态吸附量最大,为1.98 mg/g,在偏酸性或偏碱性pH值下,其吸附量均降低(图2-a)。在pH值为4~8时,芡种壳粉对盐基品红的吸附量较大,最高可达1.90 mg/g,略低于亚甲基蓝,但当pH值>8或pH值<4时,其吸附量急速下降至 1.6 mg/g 左右(图2-b)。
芡种壳粉对上述2种染料的吸附性质受体系pH值的影响很大,原因主要涉及2个方面。首先,不同pH值下,2种染料本身的分子结构会发生变化,其颜色也会发生很大变化,尤其是在偏酸或偏碱时;其次,pH值也改变了芡种壳纤维素和多酚物质的结合方式,从而影响了他们对染料的吸附。从亚甲基蓝和盐基品红2种染料分子结构(图3)可以推测,在较低pH值时,体系中大量的H+会与亚甲基蓝分子中的噻嗪结构和二甲氨基团结合,形成氢键,导致亚甲基蓝与芡种壳中纤维素及多酚分子的结合减弱,表现为吸附量的显著降低。对盐基品红而言,在低pH值时,吸附量下降是因为盐基品红结构中的氨基与亚氨基结合H+,减弱了芡种壳与盐基品红形成的氢键作用所致。在碱性时,盐基品红溶液本身的红色会逐渐褪去,成为无色,盐基品红分子结构显然已经发生了变化,成为一种无色物质,此时已不能根据溶液吸光度的变化计算芡种壳渣对它的吸附量。
2.3 芡种壳粉对染料的吸附动力学模型
为研究吸附剂对2种染料的吸附机制,利用准一级动力学方程和准二级动力学方程分别对其吸附过程进行拟合,用2种模型线性化后所得方程的R2来检验拟合结果[12-13]。
常用的准一级动力学模型的数学表达式为
ln(Qe-Qt)=lnQe-K1t。
准二级动力学模型的数学表达式为
t/Qt=1/(K2Q2e)+t/Qe。
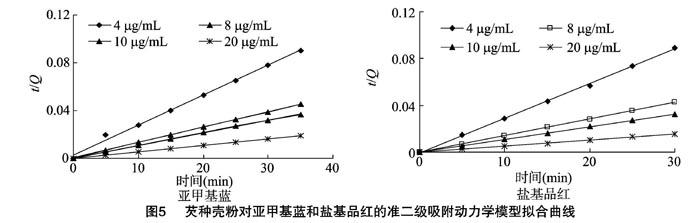
式中:Qt为时间t时的吸附量(μg/g);t为吸附时间;K1为准一级动力学速率常数(min-1);K2为准二级动力学速率常数[g/(μg·min)]。分别以ln(Qe-Qt)对t,t/Qt对t作图,结果如图4和图5所示,2种染料在相应模型下的参数见表1。
由表1可见,芡种壳渣对亚甲基蓝和盐基品红的吸附均可用准二级动力学模型很好地进行模拟,R2均在 0.999 0 以上,甚至达到1.000,而准一级动力学模型的拟合效果不好,
说明其吸附动力学更接近准二级动力学模型。准二级动力学方程常用于描述反应速度与2种反应物浓度成正比的情况。因此,本试验动力学拟合结果提示,芡种壳渣对亚甲基蓝和盐基品红的吸附更像是化学吸附。研究发现,芡种壳中含有大量的酚类物质[7],这些多酚虽然可被有机溶剂萃取,但芡种壳渣中仍残留有许多多酚物质,这些多酚物质被其中的纤维素类物质紧紧吸附而得以固定[8]。因此,不难推测出在整个吸附体系中这些酚类物质极有可能也参与了吸附过程。
亚甲基蓝分子结构中含有二甲氨基[—N—(CH3)2—]和噻嗪结构,盐基品红分子中含有氨基(—NH2)和亚氨基(—NH—),这些结构中的氮原子均含有孤对电子(图3)。当亚甲基蓝结构中氨基中的氢原子被烷基取代后,由于烷基的给电子诱导效应使氮原子上的电子密度增高,因此碱性增强。当盐基品红结构中氨基中氢原子被芳香烃取代时,芳香烃由于氮原子上的孤对电子与苯环共轭,提供电子能力较低,但苯环上含有给电子取代基且与氨基对位,所以碱性增强。因此,这2种染料均可与被芡种壳渣固定的多酚物质发生反应,进而被芡种壳渣所吸附。
2.4 吸附等温线
目前,用于描述吸附平衡行为的理论主要有Langmuir的单分子层吸附理论和Freundlich经验方程,此外,还包括Dubinin-Astskhow式和BET式(指解释气体分子在固体表面吸附现象的理论)等[14]。为探讨芡种壳粉作为吸附剂对水相中亚甲基蓝和盐基品红这2种染料的吸附行为,本研究分析了不同温度下的吸附等温线,并分别用Freundlich方程和Langmuir方程对试验数据进行拟合,结果分别见图6和表2。
Freundlich方程的参数n为吸附指数,其值一般在0~10,n≥2時吸附过程易进行,n>1时为优惠型吸附[15]。本试验中,在不同温度下,芡种壳粉对亚甲基蓝吸附过程中的n>1, 而对盐基品红吸附的n<1, 因此,芡种壳粉对亚甲基蓝的吸附为优惠型吸附,而对盐基品红的吸附为非优惠型吸附。Langmuir方程的参数α是和溶质与吸附剂间结合相关的特征参数,是吸附速率与解吸速率的比值,其大小能反映吸附反应的自发程度,α值越大,反应的自发程度越高,生成物越稳定,吸附剂对溶质的吸附能力越强[16]。本试验中,在不同温度下,芡种壳粉对亚甲基蓝吸附过程中的α值虽明显低于盐基品红的,但还不能代表芡种壳粉与亚甲基蓝的吸附产物较不稳定,而与盐基品红的吸附产物比较稳定,因为本试验中所得模型的相关性很低。
Langmuir方程能描述溶液中溶质在固体表面吸附的全过程,参数Qmax表示固体对溶质的理论饱和吸附量,即芡种壳渣对染料的最大吸附容量。本试验中,芡种壳粉对亚甲基蓝的理论饱和吸附量在35 ℃时最高,当温度升高至45 ℃时,不利于吸附的进行。相对而言,芡种壳粉对盐基品红的理论饱和吸附量均远低于亚甲基蓝的理论饱和吸附量,但温度的影响趋势基本一致。Freundlich方程不能计算理论吸附饱和量,但参数Kf与参数Qmax呈一致性变化,反映了固体表面吸附溶质的容量,Kf值越大,吸附量越大[17-18]。
3 结论
芡种壳粉对亚甲基蓝和盐基品红2种染料的吸附过程符合准二级动力学方程,吸附行为更接近Freundlich吸附等温式,吸附剂对这2种染料的吸附是表面吸附。pH值对吸附过程影响较大,对亚甲基蓝的吸附量在中性条件下最大,对盐基品红的吸附在弱碱性(pH值为8.21)条件下最大。温度对吸附过程也有较大影响,在25~45 ℃范围内,芡种壳粉对亚甲基蓝的理论饱和吸附量在35 ℃时最高,当温度升高至45 ℃时,饱和吸附量则明显降低。
芡种壳粉对2种染料的饱和吸附量均较大。在浓度为20 μg/mL时,芡种壳粉对亚甲基蓝和盐基品红浓度的饱和吸附量分别为49.20、47.40 mg/g。芡种壳粉对亚甲基蓝的吸附为优惠型吸附,而对盐基品红的吸附为非优惠型吸附,因此,若作为染料吸附剂,芡种壳粉更适合用于亚甲基蓝的吸附,不适合用来吸附盐基品红。
参考文献:
[1]Gil A,Assis F C,Albeniz S,et al. Removal of dyes from wastewaters by adsorption on pillared clays[J]. Chemical Engineering Journal,2011,168(3):1032-1040.
[2]Wan Ngah W S,Hanafiah M A K M. Removal of heavy metal ions from wastewater by chemically modified plant wastes asadsorbents:a review[J]. Bioresource Technology,2008,99(10):3935-3948.
[3]Bulut Y,Aydin H. A kinetics and thermodynamics study of methylene blue adsorption on wheat shells[J]. Desalination,2006,194(1/2/3):259-267.
[4]施文健,陈肖云,张元璋,等. 两性纤维素对持久性污染物的吸附特征[J]. 高分子材料科学与工程,2011,27(6):49-52.
[5]王和才. 芡实种皮总鞣质的提取及含量测定[J]. 食品工业科技,2009,30(8):224-226.
[6]孙文凯,袁怀波,许 卫,等. 芡实壳提取物抗氧化能力研究[J]. 食品工业科技,2011,32(4):100-102.
[7]张 汆,薛连海,贾小丽,等. D101树脂分离纯化芡实多酚的特性研究[J]. 食品科学,2009,30(20):260-264.
[8]石 碧,狄 莹. 植物多酚[M]. 北京:科学出版社,2000:292-306.
[9]Racanicci A C. Allesen-Holm B H,Skibsted L H. Sensory evaluation of precooked chicken meat with mate (Ilex paraguariensis) added as antioxidant[J]. European Food Research and Technology,2009,229(2):277-280.
[10]Dogan M,Ozdemir Y,Alkan M. Adsorption kinetics and mechanism of cationic methyl violet and methylene blue dyes onto sepiolite[J]. Dyes and Pigments,2007,75(3):701-713.
[11]Weng C H,Pan Y F. Adsorption of a cationic dye (methylene blue) onto spent activated clay[J]. Journal of Hazardous Materials,2007,144(1/2):355-362.[HJ1.62mm]
[12]Bhattacharyya K G,Sharma A. Kinetics and thermodynamics of methylene blue adsorption on neem (Azadirachta indica) leaf powder[J]. Dyes and Pigments,2005,65(1):51-59.
[13]化全縣,汤建伟,刘 咏,等. 钢渣对废水中磷的吸附性能[J]. 过程工程学报,2010,10(1):75-79.
[14]近藤精一,石川达雄,安布郁夫. 吸附科学[M]. 北京:化学工业出版社,2005:36-45.
[15]林春香,詹怀宇,刘明华,等. 球形纤维素吸附剂对Cu2+的吸附动力学与热力学研究[J]. 离子交换与吸附,2010,26(3):226-238.
[16]王 菲,王连军,李健生,等. 大孔螯合树脂对Pb2+的吸附行为及机理[J]. 过程工程学报,2008,8(3):466-471.
[17]Bozi[KG-*5]c[DD(-1*2][HT6]′[KG*2]D,Stankovi[KG-*5]c[DD(-1*2][HT6]′[KG*2]V,Gorgievski M,et al. Adsorption of heavy metal ions by sawdust of deciduous trees[J]. Journal of Hazardous Materials,2009,171(1/2/3):684-692.
[18]Auta M,Hameed B H. Optimized waste tea activated carbon for adsorption of methylene blue and acid blue 29 dyes using response surface methodology[J]. Chemical Engineering Journal,2011,175(15):233-243.
