舒芬太尼与芬太尼用于危重症儿童镇痛、镇静的效果比较
2019-08-20刘燕好廖世雄李楚云陈美玲唐尚鸿
刘燕好,廖世雄,李楚云,陈美玲,唐尚鸿
(1.惠州市妇幼保健计划生育服务中心药剂科,广东 惠州516001; 2.惠州市中心人民医院药学部,广东 惠州 516001; 3.惠州市妇幼保健计划生育服务中心儿童重症病区,广东 惠州 516001)
儿科重症监护病房(pediatric intensive care unit,PICU)中的患儿常存在疼痛、焦虑和恐惧等情况,通常需要使用药物治疗以减轻危重患儿的应激反应,减少氧耗,安全有效地实施各种操作和治疗,帮助患儿顺利渡过病情危险期。舒芬太尼为强效脂溶性阿片类镇静药,其镇痛效果非常好,安全性高,目前已广泛用于全身麻醉诱导、术中维持及术后镇痛[1-4]。本研究比较了PICU危重症儿童应用舒芬太尼与芬太尼镇痛、镇静的效果,以期为临床提供用药参考,现报告如下。
1 资料与方法
1.1 资料来源
回顾性选取2018年1—6月惠州市妇幼保健计划生育服务中心PICU收治的使用芬太尼的患儿101例作为对照组,2018年7—12月使用舒芬太尼的患儿99例作为观察组。纳入标准:年龄≤16岁;满足以下标准之一的PICU患儿,即机械通气过程中人机不协调,严重低氧血症,血流动力学不稳定等。排除标准:对阿片类药物过敏者;昏迷者[格拉斯哥昏迷量表(glasgow coma scale,GCS)评分<8分],麻醉术后患儿应恢复到GCS>8分后再实施镇痛。两组患儿的一般资料相似,具有可比性,见表1。

表1 两组患儿的一般资料比较Tab 1 Comparison of general information before two groups
1.2 方法
(1)镇痛计划:镇痛目标为面部表情疼痛量表(faces pain scale,FPS)评分≤2分。FPS是根据6个水平排列的面部表情(如微笑、皱眉、哭泣等)提示不同程度疼痛时的表情图,从不痛到疼痛难忍分别对应于0—10分[5]。当镇痛药用量达限定剂量[舒芬太尼为0.3 μg/(kg·h),芬太尼为2 μg/(kg·h)]而FPS仍不能达标时,维持镇痛限定剂量并加用咪达唑仑注射液(规格:1ml∶5mg)3 μg/(kg·h)。镇痛/镇静时间限定为48~168 h。(2)观察组患儿根据《儿童重症监护治疗病房镇痛和镇静治疗专家共识》(2013版)[6]推荐,使用枸橼酸舒芬太尼注射液(规格:1 ml∶50 μg)的负荷剂量为0.1~0.3 μg/(kg·h),维持剂量为缓慢静脉注射0.03~ 0.05 μg/(kg·h);当泵速为0.3 μg/(kg·h),而FPS评分仍不能≤2分,则维持镇痛限定泵速0.3 μg/(kg·h)并加用咪达唑仑3 μg/(kg·h);使用枸橼酸舒芬太尼注射液镇痛的平均总用药时间为75.6 h,使用咪达唑仑镇静的平均总用药时间为43.2 h。(3)对照组患儿根据《儿童重症监护治疗病房镇痛和镇静治疗专家共识》(2013版)[5]推荐,使用枸橼酸芬太尼注射液(规格:2 ml∶0.1 mg)的负荷剂量为1~2 μg/(kg·h),直至FPS评分≤2分;然后改用维持剂量1 μg/(kg·h),根据FPS评分是否≤2分调节泵速;当泵速为2 μg/(kg·h),而FPS评分仍不能≤2分,维持镇痛限定泵速2 μg/(kg·h)并加用咪达唑仑3 μg/(kg·h)。使用芬太尼镇痛的平均总用药时间77.1 h,使用咪达唑仑镇静的平均总用药时间为44.3 h。
1.3 监测指标
观察两组患儿镇痛前后的生命体征[心率、呼吸频率、平均动脉压(MAP)及脉搏血氧饱和度(SpO2)]、肝功能指标[天门冬氨酸氨基转移酶(AST)、丙氨酸氨基转移酶(ALT)、总胆红素(TBIL)、白蛋白(ALB)及总蛋白(TP)]水平、肾功能指标[肌酐(Cr)、尿素氮(BUN)]水平及血气分析指标[动脉血二氧化碳分压(PaCO2)、动脉血氧分压(Pa02)]水平,并比较两组患儿镇痛效果和不良反应发生情况的差异。
1.4 统计学方法
2 结果
2.1 两组患儿镇痛前后生命体征比较
镇痛后,两组患儿心率、呼吸频率、MAP及SpO2的差异均无统计学意义(P>0.05),见表2。
2.2 两组患儿镇痛前后肝功能指标水平比较
镇痛后,两组患儿ALT、AST、TBIL、ALB及TP水平的差异均无统计学意义(P>0.05),见表3。
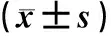
表2 两组患儿镇痛前后生命体征比较Tab 2 Comparison of vital signs between two groups before and after
注:1 mm Hg=0.133 kPa
Note:1 mm Hg=0.133 kPa
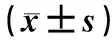
表3 两组患儿镇痛前后肝功能指标水平比较Tab 3 Comparison of liver function indices between two groups before and after
2.3 两组患儿镇痛前后肾功能指标水平比较
镇痛后,两组患儿Cr、BUN水平的差异均无统计学意义(P>0.05),见表4。
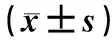
表4 两组患儿镇痛前后肾功能指标水平比较Tab 4 Comparison of renal function indices between two groups before and after
2.4 两组患儿镇痛前后血气分析指标水平比较
镇痛后,两组患儿PaCO2、PaO2水平的差异均无统计学意义(P>0.05),见表5。
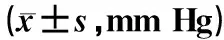
表5 两组患儿镇痛前后血气分析指标水平比较Tab 5 Comparison of indices of blood gas between two groups
2.5 两组患儿镇痛效果比较
观察组患儿的镇痛药总量明显少于对照组;但由于舒芬太尼与5倍芬太尼等效剂量[7],故观察组患儿的镇痛药总量与对照组(芬太尼5倍剂量)的差异无统计学意义(P>0.05)。给药第3日,两组患儿镇痛达标率、镇静达标率的差异均无统计学意义(P>0.05),见表6。
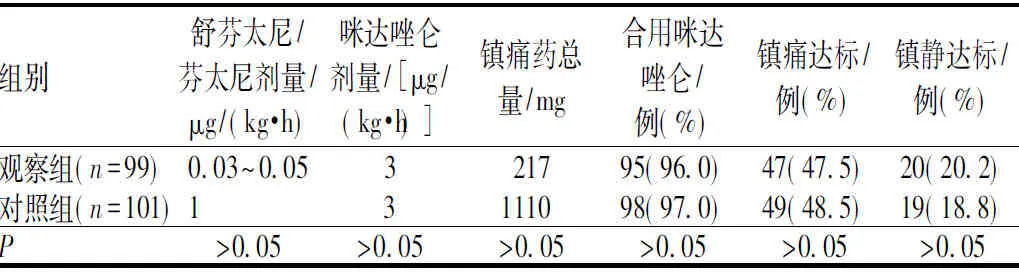
表6 两组患儿镇痛效果比较Tab 6 Comparison of analgesia effects between two groups
2.6 两组患儿不良反应发生情况比较
两组患儿不良反应发生率的差异无统计学意义(P>0.05);但观察组患儿的低血压发生率明显低于对照组,差异有统计学意义(P<0.05),见表7。
3 讨论
相比成人日渐臻熟的镇痛镇静治疗方案,近20年关于儿童疼痛的问题才逐渐被重视[8]。因为儿童生理及心理处于动态发展过程中,针对儿童的镇痛镇静技术与成人有明显不同[9]。PICU患儿处于强烈的应激环境中,包括:(1)创伤、手术、缺氧和感染等引发应激反应,频繁的检查和有创性诊疗操作;(2)常与父母隔离,大量陌生面孔和仪器的出现,噪音和长明灯扰乱饮食、睡眠及生物钟;(3)各种插管和长期卧床;

表7 两组患儿不良反应发生情况比较[例(%)]Tab 7 Comparison of incidence of adverse drug reactions between two groups [cases(%)]
(4)对疾病预后的担心和对死亡的恐惧[7,10]。因而,PICU中患儿镇痛镇静的治疗原则应是先镇痛后镇静再肌松,不论患儿是否需要镇静,所有危重症患儿都应采取适当的镇痛措施[11]。
舒芬太尼属于阿片受体激动剂,与阿片受体的结合能力比芬太尼强7~10倍。但相关研究结果显示,舒芬太尼对于重症
加强护理病房需要气管插管及机械通气的患者前5 d的有效镇痛剂量为0.15 μg/kg,5 d后约40%的患者需要增加剂量[12]。而舒芬太尼对血流动力学的影响与芬太尼相似,能使心率、心排血指数、MAP及心肌耗氧量降低,但在大剂量使用时,可能导致心排血指数、MAP降低,心率减慢[13]。另外,舒芬太尼可抑制呼吸,但其对呼吸的抑制呈剂量依赖性,镇痛剂量下的舒芬太尼无明显的呼吸抑制作用,且舒芬太尼对呼吸的抑制作用较芬太尼更小[14]。
本研究结果显示,镇痛后,两组患儿心率、呼吸频率、MAP、SpO2、肝功能指标水平、肾功能指标水平、PaCO2及Pa02水平的差异均无统计学意义(P>0.05)。两组患儿不良反应发生率的差异无统计学意义(P>0.05);但观察组患儿低血压发生率明显低于对照组,差异有统计学意义(P<0.05);本研究中无成瘾性发生,也无骨骼肌强直现象,与既往研究结果一致[15-17]。
综上所述,舒芬太尼与芬太尼用于危重症儿童的镇痛效果相近,但应用舒芬太尼的患儿低血压发生率较低。
